УЗИ с контрастированием
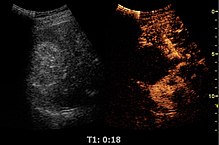
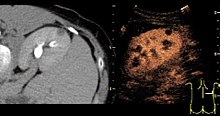
Ультразвук с контрастным усилением ( CEUS ) — это применение ультразвукового контрастного вещества к традиционной медицинской сонографии . для ультразвука Контрастные агенты основаны на различных способах отражения звуковых волн от границ раздела веществ. Это может быть поверхность небольшого воздушного пузырька или более сложной структуры. Коммерчески доступные контрастные вещества представляют собой газонаполненные микропузырьки , которые вводятся внутривенно в большой круг кровообращения . Микропузырьки обладают высокой степенью эхогенности (способностью объекта отражать ультразвуковые волны). Существует большая разница в эхогенности газа в микропузырьках и мягких тканях тела. Таким образом, ультразвуковая визуализация с использованием микропузырьковых контрастных агентов усиливает обратное рассеяние ультразвука (отражение) ультразвуковых волн, создавая сонограмму с повышенным контрастом из-за высокой разницы в эхогенности. Ультразвуковое исследование с контрастным усилением можно использовать для визуализации перфузии крови в органах, измерения скорости кровотока в органах. сердце и другие органы, а также для других целей.
Нацеливающие лиганды , которые связываются с рецепторами, характерными для внутрисосудистых заболеваний, могут быть конъюгированы с микропузырьками , что позволяет комплексу микропузырьков избирательно накапливаться в интересующих областях, таких как больные или аномальные ткани. Эта форма молекулярной визуализации, известная как целевое ультразвуковое исследование с контрастным усилением, генерирует сильный ультразвуковой сигнал только в том случае, если целевые микропузырьки связываются в интересующей области. Прицельное ультразвуковое исследование с контрастным усилением может иметь множество применений как в медицинской диагностике , так и в медицинской терапии. Однако таргетная методика еще не одобрена FDA для клинического использования в США.
Ультразвуковое исследование с контрастным усилением считается безопасным для взрослых, сравнимым с безопасностью контрастных веществ для МРТ и лучшим, чем радиоконтрастные вещества, используемые при контрастной КТ . Более ограниченные данные о безопасности у детей позволяют предположить, что такое использование так же безопасно, как и у взрослого населения. [2]
Пузырьковая эхокардиограмма
[ редактировать ]Эхокардиограмма – исследование сердца с помощью ультразвука. Пузырьковая эхокардиограмма является ее расширением, при которой в качестве контрастного вещества во время исследования используются простые пузырьки воздуха, и ее часто приходится запрашивать отдельно.
Хотя цветная допплерография может использоваться для обнаружения аномальных потоков между камерами сердца (например, стойкого (открытого) овального окна ), она имеет ограниченную чувствительность . При специальном поиске такого дефекта небольшие пузырьки воздуха можно использовать в качестве контрастного вещества и вводить внутривенно, где они попадают в правую часть сердца. Тест будет положительным на аномальную коммуникацию, если видно, что пузырьки проходят в левую часть сердца. (Обычно они выходят из сердца через легочную артерию и останавливаются в легких.) Эта форма пузырькового контрастного вещества создается на специальной основе врачом, проводящим тестирование, путем перемешивания физиологического раствора (например, путем быстрого и многократного переноса физиологический раствор между двумя соединенными шприцами) непосредственно перед инъекцией. [ нужна ссылка ]
Микропузырьковые контрастные вещества
[ редактировать ]Общие характеристики
[ редактировать ]Существует множество микропузырьковых контрастных веществ. Микропузырьки различаются по составу оболочки, составу газового ядра и по тому, нацелены они или нет. [ нужна ссылка ]
- Оболочка микропузырьков : выбор материала оболочки определяет, насколько легко микропузырьки усваиваются иммунной системой . Более гидрофильный материал имеет тенденцию легче усваиваться, что сокращает время пребывания микропузырьков в циркуляции. Это сокращает время, доступное для контрастной визуализации. Материал оболочки также влияет на механическую эластичность микропузырьков. Чем эластичнее материал, тем большую акустическую энергию он может выдержать, прежде чем лопнет. [3] Чаще всего оболочки микропузырьков состоят из альбумина , галактозы , липидов или полимеров . [4] Гидрофобные частицы также применялись для стабилизации оболочек микропузырьков. [5]
- Газовое ядро микропузырька : Газовое ядро является основной частью контрастного для ультразвука микропузырька, который определяет его эхогенность. Пузырьки газа, подвергающиеся воздействию ультразвука, пульсируют и рассеивают характерный сигнал. Этот сигнал проявляется как высокоамплитудный объект на сонограмме с контрастным усилением. Газовые ядра могут состоять из воздуха или тяжелых газов, таких как перфторуглерод или азот . [4] Тяжелые газы менее растворимы в воде, поэтому вероятность их утечки из микропузырька, приводящей к растворению микропузырька, меньше. [3] В результате микропузырьки с тяжелыми газовыми ядрами дольше сохраняются в циркуляции. Для усиления гармонических пульсаций к газовому содержимому добавлены жидкие и твердые ядра. [6]
Независимо от состава оболочки или газового ядра, размер микропузырьков довольно однороден. Они лежат в пределах 1–4 микрометров в диаметре. Это делает их меньше эритроцитов , что позволяет им легко проходить через кровообращение и микроциркуляцию.
Конкретные агенты
[ редактировать ]- Липидные микросферы перфлутрена (торговые марки Definity, Luminity) представляют собой перфторуглеродные эмульсии, состоящие из октафторпропана, инкапсулированного во внешнюю липидную оболочку . [7] [8]
- Газовое ядро из октафторпропана с оболочкой из альбумина ( Optison ) — еще одна перфторуглеродная эмульсия , которая представляет собой микропузырьки, одобренные Управлением по контролю за продуктами и лекарствами (FDA) и произведенные GE Healthcare ).
- гексафторида серы Микропузырьки ( SonoVue Bracco (компания) ). В основном его используют для характеристики поражений печени, которые невозможно правильно идентифицировать с помощью обычного ультразвука (b-режим). Он остается видимым в крови от 3 до 8 минут и выводится через легкие. [9]
- Воздух внутри липидно-галактозной оболочки (ранее Levovist, микропузырьки, одобренные FDA, производства Schering ). [4]
- Липидные микросферы перфлексана (ранее Imagent или Imavist) представляли собой инъекционную суспензию, разработанную Alliance Pharmaceutical, одобренную FDA (в июне 2002 г.) для улучшения визуализации камеры левого желудочка сердца, очерчивания границ эндокарда у пациентов с субоптимальными эхокардиограммами. Помимо использования для оценки сердечной функции и перфузии, он также используется в качестве усилителя изображений простаты, печени, почек и других органов. [10]
Целевые микропузырьки
[ редактировать ]Направленные микропузырьки находятся на стадии доклинической разработки. Они сохраняют те же общие характеристики, что и нецелевые микропузырьки, но оснащены лигандами, которые связывают специфические рецепторы, экспрессируемые интересующими типами клеток, такими как воспаленные клетки или раковые клетки. Разрабатываемые в настоящее время микропузырьки состоят из липидной монослойной оболочки с газовым ядром из перфторуглерода. Липидная оболочка также покрыта слоем полиэтиленгликоля (ПЭГ). ПЭГ предотвращает агрегацию микропузырьков и делает микропузырьки более инертными. Он временно «скрывает» микропузырьки от поглощения иммунной системой, увеличивая время циркуляции и, следовательно, время визуализации. [11] Помимо слоя ПЭГ, оболочка модифицирована молекулами, позволяющими прикреплять лиганды , связывающие определенные рецепторы . Эти лиганды прикрепляются к микропузырькам с помощью карбодиимида , малеимида или биотин-стрептавидина. [11] Биотин-стрептавидин является наиболее популярной стратегией сочетания, поскольку биотина сродство к стрептавидину очень сильное, и лиганды легко пометить биотином. В настоящее время эти лиганды представляют собой моноклональные антитела, полученные из культур клеток животных, которые специфически связываются с рецепторами и молекулами, экспрессируемыми клетками-мишенями. Поскольку антитела не гуманизированы, они будут вызывать иммунный ответ при использовании в терапии человека. Гуманизация антител — дорогостоящий и трудоемкий процесс, поэтому было бы идеально найти альтернативный источник лигандов, например синтетически изготовленные нацеливающие пептиды , которые выполняют ту же функцию, но без проблем с иммунитетом. [ нужна ссылка ]
Типы
[ редактировать ]Существует две формы ультразвукового исследования с контрастным усилением: нецелевое (используется сегодня в клинике) и таргетное (в стадии доклинической разработки). Эти два метода немного отличаются друг от друга.
Нецелевой CEUS
[ редактировать ]Нецелевые микропузырьки, такие как вышеупомянутые SonoVue, Optison или Levovist, вводятся внутривенно в системный кровоток небольшим болюсом. Микропузырьки будут оставаться в системном кровообращении в течение определенного периода времени. В это время ультразвуковые волны направляются на интересующую область. Когда микропузырьки в крови проходят мимо окна визуализации, их сжимаемые газовые ядра колеблются в ответ на высокочастотное звуковое энергетическое поле, как описано в статье об ультразвуке . Микропузырьки отражают уникальное эхо , которое резко контрастирует с окружающей тканью из-за несоответствия на порядки величины между эхогенностью микропузырьков и ткани. Ультразвуковая система преобразует сильную эхогенность в контрастное изображение интересующей области. Таким образом, эхо кровотока усиливается, что позволяет врачу отличить кровь от окружающих тканей. [ нужна ссылка ]
Целевой CEUS
[ редактировать ]Прицельное УЗИ с контрастным усилением работает аналогичным образом, с некоторыми изменениями. Микропузырьки, нацеленные на лиганды, которые связывают определенные молекулярные маркеры, экспрессируемые в интересующей области визуализации, по-прежнему вводятся системно небольшими болюсами. Микропузырьки теоретически путешествуют по кровеносной системе, в конечном итоге находя соответствующие цели и специфически связываясь. Затем ультразвуковые волны можно направить на интересующую область. Если в этой области образовалось достаточное количество микропузырьков, их ядра из сжимаемого газа колеблются в ответ на высокочастотное звуковое энергетическое поле, как описано в статье об ультразвуке . Целевые микропузырьки также отражают уникальное эхо, которое резко контрастирует с окружающей тканью из-за несоответствия на порядки величины между эхогенностью микропузырьков и ткани. Ультразвуковая система преобразует сильную эхогенность в контрастное изображение интересующей области, выявляя расположение связанных микропузырьков. [12] Обнаружение связанных микропузырьков может затем показать, что интересующая область экспрессирует тот конкретный молекулярный маркер, который может указывать на определенное болезненное состояние, или идентифицировать конкретные клетки в интересующей области. [ нужна ссылка ]
Приложения
[ редактировать ]Нецелевое ультразвуковое исследование с контрастным усилением в настоящее время применяется в эхокардиографии и радиологии . Целевой ультразвук с контрастным усилением разрабатывается для различных медицинских применений.
Нецелевой CEUS
[ редактировать ]Нецелевые микропузырьки, такие как Оптисон и Левовист, в настоящее время используются в эхокардиографии. Кроме того, СоноВью [13] Ультразвуковое контрастное вещество используется в радиологии для характеристики поражений.
- Очертание границ органов : микропузырьки могут усилить контраст на границе между тканью и кровью. Более четкое представление об этом интерфейсе дает клиницисту лучшее представление о структуре органа. Структура ткани имеет решающее значение для эхокардиограммы: истончение, утолщение или неровности сердечной стенки указывают на серьезное заболевание сердца, требующее либо наблюдения, либо лечения.
- Объем крови и перфузия : ультразвук с контрастным усилением обещает (1) оценить степень перфузии крови в интересующем органе или области и (2) оценить объем крови в интересующем органе или области. При использовании в сочетании с ультразвуковой допплерографией микропузырьки могут измерять скорость кровотока в миокарде для диагностики проблем с клапанами. И относительная интенсивность эха микропузырьков [14] также может дать количественную оценку объема крови.
- Характеристика поражения : ультразвуковое исследование с контрастным усилением играет роль в дифференциации доброкачественных и злокачественных очаговых поражений печени. Эта дифференциация основана на наблюдении [15] или обработка [16] [17] динамического сосудистого рисунка в очаге поражения по отношению к окружающей его тканевой паренхиме .
Целевой CEUS
[ редактировать ]- Воспаление . Контрастные вещества могут быть предназначены для связывания с определенными белками, которые экспрессируются при воспалительных заболеваниях, таких как болезнь Крона , атеросклероз и даже сердечные приступы . Клетки, представляющие интерес в таких случаях, представляют собой эндотелиальные клетки кровеносных сосудов и лейкоциты :
- Воспаленные кровеносные сосуды специфически экспрессируют определенные рецепторы, функционирующие как молекулы клеточной адгезии , такие как VCAM-1, ICAM-1, E-селектин . Если на микропузырьки воздействуют лиганды, связывающие эти молекулы, их можно использовать в контрастной эхокардиографии для обнаружения начала воспаления. Раннее выявление позволяет разработать более эффективные методы лечения. Были предприняты попытки снабдить микропузырьки моноклональными антителами, которые связывают P-селектин , ICAM-1 и VCAM-1 . [4] но адгезия к молекулярной мишени была плохой, и большая часть микропузырьков, связавшихся с мишенью, быстро отделялась, особенно при высоких напряжениях сдвига, имеющих физиологическое значение . [18]
- Лейкоциты обладают высокой эффективностью адгезии, отчасти благодаря двухлигандной системе остановки клеток селектин - интегрин . [19] Одна пара лиганд:рецептор ( PSGL-1 :селектин) обладает быстрой скоростью включения связи, замедляя движение лейкоцитов, и позволяет второй паре (интегрин: суперсемейство иммуноглобулинов ), которая имеет более медленную скорость включения, но медленную скорость отключения, останавливать лейкоцитов, кинетически усиливающих адгезию. Были предприняты попытки заставить контрастные вещества связываться с такими лигандами с помощью таких методов, как нацеливание двух лигандов на отдельные рецепторы на полимерные микросферы. [20] [21] и биомимикрия системы остановки клеток селектин-интегрин лейкоцитов, [22] продемонстрировав повышенную эффективность адгезии, но все же недостаточно эффективный, чтобы позволить клиническое использование целевого ультразвука с контрастным усилением при воспалении.
- Тромбоз и тромболизис . Активированные тромбоциты являются основными компонентами тромбов (тромбов). Микропузырьки могут быть конъюгированы с рекомбинантным одноцепочечным вариабельным фрагментом, специфичным к активированному гликопротеину IIb/IIIa (GPIIb/IIIa), который является наиболее распространенным поверхностным рецептором тромбоцитов. Несмотря на высокое напряжение сдвига в области тромба, микропузырьки, нацеленные на GPIIb/IIIa, будут специфически связываться с активированными тромбоцитами и позволять проводить молекулярную визуализацию тромбоза в режиме реального времени, например, при инфаркте миокарда , а также отслеживать успех или неудачу фармакологического тромболизиса. [23]
- Рак : раковые клетки также экспрессируют определенный набор рецепторов, в основном рецепторы, которые стимулируют ангиогенез или рост новых кровеносных сосудов. Если на микропузырьки воздействуют лиганды, которые связывают рецепторы, такие как VEGF или активированный гликопротеин IIb/IIIa , они могут неинвазивно и специфично идентифицировать области рака. [24]
- Доставка генов : векторную ДНК можно конъюгировать с микропузырьками. На микропузырьки можно воздействовать с помощью лигандов, которые связываются с рецепторами, экспрессируемыми интересующим типом клеток. Когда целевой микропузырек накапливается на поверхности клетки вместе с полезной нагрузкой ДНК, можно использовать ультразвук, чтобы лопнуть микропузырьк. Сила, связанная с разрывом, может временно сделать проницаемыми окружающие ткани и позволить ДНК более легко проникнуть в клетки. Направленные тераностические микропузырьки (направленные на VCAM-1 ) использовались для доставки миР126 в доклинических условиях, чтобы остановить развитие ААА in vivo. [25]
- Доставка лекарств : лекарства могут быть включены в липидную оболочку микропузырька. Большой размер микропузырьков по сравнению с другими средствами доставки лекарств, такими как липосомы, может позволить доставить большее количество лекарства на одно средство. Направляя загруженный лекарством микропузырек лигандами, которые связываются с определенным типом клеток, микропузырьки не только будут доставлять лекарство конкретно, но также могут обеспечить подтверждение того, что лекарство доставлено, если область визуализируется с помощью ультразвука. [26] Доставка лекарств под контролем ультразвука успешно применяется при лечении рака поджелудочной железы . [27] [28]
Преимущества
[ редактировать ]Помимо сильных сторон, упомянутых в статье о медицинской сонографии , ультразвук с контрастным усилением добавляет следующие дополнительные преимущества:
- Тело на 73% состоит из воды и, следовательно, акустически однородно. Кровь и окружающие ткани имеют одинаковую эхогенность, поэтому с помощью традиционного ультразвука также трудно четко определить степень кровотока, перфузии или границу раздела между тканью и кровью. [4]
- Ультразвуковая визуализация позволяет оценить кровоток в режиме реального времени. [29]
- Разрушение микропузырьков ультразвуком [30] в плоскости изображения позволяет провести абсолютную количественную оценку перфузии тканей. [31]
- Ультразвуковая молекулярная визуализация безопаснее, чем методы молекулярной визуализации, такие как радионуклидная визуализация, поскольку она не требует облучения. [29]
- Альтернативные методы молекулярной визуализации, такие как МРТ , ПЭТ и ОФЭКТ, очень дороги. Ультразвук, с другой стороны, очень экономически эффективен и широко доступен. [12]
- Поскольку микропузырьки могут генерировать такие сильные сигналы, необходима меньшая внутривенная доза, микрограммы микропузырьков необходимы по сравнению с миллиграммами для других методов молекулярной визуализации, таких как контрастные вещества для МРТ . [12]
- Стратегии нацеливания на микропузырьки универсальны и модульны. Нацеливание на новую область влечет за собой только конъюгацию нового лиганда.
- Активное нацеливание может быть увеличено (улучшенная адгезия микропузырьков) за счет силы акустического излучения . [32] [33] с использованием системы клинической ультразвуковой визуализации в 2D-режиме [34] [35] и 3D-режим. [36]
Недостатки
[ редактировать ]Помимо недостатков, упомянутых в разделе «Медицинская сонография» , УЗИ с контрастным усилением имеет следующие недостатки:
- Микропузырьки не задерживаются в обращении очень долго. У них малое время пребывания в циркуляции, поскольку они либо поглощаются клетками иммунной системы, либо поглощаются печенью или селезенкой , даже когда они покрыты ПЭГ. [12]
- Ультразвук производит больше тепла по мере увеличения частоты, поэтому частоту ультразвука необходимо тщательно контролировать.
- Микропузырьки лопаются при низких частотах ультразвука и при высоких механических индексах (МИ), которые являются мерой отрицательного акустического давления системы ультразвуковой визуализации. Увеличение MI повышает качество изображения, но есть компромиссы с разрушением микропузырьков. Разрушение микропузырьков может вызвать локальные разрывы микроциркуляторных сосудов и гемолиз . [11]
- Нацеливающие лиганды могут быть иммуногенными, поскольку в настоящее время нацеливающие лиганды, используемые в доклинических экспериментах, получены из культуры животных . [11]
- Низкая целевая эффективность адгезии микропузырьков, что означает, что небольшая часть введенных микропузырьков связывается с интересующей областью. [18] Это одна из основных причин, по которой прицельное ультразвуковое исследование с контрастным усилением остается на доклинических стадиях разработки.
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а б Содержимое изначально скопировано с: Хансен, Кристоффер; Нильсен, Майкл; Эвертсен, Кэролайн (2015). «Ультрасонография почек: иллюстрированный обзор» . Диагностика . 6 (1): 2. doi : 10.3390/diagnostics6010002 . ISSN 2075-4418 . ПМЦ 4808817 . ПМИД 26838799 . (CC-BY 4.0)
- ^ Сидху, Пол; Кантисани, Вито; Деганелло, Аннамария; Дитрих, Кристоф; Дюран, Кармина; Франке, Дорис; Харканьи, Золтан; Косиак, Войцех; Миле, Витторио; Нтулия, Айкатерини; Пискунович, Мацей; Селларс, Мария; Гилья, Одд (2016). «Роль ультразвука с контрастным усилением (CEUS) в педиатрической практике: заявление о позиции EFSUMB» . Ultraschall in der Medizin – Европейский журнал ультразвука . 38 (1): 33–43. дои : 10.1055/s-0042-110394 . ISSN 0172-4614 . ПМИД 27414980 .
- ^ Jump up to: а б Маккалок М.; Грессер К.; Моос С.; Одабашян Дж.; Джаспер С.; Беднарц Дж.; Берджесс П.; Карни Д.; Мур В.; Сиск Э.; Вагонер А.; Витт С.; Адамс Д. (2000). «Ультразвуковая контрастная физика: Серия по контрастной эхокардиографии, статья 3». J Am Soc Эхокардиогр . 13 (10): 959–67. дои : 10.1067/mje.2000.107004 . ПМИД 11029724 .
- ^ Jump up to: а б с д и Линднер-младший (2004). «Микропузырьки в медицинской визуализации: текущие применения и будущие направления». Nat Rev Drug Discov . 3 (6): 527–32. дои : 10.1038/nrd1417 . ПМИД 15173842 . S2CID 29807146 .
- ^ Андертон Н., Карлсон К.С., Мацумото Р., Симидзу Р.И., Поортинга А.Т., Кудо Н., Постема М. (2022). «О жесткости четырехсот микропузырьков, стабилизированных по Пикерингу» . Японский журнал прикладной физики . 61 (СГ): СГ8001. Бибкод : 2022JaJAP..61G8001A . дои : 10.35848/1347-4065/ac4adc . S2CID 245915590 .
- ^ Панфилова А., Чен П., ван Слоун Р., Вейкстра Х., Постема М., Миши М. (2021). «Экспериментальная акустическая характеристика эндоскелетного противопузырчатого контрастного вещества: первые результаты» . Медицинская физика . 48 (11): 6765–6780. Бибкод : 2021MedPh..48.6765P . дои : 10.1002/mp.15242 . ПМЦ 9293338 . ПМИД 34580883 .
- ^ «Дефинити- перфлутрен инъекционный, суспензия» . ДейлиМед . 19 августа 2020 г. Проверено 22 октября 2020 г.
- ^ «Светимость ЭПАР» . Европейское агентство лекарственных средств (EMA) . 17 сентября 2018 года . Проверено 22 октября 2020 г.
- ^ «SonoVue, МНН-гексафторид серы - Приложение I - Краткое описание характеристик продукта» (PDF) . Европейское агентство по лекарственным средствам . Проверено 24 февраля 2019 г.
- ^ «Перфлексан: (AF0150, AFO 150, Imagent, Imavist™)» . Лекарства в исследованиях и разработках , Том 3, номер 5, 2002 г., стр. 306–309 (4) . Адис Интернешнл . Проверено 8 марта 2010 г.
- ^ Jump up to: а б с д Клибанов А.Л. (2005). «Газонаполненные микропузырьки, несущие лиганды: контрастные вещества для ультразвукового исследования для целенаправленной молекулярной визуализации». Биоконъюг. Хим . 16 (1): 9–17. дои : 10.1021/bc049898y . ПМИД 15656569 .
- ^ Jump up to: а б с д Клибанов А.Л. (1999). «Направленная доставка газонаполненных микросфер, контрастных веществ для ультразвуковой визуализации». Adv Drug Deliv Rev. 37 (1–3): 139–157. дои : 10.1016/s0169-409x(98)00104-5 . ПМИД 10837732 .
- ^ Шнайдер, М. (ноябрь 1999 г.). «SonoVue, новый контрастный агент для ультразвуковых исследований». Евро. Радиол . 9 (дополнение 3): S347–S348. дои : 10.1007/pl00014071 . ПМИД 10602926 . S2CID 19613214 .
- ^ Рогнин, Н.Г.; Фринкинг, П.; Коста, М.; Ардити, М. (ноябрь 2008 г.). «Количественная оценка перфузии in vivo с помощью контрастного ультразвука: проверка использования линеаризованных видеоданных по сравнению с необработанными радиочастотными данными». 2008 Симпозиум IEEE по ультразвуку . стр. 1690–1693. дои : 10.1109/ULTSYM.2008.0413 . ISBN 978-1-4244-2428-3 . S2CID 45679140 .
- ^ Клодон, М; Дитрих, см.; Чой, Би.; Косгроув, DO; Кудо, М.; Нолсё, CP.; Пискалья, Ф.; Уилсон, старший; Барр, Р.Г.; Чаммас, MC.; Чаубал, штат Нью-Йорк; Чен, Миннесота; Клеверт, округ Колумбия; Корреас, Дж. М.; Дин, Х.; Форсберг, Ф.; Фаулкс, Дж.Б.; Гибсон, штат РН; Гольдберг, BB.; Лассау, Н.; Лин, Эл.; Мэттри, РФ; Мориясу, Ф.; Солбиати, Л.; Уэскотт, HP.; Сюй, HX (февраль 2013 г.). «Руководство и рекомендации по надлежащей клинической практике для ультразвукового исследования с контрастным усилением (CEUS) в обновлении печени 2012: инициатива WFUMB-EFSUMB в сотрудничестве с представителями AFSUMB, AIUM, ASUM, FLAUS и ICUS» . УЗИ Мед Биол . 39 (2): 187–210. doi : 10.1016/j.ultrasmedbio.2012.09.002 . hdl : 11585/144895 . ПМИД 23137926 . S2CID 2224370 .
- ^ Рогнин, Н.Г.; Ардити, М.; Мерсье, Л.; Фринкинг, PJA; Шнайдер, М.; Перрену, Г.; Анай, А.; Мьюули, Дж.; Транквар, Ф. (ноябрь 2010 г.). «Параметрическая визуализация для характеристики очаговых поражений печени при ультразвуковом исследовании с контрастным усилением». Транзакции IEEE по ультразвуку, сегнетоэлектрике и контролю частоты . 57 (11): 2503–2511. дои : 10.1109/TUFFC.2010.1716 . ПМИД 21041137 . S2CID 19339331 .
- ^ Анай, А; Перрено, Ж.; Рогнин Н.; Ардити, М.; Мерсье, Л.; Фринкинг, П.; Руффье, К.; Питернс, П.; Меули, Р.; Мьюули, Дж.Й. (октябрь 2011 г.). «Дифференциация очаговых поражений печени: полезность параметрической визуализации с УЗИ с контрастным усилением». Радиология . 261 (1): 300–310. дои : 10.1148/радиол.11101866 . ПМИД 21746815 .
- ^ Jump up to: а б Такалкар А.М.; Клибанов А.Л.; Рычак Ю.Ю.; Линднер-младший; Лей К. (2004). «Динамика связывания и отделения микропузырьков, нацеленных на P-селектин, в условиях контролируемого сдвигового потока». Дж. Контроль. Выпускать . 96 (3): 473–482. дои : 10.1016/j.jconrel.2004.03.002 . ПМИД 15120903 .
- ^ Эниола АО; Уиллкокс П.Дж.; Хаммер Д.А. (2003). «Взаимодействие между перекатыванием и прочной адгезией выяснено с помощью бесклеточной системы, созданной с двумя отдельными парами рецептор-лиганд» . Биофиз. Дж . 85 (4): 2720–31. Бибкод : 2003BpJ....85.2720E . дои : 10.1016/s0006-3495(03)74695-5 . ПМК 1303496 . ПМИД 14507735 .
- ^ Эниола АО; Хаммер Д.А. (2005). «Характеристика in vitro миметика лейкоцитов для нацеливания терапевтических средств на эндотелий с использованием двух рецепторов». Биоматериалы . 26 (34): 7136–44. doi : 10.1016/j.bimaterials.2005.05.005 . ПМИД 15953632 .
- ^ Веллер Дж. Э.; Вильянуэва ФС; Том ЭМ; Вагнер В.Р. (2005). «Таргетные контрастные вещества для ультразвука: оценка эндотелиальной дисфункции in vitro и множественное нацеливание на ICAM-1 и сиалил Льюиса (x)». Биотехнология. Биоинж . 92 (6): 780–8. дои : 10.1002/бит.20625 . ПМИД 16121392 .
- ^ Рычак Дж. Дж., А. Л. Клибанов, В. Ян, Б. Ли, С. Актон, А. Леппанен, Р. Д. Каммингс и К. Лей. «Усиленная адгезия микропузырьков к P-селектину с помощью физиологически настроенного нацеливающего лиганда», 10-й симпозиум по исследованию ультразвукового контраста в радиологии, Сан-Диего, Калифорния, март 2005 г.
- ^ Ван, X; Хагемейер, CE; Хоманн, доктор медицинских наук; Лейтнер, Э; Армстронг, ПК; Цзя, Ф; Ольщевский, М; Иглы, А; Питер, К; Инго, А. (июнь 2012 г.). «Новые микропузырьки, нацеленные на одноцепочечные антитела, для молекулярной ультразвуковой визуализации тромбозов: валидация уникального неинвазивного метода быстрого и чувствительного обнаружения тромбов и мониторинга успеха или неудачи тромболизиса у мышей» . Тираж . 125 (25): 3117–3126. doi : 10.1161/CIRCULATIONAHA.111.030312 . ПМИД 22647975 .
- ^ Яп, МЛ; Макфадьен, доктор юридических наук; Ван, X; Хоманн, доктор медицинских наук; Зиглер, М; Яо, Ю; Фам, А; Харрис, М; Доннелли, PS; Хогарт, премьер-министр; Питерс, Джорджия; Лим, Б; Питер, К. (июнь 2017 г.). «Нацеливание на активированные тромбоциты: уникальный и потенциально универсальный подход к визуализации рака» . Тераностика . 7 (10): 2565–2574. дои : 10.7150/thno.19900 . ПМЦ 5558553 . ПМИД 28819447 .
- ^ Ван, X; Сирл, АК; Хоманн, доктор медицинских наук; Лю, АО; Авраам, МК; Паласубраманиам, Дж; Лим, Б; Яо, Ю; Уоллерт, М; Ю, Е; Чен, ЮК; Питер, К. (апрель 2018 г.). «Двунаправленная тераностическая доставка миР останавливает развитие аневризмы брюшной аорты» . Молекулярная терапия . 25 (4): 1056–1065. дои : 10.1016/j.ymthe.2018.02.010 . ПМК 6080135 . ПМИД 2952574 .
- ^ Ван, X; Гканатсас, Ю; Паласубраманиам, Дж; Хоманн, доктор медицинских наук; Чен, ЮК; Лим, Б; Хагемейер, CE; Питер, К. (март 2016 г.). «Тераностические микропузырьки, нацеленные на тромб: новая технология одновременной быстрой ультразвуковой диагностики и бескровного фибринолитического лечения тромбозов» . Тераностика . 6 (5): 726–738. дои : 10.7150/thno.14514 . ПМЦ 4805666 . ПМИД 27022419 .
- ^ Димчевски Г., Котопоулис С., Бьонес Т., Хоем Д., Шётт Дж., Йерцен Б.Т., Бирманн М., Молвен А., Сорби Х., Мак Кормак Е., Постема М., Гилья ОХ (2016). «Клиническое испытание на людях с использованием ультразвука и микропузырьков для улучшения лечения гемцитабином неоперабельного рака поджелудочной железы» . Журнал контролируемого выпуска . 243 : 172–181. дои : 10.1016/j.jconrel.2016.10.007 . HDL : 1956/16668 . ПМИД 27744037 .
- ^ Сёрейде К., Штеттнер С. (2021 г.). Сёрейде К., Штеттнер С. (ред.). Учебник «Рак поджелудочной железы: принципы и практика хирургической онкологии» . Гейдельберг: Спрингер. дои : 10.1007/978-3-030-53786-9 . ISBN 978-3-030-53786-9 . S2CID 231793989 .
- ^ Jump up to: а б Lindner, J.R., A.L. Klibanov, and K. Ley. Targeting inflammation, In: Biomedical aspects of drug targeting. (Muzykantov, V.R., Torchilin, V.P. , eds.) Kluwer, Boston, 2002; pp. 149–172.
- ^ Вэй, К; Джаявира, Арканзас; Фирузан, С; Линка, А; Скиба, ДМ; Каул, С. (февраль 1998 г.). «Количественная оценка кровотока в миокарде при ультразвуковом разрушении микропузырьков, вводимых в виде постоянной венозной инфузии» . Тираж . 97 (5): 473–483. дои : 10.1161/01.cir.97.5.473 . ПМИД 9490243 .
- ^ Ардити, М; Фринкинг, PJA.; Чжоу, X.; Рогнин, Н.Г. (июнь 2006 г.). «Новый формализм количественной оценки тканевой перфузии методом разрушения-восполнения при контрастной ультразвуковой визуализации». Транзакции IEEE по ультразвуку, сегнетоэлектрике и контролю частоты . 53 (6): 1118–1129. дои : 10.1109/TUFFC.2006.1642510 . ПМИД 16846144 . S2CID 6328131 .
- ^ Рычак, Джей Джей; Клибанов А.Л.; Хоссак, Дж. А. (март 2005 г.). «Сила акустического излучения усиливает целенаправленную доставку микропузырьков с ультразвуковым контрастом: проверка in vitro». Транзакции IEEE по ультразвуку, сегнетоэлектрике и контролю частоты . 52 (3): 421–433. дои : 10.1109/TUFFC.2005.1417264 . ПМИД 15857050 . S2CID 25032596 .
- ^ Дейтон, П; Клибанов А; Бранденбургер, Г; Феррара, К. (октябрь 1999 г.). «Сила акустического излучения in vivo: механизм, помогающий нацеливаться на микропузырьки» . УЗИ Мед Биол . 25 (8): 1195–1201. дои : 10.1016/s0301-5629(99)00062-9 . ПМИД 10576262 .
- ^ Фринкинг, Пи Джей; Тарди, я; Тераулаз, М; Ардити, М; Пауэрс, Дж; Почон, С; Транквар, Ф (август 2012 г.). «Влияние силы акустического излучения на эффективность связывания BR55, VEGFR2-специфического ультразвукового контрастного вещества» . УЗИ Мед Биол . 38 (8): 1460–1469. doi : 10.1016/j.ultrasmedbio.2012.03.018 . ПМИД 22579540 .
- ^ Гесснер, Р.К.; Стритер, Дж. Э.; Котадия, Р; Фейнгольд, С; Дейтон, Пенсильвания (апрель 2012 г.). «Подтверждение in vivo применения силы акустического излучения для повышения диагностической полезности молекулярной визуализации с использованием трехмерного ультразвука» . УЗИ Мед Биол . 38 (4): 651–660. doi : 10.1016/j.ultrasmedbio.2011.12.005 . ПМЦ 3355521 . ПМИД 22341052 .
- ^ Рогнин, Н.Г.; Унникришнан, С.; Клибанов, АЛ. (сентябрь 2013 г.). «Улучшение молекулярной ультразвуковой визуализации с помощью силы объемного акустического излучения (VARF): доклиническая проверка in vivo на мышиной модели опухоли» . Тезисы докладов Всемирного конгресса молекулярной визуализации 2013 г. Архивировано из оригинала 11 октября 2013 г.