Соединения серы
Соединения серы — это химические соединения, образующие элемент серу (S). Обычные степени окисления серы варьируются от -2 до +6. Сера образует устойчивые соединения со всеми элементами, кроме благородных газов .
Реакции переноса электрона
[ редактировать ]
3 )
Поликатионы серы, S 8 2+ , С 4 2+ и С 16 2+ образуются при взаимодействии серы с окислителями в сильнокислом растворе. [1] О окрашенных растворах, получаемых при растворении серы в олеуме , впервые сообщил еще в 1804 году К. Ф. Бухольц, но причина окраски и структура поликатионов были установлены только в конце 1960-х годов. С 8 2+ темно-синий, S 4 2+ желтый и S 16 2+ красный. [2]
Восстановление серы дает различные полисульфиды формулы S x 2- , многие из которых были получены в кристаллической форме. Показательным является производство тетрасульфида натрия:
- 4 Na + S 8 → 2 Na 2 S 4
Некоторые из этих дианионов диссоциируют с образованием анионов-радикалов , таких как S 3 − придает синий цвет камню лазурит .

Эта реакция подчеркивает отличительное свойство серы: ее способность к катенации (связыванию между собой путем образования цепей). Протонирование этих полисульфид-анионов приводит к образованию полисульфанов H 2 S x, где x = 2, 3 и 4. [4] В конечном итоге при восстановлении серы образуются сульфидные соли:
- 16 Na + S 8 → 8 Na 2 S
Взаимное превращение этих видов используется в натриево-серной батарее .
Сероводород
[ редактировать ]Обработка серы водородом дает сероводород . При растворении в воде сероводород имеет слабокислую реакцию: [5]
- Ч 2 С ⇌ ВС − + Ч +
Газообразный сероводород и гидросульфид-анион чрезвычайно токсичны для млекопитающих из-за ингибирования способности гемоглобина переносить кислород и некоторых цитохромов аналогично цианиду и азиду .
Оксиды
[ редактировать ]Два основных оксида серы получаются путем сжигания серы:
- S + O 2 → SO 2 ( диоксид серы )
- 2 SO 2 + O 2 → 2 SO 3 ( триоксид серы )
Наблюдаются многие другие оксиды серы, включая оксиды с высоким содержанием серы , включая монооксид серы, монооксид дисеры, диоксиды дисеры и высшие оксиды , содержащие пероксогруппы.
Галогениды
[ редактировать ]Сера реагирует с фтором с образованием высокореактивного тетрафторида серы и высокоинертного гексафторида серы . [6] В то время как фтор дает соединения S(IV) и S(VI), хлор дает производные S(II) и S(I). Так, в результате хлорирования серы возникают дихлорид серы , дихлорид дисеры и высшие хлорсульфаны. Сульфурилхлорид и хлорсерная кислота являются производными серной кислоты; Тионилхлорид (SOCl 2 ) — распространенный реагент в органическом синтезе . [7]
Псевдогалогениды
[ редактировать ]Сера окисляет цианид и сульфит с образованием тиоцианата и тиосульфата соответственно.
Сульфиды металлов
[ редактировать ]Сера реагирует со многими металлами. Электроположительные металлы дают полисульфидные соли. Медь , цинк и серебро тускнеют от серы. Хотя известно множество сульфидов металлов , большинство из них получаются в результате высокотемпературных реакций элементов. [8] Сульфидные минералы содержат сульфид ( S 2- ) или дисульфид (S 2 2- ) анионы. Типичные примеры:
- Акантит Аг 2 С
- Халькоцит Cu 2 S
- Галенит ПбС
- Сфалерит ZnS
- Халькопирит CuFeS 2
- Миллерит НиС
- Киноварь HgS
- Стибнит Sb2SСб2С3
- Пирит ФеС 2
- Молибденит МоС 2
Органические соединения
[ редактировать ]- Иллюстративные сероорганические соединения
- Аллицин , химическое соединение в чесноке.
- ( R ) -цистеин , аминокислота, содержащая тиоловую группу.
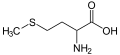
- Метионин — аминокислота , содержащая тиоэфир.
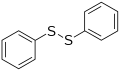
- Дифенилдисульфид , представитель дисульфида.
- Перфтороктансульфоновая кислота , поверхностно-активное вещество.
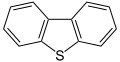
- Дибензотиофен , компонент сырой нефти.
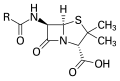
- Пенициллин , антибиотик, где «R» — переменная группа.
Некоторые из основных классов серосодержащих органических соединений включают следующие: [9]
- Тиолы или меркаптаны (названные так потому, что они улавливают ртуть в качестве хелаторов ) являются серными аналогами спиртов ; обработка тиолов основанием дает тиолат- ионы.
- Тиоэфиры — серосодержащие аналоги простых эфиров .
- Ионы сульфония имеют три группы, присоединенные к катионному серному центру. Диметилсульфониопропионат (ДМСП) является одним из таких соединений, играющих важную роль в цикле морской органической серы .
- Сульфоксиды и сульфоны представляют собой тиоэфиры с одним и двумя атомами кислорода, присоединенными к атому серы соответственно. Самый простой сульфоксид, диметилсульфоксид , является распространенным растворителем; обычный сульфон — сульфолан .
- Сульфоновые кислоты используются во многих моющих средствах.
Соединения с кратными связями углерод-сера встречаются редко, исключением является сероуглерод — летучая бесцветная жидкость, структурно похожая на диоксид углерода. Его используют в качестве реагента для получения полимерного вискозы и многих сероорганических соединений. В отличие от угарного газа , моносульфид углерода стабилен только в виде чрезвычайно разбавленного газа, встречающегося между солнечными системами. [10]
Сероорганические соединения ответственны за некоторые неприятные запахи разлагающихся органических веществ. Они широко известны как одорант бытового природного газа, запах чеснока и спрей от скунса. Не все органические соединения серы пахнут неприятно при любых концентрациях: серосодержащий монотерпеноид ( меркаптан грейпфрута ) в небольших концентрациях имеет характерный запах грейпфрута, но в более высоких концентрациях имеет характерный тиоловый запах. Сернистый иприт , сильнодействующее нарывное вещество , использовался во время Первой мировой войны как обездвиживающее средство. [11]
Связи сера-сера представляют собой структурный компонент, используемый для придания жесткости резине, подобно дисульфидным мостикам, которые придают жесткость белкам (см. биологические характеристики ниже). В наиболее распространенном типе промышленного «отверждения» или отверждения и упрочнения натурального каучука элементарная сера нагревается вместе с каучуком до такой степени, что химические реакции образуют дисульфидные мостики между изопреновыми звеньями полимера. Этот процесс, запатентованный в 1843 году, сделал каучук основным промышленным продуктом, особенно в автомобильных шинах. Из-за высокой температуры и серы процесс был назван вулканизацией , в честь римского бога кузницы и вулканизма .
См. также
[ редактировать ]- Категория:Соединения серы
- Кислородные соединения
- Соединения селена
- Соединения фосфора
- Соединения хлора
Ссылки
[ редактировать ]- ^ Шрайвер, Аткинс. Неорганическая химия, пятое издание. WH Freeman and Company, Нью-Йорк, 2010 г.; стр. 416
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . стр. 645–665. ISBN 978-0-08-037941-8 .
- ^ Фухимори, Тошихико; Морелос-Гомес, Аарон; Чжу, Чжэнь; Мурамацу, Хироюки; Футамура, Рюсуке; Урита, Коки; Терронес, Маурисио; Хаяси, Такуя; Эндо, Моринобу; Янг Хонг, Санг; Чул Чой, Янг; Томанек, Дэвид; Канеко, Кацуми (2013). «Проведение линейных цепочек серы внутри углеродных нанотрубок» . Природные коммуникации . 4 : 2162. Бибкод : 2013NatCo...4.2162F . дои : 10.1038/ncomms3162 . ПМЦ 3717502 . ПМИД 23851903 .
- ^ Справочник по препаративной неорганической химии, 2-е изд. Под редакцией Г. Брауэра, Academic Press, 1963, Нью-Йорк. Том. 1. п. 421.
- ^ Гринвуд, Нью-Йорк; и Эрншоу, А. (1997). Химия элементов (2-е изд.), Оксфорд: Баттерворт-Хайнеманн. ISBN 0-7506-3365-4 .
- ^ Гашек, WR (1961). «1,1,1-Трифторгептан». Органические синтезы . 41 : 104. дои : 10.1002/0471264180.os041.28 .
- ^ Рутенберг, М.В.; Хорнинг, ЕС (1950). «1-Метил-3-этилоксиндол». Органические синтезы . 30:62 . дои : 10.15227/orgsyn.030.0062 .
- ^ Воган, Дэвид Дж.; Крейг, Джеймс Р. (1978). Минеральная химия сульфидов металлов . Кембриджская серия по наукам о Земле. Кембридж, Лондон, Нью-Йорк [и т. д.]: Издательство Кембриджского университета. ISBN 978-0-521-21489-6 .
- ^ Кремлин Р.Дж. (1996). Введение в сероорганическую химию . Чичестер: Джон Уайли и сыновья. ISBN 0-471-95512-4 .
- ^ Уилсон, RW ; Пензиас, АА ; Ваннье, П.Г.; Линке, РА (15 марта 1976 г.). «Содержание изотопов в межзвездном моносульфиде углерода» . Астрофизический журнал . 204 : Л135–Л137. Бибкод : 1976ApJ...204L.135W . дои : 10.1086/182072 .
- ^ Бануб, Джозеф (2011). Обнаружение биологических агентов для предотвращения биотерроризма . Наука НАТО ради мира и безопасности. Серия A: Химия и биология. п. 183. Бибкод : 2011dbap.book.....B . дои : 10.1007/978-90-481-9815-3 . ISBN 978-90-481-9815-3 . OCLC 697506461 .