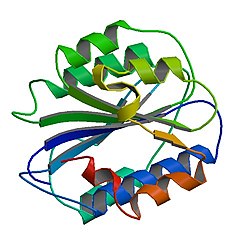
фактор фон Виллебранда
| ФВФ | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | VWF , F8VWD, фактор Виллебранда | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | ОМИМ : 613160 ; МГИ : 98941 ; Гомологен : 466 ; GeneCards : VWF ; ОМА : VWF – ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
Фактор фон Виллебранда ( VWF ) ( Немецкий: [fɔn ˈvɪləbʁant] ) — крови гликопротеин , который способствует гемостазу , в частности, тромбоцитов адгезии . Он недостаточен и/или дефектен при болезни фон Виллебранда и участвует во многих других заболеваниях, включая тромботическую тромбоцитопеническую пурпуру , синдром Хейде и, возможно, гемолитико-уремический синдром . [5] Предполагается, что повышенные уровни в плазме при многих сердечно-сосудистых, неопластических, метаболических (например, диабете) заболеваниях и заболеваниях соединительной ткани возникают в результате неблагоприятных изменений эндотелия и могут предсказать повышенный риск тромбоза . [6]
Биохимия [ править ]
Синтез [ править ]
ФВ — крупный мультимерный гликопротеин , присутствующий в плазме крови и конститутивно продуцируемый в виде сверхкрупного ФВ в эндотелии (в тельцах Вейбеля-Паладе ), мегакариоцитах (α-гранулах тромбоцитов ) и субэндотелиальной соединительной ткани . [5]
Структура [ править ]
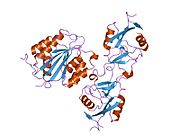
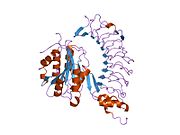
Основным мономером ФВ является белок, состоящий из 2050 аминокислот . Каждый мономер содержит ряд определенных доменов с определенной функцией; заслуживающие внимания элементы: [5]
- домен D'/D3, который связывается с фактором VIII ( домен типа D фактора Виллебранда ). [7]
- домен A1, который связывается с:
- тромбоцитов GPIb-рецептор
- гепарин
- возможно, коллаген
- домен А2, который должен частично развернуться, чтобы обнажить скрытый сайт расщепления для специфической протеазы ADAMTS13 , которая инактивирует VWF, образуя мультимеры гораздо меньшего размера. На частичное разворачивание влияет сдвиговый поток в крови, связывание кальция и комок соседнего с последовательностью «вицинального дисульфида» на С-конце А2-домена. [8] [9]
- Домен А3, который связывается с коллагеном ( домен фактора Виллебранда типа А )
- домен C4, в котором мотив RGD связывается с интегрином тромбоцитов α IIb β 3, когда он активируется ( домен фактора фон Виллебранда типа C )
- другие домены C, которые могут взаимодействовать в димерах ER: более крупный белок показывает шесть шариков (C и C-подобных) доменов под крио-ЭМ . [7]
- домен « цистинового узла » (на С-конце белка), который VWF разделяет с тромбоцитарным фактором роста (PDGF), трансформирующим фактором роста -β (TGFβ) и β- хорионическим гонадотропином человека (βHCG, гормона беременности). тестовая слава). ( домен типа C фактора фон Виллебранда )
Мономеры впоследствии N-гликозилируются , организуются в димеры в эндоплазматическом ретикулуме и в мультимеры в аппарате Гольджи путем сшивания остатков цистеина через дисульфидные связи . Что касается гликозилирования, VWF является одним из немногих белков, несущих антигены системы групп крови АВО . [5] Факторы Виллебранда, выходящие из аппарата Гольджи, упаковываются в запасающие органеллы, тельца Вейбеля-Палада (WPB) в эндотелиальных клетках и α-гранулы в тромбоцитах. [10]
Мультимеры VWF могут быть чрезвычайно большими, >20 000 кДа , и состоять из более чем 80 субъединиц по 250 кДа каждая. Функциональны только крупные мультимеры. Некоторые продукты расщепления, образующиеся в результате продукции VWF, также секретируются, но, вероятно, не несут никакой функции. [5]

Функция [ править ]

Основная функция фактора фон Виллебранда — связывание с другими белками, в частности с фактором VIII , и он важен для адгезии тромбоцитов к местам ран. [5] Он не является ферментом и, следовательно, не обладает каталитической активностью.
VWF связывается с рядом клеток и молекул. Наиболее важные из них: [5]
- Фактор VIII связан с VWF, пока неактивен в обращении; фактор VIII быстро деградирует, если не связан с VWF. Фактор VIII высвобождается из ФВ под действием тромбина . В отсутствие ФВ фактор VIII имеет период полураспада 1–2 часа; при переносе интактным фактором ФВ период полувыведения фактора VIII составляет 8–12 часов.
- ФВ связывается с коллагеном, например, когда коллаген оказывается под эндотелиальными клетками из-за повреждения кровеносного сосуда. Эндотелий также высвобождает фактор Виллебранда, который образует дополнительные связи между гликопротеином Ib/IX/V тромбоцитов и фибриллами коллагена.
- VWF связывается с GpIb тромбоцитов , когда он образует комплекс с gpIX и gpV ; это связывание происходит при любых обстоятельствах, но наиболее эффективно при высоком напряжении сдвига (т.е. при быстром кровотоке в узких кровеносных сосудах, см. ниже).
- Фактор Виллебранда связывается с другими рецепторами тромбоцитов, когда они активируются, например, тромбином (т.е. когда стимулируется коагуляция).
Фактор Виллебранда играет важную роль в свертывании крови. кровотока Таким образом, дефицит или дисфункция ФВ (болезнь фон Виллебранда) приводит к склонности к кровотечениям, которая наиболее выражена в тканях, имеющих высокий сдвиг в узких сосудах. Исследования показывают, что в этих обстоятельствах ФВ разворачивается, замедляя прохождение тромбоцитов. [5] Недавние исследования также показывают, что фактор фон Виллебранда участвует в формировании самих кровеносных сосудов , что может объяснить, почему у некоторых людей с болезнью фон Виллебранда развиваются сосудистые пороки развития (преимущественно в пищеварительном тракте ), которые могут вызывать обильное кровотечение . [11]
Катаболизм [ править ]
Биологическое расщепление ( ) опосредовано ферментом ADAMTS13 (аббревиатура от « металлопротеаза катаболизм и с мотивом дисинтегриноподобная тромбоспондина 1 VWF в значительной степени типа № 13 »). Это металлопротеиназа , которая расщепляет VWF между тирозином в положении 842 и метионином в положении 843 (или 1605–1606 гена) в домене А2. Это расщепляет мультимеры на более мелкие единицы, которые разлагаются другими пептидазами . [12]
Период полувыведения фактора Виллебранда из плазмы человека составляет около 16 часов; Вариации гликозилирования молекул фактора Виллебранда у разных людей приводят к более широкому диапазону от 4,2 до 26 часов. Клетки печени, а также макрофаги поглощают vWF для выведения через ASGPR и LRP1 . SIGLEC5 и CLEC4M также распознают vWF. [10]
в болезни Роль
Наследственные или приобретенные дефекты ФВ приводят к болезни фон Виллебранда (БВ) — кровоточащему диатезу кожи и слизистых оболочек, вызывающему носовые кровотечения , меноррагии и желудочно-кишечные кровотечения . Точка возникновения мутации определяет тяжесть геморрагического диатеза. Существует три типа (I, II и III), а тип II подразделяется на несколько подтипов. Лечение зависит от характера нарушения и тяжести симптомов. [13] Большинство случаев фВБ являются наследственными, но аномалии ФВ могут быть приобретенными; стеноз аортального клапана , например, связан с болезнью Виллебранда IIA типа, вызывающей желудочно-кишечное кровотечение – связь, известную как синдром Хейде . [14]
При тромботической тромбоцитопенической пурпуре (ТТП) и гемолитико-уремическом синдроме (ГУС) ADAMTS13 либо недостает, либо ингибируется антителами, направленными к этому ферменту. Это приводит к уменьшению распада сверхкрупных мультимеров ФВ и микроангиопатической гемолитической анемии с отложением фибрина и тромбоцитов в мелких сосудах и некрозу капилляров. При ТТП наиболее явно поражаемым органом является мозг; при ГУС — почки. [15]
перенесших ишемический инсульт (из-за свертывания крови). Более высокие уровни VWF чаще встречаются среди людей, впервые [16] человека ADAMTS13 не влияет на возникновение заболевания, и единственным значимым генетическим фактором является группа крови . Было обнаружено, что высокие уровни VWF в плазме являются независимым предиктором сильного кровотечения у пациентов с фибрилляцией предсердий, получающих антикоагулянты . [17] ФВ является маркером эндотелиальной дисфункции и постоянно повышается при фибрилляции предсердий, что связано с неблагоприятными исходами. [18]
История [ править ]
VWF назван в честь Эрика Адольфа фон Виллебранда , финского врача, который в 1926 году впервые описал наследственное нарушение свертываемости крови в семьях с Аландских островов . Хотя фон Виллебранд не определил точную причину, он отличал болезнь фон Виллебранда (БВВ) от гемофилии и других форм геморрагического диатеза . [19]
В 1950-х годах было показано, что фВБ вызван дефицитом фактора плазмы (а не расстройствами тромбоцитов), а в 1970-х годах был очищен белок ФВ. [5] Харви Дж. Вайс [20] и его коллеги разработали количественный анализ функции ФВ, который остается основой лабораторных исследований.оценка БВ по сей день. [21]
Взаимодействие [ править ]
Было показано, что фактор фон Виллебранда взаимодействует с коллагеном типа I, альфа 1 . [22]
Недавно сообщалось, что сотрудничество и взаимодействие факторов фон Виллебранда повышают вероятность адсорбции при первичном гемостазе. Такое сотрудничество доказывается расчетом вероятности адсорбции протекающего ФВ при его пересечении с другим адсорбированным. Такое взаимодействие осуществляется в широком диапазоне скоростей сдвига. [23]
См. также [ править ]
Ссылки [ править ]
- ↑ Перейти обратно: Перейти обратно: а б с GRCh38: Версия Ensembl 89: ENSG00000110799 – Ensembl , май 2017 г.
- ↑ Перейти обратно: Перейти обратно: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000001930 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ↑ Перейти обратно: Перейти обратно: а б с д и ж г час я Сэдлер Дж. Э. (1998). «Биохимия и генетика фактора фон Виллебранда» . Ежегодный обзор биохимии . 67 : 395–424. doi : 10.1146/annurev.biochem.67.1.395 . ПМИД 9759493 .
- ^ Шахиди М (2017). «Тромбоз и фактор Виллебранда». Тромбоз и эмболия: от исследований к клинической практике . Достижения экспериментальной медицины и биологии. Том. 906. стр. 285–306. дои : 10.1007/5584_2016_122 . ISBN 978-3-319-22107-6 . ПМИД 27628010 .
- ↑ Перейти обратно: Перейти обратно: а б Чжоу Ю.Ф., Энг Э.Т., Чжу Дж., Лу С., Уолц Т., Спрингер Т.А. (июль 2012 г.). «Последовательность и структурные отношения внутри фактора фон Виллебранда» . Кровь . 120 (2): 449–458. doi : 10.1182/blood-2012-01-405134 . ПМЦ 3398765 . ПМИД 22490677 .
- ^ Якоби А.Дж., Машаги А., Танс С.Дж., Хейзинга Э.Г. (июль 2011 г.). «Кальций модулирует восприятие силы с помощью домена фактора А2 фон Виллебранда» . Природные коммуникации . 2 : 385. Бибкод : 2011NatCo...2..385J . дои : 10.1038/ncomms1385 . ПМК 3144584 . ПМИД 21750539 .
- ^ Люкен Б.М., Винн Л.И., Эмсли Дж., Лейн Д.А., Кроули Дж.Т. (июнь 2010 г.). «Важность вицинальных цистеинов C1669 и C1670 для функции домена фактора А2 фон Виллебранда» . Кровь . 115 (23): 4910–4913. дои : 10.1182/кровь-2009-12-257949 . ПМК 2890177 . ПМИД 20354169 .
- ↑ Перейти обратно: Перейти обратно: а б Лентинг П.Дж., Кристоф О.Д., Денис К.В. (март 2015 г.). «Биосинтез, секреция и клиренс фактора фон Виллебранда: соединение дальних концов» . Кровь . 125 (13): 2019–2028. дои : 10.1182/blood-2014-06-528406 . ПМИД 25712991 . S2CID 27785232 .
- ^ Рэнди А.М., Лаффан М.А. (январь 2017 г.). «Фактор фон Виллебранда и ангиогенез: фундаментальные и прикладные вопросы» . Журнал тромбозов и гемостаза . 15 (1): 13–20. дои : 10.1111/jth.13551 . hdl : 10044/1/42796 . ПМИД 27778439 . S2CID 3490036 .
- ^ Леви Г.Г., Мотто Д.Г., Гинзбург Д. (июль 2005 г.). «ADAMTS13 исполняется 3 года» . Кровь . 106 (1): 11–17. дои : 10.1182/кровь-2004-10-4097 . ПМИД 15774620 . S2CID 25645477 .
- ^ Сэдлер Дж.Э., Бадде Ю., Эйкенбум Дж.К., Фавалоро Э.Дж., Хилл Ф.Г., Холмберг Л. и др. (октябрь 2006 г.). «Обновленная информация о патофизиологии и классификации болезни фон Виллебранда: отчет Подкомитета по фактору фон Виллебранда». Журнал тромбозов и гемостаза . 4 (10): 2103–2114. дои : 10.1111/j.1538-7836.2006.02146.x . ПМИД 16889557 . S2CID 23875096 .
- ^ Винсентелли А., Сьюзен С., Ле Турно Т., Сикс И., Фабр О., Жютье Ф. и др. (июль 2003 г.). «Приобретенный синдром фон Виллебранда при аортальном стенозе» . Медицинский журнал Новой Англии . 349 (4): 343–349. doi : 10.1056/NEJMoa022831 . ПМИД 12878741 .
- ^ Моак Дж.Л. (январь 2004 г.). «Фактор фон Виллебранда, ADAMTS-13 и тромботическая тромбоцитопеническая пурпура». Семинары по гематологии . 41 (1): 4–14. doi : 10.1053/j.seminhematol.2003.10.003 . ПМИД 14727254 .
- ^ Денорм Ф, Де Мейер СФ (сентябрь 2016 г.). «Ось VWF-GPIb при ишемическом инсульте: уроки моделей на животных». Тромбоз и гемостаз . 116 (4): 597–604. дои : 10.1160/TH16-01-0036 . ПМИД 27029413 . S2CID 4964177 .
- ^ Ролдан В., Марин Ф., Муинья Б., Торрегроса Х.М., Эрнандес-Ромеро Д., Вальдес М. и др. (июнь 2011 г.). «Уровни фактора фон Виллебранда в плазме являются независимым фактором риска неблагоприятных событий, включая смертность и сильное кровотечение у пациентов с фибрилляцией предсердий, получающих антикоагулянты» . Журнал Американского колледжа кардиологов . 57 (25): 2496–2504. дои : 10.1016/j.jacc.2010.12.033 . ПМИД 21497043 .
- ^ Хан А.А., Томас Г.Н., Лип Г., Шанцила А. (2020). «Эндотелиальная функция у больных мерцательной аритмией» . Анналы медицины . 52 (1–2): 1–11. дои : 10.1080/07853890.2019.1711158 . ПМЦ 7877921 . ПМИД 31903788 .
- ^ фон Виллебранд Э.А. (1926). «Наследственная псевдогемофилия» [Наследственная псевдогемофилия]. Fin Läkaresällsk Handl (на шведском языке). 68 : 87–112. Воспроизведено в Фон Виллебранд Э.А. (май 1999 г.). «Наследственная псевдогемофилия». Гемофилия . 5 (3): 223–31, обсуждение 222. doi : 10.1046/j.1365-2516.1999.00302.x . ПМИД 10444294 . S2CID 221750622 .
- ^ Вайс Х.Дж., Хойер И.В. (декабрь 1973 г.). «Фактор фон Виллебранда: диссоциация от прокоагулянтной активности антигемофильного фактора». Наука . 182 (4117): 1149–1151. Бибкод : 1973Sci...182.1149W . дои : 10.1126/science.182.4117.1149 . ПМИД 4127287 . S2CID 41340436 .
- ^ Вайс Х.Дж., Роджерс Дж., Брэнд Х. (ноябрь 1973 г.). «Дефектная ристоцетин-индуцированная агрегация тромбоцитов при болезни фон Виллебранда и ее коррекция фактором VIII» . Журнал клинических исследований . 52 (11): 2697–2707. дои : 10.1172/JCI107464 . ПМК 302536 . ПМИД 4201262 .
- ^ Парети Ф.И., Фуджимура Ю., Дент Дж.А., Холланд Л.З., Циммерман Т.С., Руджери З.М. (ноябрь 1986 г.). «Выделение и характеристика коллагенсвязывающего домена в факторе фон Виллебранда человека» . Журнал биологической химии . 261 (32): 15310–15315. дои : 10.1016/S0021-9258(18)66869-3 . ПМИД 3490481 .
- ^ Хейдари М., Мехрбод М., Эйтехади М.Р., Мофрад М.Р. (август 2015 г.). «Сотрудничество факторов фон Виллебранда усиливает механизм адсорбции» . Журнал Королевского общества, Интерфейс . 12 (109): 20150334. doi : 10.1098/rsif.2015.0334 . ПМЦ 4535404 . ПМИД 26179989 .
Внешние ссылки [ править ]
- Запись GeneReviews/NCBI/NIH/UW о дефиците фактора фон Виллебранда. Включает: болезнь Виллебранда типа 1, болезнь фон Виллебранда типа 2А, болезнь фон Виллебранда типа 2B, болезнь фон Виллебранда типа 2M, болезнь фон Виллебранда типа 2N, болезнь фон Виллебранда типа 3.
- Обзор всей структурной информации, доступной в PDB для UniProt : P04275 (фактор фон Виллебранда) в PDBe-KB .