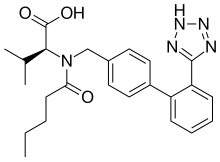
Валсартан
 | |
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Диован и другие |
| AHFS / Drugs.com | Монография |
| Медлайн Плюс | а697015 |
| Данные лицензии | |
| Беременность категория |
|
| Маршруты администрация | Через рот |
| Класс препарата | Антагонист рецепторов ангиотензина II |
| код АТС | |
| Юридический статус | |
| Юридический статус | |
| Фармакокинетические данные | |
| Биодоступность | 25% |
| Связывание с белками | 95% |
| Период полувыведения | 6 часов |
| Экскреция | Почки 30%, желчные протоки 70% |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| ИЮФАР/БПС | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| КЭБ | |
| ХЭМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.113.097 |
| Химические и физические данные | |
| Формула | С 24 Н 29 Н 5 О 3 |
| Молярная масса | 435.528 g·mol −1 |
| 3D model ( JSmol ) | |
| (проверять) | |
Валсартан под торговой маркой Diovan , продаваемый, среди прочего, , представляет собой лекарство, используемое для лечения высокого кровяного давления , сердечной недостаточности и диабетической болезни почек . [ 8 ] Он принадлежит к классу препаратов, называемых блокаторами рецепторов ангиотензина II (БРА). Это разумное начальное лечение высокого кровяного давления. [ 8 ] Его принимают внутрь . [ 8 ]
Общие побочные эффекты включают чувство усталости, головокружение, повышенное содержание калия в крови , диарею и боль в суставах. [ 8 ] Другие серьезные побочные эффекты могут включать проблемы с почками , низкое кровяное давление и ангионевротический отек . [ 8 ] Использование во время беременности может нанести вред ребенку, поэтому использование при грудном вскармливании не рекомендуется. [ 9 ] Это антагонист рецепторов ангиотензина II , который блокирует действие ангиотензина II . [ 8 ]
Валсартан был запатентован в 1990 году и начал использоваться в медицине в 1996 году. [ 10 ] Он доступен в виде непатентованного лекарства . [ 11 ] В 2021 году это было 120-е место среди наиболее часто назначаемых лекарств в США: на него было выписано более 5 миллионов рецептов. [ 12 ] [ 13 ] Доступны версии в виде комбинации валсартана/гидрохлоротиазида . [ 14 ] валсартан/амлодипин , [ 15 ] валсартан/амлодипин/гидрохлоротиазид , [ 16 ] валсартан/небиволол , [ 17 ] и валсартан/сакубитрил . [ 8 ] [ 18 ]
Медицинское использование
[ редактировать ]Валсартан используется для лечения высокого кровяного давления , сердечной недостаточности и для снижения смертности людей с дисфункцией левого желудочка после сердечного приступа . [ 19 ] [ 7 ]
Повышенное артериальное давление
[ редактировать ]Валсартан (и другие БРА) являются подходящим вариантом начального лечения для большинства людей с высоким кровяным давлением и отсутствием других сопутствующих заболеваний, равно как и ингибиторы АПФ , тиазидные диуретики и блокаторы кальциевых каналов . [ 20 ] Если у пациентов имеется сопутствующий диабет или заболевание почек, можно рассмотреть возможность применения БРА или ингибиторов АПФ вместо других классов лекарств от артериального давления. [ 21 ] [ 22 ]
Сердечная недостаточность
[ редактировать ]Валсартан снижает уровень смертности и госпитализаций по поводу сердечной недостаточности при использовании отдельно или в сочетании с бета-блокаторами при лечении сердечной недостаточности. [ 23 ] Важно отметить, что комбинация валсартана и ингибиторов АПФ не показала преимуществ в заболеваемости или смертности, а скорее увеличивает риск смертности при добавлении к терапии комбинацией бета-блокаторов и ингибиторов АПФ, а также увеличивает риск нежелательных явлений, таких как гиперкалиемия , гипотония и почечная недостаточность . [ 23 ] [ 24 ] Как показано в исследовании PARADIGM-HF, валсартан в сочетании с сакубитрилом для лечения сердечной недостаточности значительно снижает смертность от всех причин, а также сердечно-сосудистую смертность и количество госпитализаций по поводу сердечной недостаточности. [ 25 ]
Диабетическая болезнь почек
[ редактировать ]У людей с диабетом 2 типа антигипертензивная терапия валсартаном снижает скорость прогрессирования альбуминурии (альбумин в моче), способствует регрессу до нормоальбуминурии и может снизить скорость прогрессирования до терминальной стадии заболевания почек. [ 26 ] [ 27 ] [ 28 ]
Противопоказания
[ редактировать ]На упаковке валсартана имеется предупреждение о том, что препарат не следует использовать с ингибитором ренина алискиреном у людей с диабетом. В нем также говорится, что безопасность препарата при тяжелой почечной недостаточности не установлена. [ 7 ]
На валсартане имеется предупреждение о токсичности для плода. [ 7 ] [ 9 ] Прекращение приема этих препаратов рекомендуется сразу же после обнаружения беременности и следует начать прием альтернативных препаратов. [ 7 ] Грудное вскармливание не рекомендуется. [ 7 ] [ 29 ] [ 30 ]
Побочные эффекты
[ редактировать ]Побочные эффекты зависят от причины применения препарата.
Сердечная недостаточность
[ редактировать ]Побочные эффекты основаны на сравнении с плацебо у людей с сердечной недостаточностью. [ 7 ] Наиболее распространенные побочные эффекты включают головокружение (17% против 9%), низкое кровяное давление (7% против 2%) и диарею (5% против 4%). [ 7 ] Менее распространенные побочные эффекты включают боль в суставах , усталость и боль в спине (все 3% против 2%). [ 7 ]
Гипертония
[ редактировать ]Клинические испытания лечения гипертонии валсартаном по сравнению с плацебо демонстрируют такие побочные эффекты, как вирусная инфекция (3% против 2%), утомляемость (2% против 1%) и боль в животе (2% против 1%). Незначительные побочные эффекты, которые возникали при >1%, но были аналогичны частоте в группе плацебо, включают: [ 7 ]
- головная боль
- головокружение
- инфекция верхних дыхательных путей
- кашель
- диарея
- ринит / синусит
- тошнота
- фарингит
- отек
- артралгия
Почечная недостаточность
[ редактировать ]Люди, получающие БРА, включая валсартан или диуретики, подвержены развитию нарушений почечного кровотока, таких как аномальное сужение кровеносных сосудов в почках, гипертония , стеноз почечной артерии , сердечная недостаточность , хроническое заболевание почек , тяжелая застойная сердечная недостаточность или истощение объема жидкости. у которых функция почек частично зависит от активности ренин-ангиотензиновой системы, такой как вазоконстрикция эфферентных артериол, вызванная ангиотензином II, имеют высокий риск ухудшения функции почек, включая острую почечную недостаточность , олигурию , ухудшение азотемии или повышение креатинина в сыворотке . [ 7 ] Когда приток крови к почкам снижается, почки активируют ряд реакций, которые вызывают высвобождение ангиотензина, который сужает кровеносные сосуды и облегчает кровоток в почках. [ 31 ] Пока ухудшение функции нефронов прогрессирует или достигает клинически значимого уровня, оправдано приостановление или прекращение приема валсартана. [ 7 ] [ 32 ] [ 33 ] [ 34 ]
Взаимодействия
[ редактировать ]В информации о рецептах в США перечислены следующие лекарственные взаимодействия валсартана:
- Другие ингибиторы ренин-ангиотензиновой системы могут повышать риск низкого кровяного давления, проблем с почками и гиперкалиемии.
- Калийсберегающие диуретики, калия добавки , заменители соли, содержащие калий, могут повышать риск гиперкалиемии .
- НПВП могут увеличить риск проблем с почками и препятствовать снижению артериального давления.
- Валсартан может повышать концентрацию лития . [ 7 ]
- Валсартан и другие лекарства от артериального давления, связанные с ангиотензином, могут взаимодействовать с антибиотиками ко-тримоксазолом или ципрофлоксацином, увеличивая риск внезапной смерти из-за остановки сердца . [ 35 ]
Взаимодействие с едой
[ редактировать ]При приеме таблетки прием пищи снижает воздействие валсартана на лиц, принимающих таблетки валсартана, примерно на 40 %, а пиковую концентрацию в плазме (Cmax) — примерно на 50 %, о чем свидетельствует изменение AUC. [ 7 ]
Фармакология
[ редактировать ]Механизм действия
[ редактировать ]Валсартан блокирует действие ангиотензина II , которое включает сужение кровеносных сосудов и активацию альдостерона , снижая артериальное давление. [ 36 ] Препарат связывается с рецепторами ангиотензина I типа (АТ1), действуя как антагонист. [ 37 ] Этот механизм действия отличается от механизма действия ингибиторов АПФ, которые блокируют превращение ангиотензина I в ангиотензин II. Поскольку валсартан действует на рецептор, он может обеспечить более полный антагонизм к ангиотензину II, поскольку ангиотензин II вырабатывается другими ферментами, а также АПФ. Кроме того, валсартан не влияет на метаболизм брадикинина, как ингибиторы АПФ. [ 36 ]
Фармакодинамика
[ редактировать ]Фармакокинетика
[ редактировать ]Пиковая концентрация валсартана в плазме достигается через 2–4 часа после приема. [ 7 ] Значения AUC и Cmax валсартана находятся в приблизительно линейной зависимости от дозы в пределах терапевтического диапазона доз. Благодаря относительно короткому периоду полувыведения концентрация валсартана в плазме не накапливается в ответ на повторный прием. [ 7 ]
Общество и культура
[ редактировать ]Экономика
[ редактировать ]В 2010 году валсартан (торговое название Diovan) достиг годового объема продаж в 2,052 миллиарда долларов США в США и 6,053 миллиарда долларов США во всем мире. [ 38 ] Срок действия патентов на валсартан и валсартан/гидрохлоротиазид истек в сентябре 2012 года. [ 39 ] [ 40 ]
Комбинации
[ редактировать ]
Валсартан комбинируется с амлодипином или гидрохлоротиазидом (ГХТЗ) (или с ними обоими) в форме одной таблетки для лечения гипертонии несколькими препаратами. [ 8 ] [ 41 ] [ 42 ] [ 43 ] Валсартан также доступен в виде комбинации валсартан/сакубитрил . [ 18 ] [ 44 ] [ 45 ] Применяется для лечения сердечной недостаточности со сниженной фракцией выброса. [ 45 ] [ 46 ]
Напоминает
[ редактировать ]
В июле 2018 года Европейское агентство по лекарственным средствам (EMA) отозвало некоторые партии валсартана и таблеток, покрытых пленочной оболочкой валсартан/гидрохлоротиазид, распространявшихся в 22 странах Европейского Союза. [ 47 ] Zhejiang Huahai Pharmaceutical Co. (ZHP) в Линьхае, Китай, производила основной ингредиент, загрязненный N-нитрозодиметиламином (НДМА), канцерогеном . [ 48 ] Активный фармацевтический ингредиент впоследствии был импортирован рядом производителей непатентованных лекарств, включая Novartis , и продавался в Европе и Азии под торговой маркой их дочерней компании Sandoz , а также в Великобритании компаниями Dexcel Pharma Ltd и Accord Healthcare. [ 47 ]
Валсартан был отозван в Канаде. [ 49 ] [ 50 ] Власти считают, что степень загрязнения незначительна. [ 51 ] В июле 2018 года Национальное агентство по контролю за лекарствами и продуктами питания (NA-DFC или Badan POM Indonesia) объявило о добровольном отзыве двух продуктов, содержащих валсартан, производства Actavis Indonesia и Dipa Pharmalab Intersains. [ 52 ] США В июле 2018 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) объявило о добровольном отзыве некоторых поставок валсартана и валсартана/гидрохлоротиазида в США, распространяемых компаниями Solco Healthcare LLC, Major Pharmaceuticals и Teva Pharmaceutical Industries . [ 53 ] [ 48 ] Аналогичный отзыв инициировало Министерство здравоохранения Гонконга. [ 54 ] В августе 2018 года FDA опубликовало два обширных обновленных списка, в которых сотни конкретных американских продуктов, содержащих валсартан, были классифицированы как включенные и исключенные из отзыва. [ 55 ] [ 56 ] Неделю спустя FDA назвало еще двух производителей лекарств, Zhejiang Tianyu Pharmaceuticals из Китая и Hetero Labs Limited из Индии, как дополнительные источники загрязненного ингредиента валсартана . [ 57 ] [ 56 ]
В сентябре 2018 года FDA объявило, что повторное тестирование всех поставок валсартана выявило вторую канцерогенную примесь, N-нитрозодиэтиламин (NDEA), в отозванных продуктах, производимых ZHP в Китае и продаваемых в США под брендом Torrent Pharmaceuticals (Индия). [ 58 ]
Согласно анализу отчетов национальных медицинских агентств, проведенному Reuters в 2018 году , более 50 компаний по всему миру отозвали монопрепараты валсартана или комбинированные продукты, изготовленные из испорченного ингредиента валсартана. Загрязнение, вероятно, присутствовало с 2012 года, когда производственный процесс был изменен и одобрен органами EDQM и FDA. По результатам проверок, проведенных в конце 2018 года, оба ведомства приостановили действие сертификатов пригодности китайского и индийского производителей для поставок валсартана в ЕС и США. [ 59 ]
В 2019 году из-за присутствия примеси NDMA было отозвано еще много препаратов валсартана и его комбинаций. [ 60 ] [ 61 ]
В августе 2020 года Европейское агентство по лекарственным средствам (EMA) предоставило держателям регистрационных удостоверений рекомендации о том, как избежать присутствия примесей нитрозаминов в лекарствах для человека, и попросило их проверить все химические и биологические лекарства для человека на предмет возможного присутствия нитрозаминов и проверить их эффективность. продукты под угрозой. [ 62 ]
Нехватка
[ редактировать ]С июля 2018 года многочисленные отзывы о лекарственных препаратах лозартана , валсартана и ирбесартана привели к заметному дефициту этих жизненно важных лекарств в Северной Америке и Европе, особенно валсартана. В марте 2019 года FDA одобрило дополнительную непатентованную версию Диована™ для решения этой проблемы. [ 63 ] По данным агентства, дефицит валсартана был решен в апреле 2020 года. [ 64 ] но доступность генерической формы оставалась нестабильной до июля 2020 года. Аптеки Европейского Союза были уведомлены о том, что поставки препарата, особенно в более высоких дозированных формах, будут оставаться нестабильными вплоть до декабря 2020 года. [ 65 ]
Исследовать
[ редактировать ]У людей с нарушенной толерантностью к глюкозе валсартан может снизить частоту развития сахарного диабета 2 типа . Однако абсолютное снижение риска невелико (менее 1 процента в год), а диета, физические упражнения или другие лекарства могут оказаться более защитными. В том же исследовании не было показано снижения частоты сердечно-сосудистых событий (включая смерть). [ 66 ]
В одном исследовании с участием людей без диабета валсартан снижал риск развития сахарного диабета по сравнению с амлодипином , главным образом у людей с гипертонией. [ 67 ]
Проспективное исследование продемонстрировало снижение заболеваемости и прогрессирования болезни Альцгеймера и деменции. [ 68 ]
Ссылки
[ редактировать ]- ^ «Использование валсартана во время беременности» . Наркотики.com . 28 марта 2019 г. Проверено 12 февраля 2020 г.
- ^ «Список всех лекарств с предупреждениями о черном ящике, полученный FDA (используйте ссылки «Загрузить полные результаты» и «Просмотреть запрос»).» . nctr-crs.fda.gov . FDA . Проверено 22 октября 2023 г.
- ^ «Диован валсартан 40 мг таблетки, покрытые пленочной оболочкой» блистерная упаковка . Управление терапевтических товаров (TGA) . Архивировано из оригинала 25 октября 2021 года . Проверено 24 октября 2021 г.
- ^ «Диован валсартан 80 мг таблетки, покрытые пленочной оболочкой» блистерная упаковка . Управление терапевтических товаров (TGA) . Архивировано из оригинала 25 октября 2021 года . Проверено 24 октября 2021 г.
- ^ «Диован валсартан 160 мг таблетки, покрытые пленочной оболочкой» блистерная упаковка . Управление терапевтических товаров (TGA) . Архивировано из оригинала 25 октября 2021 года . Проверено 24 октября 2021 г.
- ^ «Валсартан 160 мг капсулы – Краткое описание характеристик препарата (SmPC)» . (эмс) . 19 февраля 2019 года. Архивировано из оригинала 13 февраля 2020 года . Проверено 12 февраля 2020 г.
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п «Диован-валсартан таблетка» . ДейлиМед . 12 июня 2019 года . Проверено 12 февраля 2020 г.
- ^ Перейти обратно: а б с д и ж г час «Монография Валсартана для профессионалов» . Наркотики.com . Американское общество фармацевтов систем здравоохранения . Проверено 3 марта 2019 г.
- ^ Перейти обратно: а б «Предупреждения о валсартане при беременности и грудном вскармливании» . Наркотики.com . Проверено 3 марта 2019 г.
- ^ Фишер Дж., Ганеллин Ч.Р., ред. (2006). Открытие аналоговых лекарств . Джон Уайли и сыновья. п. 470. ИСБН 9783527607495 .
- ^ Британский национальный формуляр: BNF 76 (76-е изд.). Фармацевтическая пресса. 2018. с. 179. ИСБН 9780857113382 .
- ^ «Топ-300 2021 года» . КлинКальк . Архивировано из оригинала 15 января 2024 года . Проверено 14 января 2024 г.
- ^ «Валсартан – статистика применения препарата» . КлинКальк . Проверено 14 января 2024 г.
- ^ «Дополнительная информация для пациентов о валсартане и гидрохлоротиазиде» . Наркотики.com . 29 января 2024 г. Проверено 7 февраля 2024 г.
- ^ «Дополнительная информация для пациентов об амлодипине и валсартане» . Наркотики.com . 27 июня 2023 г. Проверено 7 февраля 2024 г.
- ^ «Дополнительная информация для пациентов об амлодипине, валсартане и гидрохлоротиазиде» . Наркотики.com . 2 декабря 2023 г. Проверено 7 февраля 2024 г.
- ^ «Дополнительная информация для пациентов о небивололе и валсартане» . Наркотики.com . 14 октября 2023 г. Проверено 7 февраля 2024 г.
- ^ Перейти обратно: а б «Сакубитрил и Валсартан Монография для профессионалов» . Наркотики.com . 7 ноября 2019 года . Проверено 12 февраля 2020 г.
- ^ Ранда HD (2011). «Глава 26. Ренин и ангиотензин». В Брантоне Л.Л., Чабнере Б., Ноллманне Б.К. (ред.). Фармакологические основы терапии Гудмана и Гилмана (12-е изд.). Нью-Йорк: МакГроу-Хилл. ISBN 978-0-07-162442-8 .
- ^ Эттехад Д., Эмдин К.А., Киран А., Андерсон С.Г., Каллендер Т., Эмберсон Дж. и др. (март 2016 г.). «Снижение артериального давления для профилактики сердечно-сосудистых заболеваний и смерти: систематический обзор и метаанализ» . Ланцет . 387 (10022): 957–967. дои : 10.1016/s0140-6736(15)01225-8 . ПМИД 26724178 . S2CID 8868485 .
- ^ Бреннер Б.М., Купер М.Э., де Зеу Д., Кин В.Ф., Митч В.Е., Парвинг Х.Х. и др. (сентябрь 2001 г.). «Влияние лозартана на почечные и сердечно-сосудистые исходы у пациентов с диабетом 2 типа и нефропатией». Медицинский журнал Новой Англии . 345 (12): 861–869. дои : 10.1056/nejmoa011161 . hdl : 2445/122643 . ПМИД 11565518 .
- ^ Мансия Г., Фагард Р., Наркевич К., Редон Дж., Занкетти А., Бём М. и др. (июль 2013 г.). «Руководство ESH/ESC по лечению артериальной гипертензии 2013 года: Целевая группа по лечению артериальной гипертензии Европейского общества гипертонии (ESH) и Европейского общества кардиологов (ESC)» . Европейский кардиологический журнал . 34 (28): 2159–2219. doi : 10.1093/eurheartj/eht151 . hdl : 1854/LU-4127523 . ПМИД 23771844 .
- ^ Перейти обратно: а б Кон Дж.Н., Тоньони Дж. (декабрь 2001 г.). «Рандомизированное исследование блокатора рецепторов ангиотензина валсартана при хронической сердечной недостаточности» . Медицинский журнал Новой Англии . 345 (23): 1667–1675. doi : 10.1056/NEJMoa010713 . ПМИД 11759645 .
- ^ Макани Х., Бангалор С., Десуза К.А., Шах А., Мессерли Ф.Х. (январь 2013 г.). «Эффективность и безопасность двойной блокады ренин-ангиотензиновой системы: метаанализ рандомизированных исследований» . БМЖ . 346 (1 января 28): f360. дои : 10.1136/bmj.f360 . ПМЦ 3556933 . ПМИД 23358488 .
- ^ МакМюррей Дж.Дж., Пакер М., Десаи А.С., Гонг Дж., Лефковиц М.П., Ризкала А.Р. и др. (сентябрь 2014 г.). «Ингибирование ангиотензина-неприлизина по сравнению с эналаприлом при сердечной недостаточности» . Медицинский журнал Новой Англии . 371 (11): 993–1004. дои : 10.1056/NEJMoa1409077 . hdl : 2445/178508 . ПМИД 25176015 . S2CID 11383 .
- ^ Виберти Дж., Уилдон, Нью-Мексико (август 2002 г.). «Снижение микроальбуминурии валсартаном у пациентов с сахарным диабетом 2 типа: эффект, независимый от артериального давления» . Тираж . 106 (6): 672–678. дои : 10.1161/01.CIR.0000024416.33113.0A . ПМИД 12163426 . S2CID 5887738 .
- ^ Галле Дж., Шведхельм Э., Пинетти С., Бегер Р.Х., Ваннер С. (октябрь 2008 г.). «Антипротеинурические эффекты блокаторов рецепторов ангиотензина: телмисартан по сравнению с валсартаном у пациентов с артериальной гипертензией, сахарным диабетом 2 типа и явной нефропатией» . Нефрология, Диализ, Трансплантация . 23 (10): 3174–3183. дои : 10.1093/ndt/gfn230 . ПМИД 18450829 .
- ^ Холленберг Н.К., Парвинг Х.Х., Виберти Г., Ремуцци Г., Риттер С., Зеленкофске С. и др. (сентябрь 2007 г.). «Реакция альбуминурии на очень высокие дозы валсартана при сахарном диабете 2 типа». Журнал гипертонии . 25 (9): 1921–1926. дои : 10.1097/HJH.0b013e328277596e . ПМИД 17762658 . S2CID 25150658 .
- ^ «Монография о продукции Диована» . База данных о лекарственных препаратах Министерства здравоохранения Канады . Novartis Pharmaceuticals Canada Inc. Архивировано из оригинала 30 декабря 2012 года . Проверено 5 ноября 2015 г.
- ^ «Монография о продукте - ПрДИОВАН® (валсартан)» (PDF) . pdf.hres.ca. 12 мая 2015 г.
- ^ Кумар А., Фаусто А. (2010). «11». Патологические основы болезней (8-е изд.). Сондерс Эльзевир. п. 493. ИСБН 978-1-4160-3121-5 .
- ^ Смит С.К., Бенджамин Э.Дж., Боноу Р.О., Браун Л.Т., Крегер М.А., Франклин Б.А. и др. (ноябрь 2011 г.). «Вторичная профилактика и терапия снижения риска AHA/ACCF для пациентов с ишемической болезнью сердца и другими атеросклеротическими сосудистыми заболеваниями: обновление 2011 г.: рекомендации Американской кардиологической ассоциации и Фонда Американского колледжа кардиологов» . Тираж . 124 (22). Ovid Technologies (Wolters Kluwer Health): 2458–2473. doi : 10.1161/cir.0b013e318235eb4d . ПМИД 22052934 .
- ^ «Клиническое практическое руководство KDIGO по оценке и лечению хронической болезни почек, 2012 г.» (PDF) . КДИГО. Январь 2013 г. Архивировано из оригинала (PDF) 6 февраля 2019 г.
- ^ Зар Т., Гребер С., Перазелла М.А. (7 июня 2007 г.). «Распознавание, лечение и профилактика токсичности пропиленгликоля». Семинары по диализу . 20 (3). Уайли: 217–219. дои : 10.1111/j.1525-139x.2007.00280.x . ПМИД 17555487 . S2CID 41089058 .
- ^ Фралик М., Макдональд Э.М., Гомес Т., Антониу Т., Холландс С., Мамдани М.М. и др. (октябрь 2014 г.). «Ко-тримоксазол и внезапная смерть у пациентов, получающих ингибиторы ренин-ангиотензиновой системы: популяционное исследование» . БМЖ . 349 : г6196. дои : 10.1136/bmj.g6196 . ПМЦ 4214638 . ПМИД 25359996 .
- ^ Перейти обратно: а б Кацунг Б.Г., Тревор Эй.Дж. (2015). «Глава 11» . Базовая и клиническая фармакология (13-е изд.). Макгроу-Хилл Образование. ISBN 978-0071825054 .
- ^ Унгер Т. (ноябрь 1999 г.). «Значение блокады рецепторов ангиотензина 1 типа: чем отличаются блокаторы рецепторов ангиотензина II?». Американский журнал кардиологии . 84 (10А): 9С–15С. дои : 10.1016/s0002-9149(99)00728-6 . ПМИД 10588089 .
- ^ «Годовой отчет Novartis за 2010 год» (PDF) .
- ^ Мёллер П. (29 апреля 2011 г.). «Лекарства-блокбастеры, которые скоро станут дженериками» . Новости США и мировой отчет .
- ^ Фон Шапер Э (5 августа 2011 г.). «Хименес из Novartis имеет планы блокбастера в отношении Диована после истечения срока действия патента» . Блумберг.
- ^ «Эксфорж-амлодипина безилат и валсартан таблетки, покрытые пленочной оболочкой» . ДейлиМед . 12 июня 2019 года . Проверено 12 февраля 2020 г.
- ^ «Диован HCT-валсартан и гидрохлоротиазид таблетки, покрытые пленочной оболочкой» . ДейлиМед . Проверено 12 февраля 2020 г.
- ^ «Эксфорж HCT-амлодипин валсартан и гидрохлоротиазид таблетка, покрытая пленочной оболочкой» . ДейлиМед . Проверено 12 февраля 2020 г.
- ^ «Энтресто-сакубитрил и валсартан таблетки, покрытые пленочной оболочкой» . ДейлиМед . 1 сентября 2019 года . Проверено 12 февраля 2020 г.
- ^ Перейти обратно: а б Фала Л (сентябрь 2015 г.). «Энтресто (сакубитрил/валсартан): первый в своем классе ингибитор ангиотензиновых рецепторов неприлизина, одобренный FDA для лечения пациентов с сердечной недостаточностью» . Американские льготы по здоровью и лекарствам . 8 (6): 330–334. ПМК 4636283 . ПМИД 26557227 .
- ^ Халил П., Каббах Г., Саид С., Мукерджи Д. (2018). «Энтресто, новая панацея от сердечной недостаточности?». Сердечно-сосудистые и гематологические средства в медицинской химии . 16 (1): 5–11. дои : 10.2174/1871525716666180313121954 . ПМИД 29532764 . S2CID 3880750 .
- ^ Перейти обратно: а б Кристенсен Дж. «Обычный сердечный препарат отозван в 22 странах из-за возможной связи с раком» . CNN . Проверено 14 июля 2018 г.
- ^ Перейти обратно: а б Эдни А., Берфилд С., Ю Э (12 сентября 2019 г.). «Канцерогены проникли в поставки непатентованных лекарств в США» Bloomberg News . Проверено 17 сентября 2019 г.
- ^ «Несколько препаратов, содержащих валсартан, отзываются из-за загрязнения потенциальным канцерогеном» . Здоровье Канады . 9 июля 2018 года . Проверено 15 июля 2018 г.
- ^ «Групповой иск по валсартану» . valsartanclassaction.com . Проверено 15 июля 2018 г.
- ^ «Примеси нитрозаминов в лекарственных препаратах: Рекомендации» . Здоровье Канады . 4 апреля 2022 г.
- ^ «Разъяснения БПОМ РИ по поводу отмены антигипертензивных препаратов, содержащих действующее вещество Валсартан» . Национальное агентство по контролю за лекарствами и продуктами питания Республики Индонезия (Бадан ПОМ) (на индонезийском языке). Архивировано из оригинала 13 ноября 2019 года . Проверено 18 июля 2018 г.
- ^ Кристенсен Дж. «FDA присоединяется к отзыву обычных сердечных препаратов в 22 странах» . CNN . Проверено 15 июля 2018 г.
- ^ «Министерство здравоохранения Гонконга отзывает пять сердечных препаратов, содержащих валсартан, произведенных в Китае» . Южно-Китайская Морнинг Пост . 20 июля 2018 года . Проверено 20 июля 2018 г.
- ^ «Информация FDA об отзыве валсартана» . Управление по контролю за продуктами и лекарствами (FDA) . 2 августа 2018 года . Проверено 8 августа 2018 г.
- ^ Перейти обратно: а б «Обновления FDA и объявления для прессы об отзыве блокаторов рецепторов ангиотензина II (ARB) (валсартан, лозартан и ирбесартан)» . Управление по контролю за продуктами и лекарствами (FDA) . 20 августа 2018 года . Проверено 17 сентября 2019 г.
- ^ Вендлинг П. (13 августа 2018 г.). «Все больше производителей лекарств отмечено ростом отзыва валсартана» . ВебМД . Проверено 13 августа 2018 г.
- ^ «FDA предоставляет обновленную информацию о продолжающемся расследовании продуктов валсартана и сообщает об обнаружении дополнительных примесей, выявленных в уже отозванных продуктах одной фирмы» . Управление по контролю за продуктами и лекарствами (FDA) (пресс-релиз). 13 сентября 2018 года . Проверено 14 сентября 2018 г.
- ^ Харни А., Хиршлер Б. (22 августа 2018 г.). «Токсин, лежащий в основе отзыва лекарств, указывает на дыры в системе медицинской безопасности» . Рейтер . Проверено 23 ноября 2018 г.
- ^ Абдин А.Ю., Йебоа П., Джейкоб С. (февраль 2020 г.). «Химические примеси: эпистемологическая загадка с серьезными побочными эффектами» . Международный журнал экологических исследований и общественного здравоохранения . 17 (3): 1030. doi : 10.3390/ijerph17031030 . ПМК 7038150 . ПМИД 32041209 .
- ^ «Отзыв АРБ: валсартан, лозартан и ирбесартан» . США Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) . 3 февраля 2020 г. Проверено 12 февраля 2020 г.
- ^ «Примеси нитрозаминов» . Европейское агентство по лекарственным средствам . 23 октября 2019 г. Проверено 6 августа 2020 г. Текст скопирован из источника, права на который принадлежат Европейскому агентству по лекарственным средствам. Воспроизведение разрешено при условии указания источника.
- ^ Клэнтон Н. (21 марта 2019 г.). «FDA одобряет непатентованный препарат от артериального давления после отзыва препарата» . айк . Проверено 13 июля 2020 г.
- ^ Текущая и решенная нехватка и прекращение производства лекарств, сообщенная в FDA США Управление по контролю за продуктами и лекарствами (FDA). Проверено 13 июля 2020 г.
- ^ Нехватка поставок Валсартана-КТ 160 мг . Желтый список (на немецком языке). Фарминдекс . Проверено 13 июля 2020 г.
- ^ МакМюррей Дж.Дж., Холман Р.Р., Хаффнер С.М., Бетел М.А., Хольцхауэр Б., Хуа Т.А. и др. (апрель 2010 г.). «Влияние валсартана на заболеваемость диабетом и сердечно-сосудистыми заболеваниями» . Медицинский журнал Новой Англии . 362 (16): 1477–1490. дои : 10.1056/NEJMoa1001121 . hdl : 2381/21817 . ПМИД 20228403 . S2CID 18710004 .
- ^ Кьельдсен С.Е., Макиннес Г.Т., Мансия Г., Хуа Т.А., Юлиус С., Вебер М.А. и др. (2008). «Прогрессивные эффекты валсартана по сравнению с амлодипином в профилактике диабета в зависимости от категорий диабетогенного риска у пациентов с гипертонической болезнью: исследование VALUE». Артериальное давление . 17 (3): 170–177. дои : 10.1080/08037050802169644 . ПМИД 18608200 . S2CID 3426921 .
- ^ Ли Н.К., Ли А., Уитмер Р.А., Кивипелто М., Лоулер Э., Казис Л.Е. и др. (январь 2010 г.). «Использование блокаторов рецепторов ангиотензина и риск деменции у преимущественно мужского населения: проспективный когортный анализ» . БМЖ . 340 : b5465. дои : 10.1136/bmj.b5465 . ПМК 2806632 . ПМИД 20068258 .