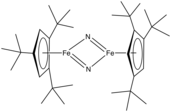
Металлический комплекс нитридо
Комплексы нитридо металла представляют собой координационные соединения и металлические кластеры , которые содержат атом азота, связанного только с переходными металлами. Эти соединения являются молекулярными , т.е. дискретными в отличие от полимерных, плотных нитридных материалов, которые полезны в материаловедении . [ 1 ] Различие между молекулярными и твердыми полимерами не всегда очень ясно, как показано материалами Li 6 Mon 4 и более конденсированными производными, такими как NA 3 Mon 3 . Комплексы нитридо переходных металлов привлекли интерес частично, потому что предполагается, что фиксация азота проходит через промежуточные продукты нитридо. Комплексы нитридо давно известны, первым примером являются соли [OSO 3 N] − , описано в 19 веке. [ 2 ]
Структурные тенденции
[ редактировать ]Мононуклеарные комплексы оснащены нитридными лигандами терминала, обычно с короткими расстояниями Mn, соответствующими множественным связям металлического лиганда . Например, в анионе в PPH 4 [Moncl 4 ] расстояние MO-N составляет 163,7 вечера. Появление терминальных нитридо -лигандов следуют закономерностям, наблюдаемым для Oxo Complexes: они чаще встречаются для ранних и более тяжелых металлов. Многие биологические и полинуклеарные комплексы известны с помощью лигандов-нитридо. [ 3 ] Также возможны более экзотические комплексы нитридо-металлов, такие как недавно сообщенное соединение, содержащее связи с терминальным нитридом урана (-U®N). [ 4 ]
- Пример металлических комплексов нитридо
-
[OsNO 3 ] − , изоэлектронный с тетроксидом осмия .
-
[Moncl 4 ] − , квадратный пирамидальный комплекс MO (VI).
-
[W 2 (M-N) Cl 10 ] − , содержащий два центра W (VI), соединенных нитридо -лигандом.
-
[IR 3 N (SO 4 ) 6 (H 2 O) 3 ] 4− , структурно связан с основным ацетатом железа .
-
Урановый нитридо комплекс.
Подготовительные маршруты
[ редактировать ]Нитриды металлов производятся с использованием различных источников азота. Первый пример выше подготовлен из амида (NH 2 − ) как n 3− источник: [ 5 ]
- Oso 4 + knh 2 → koso 3 n + h 2 o
Чаще всего комплексы нитридо продуцируются путем разложения комплексов азидо . [ 6 ] Движущей силой этих реакций является большая стабильность n 2 . Азотный трихлорид является эффективным реагентом, дающим хлоро-нитридо комплексы. В некоторых случаях даже N 2 и нитрилы могут служить источниками нитридных лигандов. [ 7 ]
Реакции нитридо лигандов
[ редактировать ]Нитридный лиганд может быть как электрофильным, так и нуклеофильным. [ 8 ] [ 9 ] Терминальные нитриды ранних металлов имеют тенденцию быть основными и окисляемыми, тогда как нитриды более поздних металлов имеют тенденцию окислять и электрофильные. Первое поведение иллюстрируется их N- протонированием и n- алкилированием . Комплексы Nitrido RU и OS часто добавляют органорофосфины с получением иминофосфиновых производных, содержащих R 3 PN − лиганд.
Интерстициальные нитриды
[ редактировать ]Из -за способности нитридо -лигандов служить в качестве мостового лиганда , известно, что несколько металлических кластеров содержат нитридные лиганды в своем центре. Такие нитридо -лиганды называются интерстициальными . В некоторых случаях нитрид полностью заключен в центр шести или более металлов и не может подвергаться реакциям, хотя он способствует интерметаллической связи. [ 10 ]

Смотрите также
[ редактировать ]Общие ссылки
[ редактировать ]- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2 -е изд.). Баттерворт-Хейнеманн . ISBN 978-0-08-037941-8 .
- ^ Fritzsche, J.; Струве, Х. (1847). «О османской кислоте Осмия» . Журнал практической химии . 41 (1): 97–113. Doi : 10.1002/prac.18470410113 .
- ^ Элега, Курт; Strähle, Joachim (1992). «Нитридо комплексы переходных металлов». Applied Chemistry International Edition на английском языке . 31 (8): 955–978. Doi : 10.1002/ani.199209551 .
- ^ Король, Дэвид М.; Тунец, Флориана; Макиннес, Эрик Дж.Л.; МакМастер, Джонатан; Льюис, Уильям; Блейк, Александр Дж.; Лиддл, Стивен Т. (2012). «Синтез и структура терминального комплекса нитрида урана» . Наука . 337 (6095): 717–720. Bibcode : 2012sci ... 337..717K . doi : 10.1126/science.1223488 . PMID 22745250 .
- ^ Grube, H.L. (1956). «Платиновые металлы: калий Osmiamate» . В Брауэре, Георг (ред.). Справочник по подготовительной неорганической химии . Тол. 2. Перевод Стехера, Пол Г. (2 -е изд.). Нью -Йорк, Нью -Йорк: Академическая пресса. п. 1605. LCCN 63-14307 -через интернет-архив.
- ^ Рейнерс, Матиас; Маекава, Миюки; Daniliuc, Константин Г.; Фрейтаг, Матиас; Джонс, Питер Г.; Белый, Питер С.; Хоэнбергер, Йоханнес; Саттер, Йорг; Мейер, Карстен; Марон, Лоран; Уолтер, Марк Д. (2017). «Исследования реакционной способности [CP'FE (μ-I)] 2: нитридо-, сульфидо- и рассеянных железа комплексов, полученных из псевдогалидной активации» . Химическая наука . 8 (5): 4108–4122. doi : 10.1039/c7sc00570a . PMC 6099922 . PMID 30155215 .
- ^ Лаплаза, Каталина Э.; Джонсон, Марк Дж. Петерс, Джонас С.; Odom, Aaron L.; Ким, Эстер; Камминс, Кристофер С.; Джордж, Грэм Н.; Пикеринг, Ингрид Дж. (1996). «Расщепление динитрогена с помощью трехкоординатных комплексов молибдена (III): механистические и структурные данные1». Журнал Американского химического общества . 118 (36): 8623–8638. doi : 10.1021/ja960574x .
- ^ Dehnicke, Курт; Веллер, Фрэнк; Strähle, Joachim (2001). «Нитридо -мосты между переходными металлами и элементами основных групп, иллюстрируемых серией [M] NNA для [M] NCL». Химический Соц Преподобный 30 (2): 125–135. doi : 10.1039/a802635a .
- ^ Смит, Джереми М. (2014). «Реактивные переходные нитридные комплексы». Прогресс в неорганической химии Том 58 . Тол. 58. С. 417–470. doi : 10.1002/9781118792797.CH06 . ISBN 9781118792797 .
{{cite book}}:|journal=игнорируется ( помощь ) - ^ Gladfelter, Wayne L. (1985). Органометаллические металлические кластеры, содержащие нитрозильные и нитридо лиганды . Тол. 24. С. 41–86. doi : 10.1016/s0065-3055 (08) 60413-x . ISBN 9780120311248 .
{{cite book}}:|journal=игнорируется ( помощь )
![[Osno3] -, изоэлектронный с тетроксидом осмия.](http://upload.wikimedia.org/wikipedia/commons/thumb/f/f8/OsNO3_anion.png/165px-OsNO3_anion.png)
![[MONCL4] -, квадратный пирамидальный комплекс MO (VI).](http://upload.wikimedia.org/wikipedia/commons/thumb/2/29/MoNCl4_anion.png/170px-MoNCl4_anion.png)
![[W2 (μ-N) CL10]-, содержащий два центра W (VI), соединенных нитридо-лигандом.](http://upload.wikimedia.org/wikipedia/commons/thumb/8/82/W2NCl10_anion.png/170px-W2NCl10_anion.png)
![[IR3N (SO4) 6 (H2O) 3] 4-, структурно связано с основным ацетатом железа.](http://upload.wikimedia.org/wikipedia/commons/thumb/0/00/Ir3N%28SO4%296aq3.png/128px-Ir3N%28SO4%296aq3.png)