Бета-секретаза 1
| БАСЕ1 | |||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | BACE1 , ASP2, BACE, HSPC104, бета-секретаза 1 | ||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 604252 ; МГИ : 1346542 ; Гомологен : 8014 ; Генные карты : BACE1 ; OMA : BACE1 — ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||
| Номер ЕС | 3.4.23.46 | ||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
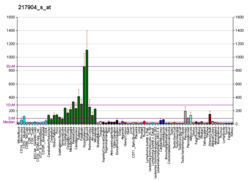
Бета-секретаза 1 , также известная как фермент 1, расщепляющий белок-предшественник бета-амилоида , фермент 1 , расщепляющий бета-сайт APP ( BACE1 ), мембраносвязанная аспарагиновая протеаза 2 , мемапсин-2 , аспартилпротеаза 2 и ASP2 , представляет собой фермент у людей это кодируется BACE1 геном . [ 5 ] Экспрессия BACE1 наблюдается преимущественно в нейронах и олигодендроцитах . [ 6 ]
BACE1 представляет собой протеазу аспарагиновой кислоты, играющую важную роль в формировании миелиновых оболочек в периферических нервных клетках: у мышей экспрессия BACE1 высока на постнатальных стадиях, когда миелинизация . происходит [ 7 ] Трансмембранный белок активного центра содержит два остатка аспартата во внеклеточном белковом домене и может функционировать как димер , его цитоплазматический хвост необходим для правильного созревания и эффективного внутриклеточного перемещения, но не влияет на активность. Он вырабатывается в виде профермента , удаление эндопротеолита происходит после выхода БАСЕ из эндоплазматической сети , в аппарате Гольджи . Кроме того, пропептид получает дополнительные сахара для увеличения молекулярной массы. [ 8 ] и хвост стал пальмитоилированным . [ нужна ссылка ]
На экспрессию BACE1 влияет воспалительное состояние: при БА цитокины являющегося снижают уровень PPAR1, ингибитором мРНК BACE1. [ нужна ссылка ]
Роль в болезни Альцгеймера
[ редактировать ]
BACE1 является основной бета-секретазой, ответственной за выработку β-амилоида пептидов в нейронах. [ 9 ]
Генерация 40 или 42 аминокислот длиной из амилоида-β пептидов , которые агрегируют в мозге пациентов с болезнью Альцгеймера, требует двух последовательных расщеплений белка-предшественника амилоида (APP). Внеклеточное расщепление APP с помощью BACE1 создает растворимый внеклеточный фрагмент и фрагмент, связанный с клеточной мембраной, называемый C99. Расщепление C99 внутри его трансмембранного домена γ-секретазой высвобождает внутриклеточный домен АРР и производит амилоид-β. Поскольку гамма-секретаза расщепляет APP ближе к клеточной мембране , чем BACE1, она удаляет фрагмент пептида амилоида-β. Первоначальное расщепление APP α-секретазой, а не BACE1, предотвращает возможное образование амилоида-β, образующего P3 . Это демонстрирует, что BACE1 и альфа-секретаза конкурируют за процессинг APP.
В отличие от APP и белков пресенилина , важных для γ-секретазы, никакие известные мутации в гене, кодирующем BACE1, не вызывают раннюю семейную болезнь Альцгеймера , которая является редкой формой заболевания. Однако было показано, что уровни этого фермента повышены при гораздо более распространенной спорадической болезни Альцгеймера с поздним началом. BACE2 является близким гомологом BACE1, о расщеплении APP in vivo не сообщалось .
Физиологическая цель расщепления АРР и других трансмембранных белков ВАСЕ неизвестна: в некоторых исследованиях было обнаружено, что ВАСЕ1 участвует в миелинизации (он экспрессируется совместно с нейрегулин 1 типа III). Аналогично процессингу APP, бета-субъединица VGSC является субстратом для BACE1. [ 10 ]
Однако мутация одного остатка в APP снижает способность BACE1 расщеплять его с образованием бета-амилоида и снижает риск болезни Альцгеймера и других когнитивных нарушений. [ 11 ] [ 12 ]
Ингибиторы ВАСЕ
[ редактировать ]Лекарства, блокирующие этот фермент (ингибиторы BACE), теоретически предотвращают накопление бета-амилоида и (согласно гипотезе амилоида ) могут помочь замедлить или остановить болезнь Альцгеймера. [ 13 ]
От болезни Альцгеймера
[ редактировать ]Несколько компаний находятся на ранних стадиях разработки и тестирования этого потенциального класса лечения. [ 14 ] [ 15 ] В марте 2008 года были опубликованы результаты фазы I для кандидата CTS-21166 от CoMentis Inc. [ 16 ]
В апреле 2012 года компания Merck & Co. , Inc. сообщила о результатах фазы I своего кандидата веруцестата (МК-8931). [ 17 ] Компания Merck начала исследование фазы II/III MK-8931 в декабре 2012 года, которое, по оценкам, завершится в июле 2019 года. [ 18 ] В феврале 2017 года компания Merck прекратила последнюю стадию исследования веруцестата для лечения легкой и умеренной болезни Альцгеймера после того, как, по мнению независимой группы экспертов, у него «практически нет шансов» на эффективность. Это произошло всего через три месяца после того, как компания Eli Lilly & Co. объявила о своей неудаче с соланезумабом .
В сентябре 2014 года AstraZeneca и Eli Lilly and Company объявили о соглашении о совместной разработке ланабецестата (AZD3293). [ 19 ] Ключевое клиническое исследование ланабецестата фазы II/III началось в конце 2014 г. [ 20 ] но было остановлено в 2018 году до запланированного завершения из-за плохих результатов. [ 21 ]
Еще одним ингибитором BACE1, дошедшим до фазы II испытаний, является ингибитор Eli Lilly LY2886721. Данные исследования фазы I были впервые представлены на конференции Международной ассоциации Альцгеймера в 2012 году. Ежедневное дозирование в течение 2 недель снижало активность BACE1 на 50–75% и Aβ42 спинномозговой жидкости на 72% (Willis et al., 2012; Bowman Rogers and Strobel). , 2013). Недавно компания Lilly сообщила, что исследование II фазы LY2886721 было прекращено из-за нарушений функции печени, обнаруженных у 4 из 45 пациентов (Rogers, 2013). Эта токсичность, однако, не обязательно связана с механизмом действия ингибитора, но может представлять собой нецелевой эффект, поскольку печень мышей с нокаутом BACE1 в норме.
Потенциальные побочные эффекты
[ редактировать ]Тесты на мышах показали, что протеазы BACE, в частности BACE1, необходимы для правильного функционирования мышечных веретен . [ 22 ] Эти результаты повышают вероятность того, что препараты, ингибирующие ВАСЕ, которые в настоящее время исследуются для лечения болезни Альцгеймера, могут иметь значительные побочные эффекты, связанные с нарушением координации движений. [ 23 ] BACE1 хотя мыши с нокаутом здоровы. [ 24 ]
Связь с плазмепсином
[ редактировать ]BACE1 отдаленно связан с патогенной протеазой аспарагиновой кислоты плазмепсином , которая является потенциальной мишенью для будущих противомалярийных препаратов. [ 25 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с GRCh38: Версия Ensembl 89: ENSG00000186318 – Ensembl , май 2017 г.
- ^ Jump up to: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000032086 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Вассар Р., Беннетт Б.Д., Бабу-Хан С., Кан С., Мендиаз Э.А., Денис П., Теплов Д.Б., Росс С., Амаранте П., Лоэлофф Р., Луо Ю., Фишер С., Фуллер Дж., Иденсон С., Лайл Дж., Яросински М.А., Бьер А.Л., Карран Э., Берджесс Т., Луис Дж.К., Коллинз Ф., Тринор Дж., Роджерс Дж., Цитрон М. (октябрь 1999 г.). «Расщепление бета-секретазой белка-предшественника амилоида болезни Альцгеймера трансмембранной аспарагиновой протеазой BACE» . Наука . 286 (5440): 735–41. дои : 10.1126/science.286.5440.735 . ПМИД 10531052 . S2CID 42481897 . Архивировано из оригинала 9 апреля 2019 г. Проверено 1 июля 2019 г.
- ^ Раджани Р.М., Эллингфорд Р., Хельмут М., Харрис С.С., Тасо О.С., Грайковски Д., Лам Ф., Арбер С., Фертан Е., Даниал Дж., Свайр М., Ллойд М., Джованнуччи Т.А., Бурденкс М., Кленерман Д., Вассар Р., Рэй С. , Сала Фригерио C, Буше Массачусетс (июль 2024 г.). «Селективное подавление бета-амилоида, полученного из олигодендроцитов, спасает нейрональную дисфункцию при болезни Альцгеймера» . ПЛОС Биология . 22 (7): e3002727. дои : 10.1371/journal.pbio.3002727 . ПМЦ 11265669 . ПМИД 39042667 .
- ^ Виллем М., Гаррат А.Н., Новак Б., Цитрон М., Кауфманн С., Риттгер А., ДеСтрупер Б., Сафтиг П., Бирчмайер С., Хаас С. (октябрь 2006 г.). «Контроль миелинизации периферических нервов с помощью бета-секретазы BACE1». Наука . 314 (5799): 664–6. Бибкод : 2006Sci...314..664W . дои : 10.1126/science.1132341 . ПМИД 16990514 . S2CID 8432207 .
- Разместить резюме в: Филлипс М.Л. (21 сентября 2006 г.). «Фермент болезни Альцгеймера, важный для миелина» . Ученый .
- ^ Капелл А., Штайнер Х., Виллем М., Кайзер Х., Мейер С., Уолтер Дж., Ламмих С., Мультауп Г., Хаас С. (06.10.2000). «Созревание и расщепление пропептида β-секретазы» . Журнал биологической химии . 275 (40): 30849–30854. дои : 10.1074/jbc.M003202200 . ISSN 0021-9258 . ПМИД 10801872 .
- ^ Цай Х., Ван Ю., Маккарти Д., Вэнь Х., Борчелт Д.Р., Прайс Д.Л., Вонг ПК (март 2001 г.). «BACE1 является основной β-секретазой для генерации нейронами пептидов Aβ». Природная неврология . 4 (3): 233–234. дои : 10.1038/85064 . ISSN 1546-1726 . ПМИД 11224536 . S2CID 11973104 .
- ^ Ким Д.Ю., Кэри Б.В., Ван Х., Ингано Л.А., Бинсток А.М., Верц М.Х., Петтингелл В.Х., Хе П., Ли В.М., Вульф С.Дж., Ковач Д.М. (июль 2007 г.). «BACE1 регулирует потенциалзависимые натриевые каналы и активность нейронов» . Природная клеточная биология . 9 (7): 755–764. дои : 10.1038/ncb1602 . ISSN 1465-7392 . ПМЦ 2747787 . ПМИД 17576410 .
- ^ «Ген, борющийся с болезнью Альцгеймера, может вдохновить на лечение» . Июль 2012 г. Архивировано из оригинала 15 мая 2012 г. Проверено 16 июля 2012 г.
- ^ Йонссон Т , Атвал Дж. К. , Стейнберг С , Снаедал Дж , Йонссон П. В. , Бьорнссон С , Стефанссон Х , Сулем П , Гудбьартссон Д , Мэлони Дж , Хойт К , Густафсон А , Лю Ю , Лу Ю , Бхангале Т , Грэм РР , Хуттенлохер Дж , Бьернсдоттир Г., Андреассен О.А., Йонссон Э.Г., Палоти А., Беренс Т.В., Магнуссон О.Т., Конг А., Торстейнсдоттир Ю., Уоттс Р.Дж., Стефанссон К. (август 2012 г.). «Мутация APP защищает от болезни Альцгеймера и возрастного снижения когнитивных функций». Природа 488 (7409): 96–9. Бибкод : 2012Природа.488...96J . дои : 10.1038/nature11283 . ПМИД 22801501 . S2CID 4333449 .
- ^ Прадипкиран Дж.А., Редди А.П., Инь Икс, Манчак М., Редди П.Х. (2020). «Защитное действие молекул ингибирующего лиганда BACE1 против индуцированной бета-амилоидом синаптической и митохондриальной токсичности при болезни Альцгеймера» . Молекулярная генетика человека . 29 (1): 49–69. дои : 10.1093/hmg/ddz227 . ПМК 7001603 . ПМИД 31595293 .
- ^ Уокер Л.К., Розен Р.Ф. (июль 2006 г.). «Лекарства от болезни Альцгеймера – что после ингибиторов холинэстеразы?». Возраст и старение . 35 (4): 332–5. doi : 10.1093/ageing/afl009 . ПМИД 16644763 .
- ^ Бакстер Э.В., Конвей К.А., Кеннис Л., Бишофф Ф., Меркен М.Х., Уинтер Х.Л., Рейнольдс Ч., Тунге Б.А., Луо К., Скотт М.К., Хуанг Ю., Брекен М., Питерс СМ, Бертелот DJ, Мазур С., Брюнзил В.Д., Джордан А.Д. , Паркер М.Х., Бойд Р.Э., Цюй Дж., Александр Р.С., Бреннеман Д.Е., Рейтц А.Б. (сентябрь 2007 г.). «2-амино-3,4-дигидрохиназолины как ингибиторы BACE-1 (фермент, расщепляющий бета-сайт АРР): использование структурно-ориентированной конструкции для преобразования микромолярного удара в наномолярный свинец». Журнал медицинской химии . 50 (18): 4261–4. дои : 10.1021/jm0705408 . ПМИД 17685503 .
- ^ «Дебют ингибитора CoMentis BACE» . Апрель 2008 г. Архивировано из оригинала 26 сентября 2013 г. Проверено 16 июля 2012 г.
- ^ «Merck представляет результаты фазы I клинического испытания по оценке исследуемого ингибитора BACE MK-8931 в Американской академии неврологии» . Апрель 2012 г. Архивировано из оригинала 28 июля 2012 г.
- ^ «Merck начинает фазу II/III исследования исследуемого ингибитора BACE, MK-8931, для лечения болезни Альцгеймера» . Декабрь 2012 г. Архивировано из оригинала 27 февраля 2017 г. Проверено 13 декабря 2012 г.
- ^ «AstraZeneca и Lilly объявляют о союзе для разработки и коммерциализации ингибитора ВАСЕ AZD3293 для лечения болезни Альцгеймера» . 16 сентября 2014 г. Архивировано из оригинала 23 сентября 2015 г. . Проверено 8 октября 2014 г.
- ^ «AstraZeneca и Lilly проводят масштабные испытания лекарства от болезни Альцгеймера» . Рейтер . Декабрь 2014 г. Архивировано из оригинала 25 октября 2015 г. Проверено 30 июня 2017 г.
- ^ «Обновленная информация о клинических испытаниях ланабецестата III фазы» . 12 июня 2018 года. Архивировано из оригинала 5 июня 2022 года . Проверено 20 июня 2018 г.
- ^ Черет С., Майкл Виллем, Флоренс Р. Фрикер, Хаген Венде (июнь 2013 г.). «Bace1 и нейрегулин-1 совместно контролируют формирование и поддержание мышечных веретен» . Журнал ЭМБО . 32 (14): 2015–28. дои : 10.1038/emboj.2013.146 . ПМЦ 3715864 . ПМИД 23792428 .
- ^ Петтерссон А., Олссон Э., Валунд Л.О. (2005). «Двигательная функция у субъектов с легкими когнитивными нарушениями и ранней болезнью Альцгеймера». Деменция и гериатрические когнитивные расстройства . 19 (5–6): 299–304. дои : 10.1159/000084555 . ISSN 1420-8008 . ПМИД 15785030 . S2CID 36382718 .
- ^ Робердс С.Л., Андерсон Дж., Баси Дж., Бьенковски М.Дж., Бранстеттер Д.Г., Чен К.С., Фридман С.Б., Фригон Н.Л., Игры Д, Ху К., Джонсон-Вуд К., Каппенман К.Е., Кавабе Т.Т., Кола И., Куэн Р., Ли М., Лю В., Моттер Р., Николс Н.Ф., Пауэр М., Робертсон Д.В., Шенк Д., Шур М., Шопп ГМ, Шак М.Э., Синха С., Свенссон К.А., Тацуно Г., Тинтруп Х., Вейсман Дж., Райт С., МакКонлог Л. (июнь 2001 г.) ). «Мыши с нокаутом BACE здоровы, несмотря на отсутствие первичной активности бета-секретазы в мозге: значение для лечения болезни Альцгеймера» . Молекулярная генетика человека . 10 (12): 1317–24. дои : 10.1093/hmg/10.12.1317 . ПМИД 11406613 .
- ^ Руссо И., Бэббит С., Муралидхаран В., Батлер Т., Оксман А., Голдберг Д.Е. (февраль 2010 г.). «Плазмепсин V лицензирует белки плазмодия для экспорта в эритроцит хозяина» . Природа . 463 (7281): 632–6. Бибкод : 2010Natur.463..632R . дои : 10.1038/nature08726 . ПМЦ 2826791 . ПМИД 20130644 .
- Разместить резюме в: «Ученые нашли идеальную мишень для лечения малярии» . ScienceDaily (пресс-релиз). 4 февраля 2010 г.
Дальнейшее чтение
[ редактировать ]- Хун Л., Хэ Х, Хуан Х, Чанг В., Тан Дж. (2005). «Структурные особенности мемапсина 2 человека (бета-секретазы) и их биологическое и патологическое значение». Acta Biochimica et Biophysica Sinica . 36 (12): 787–92. дои : 10.1093/abbs/36.12.787 . ПМИД 15592644 .
- Джонстон Дж.А., Лю В.В., Тодд С.А., Коулсон Д.Т., Мерфи С., Ирвин ГБ, Пассмор AP (2006). «Экспрессия и активность фермента, расщепляющего белок-предшественник бета-амилоида, при болезни Альцгеймера». Труды Биохимического общества . 33 (Часть 5): 1096–100. дои : 10.1042/BST20051096 . ПМИД 16246054 . S2CID 44248549 .
- Домингес Д.И., Хартманн Д., Де Струпер Б. (2006). «BACE1 и пресенилин: две необычные аспартилпротеазы, участвующие в болезни Альцгеймера». Нейродегенеративные заболевания . 1 (4–5): 168–74. дои : 10.1159/000080982 . ПМИД 16908986 . S2CID 26746944 .
- Заккетти Д., Кьерегатти Е., Беттегацци Б., Михайлович М., Соуза В.Л., Гроховаз Ф., Мелдолези Дж. (2007). «Экспрессия и активность BACE1: актуальность при болезни Альцгеймера». Нейродегенеративные заболевания . 4 (2–3): 117–26. дои : 10.1159/000101836 . ПМИД 17596706 . S2CID 32898359 .
Внешние ссылки
[ редактировать ]- Онлайн-база данных MEROPS . по пептидазам и их ингибиторам: A01.004
- Бета-секретаза: молекула месяца. Архивировано 21 ноября 2012 г. в Wayback Machine , Дэвид Гудселл, Банк данных белков RCSB.
- человека Местоположение генома BACE1 и страница сведений о гене BACE1 в браузере генома UCSC .
- Обзор всей структурной информации, доступной в PDB для UniProt : P56817 (Человеческая бета-секретаза 1) в PDBe-KB .