Металлическое соединение кластера
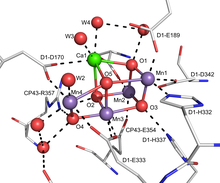
Металлические кластерные соединения представляют собой молекулярное ионное или нейтральное соединение, состоящее из трех или более металлов и имеют значительные металлические взаимодействия. [ 2 ]
Переходные металлические карбонильные кластеры
[ редактировать ]Разработка металлических карбонильных кластеров, таких как Ni (CO) 4 и Fe (CO) 5, быстро привели к изоляции Fe 2 (CO) 9 и Fe 3 (CO) 12 . Рандл и Даль обнаружили, что MN 2 (CO) 10 показали «не поддерживаемую» связь MN-MN, тем самым проверяя способность металлов связываться друг с другом в молекулах. В 1970 -х годах Паоло Чини продемонстрировал, что из платиновых металлов можно приготовить очень большие кластеры, одним из примеров является [RH 13 (Co) 24 H 3 ] 2− Полем Эта область химии кластеров получила выгоду от дифракции рентгеновских лучей с одним кристаллом .

Многие металлические карбонильные кластеры содержат лиганды, помимо CO. Например, Co -лиганд может быть заменен множеством альтернатив, таких как фосфины, изоцианиды, алкены, гидрид и т. Д. Некоторые карбонильные кластеры содержат два или более металлов. Другие содержат углеродные вершины. Одним из примеров является метилиден-трикобальтовый кластер [co 3 (ch) (co) 9 ] . [ 3 ] Вышеупомянутый кластер служит примером общего кластера с нулевой (нейтральной). Кроме того, катионный (положительно заряженный), а не нейтральный органометаллический тримолибден [ 4 ] [ 5 ] или Цунгстен [ 6 ] Кластеры также известны. Первым представителем этих ионных органометаллических кластеров является [MO 3 (CCH 3 ) 2 (O 2 CCH 3 ) 6 (H 2 O) 3 ] 2+ .
Переходные металлы.
[ редактировать ]
Галогениды низковалентных ранних металлов часто представляют собой кластеры с обширной связью ММ. Ситуация контрастирует с более высокими галогенидами этих металлов и практически всех галогенидов поздних переходных металлов, где связывание металла-галида изобилует.
Кластеры галогенидов переходного металла распространены для более тяжелых металлов: ZR, HF, NB, TA, MO, W и RE. Для самых ранних металлов ZR и HF также распространены интерстициальные карбидные лиганды. Одним из примеров является ZR 6 CCL 12 . [ 7 ] Один тип структуры имеет шесть галогенидов терминала и 12 галогеников с краями. Этот мотив иллюстрируется хлоридом вольфрама (III) , [TA 6 CL 18 ] 4− , [ 8 ] Другая общая структура имеет шесть терминальных галогенидов и 8 галогенидов, например, MO 6 Cl 14 2− .
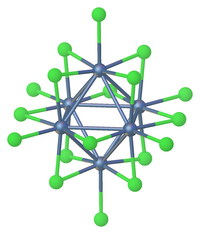
Многие из ранних металлических кластеров могут быть подготовлены только тогда, когда они включают интерстициальные атомы.
С точки зрения истории, Линус Полинг показал, что « Mocl 2 » состоял из MO 6 октаэдры. Ф. Альберт Коттон установил, что « recl 3 » на самом деле функционирует субъединицы кластера RE 3 CL 9 , которые могут быть преобразованы в множество аддуктов, не разбивая повторные связи. Поскольку это соединение является диамагнитным и не парамагнитным, - связывания Rhenium это двойные связи , а не отдельные связи. В твердом состоянии. Дополнительное мостование происходит между соседями, и когда это соединение растворяется в соляной кислоте A RE 3 CL 12 3− сложные формы. Примером тетраноклеарного комплекса является гексадекаметокситетратунгстен W 4 (OCH 3 ) 12 с вольфрамовыми отдельными связями. Связанная группа кластеров с общей формулой M x Mo 6 x 8, таких как PBMO 6 с 8 . Эти кластеры сульфидо называются фазами шеверела .
Кластеры Fe-S в биологии
[ редактировать ]В 1970 -х годах было продемонстрировано, что ферредоксин содержит Fe 4 S 4 кластеры , а более позднее нитрогеназа , как было показано, содержит отличительный активный сайт MOFE 7 S 9 . [ 10 ] Кластеры Fe-S в основном служат окислительно-восстановительными кофакторами, но некоторые имеют каталитическую функцию. В области бионорганической химии также были идентифицированы различные кластеры Fe-S, которые имеют CO в качестве лигандов.


Femoco , активное место большинства нитрогеназ , оснащено кластером Fe 7 Mos 9 C. [ 11 ]
Zintl кластеры
[ редактировать ]Соединения Zintl имеют обнаженные анионные кластеры, которые генерируются уменьшением тяжелой основной группы P , в основном металлов или полуметаллов, с щелочными металлами, часто в качестве раствора в безводной жидкости аммиака или этилендиамина . [ 12 ] Примеры анионов Zintl являются [BI 3 ] 3− , [SN 9 ] 4− , [PB 9 ] 4− и [SB 7 ] 3− . [ 13 ] Хотя эти виды называются «обнаженными кластерами», они обычно тесно связаны с катионами щелочных металлов. Некоторые примеры были выделены с использованием криптатных комплексов катиона щелочных металлов, например, [PB 10 ] 2− Анион, который имеет ограниченную квадратную антипризматическую форму. [ 14 ] Согласно правилам Уэйда (2n+2) количество кластерных электронов составляет 22 и, следовательно, кластер Closo . Соединение готовится из окисления K 4 PB 9 [ 15 ] Ау + В PPH 3 AUCL (реакцией тетрахлоруаральной кислоты и трифенилфосфина ) в этилена-диамине с 2,2,2-криптом . Этот тип кластера был уже известен как эндоэдральный ni@pb 10 2− (Клетка содержит один атом никеля ). Icosaheedral Tin SN Cluster 12 2− или Станнасферен Анион - это еще одна закрытая структура оболочки (но не изолированная) с фотоэлектронной спектроскопией . [ 16 ] [ 17 ] С внутренним диаметром 6,1 Ångstrom , он имеет сопоставимый размер для фуллерина и должен быть способен содержать небольшие атомы таким же образом, как эндоэдральные фуллерены , и действительно существует кластер SN 12 , который содержит атом IR: [ir@sn 12 ] 3− . [ 18 ]
Металлоидные кластеры
[ редактировать ]Кластеры Elementoid представляют собой лиганд-стабилизированные кластеры металлических соединений, которые обладают более прямым элементом, чем контакты с лигацией элементов. Примеры структурно охарактеризованных кластеров оснащены лигандом, стабилизированными ядрами AL 77 , GA 84 и PD 145 . [ 19 ]
Интерметаллоидные кластеры
[ редактировать ]Эти кластеры состоят как минимум из двух разных (полу) металлических элементов и обладают более прямым металлическим металлом, чем контакты с металлом. Суффикс «OID» определяет, что такие кластеры обладают в молекулярной масштабе, атома, которые появляются в объемных интерметаллических соединениях с высокими координационными количествами атомов, например, например, в фазе лав и пышных фаз. [ 20 ] Без лиганд интерметаллоидные кластеры включают также эндоэдрально заполненные кластерами Zintl. [ 13 ] [ 21 ] Синонимом стабилизированных лигандами интерметаллоидных кластеров является «молекулярный сплав». Кластеры появляются в виде дискретных единиц в интерметаллических соединениях, отделенных друг от друга электропозитивными атомами, такими как [sn @cu 12 @sn 20 ] 12− , [ 20 ] как растворимые ионы [как @ni 12 @as 20 ] 3− [ 13 ] или в виде лигандных молекул, таких как [MO (ZnCh 3 ) 9 (ZnCP*) 3 ]. [ 22 ]
Ссылки
[ редактировать ]- ^ Умена, Ясуфуми; Кавакам, Кейсуке; Шен, Цзянь-Рен; Камия, Нобуо (май 2011 г.). «Кристаллическая структура кислорода, развивающейся фотосистемы II при разрешении 1,9 Å» (PDF) . Природа . 473 (7345): 55–60. Bibcode : 2011natur.473 ... 55U . doi : 10.1038/nature09913 . PMID 21499260 . S2CID 205224374 .
- ^ Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2 -е изд.). Баттерворт-Хейнеманн . ISBN 978-0-08-037941-8 .
- ^ Д. Сейферт (1976). Химия углеродных алкилидинетрикобальт неакарбонильных кластерных комплексов . Достижения в области органометаллической химии. Тол. 14. С. 97–144. doi : 10.1016/s0065-3055 (08) 60650-4 . ISBN 9780120311149 .
- ^ А. Бино; М. Ардон; И. Маор; М. Кафтори; З. Дори (1976). [MOT 3 (OAC) 6 (Ch 3 CH 2 O) 2 (H 2 O) 3 ] 2+ и другие новые продукты реакции между гексакарбонильной и уксусной кислотой молибдена ». J. Am. Chem. Soc. 98 (22): 7093–7095. DOI : 10.1021/JA00438A067 .
- ^ А. Бино; FA хлопок; З. Дори (1981). «Новая водная химия органометаллических, тринуклеарных кластерных соединений молибдена». J. Am. Химический Соц 103 : 243–244. doi : 10.1021/ja00391a068 .
- ^ FA хлопок; З. Дори; М. Капон; Сделай Марлер; Г.М. Рейснер; W. Schwotzer; М. Шайя (1985). «Первые кластерные соединения с алкилидином тритунгстена (IV): препарат, структура и свойства [W 3 O (CCH 3 ) (O 2 CCH 3 ) 6 (H 2 O) 3 ] Br 2 *2H 2 O». Inorg. Химический 24 : 4381–4384. doi : 10.1021/ic00219a036 .
- ^ Arndt Simon "Металлические кластеры Inside Out" Фил. Транс. R. Soc. 2010 Vol. 368, 1285-1299. два : 10.1098/rsta.2009.0271
- ^ Koknat, FW; Марко, DJ "Tetradecachlohorohorohorohohofatantalum octabydrate, ta 6 cl 14 . 8h 2 o "Неорганические синтезы, 2004, том 34, с. 187-191. ISBN 0-471-64750-0 . (описывает NA 4 TA 6 CL 18 )
- ^ Джейкобсон, Роберт А.; Thaxton, Charles B. (1971). «Кристаллическая структура H 2 (TA 6 Cl 18 ) (H 2 O) 6 ». Неорганическая химия . 10 (7): 1460–1463. doi : 10.1021/ic50101a029 .
- ^ «Металлические кластеры в химии» P. Braunstein, La Oro, Pr Raithby, Eds Wiley-Vch, Weinheim, 1999. ISBN 3-527-29549-6 .
- ^ Ли, Сонни С.; Вот, Уэйн; Холм, RH (2014). «Развития в биомиметической химии кластеров кубинского типа и более высокого ядерного железа и сульфур» . Химические обзоры . 114 (7): 3579–3600. doi : 10.1021/cr4004067 . PMC 3982595 . PMID 24410527 .
- ^ С. Шарп; Ф. Краус; S. Stegmaier; А. Шир; TF Fässler (2011). «Гомоатомные ионы Zintl, соединения клетки и интерметаллоидный кластер из элементов группы 14 и группы 15». Applied Chemistry International Edition . 50 (16): 3630–3670. Doi : 10.1002/ani.201001630 . PMID 21455921 .
- ^ Jump up to: а беременный в Zintl Ions: принципы и последние разработки , серия книг: структура и связь . TF Fässler (ed.), Том 140, Springer, Heidelberg, 2011 doi : 10.1007/978-3-642-21181-2
- ^ A. Spiefsmann; SFUT 45; TF Workler (2006). "Zintl Ion [PB 10 ] 2− : Редкий пример гомоатомического кластера Closo ». Angewandte Chemie International Edition . 45 (21): 3459–3462. DOI : 10.1002/anie.200503916 . PMID 16622888 .
- ^ сам построенный нагревающим элементом калия и свинец при 350 ° C
- ^ Оловянные частицы генерируются как k + SN 12 2− путем лазерного испарения из твердой олова, содержащей 15% калия и выделенного масс -спектрометром перед анализом
- ^ Li-Feng Cui; Xin Huang; Lei-Ming Wang; Dmitry Yu. Zubarev; Alexander I. Boldyrev; Jun Li; Lai-Sheng Wang (2006). "Sn 12 2− : Stannaspherene ". J. Am. Chem. Soc. 128 (26): 8390–8391. DOI : 10.1021/JA062052F . PMID 16802791 .
- ^ J.- Q. Ван; S. Stegmaier; Б. Вахл; TF Fässler (2010). "Пошаговый синтез эндоэдрального станасферена [ir@sn 12 ] 3− через анион с закрытым кластером [SN 9 IR (COD)] 3− ". Chem. Eur. J. 16 (6): 3532–3552. doi : 10.1002/chem.200902815 . PMID 20077544 .
- ^ А. Шнепф; H. Schnöckel (2002). «Металлоидный алюминий и кластеры галлия: модификации элементов в молекулярном масштабе?». Angewandte Chemie International Edition . 114 (19): 1793–1798. doi : 10.1002/1521-3773 (20021004) 41:19 <3532 :: AID-ANIE3532> 3.0.CO; 2-4 . PMID 12370894 .
- ^ Jump up to: а беременный S. Stegmaier; TF Fässler (2011). "Бронзовая матришка - дискретный интерметаллоидный кластер [sn @cu 12 @sn 20 ] 12− В тройных фазах A 12 Cu 12 SN 21 (A = Na, K) ». J. Am. Chem. Soc. 133 (49): 19758–19768. DOI : 10.1021/ja205934p . PMID 21961732 .
- ^ TF Fässler; SD Hoffmann (2004). «Эндоэдральные ионы Zintl: интерметаллоидный кластер». Applied Chemistry International Edition . 116 (46): 6400–6406. Doi : 10.1002/anie.200460427 . PMID 15505810 .
- ^ Ра Фишер; и др. (2008). «Двенадцать одноэлектронных лигандов, координирующих один металлический центр: структура и связь [MO (ZnCh 3 ) 9 (Zncp*) 3 ]». Angewandte Chemie International Edition . 47 (47): 9150–9154. doi : 10.1002/anie.200802811 . PMID 18846517 .