Анаплазма фагоцитофилум
| Анаплазма фагоцитофилум | |
|---|---|
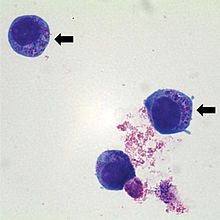 | |
| человека HL60 Клетки , содержащие Anaplasma phagocytophilum (указаны стрелками), которые при окраске красителем Райта-Гимзы представляют собой базофильные внутрицитоплазматические включения. | |
| Научная классификация | |
| Домен: | Бактерии |
| Тип: | Псевдомонадота |
| Сорт: | Альфапротеобактерии |
| Заказ: | Риккетсиалесы |
| Семья: | Эрлихиеевые |
| Род: | Анаплазма |
| Разновидность: | А. фагоцитофилум |
| Биномиальное имя | |
| Анаплазма фагоцитофилум (Фогги, 1949) Дамлер и др. 2001 г. [1] | |
| Синонимы | |
Риккетсия фагоцитофила овис | |
Anaplasma phagocytophilum (ранее Ehrlichia phagocytophilum ) [2] Грамотрицательная бактерия, необычная по своему тропизму к нейтрофилам . Он вызывает анаплазмоз у овец и крупного рогатого скота, также известный как клещевая лихорадка и пастбищная лихорадка , а также вызывает зоонозное заболевание человека - гранулоцитарный анаплазмоз . [3]
A. phagocytophilum — грамотрицательная облигатная бактерия нейтрофилов. Он вызывает у человека гранулоцитарный анаплазмоз, который представляет собой клещевое риккетсиозное заболевание. Поскольку эта бактерия проникает в нейтрофилы, она обладает уникальным адаптационным и патогенетическим механизмом. [4]
Биология
[ редактировать ]A. phagocytophilum — небольшая облигатная внутриклеточная бактерия с грамотрицательной клеточной стенкой. Его размер составляет 0,2–1,0 мкм, и в нем отсутствует механизм биосинтеза липополисахаридов. Бактерия сначала обитает в ранней эндосоме , где приобретает питательные вещества для бинарного деления и разрастается в небольшие группы, называемые морулами. Эта бактерия предпочитает расти внутри миелоидных или гранулоцитарных клеток. [4]
Хозяева
[ редактировать ]Хозяева включают козу , крупный рогатый скот , лошадь и собаку . Были подозрения на заражение крупного рогатого скота, но они были впервые подтверждены только Nieder et al. 2012. [5]
Роль в заболеваниях человека
[ редактировать ]A. phagocytophilum вызывает гранулоцитарный анаплазмоз человека (HGA). Это заболевание было впервые выявлено в 1990 году, хотя было известно, что этот возбудитель вызывает ветеринарные заболевания с 1932 года. С 1990 года заболеваемость HGA возросла, и теперь он признан в Европе. Впервые это заболевание было выявлено у пациента из Висконсина, который умер от тяжелой лихорадки через две недели после укуса клеща. На последней стадии инфекции внутри нейтрофилов крови была обнаружена группа мелких бактерий. Другие симптомы включают лихорадку, головную боль, отсутствие кожной сыпи, лейкопению , тромбоцитопению и легкое повреждение печени. [4]
Клинические признаки у животных
[ редактировать ]Заболевание мультисистемное, но наиболее тяжелыми изменениями являются анемия и лейкопения . Этот организм вызывает хромоту , которую можно спутать с симптомами болезни Лайма , другого клещевого заболевания. Это трансмиссивное зоонозное заболевание , морулу которого можно визуализировать в нейтрофилах (тип лейкоцитов) периферической крови и синовиальной жидкости. Это может вызвать летаргию , атаксию , потерю аппетита , а также слабость или боль в конечностях. [3]
Бактериальный механизм
[ редактировать ]A. phagocytophilum связывается с фукозилированными и сиалированными каркасными белками на поверхности нейтрофилов и гранулоцитов. Известно, что аппарат секреции типа IV помогает в переносе молекул между бактерией и хозяином. Наиболее изученным лигандом является PSGL-1 ( CD162 ). Бактерия прикрепляется к PSGL-1 (CD162) посредством основного поверхностного белка-2 массой 44 кДа (Msp2). После попадания бактерии в клетку эндосома прекращает созревание и не накапливает маркеры поздних эндосом или фаголизосом . Благодаря этому вакуоль не закисляется и не сливается с лизосомами . Затем A. phagocytophilum делится до лизиса клеток или до тех пор, пока бактерии не уйдут, чтобы заразить другие клетки. [4]
Эта бактерия обладает способностью влиять на нейтрофилы, изменяя их функцию. Он может пережить первую встречу с клеткой-хозяином за счет детоксикации супероксида, образующегося в результате сборки оксидазы нейтрофильных фагоцитов . Он также нарушает нормальные функции нейтрофилов, такие как адгезия эндотелиальных клеток, трансмиграция, моторику, дегрануляцию, респираторный взрыв и фагоцитоз. [4] Это вызывает увеличение секреции IL-8 , хемоаттрактанта, усиливающего фагоцитоз нейтрофилов. Целью этого является увеличение бактериальной диссеминации в нейтрофилах. [6]
Лабораторная диагностика
[ редактировать ]Эти тесты можно провести для выявления инфекции A. phagocytophilum :
- Непрямой иммунофлуоресцентный анализ является основным тестом, используемым для выявления инфекции. Образцы сыворотки острой фазы и фазы выздоровления можно оценить на предмет четырехкратного изменения титра антител к A. phagocytophilum .
- Внутриклеточные включения (морулы) визуализируются в гранулоцитах на по Райту или Гимзе . мазках крови, окрашенных
- используются анализы полимеразной цепной реакции Для обнаружения ДНК A. phagocytophilum . [7]
Антибиотикотерапия
[ редактировать ]Пациенты с HGA проходят терапию доксициклином по 100 мг два раза в день до снижения лихорадки в течение как минимум 3 дней. Этот препарат оказался наиболее полезным для пациентов, инфицированных бактериями. Некоторые другие препараты тетрациклина также эффективны. В целом, пациенты с симптомами HGA и необъяснимой лихорадкой после заражения клещом должны получать эмпирическую терапию доксициклином, пока не проведены диагностические тесты, особенно если у них наблюдается лейкопения и/или тромбоцитопения . [7]
такие антибиотики, как окситетрациклин , сульфаметазин, сульфадимидин , доксициклин и триметоприм - сульфонамиды . У животных применялись [3]
Ссылки
[ редактировать ]- ^ Страница Анаплазмы на lpsn.dsmz.de
- ^ Дамлер Дж.С., Барбет А.Ф., Беккер К.П. и др. (2001). «Реорганизация родов семейств Rickettsiaceae и Anaplasmataceae в отряд Rickettsiales: объединение некоторых видов Ehrlichia с Anaplasma, Cowdria с Ehrlichia и Ehrlichia с Neorickettsia, описания шести новых видовых комбинаций и обозначение Ehrlichia equi и «агента HGE» как субъективных. синонимы Ehrlichia phagocytophila» . Межд. Дж. Сист. Эвол. Микробиол . 51 (Часть 6): 2145–65. дои : 10.1099/00207713-51-6-2145 . ПМИД 11760958 .
- ^ Jump up to: а б с Клещевая лихорадка , рассмотренная и опубликованная WikiVet , по состоянию на 12 октября 2011 г.
- ^ Jump up to: а б с д и Дамлер Дж.С., Чой К.С., Гарсия-Гарсия Дж.К. и др. (декабрь 2005 г.). «Гранулоцитарный анаплазмоз человека и Anaplasma phagocytophilum » . Возникающая инфекция. Дис . 11 (12): 1828–34. дои : 10.3201/eid1112.050898 . ПМК 3367650 . ПМИД 16485466 .
- ^ Браун, Венди С.; Барбет, Энтони Ф. (15 февраля 2016 г.). «Стойкие инфекции и иммунитет жвачных животных к бактериям, передающимся членистоногими, семейства Anaplasmataceae». Ежегодный обзор биологических наук о животных . 4 (1). Годовые обзоры : 177–197. doi : 10.1146/annurev-animal-022513-114206 . ISSN 2165-8102 . ПМИД 26734888 .
- ^ Томас В., Фикриг Э. (июль 2007 г.). « Anaplasma phagocytophilum специфически индуцирует фосфорилирование тирозина ROCK1 во время инфекции». Клетка. Микробиол . 9 (7): 1730–7. дои : 10.1111/j.1462-5822.2007.00908.x . ПМИД 17346310 . S2CID 20043230 .
- ^ Jump up to: а б «Информация об анаплазмозе человека для медицинских работников: диагностические тесты» . Болезни . Департамент здравоохранения Миннесоты. Архивировано из оригинала 13 февраля 2019 г. Проверено 27 апреля 2011 г.
Внешние ссылки
[ редактировать ]- Anaplasma phagocytophilum HZ Страница генома
- Анаплазма + фагоцитофилум Национальной медицинской библиотеки США по медицинским предметным рубрикам (MeSH)
- Чжан Л., Лю Ю, Ни Д. и др. (ноябрь 2008 г.). «Внутрибольничная передача гранулоцитарного анаплазмоза человека в Китае» . ДЖАМА . 300 (19): 2263–70. дои : 10.1001/jama.2008.626 . ПМИД 19017912 .