ERCC4
| ERCC4 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | ERCC4 , ERCC11, FANCQ, RAD1, XPF, XFEPS, группа перекрестной комплементации эксцизионной репарации 4, эксцизионная репарация 4 ERCC, каталитическая субъединица эндонуклеазы | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 133520 ; МГИ : 1354163 ; Гомологен : 3836 ; Генные карты : ERCC4 ; OMA : ERCC4 — ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
ERCC4 представляет собой белок , называемый эндонуклеазой репарации ДНК XPF , который у человека кодируется ERCC4 геном . Вместе с ERCC1 ERCC4 образует ферментный комплекс ERCC1-XPF, который участвует в репарации ДНК и рекомбинации ДНК . [5] [6]
Фермент нуклеаза ERCC1-XPF разрезает определенные структуры ДНК. Многие аспекты этих двух генных продуктов описаны здесь вместе, поскольку они являются партнерами во время репарации ДНК. Нуклеаза ERCC1-XPF играет важную роль в пути эксцизионной репарации нуклеотидов ДНК (NER). Нуклеаза ERCC1-XPF также участвует в восстановлении двухцепочечных разрывов ДНК, а также в восстановлении повреждений «сшивки», которые вредно связывают две цепи ДНК.
Клетки с инвалидизирующими мутациями в ERCC4 более чувствительны, чем обычно, к определенным агентам, повреждающим ДНК, включая ультрафиолетовое излучение и химические вещества, которые вызывают сшивание между нитями ДНК. Генно-инженерные мыши с инвалидизирующими мутациями в ERCC4 также имеют дефекты репарации ДНК, сопровождающиеся физиологическими изменениями, вызванными метаболическим стрессом, которые приводят к преждевременному старению. [7] Полная делеция ERCC4 несовместима с жизнеспособностью мышей, и не было обнаружено ни одного человека с полной (гомозиготной) делецией ERCC4 . Редкие люди в человеческой популяции имеют наследственные мутации, которые нарушают функцию ERCC4 . Когда нормальные гены отсутствуют, эти мутации могут привести к синдромам человека, включая пигментную ксеродермию , синдром Кокейна и анемию Фанкони .
ERCC1 и ERCC4 — это названия генов человека, а Ercc1 и Ercc4 — аналогичные названия генов млекопитающих. Подобные гены со схожими функциями обнаружены у всех эукариотических организмов.
Ген
[ редактировать ]человека Ген ERCC4 может корректировать дефект репарации ДНК в специфических чувствительных к ультрафиолетовому свету (УФ) мутантных клеточных линиях, полученных из клеток яичника китайского хомячка. [8] Были выделены множественные независимые группы комплементации клеток яичника китайского хомячка (СНО). [9] и этот ген восстановил устойчивость к УФ-излучению клеток группы комплементации 4. Отражая этот метод межвидовой генетической комплементации, ген был назван «Кросс-комплементирующая эксцизионная репарация 4». [10]
человека Ген ERCC4 кодирует белок XPF из 916 аминокислот с молекулярной массой около 104 000 дальтон.
Гены, подобные ERCC4 с эквивалентными функциями (ортологами), обнаружены и в геномах других эукариот. Некоторые из наиболее изученных ортологов генов включают RAD1 у почкующихся дрожжей Saccharomyces cerevisiae и rad16+ у делящихся дрожжей Schizosaccharomyces pombe .
Белок
[ редактировать ]
Одна молекула ERCC1 и одна молекула XPF связываются вместе, образуя гетеродимер ERCC1-XPF, который представляет собой активную нуклеазную форму фермента. В гетеродимере ERCC1-XPF ERCC1 опосредует ДНК- и белок-белковые взаимодействия. XPF обеспечивает активный центр эндонуклеазы и участвует в связывании ДНК и дополнительных белок-белковых взаимодействиях. [8]
Белок ERCC4/XPF состоит из двух консервативных участков, разделенных менее консервативным участком посередине. N-концевая область гомологична нескольким консервативным доменам ДНК-хеликаз, принадлежащих к суперсемейству II, хотя XPF не является ДНК-хеликазой. [11] С-концевая область XPF включает остатки активного центра нуклеазной активности. [12] (Рисунок 1) .
Большая часть белка ERCC1 связана на уровне последовательности с С-концом белка XPF. [13] но остатки в нуклеазном домене отсутствуют. ДНК-связывающий домен «спираль-шпилька-спираль» на С-конце каждого белка.
По первичной последовательности и структурному сходству белков нуклеаза ERCC1-XPF является членом более широкого семейства структурно-специфичных ДНК-нуклеаз, состоящего из двух субъединиц. К таким нуклеазам относится, например, нуклеаза MUS81-EME1.
Структурно-специфическая нуклеаза
[ редактировать ]
Комплекс ERCC1-XPF представляет собой структурно-специфическую эндонуклеазу. ERCC1-XPF не разрезает ДНК, которая является исключительно одноцепочечной или двухцепочечной, но расщепляет фосфодиэфирный остов ДНК конкретно в местах соединения двухцепочечной и одноцепочечной ДНК. Он вводит разрез в двухцепочечной ДНК на 5'-стороне такого соединения, примерно на расстоянии двух нуклеотидов. [14] (Рисунок 2) . Эта структурная специфичность была первоначально продемонстрирована для RAD10-RAD1, дрожжевых ортологов ERCC1 и XPF. [15]
Гидрофобные мотивы спираль-шпилька-спираль в С-концевых областях ERCC1 и XPF взаимодействуют, способствуя димеризации двух белков. [16] [17] В отсутствие димеризации каталитическая активность отсутствует. Действительно, хотя каталитический домен находится внутри XPF, а ERCC1 каталитически неактивен, ERCC1 необходим для активности комплекса.
Было предложено несколько моделей связывания ERCC1-XPF с ДНК, основанных на частичных структурах соответствующих фрагментов белка с атомным разрешением. [16] Связывание ДНК, опосредованное доменами спираль-шпилька-спираль доменов ERCC1 и XPF, позиционирует гетеродимер на стыке двухцепочечной и одноцепочечной ДНК.
Нуклеотидная эксцизионная репарация (NER)
[ редактировать ]Во время эксцизионной репарации нуклеотидов несколько белковых комплексов взаимодействуют, чтобы распознать поврежденную ДНК и локально разделить спираль ДНК на небольшое расстояние по обе стороны от места повреждения ДНК. Нуклеаза ERCC1-XPF разрезает поврежденную цепь ДНК на 5'-стороне повреждения. [14] Во время NER белок ERCC1 взаимодействует с белком XPA для координации связывания ДНК и белка.
Восстановление двухцепочечного разрыва ДНК (DSB)
[ редактировать ]Клетки млекопитающих с мутантным ERCC1-XPF умеренно более чувствительны, чем нормальные клетки, к агентам (таким как ионизирующее излучение), которые вызывают двухцепочечные разрывы ДНК. [18] [19] Конкретные пути как репарации гомологичной рекомбинации, так и негомологичного соединения концов зависят от функции ERCC1-XPF. [20] [21] Соответствующей активностью ERCC1-XPF для обоих типов репарации двухцепочечных разрывов является способность удалять негомологичные 3'-одноцепочечные хвосты с концов ДНК перед повторным соединением. Эта активность необходима во время одноцепочечного отжига гомологичной рекомбинации. Обрезка 3'-одноцепочечных хвостов также необходима на механически отличном подпути негомологичного соединения концов, независимом от Ku-белков. [22] [19] Гомологичная интеграция ДНК, важный метод генетических манипуляций, зависит от функции ERCC1-XPF в клетке-хозяине. [23]
Восстановление межпрядных связей
[ редактировать ]Клетки млекопитающих, несущие мутации в ERCC1 или XPF, особенно чувствительны к агентам, вызывающим межцепочечные сшивки ДНК (ICL). [24] Межнитевые поперечные связи блокируют прогресс репликации ДНК, а структуры на заблокированных вилках репликации ДНК обеспечивают субстраты для расщепления с помощью ERCC1-XPF. [20] [25] Надрезы могут быть сделаны по обе стороны от сшивки на одной цепи ДНК, чтобы отсоединить сшивку и инициировать восстановление. Альтернативно, двухцепочечный разрыв может произойти в ДНК рядом с ICL, и последующая репарация гомологичной рекомбинации может включать действие ERCC1-XPF. Хотя ERCC1-XPF не единственная задействованная нуклеаза, она необходима для репарации ICL во время нескольких фаз клеточного цикла. [26] [27]
Клиническое значение
[ редактировать ]Пигментная ксеродерма (XP)
[ редактировать ]Некоторые люди с редким наследственным синдромом пигментной ксеродермии имеют мутации в ERCC4. Эти пациенты относятся к группе F комплементации XP (XP-F). Диагностическими признаками ХР являются сухая шелушащаяся кожа, аномальная пигментация кожи на участках, подвергающихся воздействию солнца, и сильная фоточувствительность, что сопровождается более чем 1000-кратным увеличением риска развития рака кожи, вызванного УФ-излучением. [5]
Синдром Кокейна (CS)
[ редактировать ]У большинства пациентов XP-F наблюдаются умеренные симптомы XP, но у некоторых наблюдаются дополнительные симптомы синдрома Коккейна. [28] Пациенты с синдромом Коккейна (CS) проявляют светочувствительность, а также дефекты развития и неврологические симптомы. [5] [7]
Мутации в гене ERCC4 могут привести к очень редкому синдрому XF-E. [29] У этих пациентов наблюдаются характеристики ХР и КС, а также дополнительные неврологические, гепатобилиарные, скелетно-мышечные и кроветворные симптомы.
Анемия Фанкони
[ редактировать ]У нескольких пациентов с симптомами анемии Фанкони (АФ) наблюдаются причинные мутации в гене ERCC4. Анемия Фанкони — сложное заболевание, сопровождающееся выраженными нарушениями кроветворения. Характерной особенностью FA является повышенная чувствительность к агентам, вызывающим межцепочечные сшивки ДНК. Пациенты с ФА с мутациями ERCC4 были отнесены к группе Q с комплементарной анемией Фанкони (FANCQ). [28] [30]
ERCC4 (XPF) в нормальной толстой кишке
[ редактировать ]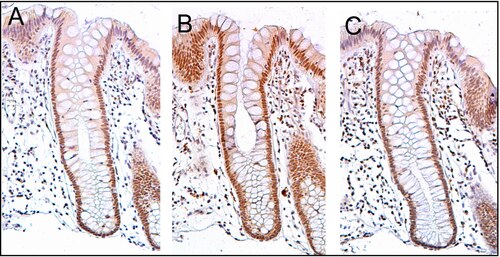
ERCC4 (XPF) обычно экспрессируется на высоком уровне в ядрах клеток внутренней поверхности толстой кишки ( см. изображение, панель C). Внутренняя поверхность толстой кишки выстлана простым столбчатым эпителием с инвагинациями . Инвагинации называются кишечными железами или криптами толстой кишки. Крипты толстой кишки имеют форму микроскопических толстостенных пробирок с центральным отверстием по всей длине трубки ( просвет крипты ). Крипты имеют длину от 75 до 110 ячеек. Репарация ДНК, включающая высокую экспрессию белков ERCC4 (XPF), PMS2 и ERCC1, по-видимому, очень активна в криптах толстой кишки в нормальном, ненеопластическом эпителии толстой кишки.
Клетки образуются в основании крипт и мигрируют вверх вдоль оси крипт, а через несколько дней попадают в просвет толстой кишки . [32] находится от 5 до 6 стволовых клеток . В основании крипт [32] среднего человека имеется около 10 миллионов крипт На внутренней поверхности толстой кишки . [31] Если стволовые клетки в основании крипты экспрессируют ERCC4 (XPF), обычно все несколько тысяч клеток крипты также будут экспрессировать ERCC4 (XPF). На это указывает коричневый цвет, видимый при иммуноокрашивании ERCC4 (XPF) почти во всех клетках крипты на панели C изображения в этом разделе. Подобная экспрессия PMS2 и ERCC1 происходит в тысячах клеток в каждой нормальной крипте толстой кишки.
Срез ткани на изображении, показанном здесь, также был для окрашивания докрашен гематоксилином ДНК в ядрах в сине-серый цвет. Ядра клеток собственной пластинки , клеток, которые находятся ниже и окружают эпителиальные крипты, в основном имеют гематоксилиновый сине-серый цвет и имеют низкую экспрессию PMS2, ERCC1 или ERCC4 (XPF). Кроме того, клетки в самых верхушках крипт, окрашенные на PMS2 (панель A) или ERCC4 (XPF) (панель C), имеют низкие уровни этих белков репарации ДНК, поэтому такие клетки также демонстрируют сине-серое окрашивание ДНК. [31]
Дефицит ERCC4 (XPF) в эпителии толстой кишки, прилегающем к раку и внутри него.
[ редактировать ]
ERCC4 (XPF) дефицитен примерно в 55% случаев рака толстой кишки и примерно в 40% крипт толстой кишки в эпителии в пределах 10 см, прилегающем к раку (в дефектах полей , из которых, вероятно, возник рак). [31] Когда ERCC4 (XPF) снижается в криптах толстой кишки при полевом дефекте, это чаще всего связано со снижением экспрессии ферментов репарации ДНК ERCC1 и PMS2, как показано на изображении в этом разделе. Дефицит ERCC1 (XPF) в эпителии толстой кишки, по-видимому, обусловлен эпигенетической репрессией. [31] Дефицит ERCC4 (XPF) приведет к снижению восстановления повреждений ДНК. Как указали Харпер и Элледж, [33] Дефекты способности правильно реагировать на повреждения ДНК и восстанавливать их лежат в основе многих форм рака. Частое эпигенетическое снижение ERCC4 (XPF) при полевых дефектах, окружающих рак толстой кишки, а также при раке (наряду с эпигенетическим снижением ERCC1 и PMS2) указывает на то, что такое снижение часто может играть центральную роль в прогрессировании рака толстой кишки.
Хотя эпигенетическое снижение экспрессии ERCC4 (XPF) часто встречается при раке толстой кишки человека, мутации ERCC4 (XPF) у людей встречаются редко. [34] Однако мутация в ERCC4 (XPF) делает пациентов склонными к раку кожи. [34] Наследственный полиморфизм ERCC4 (XPF), по-видимому, также важен при раке молочной железы. [35] Эти нечастые мутационные изменения подчеркивают вероятную роль дефицита ERCC4 (XPF) в прогрессировании рака.
Примечания
[ редактировать ]Версия этой статьи 2015 года была обновлена внешним экспертом в рамках модели двойной публикации. Соответствующая академическая рецензируемая статья была опубликована в журнале Gene и может цитироваться как: Мандира Манандхар, Карен С. Булвар, Ричард Д. Вуд (12 июня 2015 г.). «Гены и генные продукты ERCC1 и ERCC4 (XPF)» . Джин . Серия обзоров Gene Wiki. 569 (2): 153–161. дои : 10.1016/J.GENE.2015.06.026 . ISSN 0378-1119 . ПМЦ 4536074 . ПМИД 26074087 . Викиданные Q35663361 . |
Ссылки
[ редактировать ]- ^ Jump up to: а б с GRCh38: Версия Ensembl 89: ENSG00000175595 – Ensembl , май 2017 г.
- ^ Jump up to: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000022545 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Jump up to: а б с Фридберг Э.К., Уокер Г.К., Сиде В., Вуд Р.Д., Шульц Р.А., Элленбергер Т. (2006). Репарация ДНК и мутагенез . АСМ Пресс. ISBN 978-1555813192 .
- ^ «Ген Энтрез: перекрестно-комплементирующий дефицит эксцизионной репарации ERCC4 у грызунов, группа комплементации 4» .
- ^ Jump up to: а б Грегг С.К., Робинсон А.Р., Нидернхофер Л.Дж. (июль 2011 г.). «Физиологические последствия дефектов эндонуклеазы репарации ДНК ERCC1-XPF» . Восстановление ДНК . 10 (7): 781–91. дои : 10.1016/j.dnarep.2011.04.026 . ПМК 3139823 . ПМИД 21612988 .
- ^ Jump up to: а б Вестервельд А., Хоймейкерс Дж.Х., ван Дуин М., де Вит Дж., Одейк Х., Пастинк А., Вуд Р.Д., Бутсма Д. (1984). «Молекулярное клонирование гена репарации ДНК человека». Природа . 310 (5976): 425–9. Бибкод : 1984Natur.310..425W . дои : 10.1038/310425a0 . ПМИД 6462228 . S2CID 4336902 .
- ^ Буш Д., Грейнер С., Льюис К., Форд Р., Адэр Г., Томпсон Л. (сентябрь 1989 г.). «Краткое описание групп комплементации мутантов клеток CHO, чувствительных к УФ-излучению, выделенных путем крупномасштабного скрининга». Мутагенез . 4 (5): 349–54. дои : 10.1093/mutage/4.5.349 . ПМИД 2687628 .
- ^ Брукман К.В., Ламердин Дж.Э., Телен М.П., Хван М., Рирдон Дж.Т., Санкар А., Чжоу ЗК, Уолтер К.А., Пэррис К.Н., Томпсон Л.Х. (ноябрь 1996 г.). «ERCC4 (XPF) кодирует белок эксцизионной репарации нуклеотидов человека с гомологами эукариотической рекомбинации» . Молекулярная и клеточная биология . 16 (11): 6553–62. дои : 10.1128/mcb.16.11.6553 . ПМК 231657 . ПМИД 8887684 .
- ^ Сгурос Дж., Гайяр П.Х., Вуд Р.Д. (март 1999 г.). «Взаимосвязь между семейством нуклеаз репарации/рекомбинации ДНК и архейными хеликазами». Тенденции биохимических наук . 24 (3): 95–7. дои : 10.1016/s0968-0004(99)01355-9 . ПМИД 10203755 .
- ^ Энцлин Дж. Х., Шерер О. Д. (апрель 2002 г.). «Активный сайт эндонуклеазы репарации ДНК XPF-ERCC1 образует высококонсервативный нуклеазный мотив» . Журнал ЭМБО . 21 (8): 2045–53. дои : 10.1093/emboj/21.8.2045 . ПМК 125967 . ПМИД 11953324 .
- ^ Гайяр П.Х., Вуд Р.Д. (февраль 2001 г.). «Активность отдельных субъединиц ERCC1 и XPF в эксцизионной репарации нуклеотидов ДНК» . Исследования нуклеиновых кислот . 29 (4): 872–9. дои : 10.1093/нар/29.4.872 . ПМК 29621 . ПМИД 11160918 .
- ^ Jump up to: а б Сийберс А.М., де Лаат В.Л., Ариса Р.Р., Биггерстафф М., Вэй Ю.Ф., Моггс Дж.Г., Картер К.С., Шелл Б.К., Эванс Э., де Йонг М.К., Радемейкерс С., де Рой Дж., Джасперс Н.Г., Хоймейкерс Дж.Х., Вуд Р.Д. (сентябрь 1996 г.) ). «Пигментная ксеродерма группы F, вызванная дефектом структурно-специфической эндонуклеазы репарации ДНК». Клетка . 86 (5): 811–22. дои : 10.1016/s0092-8674(00)80155-5 . hdl : 1765/3110 . ПМИД 8797827 . S2CID 12957716 .
- ^ Бардуэлл А.Дж., Бардуэлл Л., Томкинсон А.Е., Фридберг ЕС (сентябрь 1994 г.). «Специфическое расщепление модельных промежуточных продуктов рекомбинации и репарации дрожжевой эндонуклеазой ДНК Rad1-Rad10». Наука . 265 (5181): 2082–5. Бибкод : 1994Sci...265.2082B . дои : 10.1126/science.8091230 . ПМИД 8091230 .
- ^ Jump up to: а б Трипсианес К., Фолкерс Г., Аб Э., Дас Д., Одейк Х., Джасперс Н.Г., Хоймейкерс Дж.Х., Каптейн Р., Боленс Р. (декабрь 2005 г.). «Структура человеческих доменов взаимодействия ERCC1/XPF демонстрирует дополняющую роль двух белков в эксцизионной репарации нуклеотидов». Структура . 13 (12): 1849–1858. дои : 10.1016/j.str.2005.08.014 . hdl : 1874/14818 . ISSN 1633-8413 . ПМИД 16338413 . S2CID 23146316 .
- ^ Фаридуния М, Венк Х, Ковачич Л, Фолкерс Г.Е., Ясперс Н.Г., Каптейн Р., Хоймейкерс Дж.Х., Боленс Р. (август 2015 г.). «Точечная мутация F231L церебро-окуло-фацио-скелетного синдрома в белке репарации ДНК ERCC1 вызывает диссоциацию комплекса ERCC1-XPF» . J Биол Хим . 290 (33): 20541–20555. дои : 10.1074/jbc.M114.635169 . ISSN 1083-351X . ПМЦ 4536458 . ПМИД 26085086 .
- ^ Вуд Р.Д., Бурки Х.Дж., Хьюз М., Поли А. (февраль 1983 г.). «Радиационно-индуцированная летальность и мутация в линии клеток CHO с дефицитом репарации». Международный журнал радиационной биологии и связанных с ней исследований в области физики, химии и медицины . 43 (2): 207–13. дои : 10.1080/09553008314550241 . ПМИД 6600735 .
- ^ Jump up to: а б Ахмад А., Робинсон А.Р., Дуенсинг А., ван Друнен Э., Беверлоо Х.Б., Вайсберг Д.Б., Хасти П., Хоймейкерс Дж.Х., Нидернхофер Л.Дж. (август 2008 г.). «Эндонуклеаза ERCC1-XPF способствует восстановлению двухцепочечных разрывов ДНК» . Молекулярная и клеточная биология . 28 (16): 5082–92. дои : 10.1128/MCB.00293-08 . ПМК 2519706 . ПМИД 18541667 .
- ^ Jump up to: а б Сарджент Р.Г., Ролиг Р.Л., Килберн А.Е., Адэр Г.М., Уилсон Дж.Х., Нэрн Р.С. (ноябрь 1997 г.). «Зависимое от рекомбинации образование делеции в клетках млекопитающих, дефицитных по гену эксцизионной репарации нуклеотидов ERCC1» . Труды Национальной академии наук Соединенных Штатов Америки . 94 (24): 13122–7. Бибкод : 1997PNAS...9413122S . дои : 10.1073/pnas.94.24.13122 . ПМК 24273 . ПМИД 9371810 .
- ^ Аль-Минави А.З., Салех-Гохари Н., Хелледей Т. (январь 2008 г.). «Эндонуклеаза ERCC1/XPF необходима для эффективного одноцепочечного отжига и конверсии генов в клетках млекопитающих» . Исследования нуклеиновых кислот . 36 (1): 1–9. дои : 10.1093/nar/gkm888 . ПМК 2248766 . ПМИД 17962301 .
- ^ Беннардо Н., Ченг А., Хуан Н., Старк Дж. М. (июнь 2008 г.). «Альтернативный-NHEJ — это механически отличный путь восстановления разрывов хромосом млекопитающих» . ПЛОС Генетика . 4 (6): е1000110. дои : 10.1371/journal.pgen.1000110 . ПМК 2430616 . ПМИД 18584027 .
- ^ Нидернхофер Л.Дж., Эссерс Дж., Вида Г., Беверлоо Б., де Вит Дж., Муйтьенс М., Одейк Х., Хоймейкерс Дж.Х., Канаар Р. (ноябрь 2001 г.). «Структурно-специфическая эндонуклеаза Ercc1-Xpf необходима для целевой замены генов в эмбриональных стволовых клетках» . Журнал ЭМБО . 20 (22): 6540–9. дои : 10.1093/emboj/20.22.6540 . ПМК 125716 . ПМИД 11707424 .
- ^ Вуд Р.Д. (июль 2010 г.). «Белки эксцизионной репарации нуклеотидов млекопитающих и восстановление межцепочечных поперечных связей» . Экологический и молекулярный мутагенез . 51 (6): 520–6. Бибкод : 2010EnvMM..51..520W . дои : 10.1002/em.20569 . ПМК 3017513 . ПМИД 20658645 .
- ^ Кляйн Доувел Д., Боонен Р.А., Лонг Д.Т., Шиповска А.А., Рэшле М., Вальтер Дж.К., Книпшеер П. (май 2014 г.). «XPF-ERCC1 действует в расцеплении межцепочечных связей ДНК в сотрудничестве с FANCD2 и FANCP/SLX4» . Молекулярная клетка . 54 (3): 460–71. doi : 10.1016/j.molcel.2014.03.015 . ПМК 5067070 . ПМИД 24726325 .
- ^ Ран Джей-Джей, генеральный директор Adair, Нэрн RS (июль 2010 г.). «Множественные роли ERCC1-XPF в восстановлении межцепочечных поперечных связей у млекопитающих». Экологический и молекулярный мутагенез . 51 (6): 567–81. Бибкод : 2010EnvMM..51..567R . дои : 10.1002/em.20583 . ПМИД 20658648 . S2CID 29240680 .
- ^ Клаусон С., Шерер О.Д., Нидернхофер Л. (октябрь 2013 г.). «Достижения в понимании сложных механизмов восстановления межцепочечных поперечных связей ДНК» . Перспективы Колд-Спринг-Харбор в биологии . 5 (10): а012732. doi : 10.1101/cshperspect.a012732 . ПМК 4123742 . ПМИД 24086043 .
- ^ Jump up to: а б Касияма К, Наказава И, Пильц Д.Т., Го С, Симада М, Сасаки К, Фосетт Х, Уинг Дж.Ф., Левин С.О., Карр Л., Ли Т.С., Ёсиура К., Утани А., Хирано А., Ямасита С., Гринблатт Д., Нардо Т. , Стефанини М., МакГиббон Д., Саркани Р., Фассихи Х., Такахаши Ю., Нагаяма Ю., Мицутаке Н., Леманн А.Р., Оги Т. (май 2013 г.). «Нарушение нуклеазы ERCC1-XPF приводит к разнообразным клиническим проявлениям и вызывает синдром Кокейна, пигментную ксеродермию и анемию Фанкони» . Американский журнал генетики человека . 92 (5): 807–19. дои : 10.1016/j.ajhg.2013.04.007 . ПМЦ 3644632 . ПМИД 23623389 .
- ^ Нидернхофер Л.Дж., Гаринис Г.А., Раамс А., Лалай А.С., Робинсон А.Р., Аппелдорн Е., Одейк Х., Остендорп Р., Ахмад А., ван Леувен В., Тейл А.Ф., Вермюлен В., ван дер Хорст Г.Т., Майнеке П., Кляйер В.Дж., Вийг Дж. , Джасперс Н.Г., Хоймейкерс Дж.Х. (декабрь 2006 г.). «Новый прогероидный синдром показывает, что генотоксический стресс подавляет соматотропную ось». Природа . 444 (7122): 1038–43. Стартовый код : 2006Natur.444.1038N . дои : 10.1038/nature05456 . ПМИД 17183314 . S2CID 4358515 .
- ^ Больоло М, Шустер Б, Стопкер С, Деркунт Б, Су Ю, Раамс А, Трухильо Х.П., Мингильон Х., Рамирес М.Дж., Пухоль Р., Женат Х.А., Батс Р., Ривер П., Книс К., Суньига С., Бенитес Х., Бюрен Х.А. , Ясперс Н.Г., Шерер О.Д., де Винтер Дж.П., Шиндлер Д., Сюрраллес Дж. (май 2013 г.). «Мутации в ERCC4, кодирующем эндонуклеазу репарации ДНК XPF, вызывают анемию Фанкони» . Американский журнал генетики человека . 92 (5): 800–6. дои : 10.1016/j.ajhg.2013.04.002 . ПМЦ 3644630 . ПМИД 23623386 .
- ^ Jump up to: а б с д и ж г Фациста А., Нгуен Х., Льюис С., Прасад А.Р., Рэмси Л., Зайтлин Б., Нфонсам В., Круз Р.С., Бернштейн Х., Пейн С.М., Стерн С., Отман Н., Банерджи Б., Бернштейн С. (2012). «Недостаточная экспрессия ферментов репарации ДНК на ранней стадии развития спорадического рака толстой кишки» . Геномная интеграция . 3 (1): 3. дои : 10.1186/2041-9414-3-3 . ПМК 3351028 . ПМИД 22494821 .
- ^ Jump up to: а б Бейкер А.М., Серезер Б., Мелтон С., Флетчер А.Г., Родригес-Хусто М., Тадроус П.Дж., Хамфрис А., Элия Г., Макдональд С.А., Райт Н.А., Саймонс Б.Д., Янсен М., Грэм Т.А. (2014). «Количественная оценка эволюции крипт и стволовых клеток в нормальной и неопластической толстой кишке человека» . Представитель ячейки . 8 (4): 940–7. дои : 10.1016/j.celrep.2014.07.019 . ПМЦ 4471679 . ПМИД 25127143 .
- ^ Харпер Дж.В., Элледж С.Дж. (2007). «Реакция на повреждение ДНК: десять лет спустя» . Мол. Клетка . 28 (5): 739–45. doi : 10.1016/j.molcel.2007.11.015 . ПМИД 18082599 .
- ^ Jump up to: а б Грегг С.К., Робинсон А.Р., Нидернхофер Л.Дж. (2011). «Физиологические последствия дефектов эндонуклеазы репарации ДНК ERCC1-XPF» . Восстановление ДНК (Амст.) . 10 (7): 781–91. дои : 10.1016/j.dnarep.2011.04.026 . ПМК 3139823 . ПМИД 21612988 .
- ^ Ли Э., Левин Э.А., Франко VI, Аллен ГО, Гонг Ф., Чжан Ю, Ху Джей Джей (2014). «Комбинированные модели генетического и пищевого риска тройного негативного рака молочной железы». Нутр Рак . 66 (6): 955–63. дои : 10.1080/01635581.2014.932397 . ПМИД 25023197 . S2CID 22065506 .







