Репликационный белок А
| Репликационный белок А | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| (гетеротример) | |||||||||||||
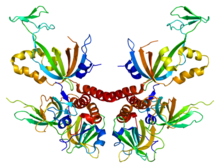 Это изображение репликационного белка А человека. Из PDB : 1L1O. Протеопедический белок A Репликационный белок A | |||||||||||||
| Функция | поврежденное связывание ДНК, связывание одноцепочечной ДНК | ||||||||||||
| |||||||||||||
Репликационный белок А ( RPA ) является основным белком , который связывается с одноцепочечной ДНК (оцДНК) в эукариотических клетках. [ 1 ] [ 2 ] In vitro RPA демонстрирует гораздо более высокое сродство к оцДНК, чем РНК или двухцепочечная ДНК. [ 3 ] RPA необходим в процессах репликации , рекомбинации и репарации, таких как эксцизионная репарация нуклеотидов и гомологичная рекомбинация . [ 2 ] [ 4 ] Он также играет роль в реагировании на поврежденную ДНК. [ 4 ]
Структура
[ редактировать ]RPA представляет собой гетеротример , состоящий из субъединиц RPA1 (RPA70) (субъединица 70 кДа), RPA2 (RPA32) (субъединица 32 кДа) и RPA3 (RPA14) (субъединица 14 кДа). Три субъединицы RPA содержат шесть OB-складок (связывание олигонуклеотидов/олигосахаридов) с ДНК-связывающими доменами (DBD), обозначенными DBDs AF, которые связывают RPA с одноцепочечной ДНК . [ 2 ] [ 3 ]
DBD A, B, C и F расположены на RPA1, DBD D расположен на RPA2, а DBD E расположен на RPA3. [ 4 ] DBD C, D и E составляют ядро тримеризации белка с гибкими линкерными областями, соединяющими их все вместе. [ 4 ] Благодаря этим гибким линкерным областям RPA считается очень гибким, и это поддерживает динамическое связывание, которого может достичь RPA. Из-за этого динамического связывания RPA также способен принимать различные конформации, что приводит к различному количеству нуклеотидов, которые он может задействовать. [ 4 ]
DBD A, B, C и D представляют собой сайты, которые участвуют в связывании оцДНК. [ 5 ] Белково-белковые взаимодействия между RPA и другими белками происходят на N-конце RPA1, в частности DBD F, наряду с C-концом RPA2. [ 5 ] Фосфорилирование RPA происходит на N-конце RPA2. [ 5 ]
RPA имеет много общих черт с комплексным гетеротримером CST, хотя RPA имеет более однородную стехиометрию 1:1:1 . [ 6 ]
Функции
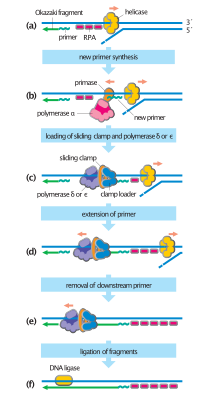
[ редактировать ]Во время репликации ДНК RPA предотвращает скручивание одноцепочечной ДНК (оцДНК) или образование вторичных структур. Это также помогает защитить оцДНК от воздействия эндонуклеаз . [ 2 ] Это позволяет ДНК разматываться, чтобы полимераза могла ее реплицировать. связывается с оцДНК во время начальной фазы гомологичной рекомбинации, важного процесса репарации ДНК и профазы I мейоза RPA также .
Гиперчувствительность к агентам, повреждающим ДНК, может быть вызвана мутациями гена RPA. [ 7 ] Как и его роль в репликации ДНК, это удерживает оцДНК от связывания самой с собой (самодополнения), так что образующаяся нуклеопротеиновая нить может затем связываться с Rad51 и его кофакторами. [ 7 ]
RPA также связывается с ДНК во время процесса эксцизионной репарации нуклеотидов. Это связывание стабилизирует ремонтный комплекс во время процесса восстановления. Бактериальный гомолог называется одноцепочечным связывающим белком (SSB).
См. также
[ редактировать ]- Одноцепочечный связывающий белок
- Репликационный белок А1
- Репликационный белок А2
- Репликационный белок А3
Ссылки
[ редактировать ]- ^ Уолд М.С. (1997). «Репликационный белок A: гетеротримерный одноцепочечный ДНК-связывающий белок, необходимый для метаболизма эукариотической ДНК». Ежегодный обзор биохимии . 66 (1): 61–92. doi : 10.1146/annurev.biochem.66.1.61 . ПМИД 9242902 .
- ^ Jump up to: а б с д Чен Р., Уолд М.С. (декабрь 2014 г.). «Репликационный белок А: первый ответчик одноцепочечной ДНК: динамические взаимодействия ДНК позволяют белку репликации А направлять промежуточные соединения одноцепочечной ДНК по различным путям синтеза или восстановления» . Биоэссе . 36 (12): 1156–1161. дои : 10.1002/bies.201400107 . ПМЦ 4629251 . ПМИД 25171654 .
- ^ Jump up to: а б Флинн Р.Л., Цзоу Л. (август 2010 г.). «Складчатые белки, связывающие олигонуклеотиды/олигосахариды: растущее семейство хранителей генома» . Критические обзоры по биохимии и молекулярной биологии . 45 (4): 266–275. дои : 10.3109/10409238.2010.488216 . ПМК 2906097 . ПМИД 20515430 .
- ^ Jump up to: а б с д и Колдуэлл CC, Spies M (октябрь 2020 г.). «Динамические элементы репликационного белка А на перекрестке репликации, рекомбинации и репарации ДНК» . Критические обзоры по биохимии и молекулярной биологии . 55 (5): 482–507. дои : 10.1080/10409238.2020.1813070 . ПМК 7821911 . ПМИД 32856505 .
- ^ Jump up to: а б с Дуэва Р., Илиакис Г. (сентябрь 2020 г.). «Репликационный белок А: многофункциональный белок, участвующий в репликации, восстановлении ДНК и не только» . НАР Рак . 2 (3): zcaa022. дои : 10.1093/narcan/zcaa022 . ПМК 8210275 . ПМИД 34316690 .
- ^ Лю Н.Ф., Чжоу Р., Чико Л., Мао Н., Стейнберг-Нейфач О., Ха Т (2013). «Комплекс CST, закрывающий теломеры, обладает необычной стехиометрией, осуществляет многочастное взаимодействие с G-хвостами и разворачивает структуры G-хвостов более высокого порядка» . ПЛОС Генетика . 9 (1): e1003145. дои : 10.1371/journal.pgen.1003145 . ПМЦ 3536697 . ПМИД 23300477 .
- ^ Jump up to: а б Ли X, Хейер В.Д. (январь 2008 г.). «Гомологичная рекомбинация в репарации ДНК и толерантность к повреждениям ДНК» . Клеточные исследования . 18 (1): 99–113. дои : 10.1038/cr.2008.1 . ПМК 3087377 . ПМИД 18166982 .