ДНК-полимераза
| ДНК-направленная ДНК-полимераза | |||
|---|---|---|---|
 Трехмерная структура ДНК-связывающих мотивов спираль-поворот-спираль в бета-полимеразе ДНК человека (на основе файла PDB 7ICG ) | |||
| Идентификаторы | |||
| Номер ЕС. | 2.7.7.7 | ||
| Номер CAS. | 9012-90-2 | ||
| Базы данных | |||
| ИнтЭнк | вид IntEnz | ||
| БРЕНДА | БРЕНДА запись | ||
| ЭксПАСи | Просмотр NiceZyme | ||
| КЕГГ | КЕГГ запись | ||
| МетаЦик | метаболический путь | ||
| ПРЯМОЙ | профиль | ||
| PDB Структуры | RCSB PDB PDBe PDBsum | ||
| Генная онтология | АмиГО / QuickGO | ||
| |||
ДНК -полимераза является членом семейства ферментов , которые катализируют синтез ДНК молекул из нуклеозидтрифосфатов , молекулярных предшественников ДНК. Эти ферменты необходимы для репликации ДНК и обычно работают группами, создавая два идентичных дуплекса ДНК из одного исходного дуплекса ДНК. Во время этого процесса ДНК-полимераза «читает» существующие цепи ДНК, чтобы создать две новые цепи, соответствующие существующим. [ 1 ] [ 2 ] [ 3 ] [ 4 ] [ 5 ] [ 6 ] Эти ферменты катализируют химическую реакцию
- дезоксинуклеозидтрифосфат + ДНК n ⇌ пирофосфат + ДНК n+1 .
ДНК-полимераза добавляет нуклеотиды к трем штриховым (3') -концам цепи ДНК, по одному нуклеотиду за раз. Каждый раз, когда клетка делится , ДНК-полимеразы дублируют ДНК клетки, чтобы копию исходной молекулы ДНК можно было передать каждой дочерней клетке. Таким образом, генетическая информация передается из поколения в поколение.
Прежде чем начнется репликация, фермент, называемый хеликазой, раскручивает молекулу ДНК из ее плотно сплетенной формы, разрывая при этом водородные связи между нуклеотидными основаниями . Это открывает или «расстегивает» двухцепочечную ДНК, образуя две одиночные цепи ДНК, которые можно использовать в качестве шаблонов для репликации в вышеуказанной реакции.
История
[ редактировать ]В 1956 году Артур Корнберг и его коллеги обнаружили ДНК-полимеразу I (Pol I) в Escherichia coli . Они описали процесс репликации ДНК, при котором ДНК-полимераза копирует базовую последовательность цепи матрицы ДНК. Позднее в 1959 году за эту работу Корнберг был удостоен Нобелевской премии по физиологии и медицине . [ 7 ] ДНК-полимераза II была открыта Томасом Корнбергом (сыном Артура Корнберга ) и Малкольмом Э. Гефтером в 1970 году, что позволило дополнительно выяснить роль Pol I в репликации ДНК E. coli . [ 8 ] Еще три ДНК-полимеразы были обнаружены в E. coli , включая ДНК-полимеразу III (открытую в 1970-х годах) и ДНК-полимеразы IV и V (открытую в 1999 году). [ 9 ] С 1983 года ДНК-полимеразы стали использоваться в полимеразной цепной реакции (ПЦР), а с 1988 года вместо них стали использоваться термостабильные ДНК-полимеразы , поскольку их не нужно добавлять в каждом цикле ПЦР.
Функция
[ редактировать ]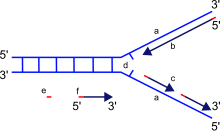

Основная функция ДНК-полимеразы — синтез ДНК из дезоксирибонуклеотидов , строительных блоков ДНК. Копии ДНК создаются путем спаривания нуклеотидов с основаниями, присутствующими на каждой цепи исходной молекулы ДНК. Это спаривание всегда происходит в определенных комбинациях: цитозин вместе с гуанином и тимин вместе с аденином образуют две отдельные пары соответственно. Напротив, РНК-полимеразы синтезируют РНК из рибонуклеотидов либо из РНК, либо из ДНК. [ нужна ссылка ]
При синтезе новой ДНК ДНК-полимераза может добавлять свободные нуклеотиды только к 3'-концу вновь образующейся цепи. Это приводит к удлинению вновь образующейся цепи в направлении 5’–3’. [ нужна ссылка ]
Важно отметить, что направленность вновь образующейся цепи (дочерней цепи) противоположна направлению движения ДНК-полимеразы вдоль матричной цепи. Поскольку ДНК-полимераза требует свободной 3'-ОН-группы для инициации синтеза, она может синтезировать только в одном направлении, удлиняя 3'-конец ранее существовавшей нуклеотидной цепи. Следовательно, ДНК-полимераза движется вдоль цепи матрицы в направлении 3'-5', а дочерняя цепь формируется в направлении 5'-3'. Это различие позволяет образовавшейся двухцепочечной ДНК состоять из двух нитей ДНК, антипараллельных друг другу. [ нужна ссылка ]
Функция ДНК-полимеразы не совсем идеальна: фермент допускает примерно одну ошибку на каждый миллиард копируемых пар оснований. Исправление ошибок — свойство некоторых, но не всех ДНК-полимераз. Этот процесс исправляет ошибки во вновь синтезированной ДНК. Когда распознается неправильная пара оснований, ДНК-полимераза перемещается назад на одну пару оснований ДНК. 3'-5'- экзонуклеазная активность фермента позволяет удалить неправильную пару оснований (эта активность известна как корректура ). После удаления основания полимераза может повторно вставить правильное основание, и репликация может продолжиться вперед. Это сохраняет целостность исходной цепи ДНК, которая передается дочерним клеткам.
Верность очень важна при репликации ДНК. Несоответствия в спаривании оснований ДНК потенциально могут привести к дисфункции белков и раку. Многие ДНК-полимеразы содержат экзонуклеазный домен, который обнаруживает несовпадения пар оснований, а затем удаляет неправильный нуклеотид для замены правильным. [ 10 ] Форма и взаимодействие пар оснований Уотсона и Крика — это то, что в первую очередь способствует обнаружению или ошибке. Водородные связи играют ключевую роль в связывании и взаимодействии пар оснований. Считается, что потеря взаимодействия, которая происходит при несовпадении, вызывает сдвиг баланса связывания матрицы-праймера с полимеразы на экзонуклеазный домен. Кроме того, включение неправильного нуклеотида приводит к замедлению полимеризации ДНК. Эта задержка дает время для переключения ДНК с сайта полимеразы на сайт экзонуклеазы. Различные конформационные изменения и потеря взаимодействия происходят при разных несовпадениях. При несоответствии пуринов и пиримидинов происходит смещение пиримидина в сторону большой бороздки, а пурина - в сторону малой бороздки. Что касается формы связывающего кармана ДНК-полимеразы, между пурином и остатками в малой бороздке происходят стерические столкновения, а важные ван-дер-ваальсовые и электростатические взаимодействия. пиримидин теряет [ 11 ] Несовпадения пиримидин:пиримидин и пурин:пурин вызывают менее заметные изменения, поскольку основания смещаются в сторону большой бороздки и возникают меньшие стерические препятствия. Однако, хотя различные несоответствия приводят к различным стерическим свойствам, ДНК-полимераза по-прежнему способна одинаково обнаруживать и дифференцировать их и поддерживать точность репликации ДНК. [ 12 ] Полимеризация ДНК также имеет решающее значение для многих процессов мутагенеза и широко используется в биотехнологиях.
Структура
[ редактировать ]Известные ДНК-полимеразы имеют высококонсервативную структуру, а это означает, что их общие каталитические субъединицы очень мало различаются от вида к виду, независимо от их доменной структуры. Консервативные структуры обычно указывают на важные, незаменимые функции клетки, поддержание которых обеспечивает эволюционные преимущества. Форму можно описать как правую руку с большим пальцем, указательным пальцем и ладонью. Пальмовый домен, по-видимому, катализирует перенос фосфорильных групп в реакции переноса фосфорила. ДНК прикрепляется к ладони, когда фермент активен. Считается, что эта реакция катализируется по двухионному механизму. Функция пальцевого домена связывает нуклеозидтрифосфаты с основанием матрицы. Домен большого пальца играет потенциальную роль в процессивности, транслокации и позиционировании ДНК. [ 13 ]
Процессивность
[ редактировать ]Быстрый катализ ДНК-полимеразы из-за ее процессивного характера. Процессивность – характеристика ферментов, функционирующих на полимерных субстратах. В случае ДНК-полимеразы степень процессивности относится к среднему количеству нуклеотидов, добавляемых каждый раз, когда фермент связывает матрицу. В среднем ДНК-полимеразе требуется около одной секунды для обнаружения и связывания соединения праймер/матрица. После связывания непроцессивная ДНК-полимераза добавляет нуклеотиды со скоростью один нуклеотид в секунду. [ 14 ] : 207–208 Однако процессивные ДНК-полимеразы добавляют несколько нуклеотидов в секунду, резко увеличивая скорость синтеза ДНК. Степень процессивности прямо пропорциональна скорости синтеза ДНК. Скорость синтеза ДНК в живой клетке впервые была определена как скорость удлинения ДНК фага Т4 в инфицированной фагом E. coli . В период экспоненциального роста ДНК при 37°С скорость составляла 749 нуклеотидов в секунду. [ 15 ]
Способность ДНК-полимеразы скользить по матрице ДНК позволяет повысить процессивность. резко возрастает Процессивность репликационной вилки . Этому увеличению способствует ассоциация ДНК-полимеразы с белками, известная как скользящий зажим ДНК . Зажимы представляют собой несколько белковых субъединиц, связанных в форме кольца. Используя гидролиз АТФ, класс белков, известных как белки, загружающие скользящие зажимы, открывают кольцевую структуру скользящих зажимов ДНК, позволяя связываться с цепью ДНК и высвобождаться из нее. Белково-белковое взаимодействие с зажимом предотвращает диффузию ДНК-полимеразы из ДНК-матрицы, тем самым гарантируя, что фермент связывается с тем же соединением праймер/матрица и продолжает репликацию. [ 14 ] : 207–208 ДНК-полимераза меняет конформацию, увеличивая сродство к зажиму, когда она связана с ним, и уменьшая сродство, когда завершает репликацию участка ДНК, чтобы обеспечить освобождение от зажима. [ нужна ссылка ]
Процессивность ДНК-полимеразы была изучена с помощью in vitro экспериментов с одиночными молекулами (а именно, с помощью оптических пинцетов и магнитных пинцетов ), которые выявили синергизм между ДНК-полимеразами и другими молекулами реплисомы ( геликазы и SSB ), а также с вилкой репликации ДНК. [ 16 ] Эти результаты привели к разработке синергетических кинетических моделей репликации ДНК, описывающих результирующее увеличение процессивности ДНК-полимеразы. [ 16 ]
Вариации между видами
[ редактировать ]| ДНК-полимеразы семейства А | |||
|---|---|---|---|
 пара c:o6-метил-гуанин в положении пары оснований полимеразы-2 | |||
| Идентификаторы | |||
| Символ | ДНК_pol_A | ||
| Пфам | PF00476 | ||
| ИнтерПро | ИПР001098 | ||
| УМНЫЙ | - | ||
| PROSITE | PDOC00412 | ||
| ОБЛАСТЬ ПРИМЕНЕНИЯ 2 | 1dpi / СКОПе / СУПФАМ | ||
| |||
| ДНК-полимеразы семейства B | |||
|---|---|---|---|
 кристаллическая структура rb69 gp43 в комплексе с ДНК, содержащей тимингликоль | |||
| Идентификаторы | |||
| Символ | DNA_pol_B | ||
| Пфам | PF00136 | ||
| Пфам Клан | CL0194 | ||
| ИнтерПро | ИПР006134 | ||
| PROSITE | PDOC00107 | ||
| ОБЛАСТЬ ПРИМЕНЕНИЯ 2 | 1ной / СКОПе / СУПФАМ | ||
| |||
| ДНК-полимераза типа B, органелларная и вирусная | |||
|---|---|---|---|
 ДНК-полимераза phi29, орторомбическая кристаллическая форма, комплекс оцДНК | |||
| Идентификаторы | |||
| Символ | DNA_pol_B_2 | ||
| Пфам | PF03175 | ||
| Пфам Клан | CL0194 | ||
| ИнтерПро | ИПР004868 | ||
| |||
На основании гомологии последовательностей ДНК-полимеразы можно разделить на семь различных семейств: A, B, C, D, X, Y и RT.
Некоторые вирусы также кодируют специальные ДНК-полимеразы, такие как ДНК-полимераза вируса гепатита В. Они могут избирательно реплицировать вирусную ДНК с помощью различных механизмов. Ретровирусы кодируют необычную ДНК-полимеразу, называемую обратной транскриптазой , которая представляет собой РНК-зависимую ДНК-полимеразу (RdDp). Он полимеризует ДНК из матрицы РНК .
| Семья [ 17 ] | Типы ДНК-полимеразы | Таксоны | Примеры | Особенность |
|---|---|---|---|---|
| А | Репликативные и репарационные полимеразы | Эукариотические и прокариотические | ДНК-полимераза Т7, Pol I, Pol γ, θ и ν | Два домена экзонуклеазы (3'-5' и 5'-3') |
| Б | Репликативные и репарационные полимеразы | Эукариотические и прокариотические | Pol II, Pol B, Pol g, Pol a, d и e | 3'-5 экзонуклеаза (корректура); некоторые вирусные полимеразы используют белковые праймеры |
| С | Репликативные полимеразы | Прокариотический | Pol III | 3'-5 экзонуклеаза (корректура) |
| Д | Репликативные полимеразы | Эвриархеота | PolD (гетеродимер DP1/DP2) [ 18 ] | Никакой «ручной» особенности, РНК-полимераза с двойным стволом ; 3'-5 экзонуклеаза (корректура) |
| Х | Репликативные и репарационные полимеразы | Эукариотический | Pol β, Pol σ, Pol λ, Pol μ и терминальная дезоксинуклеотидилтрансфераза. | шаблон по желанию; 5'-фосфатаза (только Pol β); слабая функция «рука» |
| И | Репликативные и репарационные полимеразы | Эукариотические и прокариотические | Пол я, Пол к, Пол н, [ 19 ] Pol IV, and Pol V | Синтез транслезий [ 20 ] |
| РТ | Репликативные и репарационные полимеразы | Вирусы, ретровирусы и эукариоты | Теломераза , вирус гепатита В. | РНК-зависимый |
Прокариотическая полимераза
[ редактировать ]Прокариотические полимеразы существуют в двух формах: кор-полимераза и голофермент. Core-полимераза синтезирует ДНК из матрицы ДНК, но она не может инициировать синтез самостоятельно или точно. Голофермент точно инициирует синтез.
Pol I
[ редактировать ]Прокариотические полимеразы семейства А включают фермент ДНК-полимеразу I (Pol I), который кодируется polA геном и повсеместно распространен среди прокариот . Эта репарационная полимераза участвует в эксцизионной репарации, обладая как 3'-5'-, так и 5'-3'-экзонуклеазной активностью, а также процессингом фрагментов Оказаки, образующихся во время синтеза отстающей цепи. [ 21 ] Pol I является наиболее распространенной полимеразой, на которую приходится >95% полимеразной активности в E. coli ; тем не менее, было обнаружено, что в клетках отсутствует Pol I, что позволяет предположить, что активность Pol I может быть заменена другими четырьмя полимеразами. Pol I добавляет ~15-20 нуклеотидов в секунду, демонстрируя тем самым плохую процессивность. Вместо этого Pol I начинает добавлять нуклеотиды в месте соединения праймер:матрица РНК, известном как точка начала репликации (ori). Примерно на 400 п.н. ниже источника голофермент Pol III собирается и берет на себя репликацию с очень процессивной скоростью и характером. [ 22 ]
Taq- полимераза — термостабильный фермент этого семейства, не обладающий способностью к корректуре. [ 23 ]
Pol II
[ редактировать ]ДНК-полимераза II представляет собой полимеразу семейства B, кодируемую геном polB. Pol II обладает 3'-5'-экзонуклеазной активностью и участвует в репарации ДНК , перезапуске репликации в обход повреждений, а его присутствие в клетках может прыгать от ~ 30-50 копий на клетку до ~ 200-300 во время индукции SOS. Считается также, что Pol II является резервной копией Pol III, поскольку он может взаимодействовать с голоферментными белками и приобретать высокий уровень процессивности. Считается, что основная роль Pol II заключается в способности направлять активность полимеразы на репликационную вилку и помогать остановленному Pol III обходить терминальные несовпадения. [ 24 ]
Pfu ДНК-полимераза — термостабильный фермент этого семейства, обнаруженный у гипертермофильных архей Pyrococcus Furiosus . [ 25 ] Детальная классификация делит семейство B у архей на B1, B2, B3, в котором B2 представляет собой группу псевдоферментов . Pfu принадлежит к семейству B3. Другие PolB, обнаруженные у архей, входят в состав «Каспозонов», Cas1 -зависимых транспозонов. [ 26 ] Некоторые вирусы (включая ДНК-полимеразу Ф29 ) и митохондриальные плазмиды также несут polB. [ 27 ]
Pol III
[ редактировать ]Холофермент ДНК-полимеразы III является основным ферментом, участвующим в репликации ДНК в E. coli , и принадлежит к полимеразам семейства C. Он состоит из трех узлов: ядра pol III, фактора процессивности скользящего зажима бета и комплекса зажима-нагрузки. Ядро состоит из трех субъединиц: α, концентратора полимеразной активности, ɛ, экзонуклеолитического корректора и θ, который может действовать как стабилизатор ɛ. Фактор процессивности бета-скользящего зажима также присутствует в двух экземплярах, по одному для каждого ядра, для создания зажима, который окружает ДНК, обеспечивая высокую процессивность. [ 28 ] Третья сборка представляет собой семисубъединичный (τ2γδδ ′ χψ) комплекс зажима-загрузчика.
В старой учебниковой «модели тромбона» изображен комплекс элонгации с двумя эквивалентами основного фермента в каждой репликационной вилке (RF), по одному на каждую цепь, отстающему и ведущему. [ 24 ] Однако недавние данные исследований одиночных молекул указывают на наличие в среднем трех стехиометрических эквивалентов основного фермента в каждом RF как для Pol III, так и для его аналога в B. subtilis, PolC. [ 29 ] Внутриклеточная флуоресцентная микроскопия показала, что синтез ведущей цепи не может быть полностью непрерывным, а Pol III* (т.е. субъединицы голофермента α, ε, τ, δ и χ без скользящего зажима β2) имеет высокую частоту диссоциации от активных РФ. [ 30 ] В этих исследованиях скорость оборота репликационной вилки составляла около 10 с для Pol III*, 47 с для скользящего зажима β2 и 15 м для геликазы DnaB. Это предполагает, что хеликаза DnaB может оставаться стабильно связанной с RF и служить точкой зародышеобразования компетентного голофермента. Исследования одиночных молекул in vitro показали, что Pol III* имеет высокую скорость оборота RF при избытке, но остается стабильно связанным с репликационными вилками, когда концентрация ограничена. [ 30 ] Другое исследование одиночных молекул показало, что активность хеликазы DnaB и удлинение цепи могут протекать с несвязанной стохастической кинетикой. [ 30 ]
Pol IV
[ редактировать ]В E. coli ДНК -полимераза IV (Pol IV) представляет собой склонную к ошибкам ДНК-полимеразу, участвующую в ненаправленном мутагенезе. [ 31 ] Pol IV представляет собой полимеразу семейства Y, экспрессируемую геном dinB , который включается посредством SOS-индукции, вызванной остановкой полимераз в репликационной вилке. Во время индукции SOS продукция Pol IV увеличивается в десять раз, и одной из функций в это время является вмешательство в процессивность голофермента Pol III. Это создает контрольную точку, останавливает репликацию и дает время на восстановление повреждений ДНК соответствующим путем восстановления. [ 32 ] Другая функция Pol IV заключается в осуществлении синтеза трансфузии на остановленной репликационной вилке, например, в обход аддуктов N2-дезоксигуанина с более высокой скоростью, чем при пересечении неповрежденной ДНК. Клетки, лишенные гена dinB , имеют более высокую скорость мутагенеза, вызванного агентами, повреждающими ДНК. [ 33 ]
Pol V
[ редактировать ]ДНК-полимераза V (Pol V) представляет собой ДНК-полимеразу Y-семейства, которая участвует в SOS-ответе и механизмах репарации ДНК в синтезе транслейкоза . [ 34 ] Транскрипция Pol V через гены umuDC строго регулируется, чтобы производить только Pol V, когда в клетке присутствует поврежденная ДНК, вызывающая SOS-ответ. Остановка полимераз заставляет RecA связываться с оцДНК, что приводит LexA к самоперевариванию белка . Затем LexA теряет способность подавлять транскрипцию оперона umuDC. Тот же нуклеопротеин RecA-ssDNA посттрансляционно модифицирует белок UmuD в белок UmuD'. UmuD и UmuD' образуют гетеродимер, который взаимодействует с UmuC, который, в свою очередь, активирует каталитическую полимеразную активность umuC в отношении поврежденной ДНК. [ 35 ] В E. coli была предложена полимеразная модель «пояса с инструментами» для переключения pol III на pol IV в остановленной репликационной вилке, где обе полимеразы одновременно связываются с β-зажимом. [ 36 ] Однако участие более чем одной TLS-полимеразы, работающей последовательно в обход поражения, еще не было показано в E. coli . Более того, Pol IV может с высокой эффективностью катализировать как вставку, так и удлинение, тогда как pol V считается основной SOS-полимеразой TLS. Одним из примеров является обход внутрицепочечной сшивки гуанин-тимином, где на основе разницы в мутационных сигнатурах двух полимераз было показано, что pol IV и pol V конкурируют за TLS внутрицепочечной сшивки. [ 36 ]
Семья Д
[ редактировать ]
В 1998 году семейство ДНК-полимераз D было обнаружено у Pyrococcus Furiosus и Methanococcus jannaschii . [ 38 ] Комплекс PolD представляет собой гетеродимер из двух цепей, каждая из которых кодируется DP1 (малая корректура) и DP2 (большая каталитическая). В отличие от других ДНК-полимераз, структура и механизм каталитического ядра DP2 напоминают таковые у многосубъединичных РНК-полимераз . Интерфейс DP1-DP2 напоминает интерфейс цинкового пальца эукариотической полимеразы класса B и ее небольшой субъединицы. [ 18 ] DP1, Mre11 -подобная экзонуклеаза, [ 39 ] вероятно, является предшественником небольшой субъединицы Pol α и ε , обеспечивающей возможности корректуры, ныне утраченные у эукариот. [ 26 ] Его N-концевой домен HSH по структуре подобен белкам AAA , особенно субъединице δ Pol III и RuvB . [ 40 ] DP2 имеет домен класса II KH . [ 18 ] Pyrococcus abyssi polD более термостабилен и более точен, чем Taq -полимераза, но еще не поступил в продажу. [ 41 ] Было высказано предположение, что ДНК-полимераза семейства D была первой, развившейся в клеточных организмах, и что репликативная полимераза Последнего универсального клеточного предка (LUCA) принадлежала семейству D. [ 42 ]
Эукариотическая ДНК-полимераза
[ редактировать ]Полимеразы β, λ, σ, μ (бета, лямбда, сигма, мю) и TdT
[ редактировать ]Полимеразы семейства X содержат хорошо известную эукариотическую полимеразу pol β (бета) , а также другие эукариотические полимеразы, такие как Pol σ (сигма), Pol λ (лямбда) , Pol μ (mu) и терминальную дезоксинуклеотидилтрансферазу (TdT) . Полимеразы семейства X обнаружены в основном у позвоночных животных, а некоторые - у растений и грибов. Эти полимеразы имеют высококонсервативные области, которые включают два мотива спираль-шпилька-спираль, которые необходимы во взаимодействиях ДНК-полимеразы. Один мотив расположен в домене 8 кДа, который взаимодействует с нижележащей ДНК, и один мотив расположен в домене большого пальца, который взаимодействует с цепью праймера. Pol β, кодируемый геном POLB, необходим для репарации вырезаемых оснований с короткими участками , пути репарации ДНК, который необходим для восстановления алкилированных или окисленных оснований, а также абазиновых участков . Pol λ и Pol μ, кодируемые генами POLL и POLM соответственно, участвуют в негомологичном соединении концов — механизме воссоединения двухцепочечных разрывов ДНК, вызванных перекисью водорода и ионизирующим излучением соответственно. TdT экспрессируется только в лимфоидной ткани и добавляет «n нуклеотидов» к двухцепочечным разрывам, образующимся во время Рекомбинация V(D)J для содействия иммунологическому разнообразию. [ 43 ]
Полимеразы α, δ и ε (альфа, дельта и эпсилон)
[ редактировать ]Pol α (альфа) , Pol δ (дельта) и Pol ε (эпсилон) являются членами полимераз семейства B и являются основными полимеразами, участвующими в репликации ядерной ДНК. Комплекс Pol α (комплекс pol α-ДНК-примазы) состоит из четырех субъединиц: каталитической субъединицы POLA1 , регуляторной субъединицы POLA2 , а также малой и большой субъединиц примазы PRIM1 и PRIM2 соответственно. Как только примаза создала праймер для РНК, Pol α начинает репликацию, удлиняя праймер примерно на 20 нуклеотидов. [ 44 ] Благодаря своей высокой процессивности Pol δ берет на себя синтез лидирующих и отстающих цепей от Pol α. [ 14 ] : 218–219 Pol δ экспрессируется генами POLD1 , создавая каталитическую субъединицу, POLD2 , POLD3 и POLD4 создают другие субъединицы, которые взаимодействуют с ядерным антигеном пролиферирующих клеток (PCNA), который представляет собой зажим ДНК , который позволяет Pol δ обладать процессивностью. [ 45 ] Pol ε кодируется POLE1 , каталитической субъединицей, генами POLE2 и POLE3 . Сообщалось, что функция Pol ε заключается в удлинении ведущей цепи во время репликации. [ 46 ] [ 47 ] тогда как Pol δ в первую очередь реплицирует отстающую цепь; однако недавние данные показали, что Pol δ может также играть роль в репликации ведущей цепи ДНК. [ 48 ] С-концевая «полимеразная» область Pol ε, несмотря на то, что она не требуется для полимеразной активности, [ 49 ] Считается, что он необходим для жизнеспособности клеток. Считается, что С-концевая область обеспечивает контрольную точку перед входом в анафазу, обеспечивает стабильность голофермента и добавляет к голоферменту белки, необходимые для инициации репликации. [ 50 ] Pol ε имеет более крупный «пальмовый» домен, который обеспечивает высокую процессивность независимо от PCNA. [ 49 ]
По сравнению с другими полимеразами семейства B, семейство экзонуклеаз DEDD, ответственное за корректуру, инактивировано в Pol α. [ 26 ] Pol ε уникален тем, что имеет два домена с цинковыми пальцами и неактивную копию другой полимеразы семейства B на своем С-конце. Наличие этого цинкового пальца имеет значение для происхождения эукариот, которые в данном случае помещаются в группу Асгарда с архейной полимеразой B3. [ 51 ]
Полимеразы η, ι и κ (эта, йота и каппа)
[ редактировать ]Pol η (эта) , Pol ι (йота) и Pol κ (каппа) представляют собой ДНК-полимеразы семейства Y, участвующие в репарации ДНК путем трансляционного синтеза и кодируемые генами POLH, POLI и POLK соответственно. Члены семейства Y имеют пять общих мотивов, помогающих связывать субстрат и конец праймера, и все они включают типичные домены большого пальца правой руки, ладони и пальца с добавленными доменами, такими как мизинец (LF), домен, связанный с полимеразой (PAD) или запястье. Однако активный сайт у разных членов семьи различается из-за разных заживляемых повреждений. Полимеразы семейства Y представляют собой полимеразы низкой точности, но доказано, что они приносят больше пользы, чем вреда, поскольку мутации, влияющие на полимеразу, могут вызывать различные заболевания, такие как рак кожи и пигментная ксеродерма (XPS). О важности этих полимераз свидетельствует тот факт, что ген, кодирующий ДНК-полимеразу η, называется XPV, поскольку потеря этого гена приводит к заболеванию пигментной ксеродерма. Pol η особенно важен для обеспечения точного транслезного синтеза повреждений ДНК, возникающих в результате ультрафиолетовое излучение . Функциональность Pol κ до конца не изучена, но исследователи нашли две вероятные функции. Считается, что Pol κ действует как удлинитель или вставка определенного основания при определенных повреждениях ДНК. Все три полимеразы синтеза трансформ, наряду с Rev1, рекрутируются в поврежденные очаги посредством остановленных репликативных ДНК-полимераз. Существует два пути восстановления повреждений, что позволяет исследователям прийти к выводу, что выбранный путь зависит от того, какая цепь содержит повреждение: ведущая или отстающая. [ 52 ]
Полимеразы Rev1 и ζ (дзета)
[ редактировать ]Pol ζ, еще одна полимераза семейства B, состоит из двух субъединиц Rev3 , каталитической субъединицы, и Rev7 ( MAD2L2 ), которая увеличивает каталитическую функцию полимеразы и участвует в синтезе трансфункции. Pol ζ не обладает 3'-5'-экзонуклеазной активностью и уникален тем, что может удлинять праймеры с несоответствиями по концам. Rev1 имеет три представляющие интерес области в домене BRCT , убиквитин-связывающем домене и C-концевом домене и обладает способностью к трансферазе dCMP, которая добавляет дезоксицитидин-противоположные повреждения, которые останавливают репликативные полимеразы Pol δ и Pol ε. Эти остановившиеся полимеразы активируют убиквитиновые комплексы, которые, в свою очередь, диссоциируют репликативные полимеразы и рекрутируют Pol ζ и Rev1. Вместе Pol ζ и Rev1 добавляют дезоксицитидин, и Pol ζ выходит за пределы поражения. Посредством еще невыясненного процесса Pol ζ диссоциирует, а репликационные полимеразы повторно связываются и продолжают репликацию. Pol ζ и Rev1 не необходимы для репликации, но потеря гена REV3 у почкующихся дрожжей может вызвать повышенную чувствительность к агентам, повреждающим ДНК, из-за коллапса репликационных вилок, где репликация полимеразы остановилась. [ 53 ]
Теломераза
[ редактировать ]Теломераза — это рибонуклеопротеин , функция которого заключается в репликации концов линейных хромосом, поскольку нормальная ДНК-полимераза не может реплицировать концы или теломеры . Одноцепочечный 3'-выступ двухцепочечной хромосомы с последовательностью 5'-TTAGGG-3' рекрутирует теломеразу. Теломераза действует так же, как и другие ДНК-полимеразы, удлиняя 3'-конец, но, в отличие от других ДНК-полимераз, теломераза не требует матрицы. Субъединица TERT, пример обратной транскриптазы , использует субъединицу РНК для формирования соединения праймер-матрица, которое позволяет теломеразе удлинять 3'-конец концов хромосомы. Считается, что постепенное уменьшение размера теломер в результате множества репликаций в течение жизни связано с эффектами старения. [ 14 ] : 248–249
Полимеразы γ, θ и ν (гамма, тета и ню).
[ редактировать ]Pol γ (гамма), Pol θ (тета) и Pol ν (nu) представляют собой полимеразы семейства A. Долгое время считалось, что Pol γ, кодируемая геном POLG , является единственной митохондриальной полимеразой. Однако недавние исследования показывают, что по крайней мере Pol β (бета) , полимераза семейства X, также присутствует в митохондриях. [ 54 ] [ 55 ] Любая мутация, которая приводит к ограничению или нефункционированию Pol γ, оказывает существенное влияние на мтДНК и является наиболее распространенной причиной аутосомно наследуемых митохондриальных нарушений. [ 56 ] Pol γ содержит С-концевой полимеразный домен и N-концевой 3'-5' экзонуклеазный домен, которые соединены через линкерную область, которая связывает вспомогательную субъединицу. Акцессорная субъединица связывает ДНК и необходима для процессивности Pol γ. Точечная мутация A467T в линкерной области ответственна за более трети всех митохондриальных нарушений, связанных с Pol γ. [ 57 ] Хотя многие гомологи Pol θ, кодируемые геном POLQ , обнаружены у эукариот, его функция до конца не изучена. Последовательность аминокислот на С-конце - это то, что классифицирует Pol θ как полимеразу семейства A, хотя частота ошибок для Pol θ более тесно связана с полимеразами семейства Y. Pol θ удлиняет несовпадающие концы праймера и может обходить абазические сайты путем добавления нуклеотида. Он также обладает дезоксирибофосфодиэстеразной (dRPase) активностью в полимеразном домене и может проявлять АТФазную активность в непосредственной близости от оцДНК. [ 58 ] Pol ν (nu) считается наименее эффективным из ферментов-полимераз. [ 59 ] Однако ДНК-полимераза nu играет активную роль в восстановлении гомологии во время клеточных ответов на сшивки, выполняя свою роль в комплексе с хеликазой . [ 59 ]
Растения используют две полимеразы семейства А для копирования как митохондриального, так и пластидного генома. Они больше похожи на бактериальный Pol I, чем на Pol γ млекопитающих. [ 60 ]
Обратная транскриптаза
[ редактировать ]Ретровирусы кодируют необычную ДНК-полимеразу, называемую обратной транскриптазой , которая представляет собой РНК-зависимую ДНК-полимеразу (RdDp), которая синтезирует ДНК из матрицы РНК. Семейство обратных транскриптаз содержит как функциональность ДНК-полимеразы, так и функциональность РНКазы H, которая разрушает основания РНК, спаренные с ДНК. Примером ретровируса является ВИЧ . [ 14 ] Обратная транскриптаза обычно используется для амплификации РНК в исследовательских целях. Используя матрицу РНК, ПЦР может использовать обратную транскриптазу, создавая матрицу ДНК. Эту новую матрицу ДНК затем можно использовать для типичной ПЦР-амплификации. Таким образом, продуктами такого эксперимента являются амплифицированные продукты ПЦР из РНК. [ 9 ]
Каждая частица ретровируса ВИЧ содержит два РНК генома , но после заражения каждый вирус генерирует только один провирус . [ 61 ] После заражения обратная транскрипция сопровождается переключением матрицы между двумя копиями генома (рекомбинация выбора копии). [ 61 ] В каждом цикле репликации происходит от 5 до 14 событий рекомбинации на геном. [ 62 ] Переключение шаблонов (рекомбинация), по-видимому, необходимо для поддержания целостности генома и как механизм восстановления поврежденных геномов. [ 63 ] [ 61 ]
ДНК-полимераза бактериофага Т4
[ редактировать ]Бактериофаг (фаг) Т4 кодирует ДНК-полимеразу, которая катализирует синтез ДНК в направлении от 5' к 3'. [ 64 ] Фагополимераза также обладает экзонуклеазной активностью, которая действует в направлении от 3’ к 5’. [ 65 ] и эта деятельность используется для корректуры и редактирования вновь вставленных баз. [ 66 ] Было обнаружено, что мутант фага с термочувствительной ДНК-полимеразой при выращивании при пермиссивных температурах подвергается рекомбинации с частотами, которые примерно в два раза выше, чем у фага дикого типа. [ 67 ]
Было высказано предположение, что мутационные изменения в ДНК-полимеразе фага могут стимулировать переключение цепи матрицы (рекомбинацию выбора копии) во время репликации . [ 67 ]
См. также
[ редактировать ]- Биологические машины
- секвенирование ДНК
- Ферментативный катализ
- Генетическая рекомбинация
- Молекулярное клонирование
- Полимеразная цепная реакция
- Динамика белкового домена
- Обратная транскрипция
- РНК-полимераза
- ДНК-полимераза Taq
Ссылки
[ редактировать ]- ^ Боллум Ф.Дж. (август 1960 г.). «Полимераза тимуса теленка» . Журнал биологической химии . 235 (8): 2399–2403. дои : 10.1016/S0021-9258(18)64634-4 . ПМИД 13802334 .
- ^ Фаласки А., Корнберг А. (апрель 1966 г.). «Биохимические исследования бактериального спорообразования. II. Полимераза дезоксирибонуклеиновой кислоты в спорах Bacillus subtilis» . Журнал биологической химии . 241 (7): 1478–1482. дои : 10.1016/S0021-9258(18)96736-0 . ПМИД 4957767 .
- ^ Леман И.Р., Бессман М.Дж., Симмс Э.С., Корнберг А. (июль 1958 г.). «Ферментативный синтез дезоксирибонуклеиновой кислоты. I. Получение субстратов и частичная очистка фермента из кишечной палочки» . Журнал биологической химии . 233 (1): 163–170. дои : 10.1016/S0021-9258(19)68048-8 . ПМИД 13563462 .
- ^ Ричардсон С.С., Шильдкраут С.Л., Апосян Х.В., Корнберг А. (январь 1964 г.). «Ферментативный синтез дезоксирибонуклеиновой кислоты. XIV. Дальнейшая очистка и свойства полимеразы дезоксирибонуклеиновой кислоты Escherichia coli » . Журнал биологической химии . 239 : 222–232. дои : 10.1016/S0021-9258(18)51772-5 . ПМИД 14114848 .
- ^ Шахман Х.К., Адлер Дж., Раддинг К.М., Леман И.Р., Корнберг А. (ноябрь 1960 г.). «Ферментативный синтез дезоксирибонуклеиновой кислоты. VII. Синтез полимера дезоксиаденилата и дезокситимидилата» . Журнал биологической химии . 235 (11): 3242–3249. дои : 10.1016/S0021-9258(20)81345-3 . ПМИД 13747134 .
- ^ Циммерман Б.К. (май 1966 г.). «Очистка и свойства полимеразы дезоксирибонуклеиновой кислоты Micrococcus lysodeikticus» . Журнал биологической химии . 241 (9): 2035–2041. дои : 10.1016/S0021-9258(18)96662-7 . ПМИД 5946628 .
- ^ «Нобелевская премия по физиологии и медицине 1959 года» . Нобелевский фонд . Проверено 1 декабря 2012 г.
- ^ Тессман I, Кеннеди, Массачусетс (февраль 1994 г.). «ДНК-полимераза II Escherichia coli в обход абазовых сайтов in vivo» . Генетика . 136 (2): 439–448. дои : 10.1093/генетика/136.2.439 . ПМЦ 1205799 . ПМИД 7908652 .
- ^ Перейти обратно: а б Ленинджер А.Л., Кокс М.М., Нельсон Д.Л. (2013). Ленингерские принципы биохимии (6-е изд.). Нью-Йорк: WH Freeman and Company. ISBN 978-1-4292-3414-6 . OCLC 824794893 .
- ^ Гаррет Дж. (2013). Биохимия . Мэри Финч.
- ^ Хантер В.Н., Браун Т., Ананд Н.Н., Кеннард О. (1986). «Структура пары оснований аденин-цитозин в ДНК и ее значение для восстановления несоответствия». Природа . 320 (6062): 552–555. Бибкод : 1986Natur.320..552H . дои : 10.1038/320552a0 . ПМИД 3960137 . S2CID 4319887 .
- ^ Свон М.К., Джонсон Р.Э., Пракаш Л., Пракаш С., Аггарвал А.К. (сентябрь 2009 г.). «Структурные основы высокоточного синтеза ДНК дрожжевой ДНК-полимеразой дельта» . Структурная и молекулярная биология природы . 16 (9): 979–986. дои : 10.1038/nsmb.1663 . ПМК 3055789 . ПМИД 19718023 .
- ^ Стейц Т.А. (июнь 1999 г.). «ДНК-полимеразы: структурное разнообразие и общие механизмы» . Журнал биологической химии . 274 (25): 17395–17398. дои : 10.1074/jbc.274.25.17395 . ПМИД 10364165 .
- ^ Перейти обратно: а б с д и Лосик Р., Уотсон Дж.Д., Бейкер Т.А., Белл С., Ганн А., Левин М.В. (2008). Молекулярная биология гена (6-е изд.). Сан-Франциско: Пирсон/Бенджамин Каммингс. ISBN 978-0-8053-9592-1 .
- ^ Маккарти Д., Миннер С., Бернштейн Х., Бернштейн С. (октябрь 1976 г.). «Скорость элонгации ДНК и распределение точек роста фага Т4 дикого типа и янтарного мутанта с задержкой ДНК». Журнал молекулярной биологии . 106 (4): 963–981. дои : 10.1016/0022-2836(76)90346-6 . ПМИД 789903 .
- ^ Перейти обратно: а б Харильо Х., Ибарра Б., Као-Гарсия Ф.Д. (2021). «Репликация ДНК: in vitro анализ и модели данных манипуляций с одиночными молекулами » . Журнал вычислительной и структурной биотехнологии . 19 : 3765–3778. дои : 10.1016/j.csbj.2021.06.032 . ПМЦ 8267548 . ПМИД 34285777 .
- ^ Файле Дж., Фортер П., Сен-Лин Т., Лоран Дж. (июнь 2002 г.). «Эволюция семейств ДНК-полимераз: доказательства множественного обмена генами между клеточными и вирусными белками» (PDF) . Журнал молекулярной эволюции . 54 (6): 763–773. Бибкод : 2002JMolE..54..763F . CiteSeerX 10.1.1.327.4738 . дои : 10.1007/s00239-001-0078-x . ПМИД 12029358 . S2CID 15852365 . Архивировано из оригинала (PDF) 29 июля 2020 г. Проверено 23 сентября 2019 г.
- ^ Перейти обратно: а б с Райя П., Каррони М., Анри Э., Пео-Арноде Дж., Брюле С., Беген П. и др. (январь 2019 г.). «Структура комплекса PolD DP1-DP2, связанного с ДНК, и ее значение для истории эволюции ДНК и РНК-полимераз» . ПЛОС Биология . 17 (1): e3000122. дои : 10.1371/journal.pbio.3000122 . ПМК 6355029 . ПМИД 30657780 .
- ^ Бём Э.М., Пауэрс К.Т., Кондратик К.М., Спайс М., Хаутман Дж.К., Вашингтон, штат Монтана (апрель 2016 г.). «Мотив ДНК-полимеразы η, взаимодействующий с белком пролиферирующего клеточного ядерного антигена (PCNA) (PIP), опосредует ее взаимодействие с C-концевым доменом Rev1» . Журнал биологической химии . 291 (16): 8735–8744. дои : 10.1074/jbc.M115.697938 . ПМЦ 4861442 . ПМИД 26903512 .
- ^ Ян В. (май 2014 г.). «Обзор ДНК-полимераз Y-семейства и тематическое исследование ДНК-полимеразы человека η» . Биохимия . 53 (17): 2793–2803. дои : 10.1021/bi500019s . ПМК 4018060 . ПМИД 24716551 .
- ^ Мага Г., Хубшер У., Спадари С., Виллани Дж. (2010). ДНК-полимеразы: открытие, функции характеристики в клеточных ДНК-транзакциях . Мировое научное издательство. ISBN 978-981-4299-16-9 .
- ^ Чой Ч., Бертон З.Ф., Ушева А. (февраль 2004 г.). «Аутоацетилирование факторов транскрипции как механизм контроля экспрессии генов» . Клеточный цикл . 3 (2): 114–115. дои : 10.4161/cc.3.2.651 . ПМИД 14712067 .
- ^ Чиен А., Эдгар Д.Б., Трела Дж.М. (сентябрь 1976 г.). «Полимераза дезоксирибонуклеиновой кислоты крайнего термофила Thermus aquaticus» . Журнал бактериологии . 127 (3): 1550–1557. дои : 10.1128/JB.127.3.1550-1557.1976 . ПМК 232952 . ПМИД 8432 .
- ^ Перейти обратно: а б Банах-Орловска М., Фиялковска И.Ю., Шаапер Р.М., Йончик П. (октябрь 2005 г.). «ДНК-полимераза II как фактор точности синтеза хромосомной ДНК в Escherichia coli» . Молекулярная микробиология . 58 (1): 61–70. дои : 10.1111/j.1365-2958.2005.04805.x . ПМИД 16164549 . S2CID 12002486 .
- ^ Вид белка InterPro: P61875
- ^ Перейти обратно: а б с Макарова К.С., Крупович М., Кунин Е.В. (2014). «Эволюция репликативных ДНК-полимераз у архей и их вклад в механизм репликации эукариот» . Границы микробиологии . 5 : 354. дои : 10.3389/fmicb.2014.00354 . ПМК 4104785 . ПМИД 25101062 .
- ^ Роэ М., Шраге К., Мейнхардт Ф. (декабрь 1991 г.). «Линейная плазмида pMC3-2 из Morchella conica структурно связана с аденовирусами». Современная генетика . 20 (6): 527–533. дои : 10.1007/BF00334782 . ПМИД 1782679 . S2CID 35072924 .
- ^ Олсон М.В., Даллманн Х.Г., МакГенри К.С. (декабрь 1995 г.). «Комплекс DnaX голофермента ДНК-полимеразы III Escherichia coli. Комплекс chipsi функционирует за счет увеличения сродства тау и гамма к дельта.дельта' до физиологически значимого диапазона» . Журнал биологической химии . 270 (49): 29570–29577. дои : 10.1074/jbc.270.49.29570 . ПМИД 7494000 .
- ^ Ляо Ю, Ли Ю, Шредер Дж.В., Симмонс Л.А., Битин Дж.С. (декабрь 2016 г.). «Динамика одномолекулярной ДНК-полимеразы бактериальной реплисомы в живых клетках» . Биофизический журнал . 111 (12): 2562–2569. Бибкод : 2016BpJ...111.2562L . дои : 10.1016/j.bpj.2016.11.006 . ПМК 5192695 . ПМИД 28002733 .
- ^ Перейти обратно: а б с Сюй ZQ, Диксон Н.Э. (декабрь 2018 г.). «Бактериальные реплисомы» . Современное мнение в области структурной биологии . 53 : 159–168. дои : 10.1016/j.sbi.2018.09.006 . ПМИД 30292863 .
- ^ Гудман М.Ф. (2002). «Склонные к ошибкам репарационные ДНК-полимеразы у прокариот и эукариот». Ежегодный обзор биохимии . 71 : 17–50. doi : 10.1146/annurev.biochem.71.083101.124707 . ПМИД 12045089 . S2CID 1979429 .
- ^ Мори Т., Накамура Т., Окадзаки Н., Фурукохри А., Маки Х., Акияма М.Т. (2012). «Escherichia coli DinB ингибирует развитие репликационной вилки, не вызывая существенного ответа SOS» . Гены и генетические системы . 87 (2): 75–87. дои : 10.1266/ggs.87.75 . ПМИД 22820381 .
- ^ Ярош Д.Ф., Годой В.Г., Уокер Г.К. (апрель 2007 г.). «Умелое и точное обход стойких повреждений ДНК с помощью ДНК-полимераз DinB» . Клеточный цикл . 6 (7): 817–822. дои : 10.4161/cc.6.7.4065 . ПМИД 17377496 .
- ^ Патель М., Цзян К., Вудгейт Р., Кокс М.М., Гудман М.Ф. (июнь 2010 г.). «Новая модель SOS-индуцированного мутагенеза: как белок RecA активирует ДНК-полимеразу V» . Критические обзоры по биохимии и молекулярной биологии . 45 (3): 171–184. дои : 10.3109/10409238.2010.480968 . ПМК 2874081 . ПМИД 20441441 .
- ^ Саттон, доктор медицинских наук, Уокер Г.К. (июль 2001 г.). «Управление ДНК-полимеразами: координация репликации ДНК, репарации ДНК и рекомбинации ДНК» . Труды Национальной академии наук Соединенных Штатов Америки . 98 (15): 8342–8349. Бибкод : 2001PNAS...98.8342S . дои : 10.1073/pnas.111036998 . ПМК 37441 . ПМИД 11459973 .
- ^ Перейти обратно: а б Райчаудхури П., Басу А.К. (март 2011 г.). «Генетическая потребность в мутагенезе перекрестной связи G[8,5-Me]T в Escherichia coli: ДНК-полимеразы IV и V конкурируют за рискованный обходной путь» . Биохимия . 50 (12): 2330–2338. дои : 10.1021/bi102064z . ПМК 3062377 . ПМИД 21302943 .
- ^ Мадру С., Хеннеке Г., Райя П., Югонно-Бофе I, Пеау-Арноде Г., Англия П. и др. (март 2020 г.). «Структурная основа повышенной процессивности ДНК-полимераз D-семейства в комплексе с PCNA» . Природные коммуникации . 11 (1): 1591. Бибкод : 2020NatCo..11.1591M . дои : 10.1038/s41467-020-15392-9 . ПМК 7101311 . ПМИД 32221299 .
- ^ Ишино Ю, Комори К, Канн И.К., Кога Ю (апрель 1998 г.). «Новое семейство ДНК-полимераз, обнаруженное у архей» . Журнал бактериологии . 180 (8): 2232–2236. дои : 10.1128/JB.180.8.2232-2236.1998 . ПМЦ 107154 . ПМИД 9555910 .
- ^ Соге Л., Райя П., Хеннеке Г., Деларю М. (2016). «Общая архитектура активного сайта между архейными PolD и многосубъединичными РНК-полимеразами, выявленная с помощью рентгеновской кристаллографии» . Природные коммуникации . 7 : 12227. Бибкод : 2016NatCo...712227S . дои : 10.1038/ncomms12227 . ПМЦ 4996933 . ПМИД 27548043 .
- ^ Ямасаки К., Урусибата Ю., Ямасаки Т., Арисака Ф., Мацуи И. (август 2010 г.). «Структура раствора N-концевого домена небольшой субъединицы ДНК-полимеразы D-семейства архей обнаруживает эволюционное родство с эукариотическими полимеразами B-семейства» . Письма ФЭБС . 584 (15): 3370–3375. дои : 10.1016/j.febslet.2010.06.026 . ПМИД 20598295 . S2CID 11229530 .
- ^ Исино С, Исино Ю (2014). «ДНК-полимеразы как полезные реагенты для биотехнологии - история исследований в этой области» . Границы микробиологии . 5 : 465. дои : 10.3389/fmicb.2014.00465 . ПМК 4148896 . ПМИД 25221550 .
- ^ Кунин Е.В., Крупович М., Ишино С., Ишино Ю. (июнь 2020 г.). «Механизм репликации LUCA: общий источник репликации и транскрипции ДНК» . БМК Биология . 18 (1): 61. дои : 10.1186/s12915-020-00800-9 . ПМЦ 7281927 . ПМИД 32517760 .
- ^ Ямтич Дж., Суизи Дж.Б. (май 2010 г.). «Семейство ДНК-полимераз X: функции, структура и клеточные роли» . Biochimica et Biophysical Acta (BBA) - Белки и протеомика . 1804 (5): 1136–1150. дои : 10.1016/j.bbapap.2009.07.008 . ПМК 2846199 . ПМИД 19631767 .
- ^ Чанский М.Л., Маркс А., Пит А. (2012). Основная медицинская биохимия Маркса: клинический подход (4-е изд.). Филадельфия: Wolter Kluwer Health/Lippincott Williams & Wilkins. п. глава13. ISBN 978-1608315727 .
- ^ Чунг Д.В., Чжан Дж.А., Тан С.К., Дэви Э.В., Со А.Г., Дауни К.М. (декабрь 1991 г.). «Первичная структура каталитической субъединицы ДНК-полимеразы человека дельта и хромосомное расположение гена» . Труды Национальной академии наук Соединенных Штатов Америки . 88 (24): 11197–11201. Бибкод : 1991PNAS...8811197C . дои : 10.1073/pnas.88.24.11197 . ПМК 53101 . ПМИД 1722322 .
- ^ Перселл З.Ф., Исоз И., Лундстрём Э.Б., Йоханссон Э., Кункель Т.А. (июль 2007 г.). «ДНК-полимераза дрожжей эпсилон участвует в репликации ДНК ведущей цепи» . Наука . 317 (5834): 127–130. Бибкод : 2007Sci...317..127P . дои : 10.1126/science.1144067 . ПМК 2233713 . ПМИД 17615360 .
- ^ Лухан С.А., Уильямс Дж.С., Кункель Т.А. (сентябрь 2016 г.). «ДНК-полимеразы разделяют работу по репликации генома» . Тенденции в клеточной биологии . 26 (9): 640–654. дои : 10.1016/j.tcb.2016.04.012 . ПМЦ 4993630 . ПМИД 27262731 .
- ^ Джонсон Р.Э., Классен Р., Пракаш Л., Пракаш С. (июль 2015 г.). «Основная роль ДНК-полимеразы δ в репликации как ведущих, так и отстающих цепей ДНК» . Молекулярная клетка . 59 (2): 163–175. doi : 10.1016/j.molcel.2015.05.038 . ПМЦ 4517859 . ПМИД 26145172 .
- ^ Перейти обратно: а б Дубли С., Зан К.Е. (2014). «Структурные данные о репликации ДНК эукариот» . Границы микробиологии . 5 : 444. дои : 10.3389/fmicb.2014.00444 . ПМК 4142720 . ПМИД 25202305 .
- ^ Эдвардс С., Ли К.М., Леви Д.Л., Браун Дж., Сноу П.М., Кэмпбелл Дж.Л. (апрель 2003 г.). «ДНК-полимераза эпсилон Saccharomyces cerevisiae и сигма-полимераза взаимодействуют физически и функционально, что указывает на роль полимеразы эпсилон в слипании сестринских хроматид» . Молекулярная и клеточная биология . 23 (8): 2733–2748. дои : 10.1128/mcb.23.8.2733-2748.2003 . ПМЦ 152548 . ПМИД 12665575 .
- ^ Заремба-Недзведска К., Касерес Э.Ф., Со Дж.Х., Бэкстрем Д., Юзокайте Л., Ванкастер Э. и др. (январь 2017 г.). «Асгардские археи проливают свет на происхождение сложности эукариотических клеток» . Природа 541 (7637): 353–358. Бибкод : 2017Nature.541..353Z . дои : 10.1038/nature21031 . ОСТИ 1580084 . ПМИД 28077874 . S2CID 4458094 .
- ^ Омори Х., Ханафуса Т., Охаши Э., Вазири С. (2009). Отдельные роли структурированных и неструктурированных областей ДНК-полимераз Y-семейства . Достижения в области химии белков и структурной биологии. Том. 78. стр. 99–146. дои : 10.1016/S1876-1623(08)78004-0 . ISBN 9780123748270 . ПМК 3103052 . ПМИД 20663485 .
- ^ Ган Г.Н., Виттшибен Дж.П., Виттшибен Б.О., Вуд Р.Д. (январь 2008 г.). «ДНК-полимераза дзета (pol zeta) у высших эукариот» . Клеточные исследования . 18 (1): 174–183. дои : 10.1038/cr.2007.117 . ПМИД 18157155 .
- ^ Бьенсток Р.Дж., Берд В.А., Уилсон С.Х. (октябрь 2014 г.). «Филогенетический анализ и эволюционное происхождение членов X-семейства ДНК-полимераз» . Восстановление ДНК . 22 : 77–88. дои : 10.1016/j.dnarep.2014.07.003 . ПМК 4260717 . ПМИД 25112931 .
- ^ Прасад Р., Чаглаян М., Дай Д.П., Надалутти К.А., Чжао М.Л., Гассман Н.Р. и др. (декабрь 2017 г.). «ДНК-полимераза β: недостающее звено основного механизма эксцизионной репарации в митохондриях млекопитающих» . Восстановление ДНК . 60 : 77–88. дои : 10.1016/j.dnarep.2017.10.011 . ПМЦ 5919216 . ПМИД 29100041 .
- ^ Чжан Л., Чан С.С., Вольф DJ (июль 2011 г.). «Митохондриальные нарушения дисфункции ДНК-полимеразы γ: от анатомической диагностики к молекулярной патологии» . Архивы патологии и лабораторной медицины . 135 (7): 925–934. дои : 10.5858/2010-0356-RAR.1 . ПМК 3158670 . ПМИД 21732785 .
- ^ Стампф JD, Copeland WC (январь 2011 г.). «Репликация митохондриальной ДНК и заболевания: данные о мутациях ДНК-полимеразы γ» . Клеточные и молекулярные науки о жизни . 68 (2): 219–233. дои : 10.1007/s00018-010-0530-4 . ПМК 3046768 . ПМИД 20927567 .
- ^ Хогг М., Зауэр-Эрикссон А.Е., Йоханссон Э. (март 2012 г.). «Беспорядочный синтез ДНК с помощью ДНК-полимеразы θ человека» . Исследования нуклеиновых кислот . 40 (6): 2611–2622. дои : 10.1093/nar/gkr1102 . ПМК 3315306 . ПМИД 22135286 .
- ^ Перейти обратно: а б «UniProtKB — Q7Z5Q5 (DPOLN_HUMAN)» . Унипрот . Проверено 5 июля 2018 г.
- ^ Капп Дж.Д., Нильсен Б.Л. (ноябрь 2014 г.). «Миниобзор: Репликация ДНК в митохондриях растений» . Митохондрия . 19 (Часть Б): 231–237. дои : 10.1016/j.mito.2014.03.008 . ПМЦ 417701 . ПМИД 24681310 .
- ^ Перейти обратно: а б с Роусон Дж.М., Николаичик О.А., Кил Б.Ф., Патак В.К., Ху В.С. (ноябрь 2018 г.). «Рекомбинация необходима для эффективной репликации ВИЧ-1 и поддержания целостности вирусного генома» . Исследования нуклеиновых кислот . 46 (20): 10535–10545. дои : 10.1093/nar/gky910 . ПМК 6237782 . ПМИД 30307534 .
- ^ Кромер Д., Гримм А.Дж., Шлуб Т.Э., Мак Дж., Давенпорт, член парламента (январь 2016 г.). «Оценка скорости переключения и рекомбинации матрицы ВИЧ in vivo» . СПИД . 30 (2): 185–192. дои : 10.1097/QAD.0000000000000936 . ПМИД 26691546 . S2CID 20086739 .
- ^ Ху В.С., Темин Х.М. (ноябрь 1990 г.). «Ретровирусная рекомбинация и обратная транскрипция». Наука . 250 (4985): 1227–1233. Бибкод : 1990Sci...250.1227H . дои : 10.1126/science.1700865 . ПМИД 1700865 .
- ^ Гулиан М., Лукас З.Дж., Корнберг А. (февраль 1968 г.). «Ферментативный синтез дезоксирибонуклеиновой кислоты. XXV. Очистка и свойства полимеразы дезоксирибонуклеиновой кислоты, индуцированной инфицированием фагом Т4» . Журнал биологической химии . 243 (3): 627–638. дои : 10.1016/S0021-9258(18)93650-1 . ПМИД 4866523 .
- ^ Хуанг В.М., Lehman IR (май 1972 г.). «О экзонуклеазной активности полимеразы дезоксирибонуклеиновой кислоты фага Т4» . Журнал биологической химии . 247 (10): 3139–3146. дои : 10.1016/S0021-9258(19)45224-1 . ПМИД 4554914 .
- ^ Гиллин Ф.Д., Носсал Н.Г. (сентябрь 1976 г.). «Контроль частоты мутаций с помощью ДНК-полимеразы бактериофага Т4. I. Антимутаторная ДНК-полимераза CB120 дефектна при смещении цепи» . Журнал биологической химии . 251 (17): 5219–5224. дои : 10.1016/S0021-9258(17)33149-6 . ПМИД 956182 .
- ^ Перейти обратно: а б Бернштейн Х. (август 1967 г.). «Влияние на рекомбинацию мутационных дефектов ДНК-полимеразы и дезоксицитидилатгидроксиметилазы фага Т4Д» . Генетика . 56 (4): 755–769. дои : 10.1093/генетика/56.4.755 . ПМЦ 1211652 . ПМИД 6061665 .
Дальнейшее чтение
[ редактировать ]- Бургерс П.М., Кунин Е.В., Бруфорд Э., Бланко Л., Бертис К.С., Кристман М.Ф. и др. (ноябрь 2001 г.). «Эукариотические ДНК-полимеразы: предложение по пересмотренной номенклатуре» . Журнал биологической химии . 276 (47): 43487–43490. дои : 10.1074/jbc.R100056200 . hdl : 10261/338658 . ПМИД 11579108 .
Внешние ссылки
[ редактировать ]- ДНК + полимеразы в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- PDB Молекула месяца ДНК-полимераза
- Необычный механизм репарации ДНК-полимеразы лямбда , Университет штата Огайо , 25 июля 2006 г.
- Отличная анимация ДНК-полимеразы от WEHI на 1:45 минуте, заархивировано 5 декабря 2014 г. на Wayback Machine.
- Трехмерные макромолекулярные структуры ДНК-полимеразы из банка данных EM (EMDB)