Титаноцена дихлорид
| |

| |

| |
| Имена | |
|---|---|
| Название ИЮПАК
Дихлордобис (η 5 -циклопентадиенил)титан
| |
| Другие имена
дихлорид титаноцена, дихлорбис(циклопентадиенил)титан(IV)
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.013.669 |
| Номер ЕС |
|
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 3261 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| С 10 Н 10 Cl 2 Ти | |
| Молярная масса | 248.96 g/mol |
| Появление | ярко-красное твердое вещество |
| Плотность | 1,60 г/см 3 , твердый |
| Температура плавления | 289 ° С (552 ° F; 562 К) |
| сл. соль. с гидролизом | |
| Структура | |
| Триклиника | |
| Расст. четырехгранный | |
| Опасности [ 1 ] | |
| СГС Маркировка : | |

| |
| Предупреждение | |
| Х315 , Х335 | |
| P201 , P202 , P261 , P264 , P270 , P271 , P280 , P281 , P301+P310 , P301+P312 , P302+P352 , P304+P340 , P305+P351+P338 , P308+P313 , P312 , P330 , P332+P313 , P337+P313 , P362 , P403+P233 , P405 , P501 | |
| NFPA 704 (огненный алмаз) | |
| Родственные соединения | |
Родственные соединения
|
Ферроцен Цирконоцен дихлорид Гафноцен дихлорид Ванадоцен дихлорид Ниобоцена дихлорид Танталоцена дихлорид Молибдоцен дихлорид дихлорид вольфрамоцена ТиСl 4 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
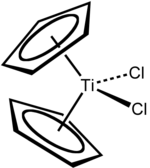
Титаноцендихлорид представляет собой титанорганическое соединение формулы ( η 5 -C 5 H 5 ) 2 TiCl 2 , обычно сокращенно Cp 2 TiCl 2 . Этот металлоцен является распространенным реагентом в металлоорганическом и органическом синтезе . Он существует в виде ярко-красного твердого вещества, которое медленно гидролизуется на воздухе. [ 2 ] Он проявляет противоопухолевую активность и является первым неплатиновым комплексом, прошедшим клинические испытания в качестве химиотерапевтического препарата. [ 3 ]
Подготовка и структура
[ редактировать ]Стандартное получение Cp 2 TiCl 2 начинается с тетрахлорида титана . Оригинальный синтез Уилкинсона и Бирмингема с использованием циклопентадиенида натрия . [ 4 ] до сих пор широко используется: [ 5 ]
- 2 NaC 5 H 5 + TiCl 4 → (C 5 H 5 ) 2 TiCl 2 + 2 NaCl
Его также можно получить, используя свежеперегнанный циклопентадиен , а не его натриевое производное: [ 6 ]
- 2 C 5 H 6 + TiCl 4 → (C 5 H 5 ) 2 TiCl 2 + 2 HCl
Ориентируясь на геометрию Ti-центра, Cp 2 TiCl 2 принимает искаженную тетраэдрическую геометрию (считая Cp монодентатным лигандом). Расстояние Ti-Cl составляет 2,37 Å, а угол Cl-Ti-Cl составляет 95°. [ 7 ]
Реакции
[ редактировать ]Реакции замещения галогенидов
[ редактировать ]Cp 2 TiCl 2 служит источником Cp 2 Ti. 2+ . Широкий спектр нуклеофилов будет вытеснять хлорид. С NaSH и полисульфидными солями получают сульфидные производные Cp 2 Ti(SH) 2 и Cp 2 TiS 5 . [ 8 ]
Реактив Петасиса Cp 2 Ti(CH 3 ) 2 получают действием хлорида метилмагния. [ 9 ] или метиллитий [ 10 ] на Cp 2 TiCl 2 . Этот реагент полезен для превращения сложных эфиров в виниловые эфиры.
Реагент Теббе Cp 2 TiCl(CH 2 )Al(CH 3 ) 2 , возникает при действии 2-х эквивалентов Al(CH 3 ) 3 на Cp 2 TiCl 2 . [ 11 ] [ 12 ]
Реакции, влияющие на лиганды Cp
[ редактировать ]Один лиганд Cp можно удалить из Cp 2 TiCl 2 с образованием тетраэдрического CpTiCl 3 . Это преобразование можно осуществить с помощью TiCl 4 или реакцией с SOCl 2 . [ 13 ]
Сэндвич-комплекс (Циклогептатриенил)(циклопентадиенил)титан получают обработкой дихлорида титаноцена циклогептатриенилом лития. [ 14 ]
Сам титаноцен, TiCp 2 , настолько реактивен, что перегруппировывается в Ti. III гидридный димер и стал предметом многочисленных исследований. [ 15 ] [ 16 ] Этот димер можно поймать, проведя восстановление дихлорида титаноцена в присутствии лигандов; в присутствии бензола комплекс образуется фульваленовый µ (η 5 :или 5 -фульвален)-ди-(μ-гидрид)-бис(η 5 -циклопентадиенилтитан), можно получить и полученный сольват структурно охарактеризовать с помощью рентгеновской кристаллографии . [ 17 ] Об этом же соединении сообщалось ранее при литийалюминийгидрида. восстановлении [ 18 ] и амальгамы натрия восстановление [ 19 ] дихлорида титаноцена и изучен 1 H ЯМР [ 20 ] до его окончательной характеристики. [ 15 ] [ 16 ]

Редокс
[ редактировать ]Восстановление цинком дает димер хлорида бис (циклопентадиенил) титана (III) опосредованном растворителем в химическом равновесии, : [ 21 ] [ 22 ]
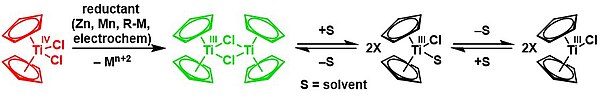
Cp 2 TiCl 2 является предшественником Ti II производные. Восстановление исследовали с использованием реактива Гриньяра и соединений алкиллития. Восстановители, с которыми удобнее работать, включают Mg, Al или Zn. Следующие синтезы демонстрируют некоторые соединения, которые могут быть получены путем восстановления дихлорида титаноцена в присутствии π-акцепторных лигандов: [ 23 ]
- Cp 2 TiCl 2 + 2 CO + Mg → Cp 2 Ti(CO) 2 + MgCl 2
- Cp 2 TiCl 2 + 2 PR 3 + Mg → Cp 2 Ti(PR 3 ) 2 + MgCl 2
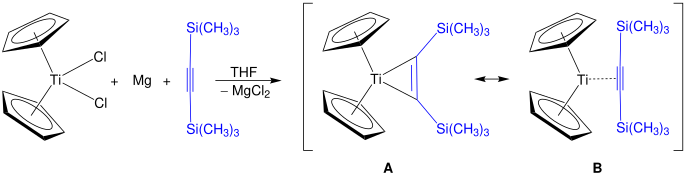
Алкиновые производные титаноцена имеют формулу (C 5 H 5 ) 2 Ti(C 2 R 2 соответствующие бензольные комплексы . ) и известны [ 24 ] Одним из семейств производных являются титаноциклопентадиены. [ 25 ] Реагент Розенталя , Cp 2 Ti(η 2 -Me 3 SiC≡CSiMe 3 ), можно получить этим методом. Показаны две структуры, A и B , которые вносят резонансный вклад в фактическую структуру реагента Розенталя. [ 26 ]
Эквиваленты титаноцена реагируют с алкенилалкинами с последующим карбонилированием и гидролизом с образованием бициклических циклопентадиенонов, что связано с реакцией Паусона-Кханда . [ 27 ] Аналогичная реакция представляет собой восстановительную циклизацию енонов с образованием соответствующего спирта стереоселективным образом. [ 28 ]
Восстановление дихлорида титаноцена в присутствии сопряженных диенов, таких как 1,3-бутадиен, дает η 3 -аллилтитановые комплексы. [ 29 ] Сходные реакции происходят с диинами. Кроме того, титаноцен может катализировать метатезис связей C–C с образованием асимметричных диинов. [ 25 ]
Дихлорид титаноцена как фотоокислительно-восстановительный катализатор для открытия эпоксидов зеленым светом. [ 30 ]
Производные (C 5 Me 5 ) 2 TiCl 2
[ редактировать ]множество аналогов Cp 2 TiCl 2 Известно . Яркими примерами являются метилированные по кольцу производные (C 5 H 4 Me) 2 TiCl 2 и (C 5 Me 5 ) 2 TiCl 2 .
Медицинские исследования
[ редактировать ]Титаноцена дихлорид исследовали как противораковое лекарство. Фактически, это был первый неплатиновый координационный комплекс и первый металлоцен, прошедший клинические испытания. [ 3 ] [ 31 ]
Ссылки
[ редактировать ]- ^ «Краткая информация о классификации и маркировке» . Проверено 5 декабря 2021 г.
- ^ Будавер С., изд. (1989). Индекс Merck (11-е изд.). Мерк и Ко., Инк.
- ^ Jump up to: а б Роат-Мэлоун, RM (2007). Биоинорганическая химия: Краткий курс (2-е изд.). Джон Уайли и сыновья . стр. 19–20. ISBN 978-0-471-76113-6 .
- ^ Уилкинсон, Г .; Бирмингем, JG (1954). «Бис-циклопентадиенильные соединения Ti, Zr, V, Nb и Ta». Дж. Ам. хим. Соц. 76 (17): 4281–4284. дои : 10.1021/ja01646a008 .
- ^ Сара Э. Джонсон; Тейлор А. Белл; Джозеф К. Уэст (2022). «Cp 2 TiCl 2 : Синтез, характеристика, моделирование и катализ». Журнал химического образования . 99 (5): 2121–2128. Бибкод : 2022JChEd..99.2121J . doi : 10.1021/acs.jchemed.1c01272 . S2CID 248287682 .
- ^ Бирмингем, JM (1965). «Синтез циклопентадиенильных соединений металлов». Адв. Металлорганический. хим. Достижения металлоорганической химии. 2 : 365–413. дои : 10.1016/S0065-3055(08)60082-9 . ISBN 9780120311026 .
- ^ Клирфилд, Авраам; Уорнер, Дэвид Кейт; Салдарриага Молина, Карлос Херман; Ропал, Раманатан; Берналь, Иван; и др. (1975). «Структурные исследования комплексов (π-C 5 H 5 ) 2 MX 2 и их производных. Структура дихлорида бис (π-циклопентадиенил) титана». Может. Дж. Чем . 53 (11): 1621–1629. дои : 10.1139/v75-228 .
- ^ Шейвер, Алан; МакКолл, Джеймс М.; Мармолехо, Габриэла (1990). «Циклометаллаполисульфаны (и селаны) бис(η5-циклопентадиенил)титана (IV), циркония (IV), молибдена (IV) и вольфрама (IV)». Циклометаллаполисульфаны (и селаны) Bis( η 5 -Циклопентадиенил) Титан(IV), Цирконий(IV), Молибден(IV) и Вольфрам(IV) . Неорганические синтезы. Том. 27. С. 59–65. дои : 10.1002/9780470132586.ch11 . ISBN 9780470132586 .
- ^ Пайак, Дж. Ф.; Хьюз, Д.Л.; Кай, Д.; Коттрелл, ИФ; Верховен, Т.Р. (2002). «Диметилтитаноцен» . Органические синтезы . 79:19 .
- ^ Клаус, К.; Бестиан, Х. (1962). «О действии водорода на некоторые металлоорганические соединения и комплексы». «Анн» Юстуса Либиха. Хим. 654 : 8–19. дои : 10.1002/jlac.19626540103 .
- ^ Херрманн, Вашингтон (1982). «Метиленовый мост». Адв. Органомет. Хим . Достижения металлоорганической химии. 20 : 159–263. дои : 10.1016/s0065-3055(08)60522-5 . ISBN 9780120311200 .
- ^ Штраус, Д.А. (2000). « μ -Хлоробис(циклопентадиенил)(диметилалюминий) -μ- метилентитан». Энциклопедия реагентов для органического синтеза . Лондон: Джон Уайли.
- ^ Чандра, К.; Шарма, РК; Кумар, Н.; Гарг, Б.С. (1980). «Подготовка η 5 -Циклопентадиенилтитан трихлорид и η 5 -Метилциклопентадиенилтитан трихлорид». Chem. Ind. – Лондон . 44 : 288–289.
- ^ Камарго, Луана К.; Бриганти, Маттео; Сантана, Франчелли С.; Стинген, Данило; Рибейро, Ронни Р.; Нуньес, Джована Г.; Соареш, Хайса Ф.; Сальвадори, Энрико; Кьеза, Марио; Бенчи, Стефано; Торре, Ренато; Сорасе, Лоренцо; Тотти, Федерико; Сессоли, Роберта (2021). «Изучение металлоорганического пути к молекулярным спиновым кубитам: случай [Cp Ti (cot)]» . Angewandte Chemie, международное издание . 60 (5): 2588–2593. дои : 10.1002/anie.202009634 . hdl : 2318/1765157 . ПМИД 33051985 . S2CID 222351619 .
- ^ Jump up to: а б Уэйлс, ПК; Куттс, RSP; Вейгольд, Х. (1974). «Титаноцен» . Металлоорганическая химия титана, циркония и гафния . Академическая пресса . стр. 229–237. ISBN 9780323156479 .
- ^ Jump up to: а б с Мехротра, RC; Сингх, А. (2000). «4.3.6 η 5 -Циклопентадиенил d-блок-металлические комплексы» . Металлоорганическая химия: унифицированный подход (2-е изд.). Нью-Дели: New Age International Publishers. Стр. 243–268. ISBN 9788122412581 .
- ^ Jump up to: а б Троянов Сергей Иванович; Антропиусова, Елена; Мах, Карел (1992). «Прямое доказательство молекулярной структуры димерного титаноцена; Рентгеновская структура μ(η 5 :или 5 -фульвален)-ди-(μ-гидрид)-бис(η 5 -циклопентадиенилтитан) · 1,5 бензол». J. Organomet. Chem. 427 (1): 49–55. doi : 10.1016/0022-328X(92)83204-U .
- ^ Антропий, Елена; Доседлова, Алена; Ганус, Владимир; Карел, Мах (1981). «Приготовление ц-(η 5 :или 5 -Фульвален)-ди-μ-гидрид-бис(η 5 -циклопентадиенилтитан) восстановлением Cp 2 TiCl 2 с помощью LiAlH 4 в ароматических растворителях». Transition Met. Chem. 6 (2): 90–93. doi : 10.1007/BF00626113 . S2CID 101189483 .
- ^ Куэнка, Томас; Херрманн, Вольфганг А.; Эшворт, Теренс В. (1986). «Химия оксофильных переходных металлов. 2. Новые производные титаноцена и цирконоцена». Металлоорганические соединения . 5 (12): 2514–2517. дои : 10.1021/om00143a019 .
- ^ Lemenovskii, D. A.; Urazowski, I. F.; Grishin, Yu K.; Roznyatovsky, V. A. (1985). " 1 Спектры ЯМР H и электронная структура биядерного ниобоцена и титаноцена, содержащих фульваленовые лиганды». J. Organomet. Chem. 290 (3): 301–305. doi : 10.1016/0022-328X(85)87293-4 .
- ^ Манзер, Ле; Минц, Э.А.; Маркс, Ти Джей (1982). «18. Циклопентадиенильные комплексы титана(III) и ванадия(III)». Неорганические синтезы . Том. 21. С. 84–86. дои : 10.1002/9780470132524.ch18 . ISBN 9780470132524 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Ньюджент, Уильям А.; РаджанБабу, ТВ (1988). «Радикалы с переходными металлами в органическом синтезе. Циклизация эпоксидных олефинов, индуцированная титаном (III)». Дж. Ам. хим. Соц. 110 (25): 8561–8562. дои : 10.1021/ja00233a051 .
- ^ Кустер, Эрик (2002). «Бис(η5-2,4-циклопентадиенил)бис(триметилфосфин)титан». Бис(5-2,4-циклопентадиенил)бис(триметилфосфин)титан . Энциклопедия реагентов для органического синтеза . Джон Уайли. дои : 10.1002/047084289X.rn00022 . ISBN 0471936235 .
- ^ Бухвальд, СЛ; Нильсен, РБ (1988). «Металлокомплексы бензинов, циклоалкинов, ациклических алкинов и алкенов 4-й группы». хим. Откр. 88 (7): 1047–1058. дои : 10.1021/cr00089a004 .
- ^ Jump up to: а б Розенталь, Уве; Пеллни, Поль-Майкл; Кирхбауэр, Фрэнк Г.; Бурлаков, Владимир Васильевич (2000). «Что делают титано- и цирконоцены с диинами и полиинами?». хим. Откр. 33 (2): 119–129. дои : 10.1021/ar9900109 . ПМИД 10673320 .
- ^ Розенталь, Уве; Бурлаков Владимир Владимирович; Арндт, Пердита; Бауманн, Вольфганг; Спанненберг, Анке (2003). «Титаноценовый комплекс бис (триметилсилил) ацетилена: синтез, структура и химия». Металлоорганические соединения . 22 (5): 884–900. дои : 10.1021/om0208570 .
- ^ Хикс, ФА; и др. (1999). «Область применения внутримолекулярной реакции типа Паусона-Ханда, катализируемой титаноценом». Дж. Ам. хим. Соц. 121 (25): 5881–5898. дои : 10.1021/ja990682u .
- ^ Каблауи, Нью-Мексико; Бухвальд, С.Л. (1998). «Разработка метода восстановительной циклизации енонов титановым катализатором». Дж. Ам. хим. Соц. 118 (13): 3182–3191. дои : 10.1021/ja954192n .
- ^ Сато, Ф.; Урабе, Хирокадзу; Окамото, Сентаро (2000). «Синтез титанорганических комплексов из алкенов и алкинов и их синтетическое применение». хим. Откр. 100 (8): 2835–2886. дои : 10.1021/cr990277l . ПМИД 11749307 .
- ^ Чжан, Чжэньхуа; Хильче, Тобиас; Слак, Дэниел; Ритдейк, Нильс Р.; Олойеде, Угочиньере Н.; Флауэрс, Роберт А.; Ганзойер, Андреас (08.06.2020). «Титаноцены как фотоокислительно-восстановительные катализаторы с использованием облучения зеленым светом» . Международное издание «Прикладная химия» . 59 (24): 9355–9359. дои : 10.1002/anie.202001508 . ISSN 1433-7851 . ПМЦ 7317808 . ПМИД 32216162 .
- ^ Чини, М.; Брэдшоу, ТД; Вудворд, С. (2017). «Использование титановых комплексов для победы над раком: взгляд с плеч титанов» (PDF) . хим. Соц. Преподобный . 46 (4): 1040–1051. дои : 10.1039/C6CS00860G . ПМИД 28124046 . Архивировано из оригинала (PDF) 19 июля 2018 г. Проверено 13 июля 2019 г.
Дальнейшее чтение
[ редактировать ]- Пайак, Дж. Ф.; Хьюз, Д.Л.; Кай, Д.; Коттрелл, ИФ; Верховен Т.Р. «Диметилтитаноценовый титан, бис( η 5 1-ил)диметил-" . Органический синтез . 79:19 -2,4-циклопентадиен - ; Сборник томов , т. 10 ..
- Гамбаротта, С.; Флориани, К.; Кьези-Вилла, А.; Гуастини, К. (1983). «Циклопентадиенилдихлортитан (III): реагент, подобный свободным радикалам, для восстановления кратных азо(N:N) связей в азо- и диазосоединениях». Дж. Ам. хим. Соц. 105 (25): 7295–7301. дои : 10.1021/ja00363a015 .
- Чирик, П.Дж. (2010). «Сэндвич-комплексы переходных металлов группы 4: все еще свежи спустя почти 60 лет». Металлоорганические соединения . 29 (7): 1500–1517. дои : 10.1021/om100016p .
