Нитрат ртути(II)
| |

| |
| Имена | |
|---|---|
| ИЮПАК имена
Динитрат ртути
Нитрат ртути(II) | |
| Другие имена
Нитрат ртути
| |
| Идентификаторы | |
| |
3D model ( JSmol )
|
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.030.126 |
| Номер ЕС |
|
ПабХим CID
|
|
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
| Число | 1625 |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| Ртуть(NO 3 ) 2 | |
| Молярная масса | 324,60 г/моль (безводный) |
| Появление | бесцветные кристаллы или белый порошок |
| Запах | острый |
| Плотность | 4,3 г/см 3 (моногидрат) |
| Температура плавления | 79 ° C (174 ° F, 352 К) (моногидрат) |
| растворимый | |
| Растворимость | растворим в азотной кислоте , ацетоне , аммиаке нерастворим в этаноле |
| −74.0·10 −6 см 3 /моль | |
| Опасности | |
| СГС Маркировка : | |
   
| |
| Опасность | |
| Х272 , Х300 , Х310 , Х330 , Х373 , Х410 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | негорючий |
| Паспорт безопасности (SDS) | КМГС 0980 |
| Родственные соединения | |
Другие анионы
|
Сульфат ртути(II) Хлорид ртути(II) |
Другие катионы
|
Нитрат цинка Нитрат кадмия |
Родственные соединения
|
Нитрат ртути(I) |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
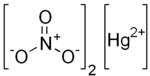
Нитрат ртути(II) представляет собой неорганическое соединение с химической формулой Hg ( NO 3 ) 2 . Это ртутная . соль кислоты азотной ХНО 3 . Содержит катионы ртути(II). ртуть 2+ и нитрат- анионы NO − 3 и кристаллизационная вода H 2 O в случае водной соли. Нитрат ртути(II) образует гидраты. Hg(NO 3 ) 2 · x H 2 O . Безводные и водные соли — бесцветные или белые растворимые кристаллические вещества, которые иногда используются в качестве реагентов . Нитрат ртути(II) получают путем обработки ртути горячей концентрированной азотной кислотой. Ни безводный, ни моногидрат не был подтвержден рентгеновской кристаллографией . [1] Безводный материал используется более широко. [ нужны разъяснения ]
Использование
[ редактировать ]Нитрат ртути(II) используется как окислитель в органическом синтезе , как нитрификатор , как аналитический реагент в лабораториях, при производстве войлока , при производстве гремучей ртути . [2] Альтернативный качественный тест Цейзеля можно провести с использованием нитрата ртути(II) вместо нитрата серебра, что приводит к образованию алого красного йодида ртути(II) . [3]
Информация о здоровье
[ редактировать ]Соединения ртути очень токсичны. Использование этого соединения шляпниками и последующее отравление упомянутых шляпников ртутью фразы « безумный как шляпник является распространенной теорией происхождения ».
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Нольте, М.; Пантенбург, И.; Мейер, Г. (9 декабря 2005 г.). «Моногидрат основного нитрата ртути, [Hg(OH)](NO 3 )(H 2 O)» . Zeitschrift für anorganische und allgemeine Chemie (на немецком языке). 632 (1). Издательство Wiley : 111–113. дои : 10.1002/zaac.200500344 . ISSN 0044-2313 . Архивировано из оригинала 27 ноября 2021 года . Проверено 16 мая 2022 г.
- ^ «Нитрата ртути моногидрат» . Химическая книга . 2023 . Проверено 30 июня 2024 г.
- ^ Ван, Зеронг (2010). «Определение Цейзеля». Комплексные органические реакции и реагенты . Джон Уайли и сыновья. стр. 3115–3118. дои : 10.1002/9780470638859.conrr689 . ISBN 9780470638859 .
Внешние ссылки
[ редактировать ]- ATSDR - Портал о токсичных веществах - Меркурий (14.11.2013)
- ATSDR – Заявление общественного здравоохранения: Ртуть (14.11.2013)
- АЦДР – ВНИМАНИЕ! Характер воздействия металлической ртути, 26.06.97 (ссылка не прослеживается, 14.11.2013)
- ATSDR - Рекомендации по медицинскому лечению ртути (14.11.2013)
- ATSDR - Токсикологический профиль: Ртуть (14.11.2013)
- Данные безопасности (MSDS) [ постоянная мертвая ссылка ] (ссылка не отслеживается, 14.11.2013)
- Нитрат ртути (ICSC)
- Меркурий. Архивировано 17 февраля 2018 г. в Wayback Machine.
- Информационные пакеты о Меркурии
- Как выполнить хорошие электрические соединения с помощью ртути , Ежемесячник Popular Science , февраль 1919 г., ненумерованная страница, отсканировано Google Books: https://books.google.com/books?id=7igDAAAAMBAJ&pg=PT14
