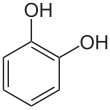
Катехол
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное имя IUPAC
Бензол-1,2-диол [ 1 ] | |||
| Другие имена
Пирокатехол [ 1 ]
1,2-бенцендиол 2-гидроксифенол 1,2-дигидроксибензол O -Benzendiol О -дигидроксибензол | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| 471401 | |||
| Чеби | |||
| Химический | |||
| Chemspider | |||
| Наркоман | |||
| Echa Infocard | 100.004.025 | ||
| ЕС номер |
| ||
| 2936 | |||
| Кегг | |||
PubChem CID
|
|||
| Rtecs номер |
| ||
| НЕКОТОРЫЙ | |||
Comptox Dashboard ( EPA )
|
|||
| Характеристики | |||
| C 6 H 6 O 2 | |||
| Молярная масса | 110.112 g·mol −1 | ||
| Появление | кристаллы белого до коричневого перья | ||
| Запах | слабый, фенольный запах | ||
| Плотность | 1,344 г/см 3 , твердый | ||
| Точка плавления | 105 ° C (221 ° F; 378 К) | ||
| Точка кипения | 245,5 ° C (473,9 ° F; 518,6 K) (Sublimes) | ||
| 312 г/л при 20 ° C [ 2 ] | |||
| Растворимость | очень растворим в пиридине растворимый в хлороформе , бензол , CCL 4 , эфир , этилацетат | ||
| log p | 0.88 | ||
| Давление паров | 20 Па (20 ° С) | ||
| Кислотность (p k a ) | 9.45, 12.8 | ||
| −6.876 × 10 −5 см 3 /мол | |||
Показатель преломления ( N D )
|
1.604 | ||
| 2,62 ± 0,03 D [ 3 ] | |||
| Структура | |||
| моноклинный | |||
| Термохимия | |||
Энтальпия STD
образование (Δ f h ⦵ 298 ) |
-354,1 кДж · −1 | ||
Энтальпия слияния (Δ f h ⦵ фьюс )
|
22,8 кДж · раз −1 (в точке плавления) | ||
| Опасности | |||
| GHS Маркировка : | |||
  
| |||
| Опасность | |||
| H301 , H311 , H315 , H317 , H318 , H332 , H341 | |||
| P261 , P301 , P302 , P305 , P310 , P312 , P330 , P331 , P338 , P351 , P352 | |||
| NFPA 704 (Огненная бриллиант) | |||
| точка возгорания | 127 ° C (261 ° F; 400 K) | ||
| 510 ° C (950 ° F; 783 K) | |||
| Взрывные пределы | 1.4%–? [ 4 ] | ||
| Смертельная доза или концентрация (LD, LC): | |||
Ld 50 ( средняя доза )
|
300 мг/кг (крыса, оральный) | ||
| Niosh (пределы воздействия на здоровье США): | |||
Пел (допустимый)
|
никто [ 4 ] | ||
Rel (рекомендуется)
|
TWA 5 ч/млн (20 мг/м 3 ) [кожа] [ 4 ] | ||
IDLH (немедленная опасность)
|
Н.д. [ 4 ] | ||
| Лист данных безопасности (SDS) | Сигма-Альдрич | ||
| Связанные соединения | |||
Связанные бензолцины
|
Резорцинол Гидрохинон | ||
Связанные соединения
|
1,2-бензохинон | ||
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |||
Катехол ( / ˈ K æ T ɪ Tʃ ɒ L / или / ˈ K æ T ɪ K ɒ L / ), также известный как пирокатехол или 1,2-дигидроксибензол , является органическим соединением с молекулярной формулой C 6 H 4 (OH) 2 . Это орто -изомер трех изомерных бензиндиолов . Это бесцветное соединение встречается естественным образом в следовых количествах. Впервые это было обнаружено разрушительной дистилляцией растительного экстракта катехина . Около 20 000 тонн катехоля в настоящее время синтетически производится ежегодно в качестве товарного органического химического вещества, в основном в качестве предшественника пестицидов, вкусов и ароматов. Небольшое количество катехоля встречается в фруктах и овощах . [ 2 ]
Изоляция и синтез
[ редактировать ]Катехол был сначала изолирован в 1839 году Эдгаром Хьюго Эмилом Рейншем (1809–1884), издав его из твердого таннического препарата катехина , который представляет собой остаток катечу , вареного или концентрированного сока мимозы катечу ( Acacia Catechu ). [ 5 ] После нагревания катехина над своей точкой разложения вещество, которое повторно поместил, впервые назвало Brenz-Katechusäure (сгоревшая кислота Catechu), сублимированное как белое удвоение . Это был продукт термического разложения флаванолов в катехине. В 1841 году и Вакенродер , и Цвенгер независимо заново открыли катехол; Сообщая об их выводах, философский журнал придумал название Pyrocatechin . [ 6 ] К 1852 году Эрдманн понял, что катехол был бензол с двумя добавленными атомами кислорода; В 1867 году август Кекуле понял, что катехол был диолом бензола, поэтому к 1868 году Катехол был перечислен как пирокатехол . [ 7 ] В 1879 году журнал химического общества рекомендовал катехолу назвать «катехол», а в следующем году он был указан как таковой. [ 8 ]
С тех пор было показано, что катехол встречается в свободной форме естественным образом в Кино и в Beechwood Tar. Его сульфоновая кислота была обнаружена в моче лошадей и людей. [ 9 ]
Катехол производится в промышленности путем с использованием гидроксилирования фенола перекиси водорода . [ 2 ]
- C 6 H 5 OH + H 2 O 2 → C 6 H 4 (OH) 2 + H 2 O
Он может быть получен путем реакции салицилальдегида с помощью основного и перекиси водорода ( окисление дакина ), [ 10 ] а также гидролиз 2-замещенных фенолов, особенно 2-хлорфенол , с горячими водными растворами, содержащими гидроксиды щелочных металлов. Его производное метилового эфира, гуакол , превращается в катехол посредством гидролиза CH 3 -O -связь, способствующая гидрооооооооооооооооооооооооооооооооооооо из гидроооооооооооооооооооооооооо для гидроооооооооооооооооооооооооо излма (HI). [ 10 ]
Реакция
[ редактировать ]Как и некоторые другие диффункциональные производные бензола, Catechol легко конденсируется , образуя гетероциклические соединения . Например, использование трихлорида фосфора или оксихлорида фосфора дает циклический фосфонит хлор или хлоро фосфонат соответственно; Хлорид сульфури дает сульфат ; и phosgene ( Cocl 2 ) дает карбонат : [ 11 ]
- C 6 H 4 (OH) 2 + XCL 2 → C 6 H 4 (O 2 x) + 2 HCl, где x = pcl или pocl; Итак 2 ; Сопутствующий
Основные решения катехол реагируют с железом (III), чтобы дать красный [Fe (C 6 H 4 O 2 ) 3 ] 3− Полем Хлорид железа дает зеленую окраску водным раствором, в то время как щелочный раствор быстро меняется на зеленый и, наконец, в черный цвет при воздействии воздуха. [ 12 ] содержащие железо, диоксигеназы, Ферменты расщепление катехоля катализируют .
Окислительно -восстановительная химия
[ редактировать ]Катехолы превращаются в полухиноновый радикал. При pH = 7 это преобразование происходит при 100 мВ: [ Цитация необходима ]
- C 6 H 4 (OH) 2 → C 6 H 4 (O) (OH) + ½ H 2
Семихиноновый радикал может быть сведен к катехолатному Дианиону, потенциал зависит от рН:
- C 6 H 4 (O) (OH) + E − → [C 6 H 4 O 2 ] 2− + H +
Катехол производится обратимым двухэлектронным снижением с двумя протоном 1,2-бензохинона ( E 0 = +795 MV против она ; E m (при рН 7) = +380 мВ против она). [ 13 ]
Катехолатный сериал, моноанионический полухинонат и бензохинон, коллективно называют диоксолентами . Диоксолентные могут функционировать как лиганды для ионов металлов. [ 14 ]
Катехольные производные
[ редактировать ]- Природные катехолы
-
Катехин , компонент чая.
-
Пикотанол , антиоксидант, найденный в некоторых красных винах.
-
Кверцетин , который встречается во многих продуктах.
Производные катехол находятся широко в природе. Они часто возникают путем гидроксилирования фенолов. [ 17 ] Шленистоногие кутикулы состоит из хитина , связанного с катехолом с белком . Кутикула может быть укреплена путем сшивки ( загара и склеротизации ), в частности, у насекомых и, конечно, с помощью биоминерализации . [ 18 ]
Синтетическое производное 4 -трет -бутилкатехол используется в качестве антиоксидантного и полимеризационного ингибитора .
Использование
[ редактировать ]Приблизительно 50% синтетического катехоля потребляется при производстве пестицидов , а остальные используются в качестве предшественника для тонких химических веществ, таких как духи и фармацевтические препараты. [ 2 ] Это общий строительный блок в органическом синтезе . [ 19 ] Несколько промышленно значимых ароматов и ароматов готовится, начиная с катехоля. Гуакол готовится метилированием катехоля, а затем превращается в ваниллин по шкале около 10 мкг в год (1990). Связанный моноэтиловый эфир катехоля, гутемол , преобразуется в этилваниллин , компонент шоколадной кондитерской. 3- Транс -сокарфилциклогексанол, широко используемый в качестве замены масла для сандалового дерева , готовится из катехола через гуакол и камфору . Пиперонал , цветочный аромат, готовится из метилена -дифира катехола с последующей конденсацией глиоксалом и декарбоксилированием . [ 20 ]
Катехол используется в качестве черно-белого разработчика фотографирования , но, за исключением некоторых применений специальных целей, его использование в значительной степени историческое. Ходят слухи, что он был кратко использован в разработчике Eastman Kodak HC-110 и, по слухам, является компонентом разработчика Tetenal Neofin Blau. [ 21 ] Это ключевой компонент Finol из фотохимии Moersch в Германии. Современное развитие катехолов было впервые зарегистрировано известным фотографом Сэнди Кинг . Его формулировка «Пирокат» популярна среди современных черно-белых фотографов. [ 22 ] Работа Кинг с тех пор вдохновила дальнейшее развитие 21-го века со стороны других, таких как Джей де Фер, с гиперкатом и застройщиками обсидианов и другими. [ 21 ]
Номенклатура
[ редактировать ]Несмотря на то, что редко встречается, официально «предпочтительным названием IUPAC » (PIN) катехоля является бензол-1,2-диол . [ 23 ] Тривиальное название Pyrocatechol является сохраняющимся названием IUPAC, согласно рекомендациям 1993 года по номенклатуре органической химии . [ 24 ] [ 25 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а беременный "Фронт". Номенклатура органической химии: рекомендации IUPAC и предпочтительные названия 2013 (Blue Book) . Кембридж: Королевское химическое общество . 2014. с. 691. DOI : 10.1039/9781849733069-FP001 . ISBN 978-0-85404-182-4 .
- ^ Jump up to: а беременный в дюймовый Fiege, Helmut; Vogenes, Heinz-leder; Hammomomoto, Toshikazu; Лето, сумо; Уйти, Тадао; Мики, Хавитор; Фудзита, успех; Buysch, Has-Josef; Гарбе, Дорокса; 2000 , ( Уилфрид Паулюс ) , 978-3-527-30385-4
- ^ Ландер, Джон Дж.; Свирбели, WJ (1945). «Дипольные моменты катехола, резорцинола и гидрохинона». Журнал Американского химического общества . 67 (2): 322–324. doi : 10.1021/ja01218a051 .
- ^ Jump up to: а беременный в дюймовый Niosh Pocket Guide к химическим опасностям. "#0109" . Национальный институт безопасности и гигиены труда (NIOSH).
- ^ Hugo Reinsch (1839) «Некоторые замечания о катечу» (некоторые наблюдения о катечу), репертуар для Pharmacie , 68 : 49-58. Reinsch Descrbe - это подготовка катехола на с. 56: «Как хорошо известно, кислота катехи уничтожается во время дистилляции, в то время как небольшая часть ее подсознания является кристаллинским подходом, но которая еще не была рассмотрена более подробно. Эта кислотность может быть той же, что и я разрушительная дистилляция катехии ; На р. 58, Reinsch называет новое соединение: «Свойства этой кислоты настолько определяются, что вас можно рассматривать как своеобразную кислотность и может быть продемонстрировано по имени бренц -катехийной кислоты». (Свойства этой кислоты настолько определенные, что можно оправданно рассматривать ее как странную кислоту и дать ей название «сгоревшая кислота».)
- ^ См.:
- H. Wackenroder (1841) «Свойства Catecho Acid» (свойства кислоты Catechu), Анналы химии и фармации , 37 : 306-320.
- Константин Цвенгер (1841) «О катехине» (на катехине), Анналы химии и фармацевта , 37 : 320-336.
- (Anon.) (1841) «На катехине (катехиновая кислота) и пирокатехин (пирокатехиновая кислота)» , Философский журнал , 19 : 194-195.
- ^ См.:
- Рудольф Вагнер (1852) «О красителях желтого древесины (Morus Tincoria.)» (По окрашению Mulberry's Mulberry (Morus Tinctoria.)), Журнал «Практическая химия» , 55 : 65-76. Озеро п. 65
- Август Кекуле (1867) «О сульфозшиных кислотах фенола» (на сульфонатах фенола) журнал для химии , Новая серия, 3 : 641–646; Озеро п. 643.
- Джозеф Альфред Наке, с Уильямом Кортисом, транс. и Томас Стивенсон, изд. Принципы химии, основанные на современных теориях , (Лондон, Англия: Генри Реншоу, 1868), с. 657. См. Также с. 720.
- ^ См.:
- В 1879 году в публикационном комитете Журнала Химического общества выпустил инструкции для его абстрактов «различать все спирты, т.е. гидроксиловые деривации углеводородов, именами заканчивающими , ..
- Уильям Аллен Миллер, изд., Элементы химии: теоретическая и практичная, часть III: химия углеродных соединений или органической химии, раздел I… , 5 -е изд. (Лондон, Англия: Longmans, Green and Co., 1880), с.524.
- ^ Zheng, LT; Ryu, GM; Квон, Б.М.; Ли, ч; Сук, К. (2008). «Противовоспалительные эффекты катехолов в липополисахарид-стимулированных клетках микроглии: ингибирование микроглиальной нейротоксичности». Европейский журнал фармакологии . 588 (1): 106–13. doi : 10.1016/j.ejphar.2008.04.035 . PMID 18499097 .
- ^ Jump up to: а беременный HD DAKIN, HT CLARKE, ER TAYLOR (1923). "Катехол". Органические синтезы . 3 : 28. doi : 10.15227/orgsyn.003.0028 .
{{cite journal}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ RS Hanslick, WF Bruce, A. Mascitti (1953). «О-фенилен карбонат». Орг Синтезатор 33 : 74. doi : 10.15227/orgsyn.033.0074 .
{{cite journal}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ Андерсон, Брайан Ф.; Бакингем, Дэвид А.; Робертсон, Глен Б.; Уэбб, Джон; Мюррей, Кит С.; Кларк, Пол Э. (1976). «Модели для бактериального хелатного энтерохелина с переносом железа» . Природа . 262 (5570): 722–724. Bibcode : 1976natur.262..722a . doi : 10.1038/262722a0 . PMID 134287 . S2CID 3045676 .
- ^ Швайгерт, Нина; Зендер, Александр Дж. Б .; Эгген, Рик Ил (2001). «Химические свойства катехолов и их молекулярные способы токсического действия в клетках, от микроорганизмов до млекопитающих. Миниревью». Экологическая микробиология . 3 (2): 81–91. doi : 10.1046/j.1462-2920.2001.00176.x . PMID 11321547 .
- ^ Гриффит, WP (1993). «Последние достижения в области химии диоксолена». Химия переходных металлов . 18 (2): 250–256. doi : 10.1007/bf00139966 . S2CID 93790780 .
- ^ ВВП : 2zi8 ; Yam KC, D'Angelo I, Kalscheuer R, Zhu H, Wang JX, Snieckus V, Ly LH, Converse PJ, Jacobs WR, Strynadka N, Eltis Ld (март 2009 г.). «Исследования расщепления кольца диоксигеназы освещают роль метаболизма холестерина в патогенезе микобактерии туберкулеза» . PLOS Pathog . 5 (3): E1000344. doi : 10.1371/journal.ppat.1000344 . PMC 2652662 . PMID 19300498 .
- ^ Saiz-Pouseu, J.; Mancebo-Aracil, J.; Надор, Ф.; Поиск, F.; Ruiz-Moline, D. (2019). " Издание 58 (3): 696–714. два 10.1002/anie.201801063: HDL 11336/94743: 29573319PMID 4228374S2CID
- ^ Болтон, Джуди Л.; Dunlap, Tareisha L.; Дитц, Биргит М. (2018). «Формирование и биологические цели ботанических о-кинонов» . Пищевая и химическая токсикология . 120 : 700–707. doi : 10.1016/j.fct.2018.07.050 . PMC 6643002 . PMID 30063944 . S2CID 51887182 .
- ^ Бриггс Дег (1999). «Молекулярная тафономия кутикул животных и растений: селективное сохранение и диагенез» . Философские транзакции Королевского общества B: биологические науки . 354 (1379): 7–17. doi : 10.1098/rstb.1999.0356 . PMC 1692454 .
- ^ Энциклопедия реагентов для органического синтеза , 2001, doi : 10.1002/047084289x , HDL : 10261/236866 , ISBN 978-0-471-93623-7
- ^ Фальбуш, Карл-Георг; Hammerschmidt, Franz-Josef; Пентен, Йоханнес; Пикенгаген, Вильгельм; Шатковский, Дитмар; Бауэр, Курт; Гарбе, Доротея; Сурбург, Хорст (2003), «Вкус и ароматы», Энциклопедия промышленной химии Ульмана , DOI : 10.1002/14356007.A11_141 , ISBN 978-3-527-30385-4
- ^ Jump up to: а беременный Стивен Г. Анхелл (2012-09-10). Поваренная книга темной комнаты . Тейлор и Фрэнсис. ISBN 978-1136092770 .
- ^ Стивен Г. Анхелл; Билл войска (1998). Фильм разрабатывает кулинарную книгу . ISBN 978-0240802770 .
- ^ Предпочтительные имена IUPAC . Сентябрь 2004 г., глава 6, секта 60–64, с. 38
- ^ IUPAC, Комиссия по номенклатуре органической химии. Руководство по номенклатуре IUPAC органических соединений (Рекомендации 1993) R-5.5.1.1 спиртов и фенолов.
- ^ Panico, R.; Powell, WH, eds. (1994). Руководство по номенклатуре IUPAC Organic Compounds 1993 . Оксфорд: Наука Блэквелла. ISBN 978-0-632-03488-8 .
Эта статья включает в себя текст из публикации, который сейчас в общественном доступе : Чисхолм, Хью , изд. (1911). " Катечу " Британская (11 -е изд.). Издательство Кембриджского университета.


![3,4-дигидрокси-9,10-секундроста-1,3,5 (10) -triene-9,17-дионера, метаболит холестерина [15]](http://upload.wikimedia.org/wikipedia/commons/thumb/d/d8/DHSA.svg/89px-DHSA.svg.png)




![Дофамин, полученный из аминокислотного тирозина, клей, используемый мидиями. [16]](http://upload.wikimedia.org/wikipedia/commons/thumb/2/2f/Dopamine.svg/180px-Dopamine.svg.png)
