Клеточная дифференциация


Клеточная дифференциация — это процесс, при котором стволовая клетка превращается из одного типа в дифференцированный. [2] [3] Обычно клетка меняется на более специализированный тип. Дифференцировка происходит несколько раз в ходе развития многоклеточного организма , поскольку он меняется от простой зиготы к сложной системе тканей и типов клеток. Дифференцировка продолжается и во взрослом возрасте, поскольку взрослые стволовые клетки делятся и создают полностью дифференцированные дочерние клетки во время восстановления тканей и нормального клеточного обмена. Некоторая дифференциация происходит в ответ на воздействие антигена . Дифференцировка резко меняет размер клетки, ее форму, мембранный потенциал , метаболическую активность и реакцию на сигналы. Эти изменения во многом обусловлены строго контролируемыми модификациями экспрессии генов и являются предметом изучения эпигенетики . За некоторыми исключениями, клеточная дифференциация почти никогда не предполагает изменения самой последовательности ДНК . Однако метаболический состав меняется весьма радикально. [4] где стволовые клетки характеризуются обильными метаболитами с сильно ненасыщенными структурами, уровень которых снижается при дифференцировке. Таким образом, разные клетки могут иметь совершенно разные физические характеристики, несмотря на одинаковый геном .
Специализированный тип дифференцировки, известный как терминальная дифференцировка , имеет важное значение в некоторых тканях, включая нервную систему позвоночных, поперечно-полосатые мышцы, эпидермис и кишечник. Во время терминальной дифференцировки клетка-предшественник, ранее способная к клеточному делению, навсегда покидает клеточный цикл, разрушает механизм клеточного цикла и часто экспрессирует ряд генов, характерных для конечной функции клетки (например, миозин и актин для мышечной клетки). Дифференцировка может продолжать происходить после терминальной дифференцировки, если емкость и функции клетки претерпевают дальнейшие изменения.
Среди делящихся клеток существует несколько уровней активности клеток , то есть способности клеток дифференцироваться в другие типы клеток. Более высокая эффективность указывает на большее количество типов клеток, которые можно получить. Клетка, способная дифференцироваться во все типы клеток, включая плацентарную ткань, известна как тотипотентная . У млекопитающих тотипотентными являются только зигота и последующие бластомеры , тогда как у растений многие дифференцированные клетки могут стать тотипотентными с помощью простых лабораторных методов. Клетка, способная дифференцироваться во все типы клеток взрослого организма, называется плюрипотентной . Такие клетки называются меристематическими клетками у высших растений и эмбриональными стволовыми клетками у животных, хотя некоторые группы сообщают о наличии взрослых плюрипотентных клеток. Вирусно-индуцированная экспрессия четырех факторов транскрипции Oct4 , Sox2 , c-Myc и Klf4 ( факторы Яманаки ) достаточна для создания плюрипотентных (iPS) клеток из взрослых фибробластов . [5] Мультипотентная клетка — это клетка, которая может дифференцироваться во множество разных, но тесно связанных типов клеток. [6] Олигопотентные клетки более ограничены, чем мультипотентные, но все же могут дифференцироваться в несколько близкородственных типов клеток. [6] Наконец, унипотентные клетки могут дифференцироваться только в один тип клеток, но способны к самообновлению . [6] В цитопатологии уровень клеточной дифференцировки используется как мера прогрессирования рака . « Степень » — это показатель того, насколько дифференцирована клетка опухоли. [7]
Типы клеток млекопитающих
[ редактировать ]Тело млекопитающих составляют три основные категории клеток: половые клетки , соматические клетки и стволовые клетки . Каждый из примерно 37,2 триллионов (3,72x10 13 ) клетки взрослого человека имеют собственную копию или копии генома , за исключением некоторых типов клеток, таких как эритроциты , у которых в полностью дифференцированном состоянии отсутствуют ядра. Большинство клеток диплоидны ; у них есть две копии каждой хромосомы . Такие клетки, называемые соматическими клетками, составляют большую часть человеческого тела, например клетки кожи и мышцы. Клетки дифференцируются, чтобы специализироваться на различных функциях. [8]
Клетки зародышевой линии — это любая линия клеток, дающая начало гаметам — яйцеклеткам и сперматозоидам — и, таким образом, продолжающаяся из поколения в поколение. С другой стороны, стволовые клетки обладают способностью делиться в течение неопределенного периода времени и давать начало специализированным клеткам. Их лучше всего описать в контексте нормального человеческого развития. [ нужна ссылка ]
Развитие начинается, когда сперматозоид оплодотворяет яйцеклетку и создает единственную клетку, способную сформировать целый организм. В первые часы после оплодотворения эта клетка делится на одинаковые клетки. У человека примерно через четыре дня после оплодотворения и после нескольких циклов деления клеток эти клетки начинают специализироваться, образуя полую сферу клеток, называемую бластоцистой . [9] Бластоциста имеет внешний слой клеток, а внутри этой полой сферы находится скопление клеток, называемое внутренней клеточной массой . Клетки внутренней клеточной массы формируют практически все ткани человеческого тела. Хотя клетки внутренней клеточной массы могут образовывать практически все типы клеток человеческого тела, они не могут образовывать организм. Эти клетки называются плюрипотентными . [10]
Плюрипотентные стволовые клетки подвергаются дальнейшей специализации в мультипотентные клетки-предшественники , которые затем дают начало функциональным клеткам. Примеры стволовых клеток и клеток-предшественников включают: [ нужна ссылка ]
- Радиальные глиальные клетки (эмбриональные нейральные стволовые клетки), которые дают начало возбуждающим нейронам в мозге плода в процессе нейрогенеза . [11] [12] [13]
- Гемопоэтические стволовые клетки (взрослые стволовые клетки) из костного мозга , которые дают начало эритроцитам , лейкоцитам и тромбоцитам .
- Мезенхимальные стволовые клетки (взрослые стволовые клетки) из костного мозга , которые дают начало стромальным клеткам, жировым клеткам и типам костных клеток.
- Эпителиальные стволовые клетки (клетки-предшественники), дающие начало различным типам клеток кожи.
- Мышечные сателлитные клетки (клетки-предшественники), которые способствуют дифференцировке мышечной ткани .
Путь, которым управляют молекулы клеточной адгезии, состоящие из четырех аминокислот: аргинина , глицина , аспарагина и серина , создается по мере того, как клеточный бластомер дифференцируется от однослойной бластулы к трем первичным слоям зародышевых клеток у млекопитающих, а именно эктодерма (перечислены от наиболее дистального ( наружного , мезодерма и энтодерма ) до проксимального (внутреннего)). Эктодерма образует кожу и нервную систему, мезодерма образует кости и мышечную ткань, а энтодерма образует ткани внутренних органов.
Дедифференцировка
[ редактировать ]
Дедифференцировка или интеграция — это клеточный процесс, наблюдаемый у более базальных форм жизни у животных, таких как черви и амфибии , где дифференцированная клетка возвращается на более раннюю стадию развития — обычно как часть регенеративного процесса. [14] [15] Дедифференцировка происходит и в растительных клетках. [16] А в клеточной культуре в лаборатории клетки могут менять форму или терять определенные свойства, такие как экспрессия белка — эти процессы также называются дедифференцировкой. [17]
Некоторые предполагают, что дедифференцировка — это отклонение, которое, вероятно, приводит к раку . [18] но другие объясняют это естественной частью иммунного ответа, которая была утеряна человеком на каком-то этапе эволюции.
Недавно открытая молекула, получившая название реверсин , аналог пурина , индуцирует дедифференцировку в мышечных трубках . Эти явно дедифференцированные клетки — теперь действующие по существу как стволовые клетки — могли затем повторно дифференцироваться в остеобласты и адипоциты . [19]

Механизмы
[ редактировать ]
Каждый специализированный тип клеток в организме экспрессирует подмножество , всех генов составляющих геном этого вида . Каждый тип клеток определяется своим особым паттерном регулируемой экспрессии генов . Таким образом, дифференцировка клеток представляет собой переход клетки от одного типа клеток к другому и включает в себя переключение с одного паттерна экспрессии генов на другой. Клеточная дифференциация во время развития может быть понята как результат работы генной регуляторной сети . Регуляторный ген и его цис-регуляторные модули являются узлами генной регуляторной сети; они получают входные данные и создают выходные данные в другом месте сети. [20] Подход системной биологии к биологии развития подчеркивает важность исследования того, как механизмы развития взаимодействуют, создавая предсказуемые закономерности ( морфогенез ). Однако недавно была предложена альтернативная точка зрения. [ когда? ] [ кем? ] . Клеточная дифференциация, основанная на стохастической экспрессии генов, является результатом дарвиновского избирательного процесса, происходящего среди клеток. В этом контексте белки и генные сети являются результатом клеточных процессов, а не их причиной. [ нужна ссылка ]
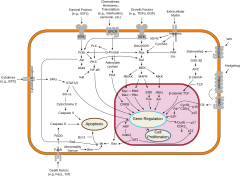
Хотя эволюционно лежащих в основе этих переключений, участвуют консервативные молекулярные процессы, у видов животных они сильно отличаются от хорошо изученных механизмов регуляции генов бактерий в клеточных механизмах , животных и даже от механизмов ближайших одноклеточных родственников . [21] В частности, дифференцировка клеток у животных сильно зависит от биомолекулярных конденсатов регуляторных белков и последовательностей ДНК- энхансеров .
Клеточная дифференциация часто контролируется клеточной передачей сигналов . Многие из сигнальных молекул, передающих информацию от клетки к клетке во время контроля клеточной дифференцировки, называются факторами роста . Хотя детали конкретных путей передачи сигнала различаются, эти пути часто разделяют следующие общие этапы. Лиганд, продуцируемый одной клеткой, связывается с рецептором во внеклеточной области другой клетки, вызывая конформационные изменения рецептора. Изменяется форма цитоплазматического домена рецептора, и рецептор приобретает ферментативную активность. Затем рецептор катализирует реакции фосфорилирования других белков, активируя их. Каскад реакций фосфорилирования в конечном итоге активирует спящий фактор транскрипции или цитоскелетный белок, тем самым способствуя процессу дифференцировки в клетке-мишени. [22] Клетки и ткани могут различаться по компетентности, своей способности реагировать на внешние сигналы. [23]
Индукция сигнала относится к каскадам сигнальных событий, во время которых клетка или ткань передает сигнал другой клетке или ткани, чтобы повлиять на ее судьбу в развитии. [23] Ямамото и Джеффри [24] исследовали роль хрусталика в формировании глаз у пещерных и поверхностных рыб, что является ярким примером индукции. [23] Путем реципрокных трансплантаций Ямамото и Джеффри [24] обнаружили, что пузырек хрусталика у поверхностных рыб может стимулировать развитие других частей глаза у рыб, обитающих в пещерах и на поверхности, тогда как пузырек хрусталика у пещерных рыб не может этого сделать. [23]
Другие важные механизмы подпадают под категорию асимметричных клеточных делений , делений, которые дают начало дочерним клеткам с различными судьбами развития. Асимметричные деления клеток могут происходить из-за асимметрично экспрессируемых материнских цитоплазматических детерминант или из-за передачи сигналов. [23] создаются отдельные дочерние клетки В первом механизме во время цитокинеза из-за неравномерного распределения регуляторных молекул в родительской клетке; Отдельная цитоплазма, которую наследует каждая дочерняя клетка, приводит к определенному паттерну дифференцировки каждой дочерней клетки. Хорошо изученным примером формирования рисунка посредством асимметричных делений является формирование рисунка оси тела у дрозофилы . Молекулы РНК являются важным типом сигнала контроля внутриклеточной дифференцировки. Молекулярная и генетическая основа асимметричного деления клеток также изучалась на зеленых водорослях рода Volvox — модельной системе для изучения того, как одноклеточные организмы могут эволюционировать в многоклеточные. [23] У Volvox carteri 16 клеток переднего полушария 32-клеточного эмбриона делятся асимметрично, каждая из которых производит одну большую и одну маленькую дочернюю клетку. Размер клетки в конце всех клеточных делений определяет, станет ли она специализированной зародышевой или соматической клеткой. [23] [25]
Эпигенетический контроль
[ редактировать ]Поскольку каждая клетка, независимо от типа клетки, обладает одним и тем же геномом , определение типа клетки должно происходить на уровне экспрессии генов . Хотя регуляция экспрессии генов может происходить посредством цис- и трансрегуляторных элементов гена , включая промотор и энхансеры , возникает проблема, как этот паттерн экспрессии поддерживается на протяжении многих поколений клеточного деления . [26] Как оказалось, эпигенетические процессы играют решающую роль в регуляции решения о выборе судьбы стволовых, предшественников или зрелых клеток . В этом разделе основное внимание будет уделено млекопитающих стволовым клеткам .
В системной биологии и математическом моделировании сетей генной регуляции прогнозируется, что детерминация клеточной судьбы будет проявлять определенную динамику, такую как конвергенция аттрактора (аттрактор может быть точкой равновесия, предельным циклом или странным аттрактором ) или колебательную. [27]
Важность эпигенетического контроля
[ редактировать ]Первый вопрос, который можно задать, — это масштабы и сложность роли эпигенетических процессов в определении судьбы клеток. Четкий ответ на этот вопрос можно увидеть в статье Листера Р. и др. , опубликованной в 2011 году. [28] об аберрантном эпигеномном программировании в индуцированных человеком плюрипотентных стволовых клетках . Поскольку считается, что индуцированные плюрипотентные стволовые клетки (ИПСК) имитируют эмбриональные стволовые клетки по своим плюрипотентным свойствам, между ними должно существовать мало эпигенетических различий. Чтобы проверить это предсказание, авторы провели полногеномное профилирование паттернов метилирования ДНК в нескольких линиях эмбриональных стволовых клеток человека (ЭСК), ИПСК и клеток-предшественников.
Женские жировые клетки, легких фибробласты и фибробласты крайней плоти были перепрограммированы в индуцированное плюрипотентное состояние с помощью генов OCT4 , SOX2 , KLF4 и MYC . Сравнивали закономерности метилирования ДНК в ЭСК, ИПСК, соматических клетках. Листер Р. и др. наблюдали значительное сходство уровней метилирования между эмбриональными и индуцированными плюрипотентными клетками. Около 80% динуклеотидов CG в ЭСК и ИПСК были метилированы, то же самое было верно только для 60% динуклеотидов CG в соматических клетках. Кроме того, соматические клетки обладали минимальным уровнем метилирования цитозина в динуклеотидах, отличных от CG, тогда как индуцированные плюрипотентные клетки обладали такими же уровнями метилирования, как и эмбриональные стволовые клетки, от 0,5 до 1,5%. Таким образом, в соответствии с их транскрипционной активностью, [28] Паттерны метилирования ДНК, по крайней мере, на геномном уровне, схожи между ЭСК и ИПСК.
Однако при более внимательном изучении закономерностей метилирования авторы обнаружили 1175 областей дифференциального метилирования динуклеотидов CG по крайней мере между одной клеточной линией ES или iPS. Сравнивая эти области дифференциального метилирования с областями метилирования цитозина в исходных соматических клетках, 44-49% дифференциально метилированных областей отражали паттерны метилирования соответствующих соматических клеток-предшественников, в то время как 51-56% этих областей были непохожи на обе клетки-предшественницы. и эмбриональные клеточные линии. Индуцированная in vitro дифференцировка линий ИПСК привела к передаче 88% и 46% гипер- и гипометилированных дифференциально-метилированных областей соответственно.
Из этого исследования легко сделать два вывода. Во-первых, эпигенетические процессы активно участвуют в определении судьбы клеток , о чем свидетельствуют сходные уровни метилирования цитозина между индуцированными плюрипотентными и эмбриональными стволовыми клетками, что соответствует их соответствующим паттернам транскрипции . Во-вторых, механизмы перепрограммирования (и, в более широком смысле, дифференцировки) очень сложны и не могут быть легко дублированы, о чем свидетельствует значительное количество дифференциально метилированных областей между линиями ES и iPS клеток. Теперь, когда эти два момента установлены, мы можем изучить некоторые эпигенетические механизмы, которые, как считается, регулируют клеточную дифференцировку.
Механизмы эпигенетической регуляции
[ редактировать ]Факторы пионера (4 октября, Sox2, Nanog)
[ редактировать ]Три фактора транскрипции, OCT4, SOX2 и NANOG – первые два из которых используются в индуцированном репрограммировании плюрипотентных стволовых клеток (iPSC), наряду с Klf4 и c-Myc – высоко экспрессируются в недифференцированных эмбриональных стволовых клетках и необходимы для поддержания их плюрипотентности . [29] Считается, что они достигают этого за счет изменений в структуре хроматина , таких как модификация гистонов и метилирование ДНК, чтобы ограничить или разрешить транскрипцию генов-мишеней. Несмотря на высокую выраженность, их уровни требуют точного баланса для поддержания плюрипотентности, нарушение которого будет способствовать дифференциации в разные линии в зависимости от того, как изменяются уровни экспрессии генов. дифференциальная регуляция уровней Oct-4 и SOX2 предшествует выбору судьбы зародышевого листка. Было показано, что [30] Повышенные уровни Oct4 и сниженные уровни Sox2 способствуют мезендодермальной судьбе, при этом Oct4 активно подавляет гены, связанные с нейральной эктодермальной судьбой. Сходным образом, повышенные уровни Sox2 и сниженные уровни Oct4 способствуют дифференцировке в сторону нейральной эктодермальной судьбы, при этом Sox2 ингибирует дифференцировку в сторону мезендодермальной судьбы. Независимо от линии дифференцировки клеток, подавление NANOG было идентифицировано как необходимая предпосылка для дифференцировки. [30]
Поликомбовый репрессивный комплекс (PRC2)
[ редактировать ]В сфере молчания генов репрессивный комплекс Polycomb 2 , один из двух классов белков семейства Polycomb (PcG), катализирует ди- и три-метилирование гистона H3 лизина 27 (H3K27me2/me3). [29] [31] [32] Связываясь с нуклеосомой, меченной H3K27me2/3, PRC1 (также комплекс белков семейства PcG) катализирует моноубиквитинилирование гистона H2A по лизину 119 (H2AK119Ub1), блокируя активность РНК-полимеразы II и приводя к подавлению транскрипции. [29] ES-клетки с нокаутом PcG не дифференцируются эффективно в три зародышевых листка, а делеция генов PRC1 и PRC2 приводит к усилению экспрессии генов, связанных с клоном, и незапланированной дифференцировке. [29] По-видимому, комплексы PcG ответственны за транскрипционную репрессию генов, способствующих дифференцировке и развитию.
Белки группы триторакса (TrxG)
[ редактировать ]С другой стороны, после получения сигналов дифференцировки белки PcG рекрутируются на промоторы транскрипционных факторов плюрипотентности. ES-клетки с дефицитом PcG могут начать дифференцировку, но не могут поддерживать дифференцированный фенотип. [29] Одновременно гены, способствующие дифференцировке и развитию, активируются регуляторами хроматина группы Trithorax (TrxG) и теряют свою репрессию. [29] [32] Белки TrxG рекрутируются в областях с высокой транскрипционной активностью, где они катализируют триметилирование лизина 4 гистона H3 ( H3K4me3 ) и способствуют активации генов посредством ацетилирования гистонов. [32] Комплексы PcG и TrxG участвуют в прямой конкуренции и считаются функционально антагонистическими, создавая при дифференцировке и развитии локусы, так называемые «бивалентные домены», и делая эти гены чувствительными к быстрой индукции или репрессии. [33]
Метилирование ДНК
[ редактировать ]Регуляция экспрессии генов дополнительно достигается за счет метилирования ДНК, при котором опосредованное ДНК-метилтрансферазой метилирование остатков цитозина в динуклеотидах CpG поддерживает наследственную репрессию за счет контроля доступности ДНК. [33] Большинство сайтов CpG в эмбриональных стволовых клетках неметилированы и, по-видимому, связаны с нуклеосомами, несущими H3K4me3. [29] При дифференцировке небольшое количество генов, включая OCT4 и NANOG, [33] метилируются, а их промоторы подавляются, чтобы предотвратить их дальнейшую экспрессию. Таким образом, эмбриональные стволовые клетки с дефицитом метилирования ДНК быстро вступают в апоптоз при дифференцировке in vitro. [29]
Позиционирование нуклеосом
[ редактировать ]Хотя последовательность ДНК большинства клеток организма одинакова, паттерны связывания факторов транскрипции и соответствующие паттерны экспрессии генов различны. В значительной степени различия в связывании транскрипционных факторов определяются доступностью хроматина к их сайтам связывания посредством модификации гистонов и/или пионерских факторов . В частности, важно знать, ли нуклеосома покрывает данный сайт связывания генома или нет. Это можно определить с помощью анализа иммунопреципитации хроматина (ChIP). [34]
Ацетилирование и метилирование гистонов
[ редактировать ]Взаимодействия ДНК-нуклеосомы характеризуются двумя состояниями: либо прочно связанными нуклеосомами и транскрипционно неактивными, называемыми гетерохроматином , либо слабосвязанными и обычно, но не всегда, транскрипционно активными, называемыми эухроматином . Эти изменения в первую очередь объясняются эпигенетическими процессами метилирования и ацетилирования гистонов, а также обратными им деметилированием и деацетилированием. Эффекты ацетилирования и деацетилирования более предсказуемы. Ацетильная группа либо добавляется, либо удаляется из положительно заряженных остатков лизина в гистонах с помощью ферментов, называемых гистон-ацетилтрансферазами или гистондеактилазами соответственно. Ацетильная группа предотвращает связь лизина с отрицательно заряженным остовом ДНК. Метилирование не так просто, поскольку ни метилирование, ни деметилирование последовательно не коррелируют ни с активацией, ни с репрессией генов. Однако неоднократно было показано, что определенные метилирования либо активируют, либо подавляют гены. Триметилирование лизина 4 на гистоне 3 (H3K4Me3) связано с активацией генов, тогда как триметилирование лизина 27 на гистоне 3 подавляет гены. [35] [36] [37]
В стволовых клетках
[ редактировать ]Во время дифференцировки стволовые клетки меняют профили экспрессии генов. Недавние исследования выявили роль позиционирования нуклеосом и модификаций гистонов во время этого процесса. [38] Этот процесс состоит из двух компонентов: выключение экспрессии генов эмбриональных стволовых клеток (ЭСК) и активация генов клеточной судьбы. Считается , что лизинспецифическая деметилаза 1 ( KDM1A ) предотвращает использование энхансерных областей генов плюрипотентности, тем самым ингибируя их транскрипцию. [39] Он взаимодействует с комплексом Mi-2/NuRD (ремоделирование нуклеосом и деацетилаза гистонов), [39] давая пример, когда метилирование и ацетилирование не являются дискретными и взаимоисключающими, а взаимосвязанными процессами.
Роль передачи сигналов в эпигенетическом контроле
[ редактировать ]Последний вопрос, который следует задать, касается роли передачи сигналов клетками во влиянии на эпигенетические процессы, управляющие дифференцировкой. Такая роль должна существовать, поскольку было бы разумно думать, что внешняя передача сигналов может привести к эпигенетическому ремоделированию, так же, как она может привести к изменениям в экспрессии генов посредством активации или репрессии различных факторов транскрипции. Доступно мало прямых данных о конкретных сигналах, которые влияют на эпигеном , и большая часть текущих знаний по этому вопросу состоит из предположений о возможных кандидатах в регуляторы эпигенетического ремоделирования. [40] Сначала мы обсудим нескольких основных кандидатов, которые, как считается, участвуют в индукции и поддержании как эмбриональных стволовых клеток, так и их дифференцированного потомства, а затем обратимся к одному примеру специфических сигнальных путей, в которых существуют более прямые доказательства их роли в эпигенетических изменениях.
Первым основным кандидатом является сигнальный путь Wnt . Путь Wnt участвует во всех стадиях дифференцировки, а лиганд Wnt3a может заменять сверхэкспрессию c-Myc при генерации индуцированных плюрипотентных стволовых клеток. [40] С другой стороны, нарушение β-catenin , компонента сигнального пути Wnt, приводит к снижению пролиферации нейральных предшественников.
Факторы роста составляют второй основной набор кандидатов в эпигенетические регуляторы клеточной дифференцировки. Эти морфогены имеют решающее значение для развития и включают костные морфогенетические белки , трансформирующие факторы роста (TGF) и факторы роста фибробластов (FGF). Было показано, что TGF и FGF поддерживают экспрессию OCT4, SOX2 и NANOG путем передачи сигналов нижестоящим белкам Smad . [40] Истощение факторов роста способствует дифференцировке ЭСК, а гены с двухвалентным хроматином могут стать либо более рестриктивными, либо пермиссивными в своей транскрипции. [40]
Некоторые другие сигнальные пути также считаются основными кандидатами. Цитокиновые факторы, ингибирующие лейкоз, связаны с поддержанием ЭСК мыши в недифференцированном состоянии. Это достигается за счет активации пути Jak-STAT3, который, как было показано, необходим и достаточен для поддержания плюрипотентности ЭСК мыши. [41] Ретиноевая кислота может индуцировать дифференцировку ЭСК человека и мыши. [40] а передача сигналов Notch участвует в пролиферации и самообновлении стволовых клеток. Наконец, Sonic hedgehog , помимо своей роли морфогена, способствует дифференцировке эмбриональных стволовых клеток и самообновлению соматических стволовых клеток. [40]
Проблема, конечно, в том, что кандидатура этих сигнальных путей была выведена прежде всего на основании их роли в развитии и клеточной дифференцировке. Хотя эпигенетическая регуляция необходима для управления клеточной дифференцировкой, ее явно недостаточно для этого процесса. Прямая модуляция экспрессии генов посредством модификации факторов транскрипции играет ключевую роль, которую следует отличать от наследственных эпигенетических изменений, которые могут сохраняться даже в отсутствие исходных сигналов окружающей среды. В настоящее время существует лишь несколько примеров сигнальных путей, приводящих к эпигенетическим изменениям, изменяющим судьбу клеток, и мы сосредоточимся на одном из них.
Экспрессия Shh (Sonic hedgehog) усиливает выработку BMI1 , компонента комплекса PcG, который распознает H3K27me3 . Это происходит Gli-зависимым образом, поскольку Gli1 и Gli2 являются нижестоящими эффекторами сигнального пути Hedgehog . В культуре Bmi1 опосредует способность пути Hedgehog способствовать самообновлению стволовых клеток молочной железы человека. [42] Как на людях, так и на мышах исследователи показали, что Bmi1 высоко экспрессируется в пролиферирующих предшественниках незрелых гранулярных клеток мозжечка. Когда Bmi1 был нокаутирован у мышей, это привело к нарушению развития мозжечка, что привело к значительному уменьшению постнатальной массы мозга, а также к нарушениям двигательного контроля и поведения. [43] Отдельное исследование показало значительное снижение пролиферации нервных стволовых клеток наряду с увеличением пролиферации астроцитов у мышей с нулевым Bmi. [44]
Альтернативная модель клеточной дифференцировки во время эмбриогенеза заключается в том, что позиционная информация основана на механической передаче сигналов цитоскелетом с использованием волн эмбриональной дифференцировки . Механический сигнал затем эпигенетически трансдуцируется через системы сигнальной трансдукции (частью которых являются специфические молекулы, такие как Wnt), что приводит к дифференциальной экспрессии генов.
Таким образом, роль передачи сигналов в эпигенетическом контроле судеб клеток у млекопитающих в значительной степени неизвестна, но существуют отдельные примеры, которые указывают на вероятное существование дальнейших подобных механизмов.
Влияние эластичности матрицы
[ редактировать ]Известно, что для достижения цели регенерации различных тканей взрослые стебли мигрируют из своих ниш, прикрепляются к новому внеклеточному матриксу (ECM) и дифференцируются. Пластичность этого микроокружения уникальна для разных типов тканей. Внеклеточный матрикс, окружающий мозг, мышцы и костные ткани, варьируется от мягкого до жесткого. Трансдукция стволовых клеток в эти типы клеток не направляется исключительно хемокиновыми сигналами и передачей сигналов от клетки к клетке. Эластичность микроокружения также может влиять на дифференцировку мезенхимальных стволовых клеток (МСК, происходящих из костного мозга). Когда МСК помещают на субстраты той же жесткости, что и мозговые, мышечные и костные ЕСМ, МСК приобретают свойства соответствующих клеток. типы. [45] Восприятие матрицы требует, чтобы клетка прижималась к матрице в местах фокальных спаек, что заставляет клеточный механопреобразователь генерировать сигнал, информирующий о том, какая сила необходима для деформации матрицы. Чтобы определить ключевых игроков в спецификации клонов, основанной на эластичности матрицы, в MSCs, были имитированы различные матричные микроокружения. В результате этих экспериментов был сделан вывод, что фокальные спайки МСК являются клеточным механопреобразователем, воспринимающим различия в эластичности матрикса. Немышечные изоформы миозина IIa-c генерируют силы в клетке, которые приводят к передаче сигналов ранних маркеров коммитации. Немышечный миозин IIa генерирует наименьшую силу, увеличивающуюся по сравнению с немышечным миозином IIc. В клетке также есть факторы, которые ингибируют немышечный миозин II, такие как блеббистатин . Это делает клетку фактически слепой к окружающему матриксу. [45] Исследователи добились определенного успеха в индукции свойств стволовых клеток в клетках HEK 239, создав мягкий матрикс без использования диффузионных факторов. [46] Свойства стволовых клеток, по-видимому, связаны с напряжением в актиновой сети клеток. Одним из выявленных механизмов дифференцировки, индуцированной матриксом, являются белки, индуцированные напряжением, которые реконструируют хроматин в ответ на механическое растяжение. [47] Путь RhoA также участвует в этом процессе. [ нужна ссылка ]
Эволюционная история
[ редактировать ]возрастом в миллиард лет , вероятно, голозойный , протист , Бицеллум бразиери , с двумя типами клеток показывает, что эволюция дифференцированной многоклеточности , возможно, но не обязательно животных линий, произошла по крайней мере 1 миллиард лет назад в пресноводных озерах. и, возможно, главным образом в пресноводных озерах, а не чем океан. [48] [49] [50] [ нужны разъяснения ]
См. также
[ редактировать ]- Межбислойные силы при слиянии мембран
- Механизм слияния
- Слияние липидных бислоев
- Межклеточные фузогены
- КАФ-1
- Список типов клеток человека, полученных из зародышевых листков
Ссылки
[ редактировать ]- ^ Кривень И.; Рёблиц, С.; Шютте, Ч. (2015). «Решение главного химического уравнения методом радиальной аппроксимации базисных функций с отслеживанием границы раздела» . Системная биология BMC . 9 (1): 67. дои : 10.1186/s12918-015-0210-y . ПМЦ 4599742 . ПМИД 26449665 .

- ^ Slack, JMW (2013) Основная биология развития. Уайли-Блэквелл, Оксфорд.
- ^ Слэк, JMW (2007). «Метаплазия и трансдифференцировка: от чистой биологии к клинике». Nature Reviews Молекулярно-клеточная биология . 8 (5): 369–378. дои : 10.1038/nrm2146 . ПМИД 17377526 . S2CID 3353748 .
- ^ Янес, Оскар; Кларк, Джули; Вонг, Диана М.; Патти, Гэри Дж.; Санчес-Руис, Антонио; Бентон, Х. Пол; Траугер, Суния А.; Деспон, Кэролайн; Дин, Шэн; Сюздак, Гэри (июнь 2010 г.). «Метаболическое окисление регулирует дифференцировку эмбриональных стволовых клеток» . Химическая биология природы . 6 (6): 411–417. дои : 10.1038/nchembio.364 . ISSN 1552-4469 . ПМЦ 2873061 . ПМИД 20436487 .
- ^ Такахаши, К; Яманака, С. (2006). «Индукция плюрипотентных стволовых клеток из культур эмбриональных и взрослых фибробластов мышей с помощью определенных факторов». Клетка . 126 (4): 663–76. дои : 10.1016/j.cell.2006.07.024 . hdl : 2433/159777 . ПМИД 16904174 . S2CID 1565219 .
- ^ Перейти обратно: а б с Шёлер, Ханс Р. (2007). «Потенциал стволовых клеток: инвентарь». У Николауса Кнопффлера; Дагмар Щипански; Стефан Лоренц Зоргнер (ред.). Биотехнология человека как социальный вызов . Издательство Эшгейт. п. 28. ISBN 978-0-7546-5755-2 .
- ^ «Словарь терминов, посвященных раку, NCI» . Национальный институт рака . Проверено 1 ноября 2013 г.
- ^ Лодиш, Харви (2000). Молекулярно-клеточная биология (4-е изд.). Нью-Йорк: WH Freeman. Раздел 14.2. ISBN 978-0-7167-3136-8 .
- ^ Кумар, Рани (2008). Учебник эмбриологии человека . ИК Международный издательский дом. п. 22. ISBN 9788190675710 .
- ^ Д. Биндер, Марк; Хирокава, Нобутака; Виндхорст, Уве (2009). Энциклопедия неврологии . Спрингер. ISBN 978-3540237358 .
- ^ Ракич, П. (октябрь 2009 г.). «Эволюция неокортекса: взгляд из биологии развития» . Обзоры природы. Нейронаука . 10 (10): 724–35. дои : 10.1038/nrn2719 . ПМЦ 2913577 . ПМИД 19763105 .
- ^ Луи, Дж. Х.; Хансен, Д.В.; Кригштейн, Арканзас (8 июля 2011 г.). «Развитие и эволюция неокортекса человека» . Клетка . 146 (1): 18–36. дои : 10.1016/j.cell.2011.06.030 . ПМК 3610574 . ПМИД 21729779 .
- ^ Раш, Б.Г.; Акман, Дж.Б.; Ракич, П. (февраль 2016 г.). «Двунаправленная радиальная активность Ca(2+) регулирует нейрогенез и миграцию во время раннего формирования кортикального столба» . Достижения науки . 2 (2): e1501733. Бибкод : 2016SciA....2E1733R . дои : 10.1126/sciadv.1501733 . ПМЦ 4771444 . ПМИД 26933693 .
- ^ Стокум Д.Л. (2004). «Регенерация амфибий и стволовые клетки». Регенерация: стволовые клетки и не только . Актуальные темы микробиологии и иммунологии. Том. 280. стр. 1–70. дои : 10.1007/978-3-642-18846-6_1 . ISBN 978-3-540-02238-1 . ПМИД 14594207 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Казимир К.М., Гейтс П.Б., Пациент Р.К., Брокс Дж.П. (1 декабря 1988 г.). «Доказательства дедифференцировки и метаплазии при регенерации конечностей амфибий в результате наследования метилирования ДНК» . Разработка . 104 (4): 657–668. дои : 10.1242/dev.104.4.657 . ПМИД 3268408 .
- ^ Джайлз К.Л. (1971). «Дедифференциация и регенерация мохообразных: выборочный обзор» . Новозеландский журнал ботаники . 9 (4): 689–94. Бибкод : 1971NZJB....9..689G . дои : 10.1080/0028825x.1971.10430231 . Архивировано из оригинала 4 декабря 2008 г. Проверено 1 января 2008 г.
- ^ Шнабель М., Марловиц С., Экхофф Г. и др. (январь 2002 г.). «Связанные с дедифференцировкой изменения в морфологии и экспрессии генов в первичных суставных хондроцитах человека в клеточной культуре» . Остеоартр. Картиль . 10 (1): 62–70. дои : 10.1053/joca.2001.0482 . ПМИД 11795984 .
- ^ Продам S (декабрь 1993 г.). «Клеточное происхождение рака: дедифференцировка или остановка созревания стволовых клеток?» . Окружающая среда. Перспектива здоровья . 101 (Приложение 5): 15–26. дои : 10.2307/3431838 . JSTOR 3431838 . ПМЦ 1519468 . ПМИД 7516873 .
- ^ Цонис П.А. (апрель 2004 г.). «Стволовые клетки из дифференцированных клеток» . Мол. Интерв . 4 (2): 81–3. дои : 10.1124/ми.4.2.4 . ПМИД 15087480 . Архивировано из оригинала 23 мая 2016 г. Проверено 26 декабря 2010 г.
- ^ Бен-Табу де-Леон С., Дэвидсон Э.Х. (2007). «Генная регуляция: сеть генного контроля в разработке» (PDF) . Annu Rev Biophys Biomol Struct . 36 (191): 191–212. doi : 10.1146/annurev.biophys.35.040405.102002 . ПМИД 17291181 .
- ^ Ньюман, Стюарт А. (2020). «Дифференциация клеток: чему мы научились за 50 лет?» . Журнал теоретической биологии . 485 : 110031. arXiv : 1907.09551 . Бибкод : 2020JThBi.48510031N . дои : 10.1016/j.jtbi.2019.110031 . PMID 31568790 .
- ^ Книсели, Карен; Гилберт, Скотт Ф. (2009). Биология развития (8-е изд.). Сандерленд, Массачусетс: Sinauer Associates. п. 147. ИСБН 978-0-87893-371-6 .
- ^ Перейти обратно: а б с д и ж г Рудель и Зоммер; Эволюция механизмов развития. Биология развития 264, 15–37, 2003 г. Рудель, Д.; Соммер, Р.Дж. (2003). «Эволюция механизмов развития» . Биология развития . 264 (1): 15–37. дои : 10.1016/S0012-1606(03)00353-1 . ПМИД 14623229 .
- ^ Перейти обратно: а б Ямамото Ю. и У.Р. Джеффри; Центральная роль хрусталика в дегенерации глаз пещерных рыб. Наука 289 (5479), 631-633, 2000 г. Ямамото, Ю.; Джеффри, WR (2000). «Центральная роль хрусталика в дегенерации глаз пещерных рыб». Наука . 289 (5479): 631–633. Бибкод : 2000Sci...289..631Y . дои : 10.1126/science.289.5479.631 . ПМИД 10915628 .
- ^ Кирк М.М., Рансик, С.Е. Макрей, Д.Л. Кирк; Взаимосвязь между размером клеток и судьбой клеток Volvox carteri . Журнал клеточной биологии 123, 191–208, 1993 г. Кирк, ММ; Рансик, А.; Макрей, SE; Кирк, Д.Л. (1993). «Взаимосвязь между размером клеток и судьбой клеток у Volvox carteri» . Журнал клеточной биологии . 123 (1): 191–208. дои : 10.1083/jcb.123.1.191 . ПМК 2119814 . ПМИД 8408198 .
- ^ Мадригал П., Денг С., Фэн Ю., Милити С., Го К.Дж., Нибхани Р., Гранди Р., Оснато А., Ортманн Д., Браун С., Пауклин С. (25 января 2023 г.). «Эпигенетические и транскрипционные регуляции определяют судьбу клеток перед делением во время дифференцировки плюрипотентных стволовых клеток человека» (PDF) . Природные коммуникации . 14 (405): 405. Бибкод : 2023NatCo..14..405M . дои : 10.1038/s41467-023-36116-9 . ПМЦ 9876972 . ПМИД 36697417 .
- ^ Рабаханте Дж. Ф., Бабьерра А. Л. (30 января 2015 г.). «Ветвление и колебания в эпигенетическом ландшафте детерминации клеточной судьбы» (PDF) . Прогресс биофизики и молекулярной биологии . 117 (2–3): 240–9. doi : 10.1016/j.pbiomolbio.2015.01.006 . ПМИД 25641423 . S2CID 2579314 .
- ^ Перейти обратно: а б Листер Р; и др. (2011). «Горячие точки аберрантного эпигеномного перепрограммирования в индуцированных человеком плюрипотентных стволовых клетках» . Природа . 471 (7336): 68–73. Бибкод : 2011Natur.471...68L . дои : 10.1038/nature09798 . ПМК 3100360 . ПМИД 21289626 .
- ^ Перейти обратно: а б с д и ж г час Кристоферсен Н.С., Хелин К. (2010). «Эпигенетический контроль судьбы эмбриональных стволовых клеток» . Джей Эксп Мед . 207 (11): 2287–95. дои : 10.1084/jem.20101438 . ПМЦ 2964577 . ПМИД 20975044 .
- ^ Перейти обратно: а б Томсон, М; Лю, С.Дж.; Цзоу, Л.Н.; Смит, З.; Мейснер, А; Раманатан, С. (2011). «Факторы плюрипотентности эмбриональных стволовых клеток регулируют дифференцировку в зародышевые листки» . Клетка . 145 (6): 875–89. дои : 10.1016/j.cell.2011.05.017 . ПМК 5603300 . ПМИД 21663792 .
- ^ Чжу, Дж.; и др. (2013). «Переходы состояний хроматина по всему геному, связанные с сигналами развития и окружающей среды» . Клетка . 152 (3): 642–654. дои : 10.1016/j.cell.2012.12.033 . ПМЦ 3563935 . ПМИД 23333102 .
- ^ Перейти обратно: а б с Гюнтер М.Г., Янг Р.А. (2010). «Репрессивная транскрипция» (PDF) . Наука . 329 (5988): 150–1. Бибкод : 2010Sci...329..150G . дои : 10.1126/science.1193995 . ПМК 3006433 . ПМИД 20616255 .
- ^ Перейти обратно: а б с Мейснер А (2010). «Эпигенетические модификации в плюрипотентных и дифференцированных клетках». Нат Биотехнология . 28 (10): 1079–88. дои : 10.1038/nbt.1684 . ПМИД 20944600 . S2CID 205274850 .
- ^ «Иммупреципитация хроматина» . www.bio.brandeis.edu . Архивировано из оригинала 25 ноября 2017 г. Проверено 26 декабря 2016 г.
- ^ Кроган Н.Дж., Довер Дж., Вуд А., Шнайдер Дж., Хайдт Дж., Боатенг М.А., Дин К., Райан О.В., Гольшани А., Джонстон М., Гринблатт Дж.Ф., Шилатифард А. (март 2003 г.). «Комплекс Paf1 необходим для метилирования гистона H3 с помощью COMPASS и Dot1p: связь элонгации транскрипции с метилированием гистонов» . Молекулярная клетка . 11 (3): 721–9. дои : 10.1016/S1097-2765(03)00091-1 . ПМИД 12667454 .
- ^ Нг ХХ, Роберт Ф., Янг Р.А., Струл К. (март 2003 г.). «Направленное привлечение метилазы гистонов Set1 путем удлинения Pol II обеспечивает локализованную метку и память о недавней транскрипционной активности» . Молекулярная клетка . 11 (3): 709–19. дои : 10.1016/S1097-2765(03)00092-3 . ПМИД 12667453 .
- ^ Бернштейн Б.Е., Камаль М., Линдблад-Тох К., Бекиранов С., Бэйли Д.К., Хьюберт Д.Д., МакМахон С., Карлссон Е.К., Кулбокас Э.Дж., Гингерас Т.Р., Шрайбер С.Л., Ландер Э.С. (январь 2005 г.). «Геномные карты и сравнительный анализ модификаций гистонов у человека и мыши» . Клетка . 120 (2): 169–81. дои : 10.1016/j.cell.2005.01.001 . ПМИД 15680324 . S2CID 7193829 .
- ^ Тейф В.Б., Вайнштейн Й., Кодрон-Хергер М., Мальм Дж.П., Март С., Хефер Т., Риппе К. (2012). «Полногеномное расположение нуклеосом во время развития эмбриональных стволовых клеток». Nat Struct Мол Биол . 19 (11): 1185–92. дои : 10.1038/nsmb.2419 . ПМИД 23085715 . S2CID 34509771 .
- ^ Перейти обратно: а б Уайт, Вашингтон; Билодо, С; Орландо, округ Колумбия; Хок, штат Ха; Фрэмптон, генеральный директор; Фостер, Коннектикут; Коули, С.М.; Янг, РА (2012). «Вывод из эксплуатации энхансера с помощью LSD1 во время дифференцировки эмбриональных стволовых клеток» . Природа . 482 (7384): 221–5. Бибкод : 2012Natur.482..221W . дои : 10.1038/nature10805 . ПМК 4144424 . ПМИД 22297846 .
- ^ Перейти обратно: а б с д и ж Мохаммад Х.П., Байлин С.Б. (2010). «Связь клеточной передачи сигналов и эпигенетического механизма». Нат Биотехнология . 28 (10): 1033–8. дои : 10.1038/nbt1010-1033 . ПМИД 20944593 . S2CID 6911946 .
- ^ Нива Х., Бердон Т., Чемберс И., Смит А. (1998). «Самообновление плюрипотентных эмбриональных стволовых клеток опосредовано активацией STAT3» . Генс Дев . 12 (13): 2048–60. дои : 10.1101/гад.13.12.2048 . ПМК 316954 . ПМИД 9649508 .
- ^ Лю С; и др. (2006). «Передача сигналов Hedgehog и BMI-1 регулируют самообновление нормальных и злокачественных стволовых клеток молочной железы человека» . Рак Рез . 66 (12): 6063–71. дои : 10.1158/0008-5472.CAN-06-0054 . ПМЦ 4386278 . ПМИД 16778178 .
- ^ Люнг С; и др. (2004). «Bmi1 необходим для развития мозжечка и сверхэкспрессируется в медуллобластомах человека». Природа . 428 (6980): 337–41. Бибкод : 2004Natur.428..337L . дои : 10.1038/nature02385 . ПМИД 15029199 . S2CID 29965488 .
- ^ Зенчак Д; и др. (2005). «Потеря Bmi1 приводит к увеличению количества астроглиальных клеток и уменьшению популяции и пролиферации нервных стволовых клеток» . Дж. Нейроски . 25 (24): 5774–83. doi : 10.1523/JNEUROSCI.3452-04.2005 . ПМК 6724881 . ПМИД 15958744 .
- ^ Перейти обратно: а б Энглер, AJ; Сен, С; Суини, HL; Дишер, Делавэр (август 2006 г.). «Эластичность матрицы определяет спецификацию происхождения стволовых клеток» . Клетка . 126 (4): 677–689. дои : 10.1016/j.cell.2006.06.044 . ПМИД 16923388 . S2CID 16109483 .
- ^ Го, Цзюнь; Ван, Юэсю; Сакс, Фредерик ; Мэн, Фаньцзе (9 декабря 2014 г.). «Актиновый стресс при перепрограммировании клеток» . Труды Национальной академии наук . 111 (49): Е5252–Е5261. Бибкод : 2014PNAS..111E5252G . дои : 10.1073/pnas.1411683111 . ISSN 0027-8424 . ПМЦ 4267376 . ПМИД 25422450 .
- ^ Гуилак, Фаршид; Коэн, Дэниел М.; Эстес, Брэдли Т.; Гимбл, Джеффри М.; Лидтке, Вольфганг; Чен, Кристофер С. (2 июля 2009 г.). «Контроль судьбы стволовых клеток путем физического взаимодействия с внеклеточным матриксом» . Клеточная стволовая клетка . 5 (1): 17–26. дои : 10.1016/j.stem.2009.06.016 . ПМЦ 2768283 . ПМИД 19570510 .
- ^ «Ископаемое возрастом в миллиард лет обнаруживает недостающее звено в эволюции животных» . физ.орг . Проверено 9 мая 2021 г.
- ^ «Окаменелость возрастом в миллиард лет найдена в скалах Торридона» . Новости Би-би-си . 29 апреля 2021 г. Проверено 22 мая 2021 г.
- ^ Стротер, Пол К.; Брейзер, Мартин Д.; Уэйси, Дэвид; Тимпе, Лесли; Сондерс, Мартин; Веллман, Чарльз Х. (13 апреля 2021 г.). «Возможное голозойное животное возрастом в миллиард лет и с дифференцированной многоклеточностью» . Современная биология . 31 (12): 2658–2665.e2. Бибкод : 2021CBio...31E2658S . дои : 10.1016/j.cub.2021.03.051 . ISSN 0960-9822 . ПМИД 33852871 .
 Доступно по лицензии CC BY 4.0 .
Доступно по лицензии CC BY 4.0 .


