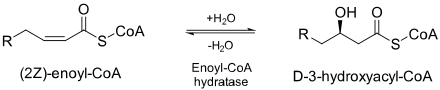
Enoyl-CoA гидратаза
| Enoyl-Coenzyme A, гидратаза/3-гидроксиацил coenzyme dehydrogenase | |||
|---|---|---|---|
 Эноил-коа гидратаза Гексамер от крысы с активным участком в оранжевом и субстрате красным. | |||
| Идентификаторы | |||
| Символ | Эххаг | ||
| Альт. символы | Эх | ||
| Ген NCBI | 1962 | ||
| HGNC | 3247 | ||
| Омим | 607037 | ||
| Refseq | NM_001966 | ||
| Uniprot | Q08426 | ||
| Другие данные | |||
| ЕС номер | 4.2.1.17 | ||
| Локус | Chr | ||
| |||
Enoyl-CoA гидратаза (ECH) или кротоназа [ 1 ] является ферментом EC 4.2.1.17 , который увлажняет двойную связь между вторым и третьим углеродами на 2-транс/cis-enoyl-coA: [ 2 ]
ECH необходим для метаболизации жирных кислот при бета -окислении для получения как ацетиловой COA, так и энергии в форме АТФ . [ 2 ]
ECH of Wabs является гексамерным белком (эта черта не универсален, но человеческий фермент также является гексамерным), что приводит к эффективности этого фермента, поскольку он имеет 6 активных сайтов. Было обнаружено, что этот фермент является высокоэффективным и позволяет людям очень быстро метаболизировать жирные кислоты в энергию. Фактически, этот фермент настолько эффективен, что скорость коротких цепных жирных кислот эквивалентна скорости реакций, контролируемых диффузией . [ 3 ]
Метаболизм
[ редактировать ]Метаболизм жирных кислот
[ редактировать ]ECH катализирует второй этап (гидратация) в расщеплении жирных кислот ( β-окисление ). [ 4 ] Метаболизм жирных кислот - это то, как человеческие тела превращают жиры в энергию. Жиры в продуктах, как правило, в форме триглицеринов . Они должны быть разбиты, чтобы жиры проходили в человеческие тела. Когда это произойдет, выделяются три жирные кислоты.
Лейциновый метаболизм
[ редактировать ]
Механизм
[ редактировать ]ECH используется при β-окислении для добавления гидроксильной группы и протона в ненасыщенный β-углерод на жирном COA. ECH функционирует, предоставляя два глутамата остатка в качестве каталитической кислоты и основания . Две аминокислоты удерживают молекулу воды на месте, позволяя ей атаковать в добавлении Syn к ненасыщенным α-β-ацил-КоА на β-углероде. Затем α-углерод захватывает еще один протон, который завершает образование бета-гидрокси ацил-КоА.

Из экспериментальных данных также известно, что никакие другие источники протонов не проживают на активном сайте . Это означает, что протон, который захватывает α-углерод, находится из воды, которая только что атаковала β-углерод. Это подразумевает, что гидроксильная группа и протон из воды добавляются с одной и той же стороны двойной связи , что добавление SYN. Это позволяет ECH сделать S -стереоизомер из 2-транс-эенойл-CoA и R-стереоизомер из 2-цис-эенойл-COA. Это стало возможным благодаря двум остаткам глутамата , которые удерживают воду в положении непосредственно рядом с ненасыщенной двойной связью α-β. Эта конфигурация требует, чтобы активный сайт для ECH был чрезвычайно жестким, чтобы удерживать воду в очень специфической конфигурации в отношении ацил-КоА. Данные для механизма этой реакции не являются окончательными относительно того, согласована ли эта реакция (показана на рисунке) или встречается на последовательных этапах. Если это происходит в последовательных этапах, промежуточное соединение идентично тому, что было бы получено из Реакция ELIMINATION ELIMINATION . [ 8 ]
ECH механически похож на фумаразу .
Ссылки
[ редактировать ]- ^ "EC 4.2.1.17" . www.sbcs.qmul.ac.uk. Получено 2018-09-05 .
- ^ Jump up to: а беременный Алленбах, L; Poirier, Y (2000). «Анализ альтернативных путей для β-окисления ненасыщенных жирных кислот с использованием трансгенных растений, синтезирующих полигидроксиалканоаты в пероксисомах» . Физиология растений . 124 (3): 1159–1168. doi : 10.1104/pp.124.3.1159 . ISSN 0032-0889 . PMC 59215 . PMID 11080293 .
- ^ Engel CK, Kiema TR, Hiltunen JK, Wierenga RK (февраль 1998 г.). «Кристаллическая структура эноил-КоА-гидратазы, комплексная с октаноил-КоА, показывает структурную адаптацию, необходимую для связывания молекулы с жирной кислотой с длинной цепью». Журнал молекулярной биологии . 275 (5): 847–59. doi : 10.1006/jmbi.1997.1491 . PMID 9480773 .
- ^ Кокс Д.Л., Нельсон М.М. (2005). Лехнингер Принципы биохимии (4 -е изд.). Нью -Йорк: WH Freeman. п. 647-43 . ISBN 978-0-7167-4339-2 .
- ^ Jump up to: а беременный Уилсон Дж. М., Фитшен П.Дж., Кэмпбелл Б., Уилсон Г.Дж., Занчи Н., Тейлор Л., Уилборн С., Калман Д.С., Стаут Дж.Р., Хоффман младший, Зигенфусс Т.Н., Лопес Х.Л., Крейдер Р.Б., Смит-Райан А.Е., Антонио Дж. (Февраль 2013 г.) Полем «Стенд международного общества спортивного питания: бета-гидрокси-бета-метилбутират (HMB)» . Журнал Международного общества спортивного питания . 10 (1): 6. doi : 10.1186/1550-2783-10-6 . PMC 3568064 . PMID 23374455 .
- ^ Jump up to: а беременный Kohlmeier M (май 2015). «Лейкин» . Метаболизм питательных веществ: структуры, функции и гены (2 -е изд.). Академическая пресса. С. 385–388. ISBN 978-0-12-387784-0 Полем Получено 6 июня 2016 года .
Энергетическое топливо: в конце концов, большая часть LEU разбивается, обеспечивая около 6,0 ккал/г. Около 60% употребления проглощенного LEU окисляется в течение нескольких часов ... Кетогенез: значительная доля (40% проглатываемой дозы) превращается в ацетил-КоА и тем самым способствует синтезу кетонов, стероидов, жирных кислот и других соединения
Рисунок 8.57: Метаболизм L -лейцина - ^ Bahnson BJ, Anderson VE, Petsko GA (февраль 2002 г.). «Структурный механизм эноил-КоА гидратазы: три атома из одной воды добавляются либо пошаговой или согласованной модой E1CB». Биохимия . 41 (8): 2621–9. doi : 10.1021/bi0158444p . PMID 11851409 .
Внешние ссылки
[ редактировать ]- Enoyl-CoA+гидратаза в Национальной медицинской библиотеке Медицинской библиотеки США (Mesh)