Электронный транспортный цепь
Цепь транспорта электронов ( и т. Д. [ 1 ] ) представляет собой серию белковых комплексов и других молекул, которые переносят электроны от доноров электронов в акцепторы электронов посредством окислительно -восстановительных реакций (как восстановление, так и окисление одновременно ) и объединяют этот электронный перенос с переносом протонов (H + ионы) через мембрану . Многие ферменты в электронном транспортном цепи встроены в мембрану .
Поток электронов через электронную переносную цепь является эксергоническим процессом . Энергия из окислительно -восстановительных реакций создает электрохимический градиент протонов , который стимулирует синтез аденозин трифосфата (АТФ). В аэробном дыхании поток электронов заканчивается молекулярным кислородом в качестве конечного акцептора электронов. В анаэробном дыхании используются другие акцепторы электронов, такие как сульфат .
В электронном транспортном цепи окислительно -восстановительные реакции обусловлены разницей в Гиббса свободной энергии реагентов и продуктов . Свободная энергия, выделяемая, когда донор и акцептор с более высокой энергией превращаются в продукты с более низкой энергией, в то время как электроны переносятся из более низкого окислительно-восстановительного потенциала , используется комплексами в цепи электронов для создания электрохимического градиента ионов Полем Именно этот электрохимический градиент ведет синтез АТФ посредством связи с окислительным фосфорилированием с АТФ -синтазой . [ 2 ]
У эукариотических организмов , цепь транспорта электронов и место окислительного фосфорилирования обнаружено на внутренней митохондриальной мембране . Энергия, выделяемая реакциями кислорода и восстановленных соединений, таких как цитохром C и (косвенно) NADH и FADH 2, используется цепью переноса электронов для протонов накачки в межмембранное пространство , генерируя электрохимический градиент над внутренней митохондриальной мембраной . В фотосинтетических эукариотах цепь транспорта электронов находится на тилакоидной мембране. Здесь световая энергия приводит к транспортировке электронов через протонный насос , а результирующий протонный градиент вызывает последующий синтез АТФ. У бактерий цепь транспорта электронов может варьироваться между видами, но всегда представляет собой набор окислительно -восстановительных реакций, которые связаны с синтезом АТФ посредством генерации электрохимического градиента и окислительного фосфорилирования через АТФ синтазу. [ 3 ]
Цепочки переноса митохондриальных электронов
[ редактировать ]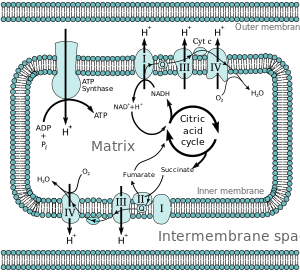
Большинство эукариотических клеток имеют митохондрии , которые продуцируют АТФ из реакций кислорода с продуктами цикла лимонной кислоты , метаболизмом жирных кислот и метаболизмом аминокислоты . На внутренней митохондриальной мембране электроны от NADH и FADH 2 проходят через цепь транспорта электронов к кислороду, что обеспечивает энергию, управляя процессом по мере его снижения до воды. [ 4 ] Цепь транспорта электронов содержит ферментативную серию доноров и акцепторов электронов. Каждый донор электронов передаст электроны акцептору с более высоким окислительно -восстановительным потенциалом, который, в свою очередь, жертвует эти электроны другому акцептору, процесс, который продолжается вниз по ряду до тех пор, пока электроны не будут переданы в кислород, акцептор клеммы в цепи. Каждая реакция высвобождает энергию, потому что донор и акцептор с более высокой энергией превращаются в продукты с более низкой энергией. С помощью переносимых электронов эта энергия используется для генерации градиента протонов через митохондриальную мембрану путем «перекачивания» протонов в межмембранное пространство, создавая состояние более высокой свободной энергии, которое может выполнять работу. Весь этот процесс называется окислительным фосфорилированием , поскольку ADP фосфорилируется в АТФ, используя электрохимический градиент, который окислительно-восстановительный реакции цепи транспорта электронов устанавливался, вызванные энергосвещающими реакциями кислорода.
Митохондриальные окислительно -восстановительные носители
[ редактировать ]Энергия, связанная с переносом электронов вниз по электронному транспортному цепи, используется для накачки протонов из митохондриальной матрицы в межмембранное пространство, создавая электрохимический градиент протонов ( ΔPH ) через внутреннюю митохондриальную мембрану. Этот градиент протонов в значительной степени, но не исключительно ответственен за потенциал митохондриальной мембраны (Δψ m ). [ 5 ] Это позволяет ATP -синтазе использовать поток H + через фермент обратно в матрицу для генерации АТФ из аденозинфосфата (ADP) и неорганического фосфата . Комплекс I (NADH Coenzyme Q REDUCTASE; помечен I) принимает электроны из цикла Krebs цикла -носителя никотинамида аденин -динуклеотид (NADH) и передает их коэнзим Q ( убиквинон ; помеченный Q), который также получает электроны из комплекса II ( duckinte dehyradone ; помечен II). Q проходит электроны в комплекс III ( цитохрома BC 1 комплекс ; помечен III), который передает их цитохрому C (Cyt C ). CYT C передает электроны в комплекс IV ( цитохром С оксидаза ; меченная IV).
Четыре мембранных комплекса были идентифицированы в митохондриях. Каждый из них является чрезвычайно сложной трансмембранной структурой, которая встроена во внутреннюю мембрану. Три из них - протонные насосы . Конструкции электрически соединены липидными электронными носителями и водорастворимыми электронными носителями. Общая транспортная цепь электронов может быть обобщена следующим образом:
NADH, H+ → Complex I → Q → Complex III → cytochrome c → Complex IV → H2O
↑
Complex II
↑
Succinate
Комплекс i
[ редактировать ]В комплексе I (NADH Ubiquinone Oxidoreductase, типа I NADH-дегидрогеназы или митохондриальный комплекс I; EC 1.6.5.3 ) два электрона удаляются из NADH и переносятся в липидный растворимый носитель, Ubiquinone (Q). Снижение продукта, убихинол (QH 2 ), свободно диффундирует в мембране, и комплекс I транслоцирует четыре протона (h + ) через мембрану, создавая протонный градиент. Комплекс I является одним из основных мест, на которых происходит преждевременная утечка электронов к кислороду, таким образом, является одним из основных мест производства супероксида . [ 6 ]
Путь электронов выглядит следующим образом:
NADH окисляется до NAD + , путем уменьшения мононуклеотида флавина до FMNH 2 на одном двухэлектронном шаге. FMNH 2 затем окисляется двумя одноэлектронными шагами через полухиноновое промежуточное звено. Таким образом, каждый электрон передается от FMNH 2 в кластер Fe-S , от кластера Fe-S до убихинона (Q). Передача первого электрона приводит к свободной ( полухиноновой ) форме Q, а перенос второго электрона уменьшает полухиноновую форму к форме убихинола, QH 2 . Во время этого процесса четыре протона перемещаются от митохондриальной матрицы в межмембранное пространство. [ 7 ] Когда электроны перемещаются через комплекс, электронный ток образуется вдоль 180 Angstrom ширины комплекса в мембране. Этот ток поддерживает активный транспорт четырех протонов в межмембранное пространство на два электрона от NADH. [ 8 ]
Комплекс II
[ редактировать ]В комплексе II ( сукцинатная дегидрогеназа или сукцинатная редуктаза; EC 1.3.5.1 ) Дополнительные электроны доставляются в бассейн хинона (Q), происходящий из сукцината и перенесенного (через флавин аденин-динуклеотид (FAD) ) в Q. Комплекс II состоит из четырех Белковые субъединицы: сукцинатная дегидрогеназа (SDHA); Сукцинатная дегидрогеназа [убихинон] железная субъединица митохондрия (SDHB); Сукцинатная дегидрогеназная комплекс субъединица C (SDHC); и сукцинатная дегидрогеназная комплекс субъединица D (SDHD). Другие доноры электронов (например, жирные кислоты и глицерин 3-фосфат) также направляют электроны в Q (через FAD). Комплекс II - это параллельный путь переноса электронов в комплекс I, но в отличие от комплекса I, протоны не транспортируются в межмембранное пространство на этом пути. Следовательно, путь через комплекс II вносит меньшую энергию в общий процесс транспортной цепи электронов.
Комплекс III
[ редактировать ]В комплексе III ( Cytochrome BC 1 Complex или CoQH 2 -CytoChrome C -редуктаза; EC 1.10.2.2 ) Q -цикл способствует градиенту протона путем асимметричного поглощения/высвобождения протонов. Два электрона удаляются из QH 2 на сайте Q O и последовательно переносятся в две молекулы цитохрома C , водорастворимого электронного носителя, расположенного в межмембранном пространстве. Два других электрона последовательно проходят через белок к сайту Q I , где хинон -часть убихинона снижается до хинола. Градиент протона образуется одним хинолом ( ) окисление на участке Q o с образованием одного хинона ( ) на Q I. сайте (В общей сложности транслоцируется четыре протона: два протона уменьшают хинон в хинол, а два протона высвобождаются из двух молекул убихинола.)
Когда перенос электрона снижается (с помощью высокого мембранного потенциала или ингибиторов дыхания, таких как антимицин А), комплекс III может утекать электроны в молекулярном кислороде, что приводит к образованию супероксида.
Этот комплекс ингибируется димеркапролом (британский анти-левейт, BAL), нафтохинон и антимицин.
Комплекс IV
[ редактировать ]В комплексе IV ( цитохром С оксидаза ; EC 1.9.3.1 ), иногда называемый цитохромом AA3, четыре электрона удаляются из четырех молекул цитохрома C и переносятся в молекулярный кислород (O 2 ) и четыре протона, продуцируя две молекулы воды. Комплекс содержит скоординированные медные ионы и несколько групп гема. В то же время восемь протонов удаляются из митохондриальной матрицы (хотя только четыре перемещаются через мембрану), способствуя градиенту протона. Точные детали протонной накачки в комплексе IV все еще изучаются. [ 9 ] Цианид является ингибитором комплекса IV.
Связь с окислительным фосфорилированием
[ редактировать ]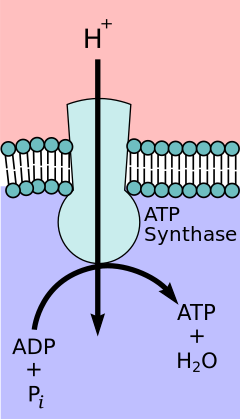
Согласно гипотезе химиомотической связи , предложенной химии Нобелевской премией в области Питером Д. Митчеллом , цепь транспорта электронов и окислительное фосфорилирование связаны с градиентом протона через внутреннюю митохондриальную мембрану. Отток протонов из митохондриальной матрицы создает электрохимический градиент (градиент протона). Этот градиент используется комплексом F O F 1 Синтазы АТФ для создания АТФ посредством окислительного фосфорилирования. АТФ -синтаза иногда описывается как комплекс V электронной транспортной цепи. [ 10 ] F o Компонент ATP -синтазы действует как ионный канал , который обеспечивает протоновый поток обратно в митохондриальную матрицу. Он состоит из субъединиц A, B и C. Протоны в межмембранном пространстве митохондрий сначала входят в комплекс АТФ синтазы через канал субъединицы . Затем протоны перемещаются в субъединицы С. [ 11 ] Количество субъединиц C определяет, сколько протонов требуется, чтобы сделать одну полную революцию. Например, у людей есть 8 субъединиц С, поэтому требуется 8 протонов. [ 12 ] После субъединиц C протоны, наконец, входят в матрицу через канал субъединицы , который открывается в митохондриальную матрицу. [ 11 ] Этот рефлюкс выпускает свободную энергию , производимую во время генерации окисленных форм электронных носителей (NAD + и Q) с энергией, предоставленной O 2 . Свободная энергия используется для управления синтезом АТФ, катализируемой компонентом F 1 комплекса. [ 13 ]
Соединение с окислительным фосфорилированием является ключевым шагом для производства АТФ. Однако в конкретных случаях разобщение двух процессов может быть биологически полезным. Необвишающий белок, термогенин - представлен во внутренней митохондриальной мембране коричневой жировой ткани - обеспечивает альтернативный поток протонов обратно во внутреннюю митохондриальную матрицу. Тироксин также является естественным некомплектором. Этот альтернативный поток приводит к термогенезу, а не к производству АТФ. [ 14 ]
Обратный электронный поток
[ редактировать ]Поток обратного электрона - это перенос электронов через электронную переносную цепь через обратные окислительно -восстановительные реакции. Обычно требуя значительного количества энергии, это может уменьшить окисленные формы доноров электронов. Например, NAD + может быть сведен к NADH в комплексе I. [ 15 ] Есть несколько факторов, которые, как было показано, вызывают обратный электронный поток. Тем не менее, необходимо проделать больше работы, чтобы подтвердить это. Одним из примеров является блокировка АТФ-синтазы, что приводит к наращиванию протонов и, следовательно, более высокой протонной силы , вызывающей обратный электронный поток . [ 16 ]
Прокариотические цепочки транспортировки электронов
[ редактировать ]В этом разделе нужны дополнительные цитаты для проверки . ( декабрь 2023 г. ) |
У эукариот NADH является наиболее важным донором электронов. Связанная цепь транспорта электронов представляет собой NADH → комплекс I → Q → комплекс III → цитохром C → комплекс IV → O 2 , где комплексы I, III и IV являются протонными насосами, в то время как Q и цитохром C являются мобильными электронными носителями. Электронным акцептором для этого процесса является молекулярный кислород.
В прокариотах ( бактерии и археи ) ситуация более сложна, потому что существует несколько разных доноров электронов и несколько разных акцепторов электронов. Обобщенная транспортная цепь электронов у бактерий:
Donor Donor Donor
↓ ↓ ↓
dehydrogenase → quinone → bc1 → cytochrome
↓ ↓
oxidase(reductase) oxidase(reductase)
↓ ↓
Acceptor Acceptor
Электроны могут войти в цепь на трех уровнях: на уровне дегидрогеназы , на уровне пула хинона или на уровне мобильного цитохромового электронного носителя. Эти уровни соответствуют последовательно более положительным окислительно -восстановительным потенциалам или последовательному снижению потенциальных различий по сравнению с акцептором терминала. Другими словами, они соответствуют последовательно меньшим изменениям свободной энергии Гиббса для общей окислительно -восстановительной реакции.
Отдельные бактерии используют несколько цепочек переноса электронов, часто одновременно. Бактерии могут использовать ряд различных доноров электронов, ряд различных дегидрогеназ, ряд различных оксидаз и редуктаз и ряд различных акцепторов электронов. Например, E.coli (при выращивании аэробной с использованием глюкозы и кислорода в качестве источника энергии) использует две различные дегидрогеназы NADH и две различные хинол оксидазы, в общей сложности четыре различных электронных транспортных цепей, работающих одновременно.
Общей особенностью всех электронных транспортных цепей является наличие протонного насоса для создания электрохимического градиента над мембраной. Цепочки переноса бактерий могут содержать до трех протонных насосов, таких как митохондрии, или они могут содержать два или по крайней мере один.
Доноры электронов
[ редактировать ]В текущей биосфере наиболее распространенными донорами электронов являются органические молекулы. Организмы, которые используют органические молекулы в качестве электронного источника, называются организмом . Хеморганатрофы (животные, грибы, протисты) и фотолитотрофы (растения и водоросли) составляют подавляющее большинство всех знакомых форм жизни.
Некоторые прокариоты могут использовать неорганическую материю в качестве источника электронов. Такой организм называется (химио) литотроф («Пожиратель рока»). Неорганические доноры электронов включают водород , угарный газ , аммиак , нитрит , серу , сульфид , оксид марганца и железо железа . Было обнаружено, что литотрофы растут в скалах в тысячи метров ниже поверхности Земли. Из -за объема их распределения литотрофы могут на самом деле превосходить по органотрофам и фототрофам в нашей биосфере .
Использование неорганических доноров электронов, таких как водород в качестве источника энергии, представляет особый интерес к изучению эволюции . Этот тип метаболизма должен логически предшествовать использованию органических молекул и кислорода в качестве источника энергии.
Дегидрогеназы: эквиваленты комплексам I и II
[ редактировать ]Бактерии могут использовать несколько разных доноров электронов. Когда органическое вещество является источником электрона, донором может быть NADH или сукцинат, и в этом случае электроны попадают в цепь транспорта электронов через надхдегидрогеназу (аналогично комплексу I в митохондриях) или сукцинатудегидрогеназы (аналогично комплексу II ). Другие дегидрогеназы могут использоваться для обработки различных источников энергии: формата-дегидрогеназы, лактатдегидрогеназы, глицеральдегид-3-фосфатдегидрогеназы, H 2 дегидрогеназа ( гидрогеназа ), цепь транспорта электронов. Некоторые дегидрогеназы также являются протонными насосами, в то время как другие всасывают электроны в бассейн хинона. Большинство дегидрогеназ показывают индуцированную экспрессию в бактериальной клетке в ответ на метаболические потребности, вызванные средой, в которой растут клетки. В случае лактатдегидрогеназы в E. coli фермент используется аэробно и в сочетании с другими дегидрогеназами. Он индуцируется и экспрессируется, когда концентрация DL-лактата в клетке высока. [ Цитация необходима ]
Носители хинона
[ редактировать ]Хиноны представляют собой подвижные, растворимые в липидах носители, которые переключают электроны (и протоны) между большими, относительно неподвижными макромолекулярными комплексами, встроенными в мембрану. Бактерии используют убихинон (коэнзим Q, тот же хинон, который использовал митохондрии) и родственные хиноны, такие как менахинон (витамин K 2 ). Archaea в роде Sulfolobus использует Caldariellaquinone. [ 17 ] Использование различных хинонов связано с небольшими изменениями окислительно -восстановительных потенциалов, вызванных изменениями в структуре. Изменение окислительно -восстановительных потенциалов этих хинонов может подходить для изменений в акцепторах электронов или изменений окислительно -восстановительных потенциалов в бактериальных комплексах. [ 18 ]
Протонные насосы
[ редактировать ]Протонный насос - это любой процесс, который создает протонное градиент по мембране. Протоны могут быть физически перемещены через мембрану, как видно в митохондриальных комплексах I и IV . Тот же эффект может быть получен путем перемещения электронов в противоположном направлении. Результатом является исчезновение протона из цитоплазмы и появление протона в периплазме. Митохондриальный комплекс III - это второй тип протонного насоса, который опосредуется хиноном ( цикл Q ).
Некоторые дегидрогеназы являются протонными насосами, а другие - нет. Большинство оксидазы и редуктазы являются протонными насосами, но некоторые нет. Цитохром BC 1 - это протонный насос, обнаруженный во многих, но не во всех бактериях (не в кишечной палочке ). Как следует из названия, бактериальный BC 1 похож на митохондриальную BC 1 ( комплекс III ).
Цитохромные электронные носители
[ редактировать ]Цитохромы - это белки, которые содержат железо. Они встречаются в двух очень разных средах.
Некоторые цитохромы представляют собой водорастворимые носители, которые переводят электроны в большие, неподвижные макромолекулярные структуры и из них, встроенные в мембрану. Мобильный цитохромный электронный носитель в митохондриях является цитохром c . Бактерии используют ряд различных мобильных цитохромовых электронных носителей.
Другие цитохромы обнаруживаются в макромолекулах, таких как комплекс III и комплекс IV . Они также функционируют как электронные носители, но в совершенно другой, внутримолекулярной, твердотельной среде.
Электроны могут войти в электронную транспортную цепь на уровне мобильного цитохрома или носителя хинона. Например, электроны из неорганических доноров электронов (нитрит, железного железа, электронного переноса) попадают в цепь переноса электронов на уровне цитохрома. Когда электроны входят на окислительно-восстановительном уровне, превышающем NADH, цепь переноса электронов должна работать на обратном направлении, чтобы получить эту необходимую молекулу с более высокой энергией.
Электронные акцепторы и терминальная оксидаза/редуктаза
[ редактировать ]В этом разделе может потребоваться очистка Википедии для соответствия стандартам качества . Конкретная проблема заключается в том, что мы говорим так, как будто оксидазы также не являются редуктазами, и как будто редуктузы также не окисляют что -то. Это испорчено. ( Декабрь 2023 г. ) |
Поскольку существует ряд различных доноров электронов (органическое вещество у органических веществ, неорганических веществ в литотрофах), существует ряд различных акцепторов электронов, как органических, так и неорганических. Как и в случае с другими этапами и т. Д., Для помощи в процессе требуется фермент.
Если кислород доступен, он чаще всего используется в качестве акцептора терминала в аэробных бактериях и факультативных анаэробных анаэробных. Оксидаза . сводит O 2 до воды, окислив что -то еще В митохондриях терминальным мембранным комплексом ( комплекс IV ) представляет собой цитохромоксидаза, которая окисляет цитохром. Аэробные бактерии используют ряд различных терминальных оксидаз. Например, E. coli ( факультативный анаэрон) не имеет цитохромоксидазы или комплекса BC 1 . В аэробных условиях он использует две разные терминальные хинол оксидазы (оба протонных насоса) для уменьшения кислорода до воды.
Бактериальные терминальные оксидазы могут быть разделены на классы в соответствии с молекулами, действующими как терминальные акцепторы электронов. Оксидазы класса I представляют собой цитохромоксидазы и используют кислород в качестве акцептора терминального электрона. Оксидазы класса II представляют собой хинол оксидазы и могут использовать различные терминальные акцепторы электронов. Оба этих класса могут быть разделены на категории, основываясь на том, какие окислительно-активные компоненты они содержат. Например, терминальные оксидазы класса 1 класса 1 гораздо более эффективны, чем терминальные оксидазы класса 2. [ 2 ]
В основном в анаэробных средах используются различные акцепторы электронов, включая нитрат, нитрит, железо железа, сульфат, углекислый газ и небольшие органические молекулы, такие как фумарат. Когда бактерии растут в анаэробной среде, акцептор терминала электрона снижается ферментом, называемым редуктазой. E. coli может использовать фумаратредуктазу, нитратредуктазу, нитритредуктазу, DMSO-редуктазу или триметиламина-N-оксидредуктазу, в зависимости от наличия этих акцепторов в окружающей среде.
Большинство терминальных оксидаз и редуктаз являются индуцируемыми . Они синтезируются организмом по мере необходимости, в ответ на конкретные условия окружающей среды.
Фотосинтетическое
[ редактировать ]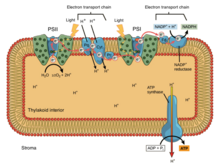
При окислительном фосфорилировании электроны переносятся из донора электронов, такого как NADH, в акцептор, такой как O 2, через цепь транспорта электронов, высвобождая энергию. При фотофосфорилировании энергия солнечного света используется для создания высокоэнергетического донора электронов, который впоследствии может уменьшить окисленные компоненты и соединять синтез АТФ посредством транслокации протона с помощью электронного транспорта. [ 9 ]
Фотосинтетические электронные транспортные цепочки, такие как митохондриальная цепь, могут рассматриваться как особый случай бактериальных систем. Они используют подвижные, растворимые в липидных носителях хинона ( филлохинон и пластохинон ) и мобильные, растворимых в воде ( цитохромы ). Они также содержат протонный насос . Протонный насос во всех фотосинтетических цепях напоминает митохондриальный комплекс III . Обычно укрепленная теория симбиогенеза предполагает, что оба органелла произошли от бактерий.
Смотрите также
[ редактировать ]- Комплекс переноса заряда
- Корр гипотеза
- Электронный эквивалент
- Гипотеза водорода
- Респирасоме
- Электрические бактерии
Ссылки
[ редактировать ]- ^ Lyall, Fiona (2010). «Биохимия». Основная наука в акушерстве и гинекологии . С. 143–171. doi : 10.1016/b978-0-443-10281-3.00013-0 . ISBN 978-0-443-10281-3 .
- ^ Jump up to: а беременный Анраку Y (июнь 1988 г.). «Цепочки переноса бактерий». Ежегодный обзор биохимии . 57 (1): 101–32. doi : 10.1146/annurev.bi.57.070188.000533 . PMID 3052268 .
- ^ Крак Ф., Вассилев I, Крёмер Джо (2015). «Микробный электронный транспорт и энергосбережение - основа для оптимизации биоэлектрохимических систем» . Границы в микробиологии . 6 : 575. DOI : 10.3389/fmicb.2015.00575 . PMC 4463002 . PMID 26124754 . - Этот источник показывает четыре и т. Д. ( Geobacter , Shewanella , Moorella , Acetobacterium ) на рисунках 1 и 2.
- ^ Waldenström JG (2009-04-24). «Биохимия. Луберт Страйер». Acta Medica Scandinavica . 198 (1–6): 436. doi : 10.1111/j.0954-6820.1975.tb19571.x . ISSN 0001-6101 .
- ^ Zorova LD, Popkov VA, Plotnikov EY, Silachev DN, Pevzner IB, Jankauskas SS, et al. (July 2018). "Mitochondrial membrane potential" . Analytical Biochemistry . 552 : 50–59. doi : 10.1016/j.ab.2017.07.009 . PMC 5792320 . PMID 28711444 .
- ^ Лорен, Биохимия, Джонсон/Коул, 2010, стр. 598-611
- ^ Garrett & Grisham, Biochemistry, Brooks/Cole, 2010, стр. 598-611
- ^ Гарретт Р., Гришам К.М. (2016). Биохимия . Бостон: Cengage. п. 687. ISBN 978-1-305-57720-6 .
- ^ Jump up to: а беременный Страйер. Биохимия . Топпан. OCLC 785100491 .
- ^ Jonckheere AI, Smeitink JA, Rodenburg RJ (март 2012 г.). «Митохондриальная АТФ -синтаза: архитектура, функция и патология» . Журнал наследственного метаболического заболевания . 35 (2): 211–25. doi : 10.1007/s10545-011-9382-9 . PMC 3278611 . PMID 21874297 .
- ^ Jump up to: а беременный Garrett RH, Grisham CM (2012). Биохимия (5 -е изд.). Cengage Learning. п. 664. ISBN 978-1-133-10629-6 .
- ^ Filingame RH, Angevine CM, Dmitriev Oy (ноябрь 2003 г.). «Механика связывания протонных движений с вращением C-кольца в ATP-синтазе» . Письма Febs . 555 (1): 29–34. doi : 10.1016/s0014-5793 (03) 01101-3 . PMID 14630314 . S2CID 38896804 .
- ^ Berg JM, Tymoczko JL, Stryer L (2002-01-01). «Градиент протона способствует синтезу АТФ» .
{{cite journal}}: CITE Journal требует|journal=( помощь ) - ^ Cannon B, Nedergaard J (январь 2004 г.). «Коричневая жировая ткань: функция и физиологическое значение» . Физиологические обзоры . 84 (1): 277–359. doi : 10.1152/physrev.00015.2003 . PMID 14715917 .
- ^ Ким Б.Х., Гэдд Г.М. (2008). «Введение в бактериальную физиологию и метаболизм». Бактериальная физиология и метаболизм . Издательство Кембриджского университета. С. 1–6. doi : 10.1017/cbo9780511790461.002 . ISBN 978-0-511-79046-1 .
- ^ Mills EL, Kelly B, Logan A, Costa AS, Varma M, Bryant CE, et al. (Октябрь 2016). «Сукцинатная дегидрогеназа поддерживает метаболическую перепрофилирование митохондрий для управления воспалительными макрофагами» . Клетка . 167 (2): 457–470.e13. doi : 10.1016/j.cell.2016.08.064 . PMC 5863951 . PMID 27667687 .
- ^ EC 1.3.5.1
- ^ Ingledew WJ, Poole RK (сентябрь 1984 г.). «Респираторные цепочки эшерухийской палой» . Микробиологические обзоры . 48 (3): 222–71. doi : 10.1128/mmbr.48.3.222-271.1984 . PMC 373010 . PMID 6387427 .
Дальнейшее чтение
[ редактировать ]- Fenchel T, King GM, Blackburn TH (сентябрь 2006 г.). Бактериальная биогеохимия: экофизиология минерального велосипеда (2 -е изд.). Elsevier. ISBN 978-0-12-103455-9 .
- Lengeler JW (январь 1999 г.). Дрюс G; Schlegel Hg (ред.). Биология прокариот . Blackwell Science. ISBN 978-0-632-05357-5 .
- Нельсон Д.Л., Кокс М.М. (апрель 2005 г.). Лехнингер Принципы биохимии (4 -е изд.). WH Freeman. ISBN 978-0-7167-4339-2 .
- Николс Д.Г., Фергюсон С.Дж. (июль 2002 г.). Биоэнергетика 3 . Академическая пресса. ISBN 978-0-12-518121-1 .
- Стимм w; Морган JJ (1996). Водная химия (3 -е изд.). Джон Уайли и сыновья . ISBN 978-0-471-51185-4 .
- Thauer RK, Jungermann K, Decker K (март 1977 г.). «Энергетическое сохранение у хемотрофных анаэробных бактерий» . Бактериологические обзоры . 41 (1): 100–80. doi : 10.1128/mmbr.41.1.100-180.1977 . PMC 413997 . PMID 860983 .
- Белый D (сентябрь 1999 г.). Физиология и биохимия прокариот (2 -е изд.). Издательство Оксфордского университета . ISBN 978-0-19-512579-5 .
- Voet D, Voet JG (Marce 2004). Биохимия Тол. 28 (3 -й и.). Джон Уайли и Звуки . стр. 124 doi : 10.1016/s0307-4412 (00) 00032-7 . ISBN 978-0-471-58651-7 Полем PMID 10878303 .
{{cite book}}:|journal=игнорируется ( помощь ) - Kim HS, Patel K, Muldoon-Jacobs K, Bisht KS, Aykin-Burns N, Pennington JD, et al. (Январь 2010). «SIRT3-это митохондрия-локализованный супрессор опухоли, необходимый для поддержания целостности митохондрий и метаболизма во время стресса» . Раковая клетка . 17 (1): 41–52. doi : 10.1016/j.ccr.2009.11.023 . PMC 3711519 . PMID 20129246 .
- Raimondi V, Ciccarese F, Stimsle V (январь 2020 г.). «Октанические пути и транспортная цепь электронов: связь с дагеросом » Br J Cancer 122 (2): 168–1 Doi : 10.1038/s41416-019-0651- Y PMC 7052168 31819197PMID
- Регуара, Джемма (29 мая 2018 г.). «Биологический транспорт электронов проходит лишнюю милю» . Труды Национальной академии наук . 115 (22): 5632–5634. Bibcode : 2018pnas..115.5632r . doi : 10.1073/pnas.1806580115 . PMC 5984551 . PMID 29769327 . - Редакционный комментарий с упоминанием двух необычных и т. Д.: Комментарий Geobacter Sulfurreducens и кабельных бактерий . Также имеет схему E. coli и т. Д.
Внешние ссылки
[ редактировать ]- Electron+Transport+Chain+Complex+белки в Национальной библиотеке Медицинской библиотеки Медицинской библиотеки (Mesh)
- Ханская академия, видео -лекция
- Путь KEGG : окислительное фосфорилирование, наложенное на гены, обнаруженные в Pseudomonas Fluorescens PF0-1. Нажмите «Помощь», чтобы узнать о праве.







