Железо-серный кластер
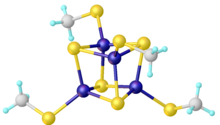
Железо-серные кластеры представляют собой молекулярные ансамбли железа и сульфида . Чаще всего они обсуждаются в контексте биологической роли железо-серных белков , которые широко распространены. [ 2 ] Многие кластеры Fe–S известны в области металлоорганической химии и как предшественники синтетических аналогов биологических кластеров (см. рисунок). Считается, что последний универсальный предок имел множество железо-серных скоплений. [ 3 ]
Металлоорганические кластеры
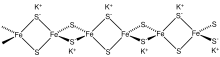
[ редактировать ]Металлоорганические кластеры Fe–S включают сульфидкарбонилы с формулами Fe 2 S 2 (CO) 6 , H 2 Fe 3 S(CO) 9 и Fe 3 S 2 (CO) 9 . Известны также соединения, в состав которых входят циклопентадиенильные лиганды, такие как (C 5 H 5 ) 4 Fe 4 S 4 . [ 4 ]

Неорганические материалы
[ редактировать ]Этот раздел нуждается в расширении . Вы можете помочь, добавив к нему . ( ноябрь 2022 г. ) |
Биологические кластеры Fe–S
[ редактировать ]Кластеры железо-сера встречаются во многих биологических системах, часто как компоненты белков- переносчиков электронов . Белки ферредоксина представляют собой наиболее распространенные в природе кластеры Fe–S. Они имеют центры либо 2Fe–2S, либо 4Fe–4S. Они встречаются во всех отраслях жизни. [ 5 ]
Кластеры Fe–S можно классифицировать по их стехиометрии Fe:S: [2Fe–2S], [4Fe–3S], [3Fe–4S] и [4Fe–4S]. [ 6 ] Кластеры [4Fe–4S] встречаются в двух формах: нормальные ферредоксины и белки железа с высоким потенциалом (HiPIP). Оба имеют кубовидную структуру, но используют разные степени окисления. Они встречаются во всех формах жизни. [ 7 ]
Соответствующей окислительно-восстановительной парой во всех белках Fe-S является Fe(II)/Fe(III). [ 7 ]
Многие кластеры были синтезированы в лаборатории по формуле [Fe 4 S 4 (SR) 4 ] 2− , которые известны многими заместителями R и многими катионами. Были подготовлены варианты, включающие неполные кубаны [Fe 3 S 4 (SR) 3 ] 3− . [ 8 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Аксель Керн; Кристиан Нэтер; Феликс Штудт; Феликс Тучек (2004). «Применение универсального силового поля к смешанным кубиновым и гетерокубановым кластерам Fe/Mo-S/Se. 1. Замещение серы на селен в ряду [Fe4X4(YCH3)4]2-; X = S/Se и Y = S /Се». Неорг. Хим . 43 (16): 5003–5010. дои : 10.1021/ic030347d . ПМИД 15285677 .
- ^ С. Дж. Липпард, Дж. М. Берг «Принципы биоинорганической химии» Университетские научные книги: Милл-Вэлли, Калифорния; 1994. ISBN 0-935702-73-3 .
- ^ Вайс, Мэдлин С. и др. «Физиология и среда обитания последнего всеобщего общего предка». Природная микробиология 1.9 (2016): 1-8.
- ^ Огино, Х.; Иномата, С.; Тобита, Х. (1998). «Абиологические железо-серные кластеры». хим. Преподобный . 98 (6): 2093–2122. дои : 10.1021/cr940081f . ПМИД 11848961 .
- ^ Джонсон, округ Колумбия; Дин, доктор медицинских наук; Смит, AD; Джонсон, МК (2005). «Структура, функции и образование биологических железо-серных кластеров». Ежегодный обзор биохимии . 74 : 247–281. doi : 10.1146/annurev.biochem.74.082803.133518 . ПМИД 15952888 .
- ^ Лилль, Роланд (2015). «Вопрос железосерного белка» . Биохимика и биофизика Acta . 1853 (6): 1251–1252. дои : 10.1016/j.bbamcr.2015.03.001 . ПМК 5501863 . ПМИД 25746719 .
- ^ Jump up to: а б Фишер, Н. (1998). «Внутримолекулярный перенос электрона в [4Fe–4S)]». Журнал EMBO : 849–858.
- ^ Рао, П.В.; Холм, Р.Х. (2004). «Синтетические аналоги активных центров железо-серных белков». хим. Преподобный . 104 (2): 527—559. дои : 10.1021/Cr020615+ . ПМИД 14871134 .