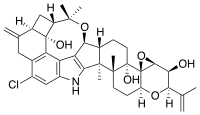
Пенитрем А
 | |
| Имена | |
|---|---|
| Другие имена Тремортин | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.162.141 |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 37 Н 44 ClNO 6 | |
| Молярная масса | 633.20136 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
Пенитрем А ( тремортин ) представляет собой индол-дитерпеноидный микотоксин , продуцируемый некоторыми видами Aspergillus , Claviceps и Penicillium , которые можно обнаружить на различных видах растений, таких как райграс . [1] Пенитрем А является одним из многих вторичных метаболитов, образующихся после синтеза паксиллина в Penicillium crostosum . [2] Пенитрем Отравление у людей и животных обычно происходит в результате употребления в пищу загрязненных пищевых продуктов видами, продуцирующими микотоксины, которые затем распространяются по организму с током крови. [2] Он обходит гематоэнцефалический барьер и оказывает токсикологическое воздействие на центральную нервную систему . [2] У людей отравление пенитремом А вызывало сильный тремор, гипертермию , тошноту / рвоту , диплопию и кровавый понос . [2] У животных симптомы отравления пенитремом А сопровождаются различными симптомами: от тремора, судорог и гипертермии до атаксии и нистагма . [2]
Рокефортин С часто выявлялся в задокументированных случаях отравления пенитремом А, что делает его возможным биомаркером для диагностики. [3]
Механизм действия
[ редактировать ]Пенитрем А ухудшает нейротрансмиссию ГАМКергических аминокислот и противодействует высокопроводящему кальцию. 2+ -активированные калиевые каналы как у людей, так и у животных. [4] Нарушение нейротрансмиссии ГАМКергических аминокислот сопровождается спонтанным высвобождением возбуждающих аминокислот глутамата и аспартата, а также тормозного нейромедиатора γ-аминомасляной кислоты (ГАМК). [4] Внезапное высвобождение этих нейротрансмиттеров приводит к несбалансированной передаче ГАМКергических сигналов, что приводит к неврологическим расстройствам, таким как тремор, связанный с отравлением пенитремом А. [4]
Пенитрем А также индуцирует выработку активных форм кислорода (АФК) в нейтрофильных гранулоцитах человека и животных. [2] Повышенное производство АФК приводит к повреждению тканей головного мозга и других пораженных органов, а также к кровоизлияниям при острых отравлениях. [2]
Синтез
[ редактировать ]У Penicillium cordosum синтез пенитрема А и других вторичных метаболитов следует за синтезом паксиллина . [5] В синтезе пенитрема А участвуют шесть ферментов окислительной трансформации (четыре монооксигеназы цитохрома Р450 и две флавинадениндинуклеотид (ФАД)-зависимые монооксигеназы ), две ацетилтрансферазы , одна оксидоредуктаза и одна пренилтрансфераза . [5] Эти ферменты кодируются кластером генов, используемых в синтезе паксиллина и синтезе пенитрема AF. [5] Путь описан ниже:
- Оксидоредуктаза катализирует восстановление кетона паксиллина, а также добавляет диметилаллильную группу к его ароматическому кольцу. [5]
- Ацетилтрансферазы катализируют удаление нижней правой гидроксильной группы промежуточного продукта и восстановление одной из близлежащих метильных групп до метиленовой группы. [5]
- Фермент окислительной трансформации катализирует присоединение гидроксильной группы к диметилаллильной группе промежуточного продукта. Двойная связь диметилаллила перемещается вниз на один атом углерода. [5]
- Пренилтрансфераза катализирует образование диметилциклопентана и циклобутана, используя ароматическую кольцевую спиртовую группу промежуточного продукта. [5]
- Фермент окислительного преобразования катализирует образование метиленциклогексана с использованием промежуточного продукта диметилциклопентана, образуя секопенитрем D. [5]
- Фермент окислительного преобразования катализирует образование циклооктана с группы циклобутана использованием спиртовой и углерода, соединяющего циклогексан и циклопентан секопенитрема D , образуя пенитрем D. [5]
- Фермент окислительного преобразования катализирует присоединение атома хлора к ароматическому кольцу пенитрема D, образуя пенитрем C. [5]
- Фермент окислительного превращения катализирует образование эпоксидного -двойной связи пенитрема С кольца у оксан , образуя пенитрем F. [5]
- Фермент окислительного преобразования катализирует присоединение гидроксильной группы к углероду, соединяющей метиленциклогексан и циклобутан пенитрема F, образуя пенитрем А. [5]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Уолтер, Шон Л. (2002). «Острое отравление пенитремом А и рокефортином у собаки» . Канадский ветеринарный журнал . 43 (5): 372–374. ISSN 0008-5286 . ПМК 339273 . ПМИД 12001505 .
- ^ Jump up to: а б с д и ж г Бернтсен, ХФ; Боген, Иллинойс; Вигестранд, МБ; Фоннум, Ф; Валаас, С.И.; Молдес-Аная, А (01 декабря 2017 г.). «Грибковый нейротоксин пенитрем А индуцирует выработку активных форм кислорода в нейтрофилах человека в субмикромолярных концентрациях». Токсикология . 392 : 64–70. дои : 10.1016/j.tox.2017.10.008 . ISSN 0300-483X . ПМИД 29037868 .
- ^ Тивари, АК (март 2009 г.). «Использование рокефортина С в качестве биомаркера интоксикации пенитремом А» . Журнал ветеринарных диагностических исследований . 21 (2): 237–239. дои : 10.1177/104063870902100210 . ПМИД 19286504 .
- ^ Jump up to: а б с Молдес-Аная, Анхель С; Фоннум, Фроде; Эриксен, Гуннар С; Рундбергет, Томас; Валаас, С. Ивар; Вигестранд, Мэттис Б (01 декабря 2011 г.). «Нейрофармакологическая оценка in vitro треморгенных синдромов, вызванных пенитремом: важность ГАМКергической системы». Нейрохимия Интернэшнл . 59 (7): 1074–1081. doi : 10.1016/j.neuint.2011.08.014 . ISSN 0197-0186 . ПМИД 21924313 . S2CID 36629380 .
- ^ Jump up to: а б с д и ж г час я дж к л Лю, Ченгвэй; Тагами, Коичи; Минами, Ацуши; Мацумото, Томоюки; Фрисвад, Йенс Кристиан; Сузуки, Хидеюки; Исикава, Джун; Гоми, Кацуя; Оикава, Хидеаки (01 апреля 2015 г.). «Восстановление биосинтетического оборудования для синтеза высокоразработанного индолдитерпена пенитрема». Angewandte Chemie, международное издание . 54 (19): 5748–5752. дои : 10.1002/anie.201501072 . ISSN 1433-7851 . ПМИД 25831977 . S2CID 205386781 .