Флумекин
 | |
| Клинические данные | |
|---|---|
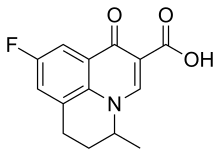
| Другие имена | 9-Фтор-6,7-дигидро-5-метил-1-оксо- 1H ,5H - бензо[ ij ]-хинолизин-2-карбоновая кислота |
| AHFS / Drugs.com | Международные названия лекарств |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Фармакокинетические данные | |
| Экскреция | моча и кал |
| Идентификаторы | |
| Номер CAS | |
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЭБИ | |
| Панель управления CompTox ( EPA ) | |
| Информационная карта ECHA | 100.050.857 |
| Химические и физические данные | |
| Формула | С 14 Н 12 Ф Н О 3 |
| Молярная масса | 261.252 g·mol −1 |
| 3D model ( JSmol ) | |
| Температура плавления | От 253 до 255 ° C (от 487 до 491 ° F) |
| | |
Флумекин [1] синтетический группы фторхинолонов. антибиотик [2] [3] используется для лечения бактериальных инфекций. Это фторхинолоновый антибактериальный препарат первого поколения, который выведен из клинического применения и больше не продается. [4] Выдача регистрационного удостоверения на флюмекин была приостановлена на всей территории ЕС. [5] Он убивает бактерии, воздействуя на ферменты, которые заставляют ДНК раскручиваться и удваиваться. Флумехин применялся в ветеринарии для лечения кишечных инфекций (всех инфекций кишечного тракта), [6] а также для лечения крупного рогатого скота, свиней, кур и рыбы, но только в ограниченном числе стран. [4] [7] [8] Его иногда использовали во Франции (и некоторых других европейских странах) для лечения инфекций мочевыводящих путей под торговым названием Апурон. [4] [9] Однако это было ограниченное указание [10] потому что были достигнуты только минимальные уровни в сыворотке. [11]
История
[ редактировать ]Первым использованным хинолоном была налидиксовая кислота (продававшаяся во многих странах под названием Неграм), за которой последовал фторхинолон флумехин. [4] Фторхинолоны первого поколения, такие как флумекин, плохо распределялись в тканях организма и имели ограниченную активность. Таким образом, они использовались в основном для лечения инфекций мочевыводящих путей. Флумехин (бензохинолизин) был впервые запатентован в 1973 году (патент Германии) компанией Rikker Labs. [12] Флумехин представляет собой известное противомикробное соединение, описанное и заявленное в пат. № 3896131 (Пример 3), 22 июля 1975 г. [13] Флумехин является первым хинолоновым соединением с атомом фтора в положении C6 родственной хинолоновой базовой молекулярной структуры. [14] Несмотря на то, что это был первый фторхинолон, его часто упускают из виду при классификации препаратов этого класса по поколениям и исключают из такого списка.
Хотя флумекин часто использовался для лечения сельскохозяйственных животных, а иногда и домашних животных, он также использовался для лечения инфекций мочевыводящих путей у людей. Флумехин использовался для временного лечения инфекций мочевыводящих путей. [9] до тех пор, пока не было сообщено о глазной токсичности. [15] [16] [17] а также повреждение печени [18] и анафилактический шок. [19] [20]
В 2008 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) потребовало, чтобы все вкладыши в упаковку препаратов хинолонов/фторхинолонов включали в черный ящик предупреждение о риске спонтанных разрывов сухожилий, которое включало бы флумехин. FDA также попросило производителей разослать письма уважаемому доктору относительно этого нового предупреждения. Подобные проблемы с сухожилиями также были связаны с приемом флумекина. [21]
Остаток препарата
[ редактировать ]Использование флумекина у сельскохозяйственных животных вызвало серьезные споры. Значительные и вредные остатки хинолонов были обнаружены у животных, обработанных хинолонами, а затем забитых и проданных в качестве пищевых продуктов. Вызывает серьезную обеспокоенность количество остатков флумекина, обнаруженных в продуктах животного происхождения, таких как рыба, птица и крупный рогатый скот. [22] [23] В 2003 году Объединенный комитет ФАО/ВОЗ по пищевым добавкам (JECFA) отменил максимальные пределы остатков (MRL) для флумекина и карбадокса на основании данных, показывающих, что оба они являются генотоксичными канцерогенами прямого действия, поэтому Комитет не смог установить допустимую суточную дозу (ADI). ) для воздействия таких остатков на человека. [24] Впоследствии, в 2006 году, JEFCA восстановил ADI после получения соответствующих доказательств, и MRL были пересмотрены. Роль JECFA заключается в оценке токсикологии, химического состава остатков и соответствующей информации, а также в выработке рекомендаций относительно допустимых уровней суточного потребления (ADI) и максимальных пределов остатков (MRL). На своей 16-й сессии, состоявшейся в мае 2006 г., Комитет по остаткам ветеринарных препаратов в пищевых продуктах (CCRVDF) запросил информацию о зарегистрированных применениях флумекина. Поскольку CCRVDF не получил никакой запрошенной информации о зарегистрированных применениях флумекина, члены комитета согласились прекратить работу над МДУ флумекина в креветках. [25] [26]
Лицензионное использование
[ редактировать ]Инфекции мочевыводящих путей (ветеринарные и человеческие) [27]
Доступность
[ редактировать ]Ветеринарное использование:
- Решение; Оральный; 20% (только по рецепту)
- Решение; Оральный; 10% (только по рецепту)
Использование человеком:
- Таблетка; Оральный; Флумехин 400 мг (снято с производства)
Способ действия
[ редактировать ]Флумекин является членом семейства хинолоновых антибиотиков , которые активны как в отношении грамположительных , так и грамотрицательных бактерий. Он действует путем ингибирования ДНК-гиразы типа II , топоизомеразы и топоизомеразы IV. [28] ферменты, необходимые для разделения бактериальной ДНК, тем самым ингибируя деление клеток.
Этот механизм также может влиять на репликацию клеток млекопитающих. В частности, некоторые родственники этого семейства лекарств (например, те, которые содержат фтор С-8), [29] проявляют высокую активность не только против бактериальных топоизомераз, но и против эукариотических топоизомераз и токсичны для культивируемых клеток млекопитающих и in vivo . моделей опухолей [30]
Хотя хинолоны высокотоксичны для клеток млекопитающих в культуре, механизм их цитотоксического действия неизвестен. Впервые о повреждении ДНК, вызванном хинолонами, было сообщено в 1986 году (Hussy et al.). [31]
Недавние исследования продемонстрировали корреляцию между цитотоксичностью хинолонов в клетках млекопитающих и индукцией микроядер. [32] [33] [34] [35]
Таким образом, некоторые фторхинолоны могут вызывать повреждение хромосом эукариотических клеток. [36] [37] [38] [39] [40] [41]
Продолжаются серьезные споры о том, следует ли считать это повреждение ДНК одним из механизмов действия, связанного с тяжелыми побочными реакциями, которые наблюдаются у некоторых пациентов после терапии фторхинолонами. [30] [42]
Побочные реакции
[ редактировать ]Флумехин вызывал тяжелую глазную токсичность, что исключало его использование у людей. [15] [16] [17] С такой терапией также связаны камни, вызванные лекарственными средствами (камни в почках). [43] [44] [45] Анафилактический шок, вызванный терапией флумехином, также был связан с его применением. [19] [20] [46] Сообщалось, что анафилактоидные реакции, такие как шок, крапивница и отек Квинке, обычно появляются в течение двух часов после приема первой таблетки. В 1996 году в досье ВОЗ было 18 отчетов. [47] Как и все препараты этого класса, терапия флумехином может привести к тяжелым реакциям со стороны центральной нервной системы (ЦНС). [48] [49] [50] фототоксичность, приводящая к кожным реакциям, таким как эритема, зуд, крапивница и сильная сыпь, [51] [52] желудочно-кишечные и неврологические расстройства. [9]
Взаимодействие с лекарственными средствами
[ редактировать ]Было обнаружено, что флумехин не оказывает влияния на фармакокинетику теофиллина . [53]
Химия
[ редактировать ]Флумехин представляет собой 9-фтор-6,7-дигидро-5-метил-1-оксо-1H,5H-бензо[ij]хинолизин-2-карбоновую кислоту. Молекулярная формула C 14 H 12 FNO 3 . Это белый порошок без запаха и вкуса, нерастворимый в воде, но растворимый в органических растворителях. [54]
Фармакокинетика
[ редактировать ]Считается, что флумехин хорошо всасывается и выводится с мочой и калом в виде глюкуронидных конъюгатов исходного препарата и 7-гидроксифлумехина. Он выводится в течение 168 часов после приема. Однако исследования, касающиеся печени теленка, выявили дополнительные неидентифицированные остатки, из которых новый метаболит ml представлял собой основной метаболит через 24 часа после последней дозы и во все последующие моменты времени. Метаболит ml, не проявлявший антимикробной активности, присутствовал как в свободной, так и в связанной с белком фракциях. Основной остаток, обнаруженный в съедобных тканях овец, свиней и кур, представлял собой исходное лекарственное средство вместе с небольшими количествами 7-гидроксиметаболита. Единственным обнаруженным остатком в форели был исходный препарат. [55]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ МНН: ломефлоксацина гидрохлорид.
- ^ Нельсон Дж. М., Чиллер Т. М., Пауэрс Дж. Х., Ангуло Ф. Дж. (апрель 2007 г.). «Устойчивые к фторхинолонам виды Campylobacter и отказ от использования фторхинолонов в птицеводстве: история успеха общественного здравоохранения» . Клинические инфекционные болезни . 44 (7): 977–980. дои : 10.1086/512369 . ПМИД 17342653 .
- ^ Кавахара С. (декабрь 1998 г.). «[Химиотерапевтические средства, находящиеся в стадии изучения]». Нихон Ринсё. Японский журнал клинической медицины (на японском языке). 56 (12): 3096–3099. ПМИД 9883617 .
- ^ Перейти обратно: а б с д «Хинолоны и фторхинолоны» . Фармакорама. Архивировано из оригинала 12 мая 2019 г. Проверено 4 апреля 2010 г.
- ^ «Инвалидизирующие и потенциально необратимые побочные эффекты приводят к приостановке или ограничению приема хинолоновых и фторхинолоновых антибиотиков» . Европейское агентство по лекарственным средствам . 11 марта 2019 г.
- ^ Фрэнсис П.Г., Уэллс Р.Дж. (1998). «Флюмекин». Объединенный комитет экспертов ФАО/ВОЗ по пищевым добавкам. Остатки некоторых ветеринарных препаратов в животных и пищевых продуктах . Рим: Продовольственная и сельскохозяйственная организация. ISBN 92-5-104128-8 . OCLC 39798999 .
- ^ Использование хинолонов у животных, употребляемых в пищу, и потенциальное воздействие на здоровье человека (PDF) . Встреча ВОЗ. Женева, Швейцария: Всемирная организация здравоохранения. Июнь 1998 г. Архивировано из оригинала (PDF) 14 января 2010 г. Крупный рогатый скот только в Европе и Латинской Америке. (Ограниченное использование в Латинской Америке), Птица только в Европе, Азии и Латинской Америке, Рыба только в Азии
- ^ Лавенберг ДЛ. «IX4Q 4586, 3,23% раствор брритрита-концентрата для использования в питьевой воде для кур, род. Переписка, опубликованная литература» (PDF) . Байер . Архивировано из оригинала (PDF) 5 октября 2012 года – через Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США.
Хиналоны часто используются для лечения тяжелых случаев заражения человека Campylobacter spp., а также в ветеринарии, особенно для лечения домашней птицы.
- ^ Перейти обратно: а б с Шена Ф.П., Джезуальдо Л., Караччиоло Дж. (январь 1988 г.). «Многоцентровое исследование флумекина при лечении инфекций мочевыводящих путей». Журнал антимикробной химиотерапии . 21 (1): 101–106. дои : 10.1093/jac/21.1.101 . ПМИД 3356617 .
- ^ Хинолоны (Третье издание, 2000 г.)Винсент Т. Андриол Глава I История и обзор Доктора Питера Болла(стр. 5)
- ^ Кинг Д.Е., Мэлоун Р., Лилли Ш. (май 2000 г.). «Новая классификация и обновленная информация о хинолоновых антибиотиках». Американский семейный врач . 61 (9): 2741–2748. ПМИД 10821154 .
- ^ «Дженерикс (Великобритания) Лтд. против Daiichi Pharmaceutical Co Ltd» . Отчеты по делам о патентах, промышленных образцах и товарных знаках . 126 (2): 102. 2009. doi : 10.1093/rpc/rcn037 .
- ^ «Замещенные бензо(ij)хинолизин-2-карбоновые кислоты и их производные - Патент 3896131» . Freepatentsonline.com . Проверено 4 апреля 2010 г.
- ^ Такахаси Х., Хаякава И., Акимото Т. (2003). «[История развития и изменения хинолоновых антибактериальных средств]». Якусигаку Дзасси (на японском языке). 38 (2): 161–179. ПМИД 15143768 .
- ^ Перейти обратно: а б Сирбат Д., Саудакс Э., Уро де Линьи Б., Хаше Э., Абеллан П., Джордж Дж.Л. (1983). «[Серозная отслойка макулы и лечение флумехином (апурон = мочевой антибактериальный препарат). По поводу 2 случаев]». Бюллетень офтальмологического общества Франции (на французском языке). 83 (8–9): 1019–1021. ПМИД 6378414 .
- ^ Перейти обратно: а б Уро де Линьи Б, Сирбат Д, Кесслер М, Трешо П, Шанлио Дж (1984). «[Побочные эффекты флумекина на глаза. 3 случая поражения желтого пятна]». Терапия (на французском языке). 39 (5): 595–600. ПМИД 6506018 .
- ^ Перейти обратно: а б Болл П. (июль 2000 г.). «Поколения хинолонов: естественная история или естественный отбор?» . Журнал антимикробной химиотерапии . 46 (Приложение Т1): 17–24. doi : 10.1093/oxfordjournals.jac.a020889 . ПМИД 10997595 .
- ^ Дюбуа А., Жанбон С., Пиньодель С., Марти-Дабл С. (февраль 1983 г.). «[Иммуноаллергический гепатит, вызванный флумехином]». Gastroenterologie Clinique et Biologique (на французском языке). 7 (2): 217–218. ПМИД 6840466 .
- ^ Перейти обратно: а б Пинцани В., Дженнаро Дж., Пети П., Блайак Дж. П. (1992). «[Анафилактический шок, вызванный флумекином]». Терапия (на французском языке). 47 (5): 440. PMID 1299991 .
- ^ Перейти обратно: а б Марсепойл Т., Блин Ф., Ло Дж.М., Хорел Д'Анкона Ф., Себба Дж.Л. (сентябрь 1985 г.). «[Случай анафилактического шока, вызванного флумехином]». Presse Médicale (на французском языке). 14 (32): 1712. PMID 2932732 .
- ^ «Фторхинолоны. Обзор – Dr.TR RAMANUJAM.MD» . Мединдия.нет . Проверено 4 апреля 2010 г.
- ^ Карбивник С.М., Хиббард Л.Е., Ли Р.Х. и др. (27–28 апреля 2005 г.). Подтверждение наличия остатков оксолиновой кислоты и флумекина в креветках методом жидкостной хроматографии с детектированием тандемной масс-спектрометрии . Наука FDA.
- ^ «Программа соблюдения требований по химиотерапии в морепродуктах: Глава 4: Пестициды и химические загрязнители» (PDF) . Руководство по программе соответствия . Управление по контролю за продуктами и лекарствами США. 7304.018. Архивировано из оригинала (PDF) 7 марта 2011 года.
Остатки обнаружены в соме/басе, креветках, лососе, форели.
- ^ «Комитет экспертов ФАО/ВОЗ по пищевым добавкам, Женева, Швейцария» . Fda.gov. 28 октября 2009 г. Проверено 4 апреля 2010 г.
- ^ «Информационный бюллетень ветеринаров FDA, том XXII, № V, 2007 г.» (PDF) . Управление по контролю за продуктами и лекарствами . Проверено 4 апреля 2010 г.
- ^ «Комитет Кодекса по остаткам ветеринарных лекарственных средств принимает ряд документов на 17-й сессии» . Fda.gov. 28 октября 2009 г. Проверено 4 апреля 2010 г.
- ^ Информация ВОЗ о лекарствах, том. 2, № 3, 1988 г.
- ^ Дрлица К., Чжао X (сентябрь 1997 г.). «ДНК-гираза, топоизомераза IV и 4-хинолоны» . Обзоры микробиологии и молекулярной биологии . 61 (3): 377–392. дои : 10.1128/mmbr.61.3.377-392.1997 . ПМК 232616 . ПМИД 9293187 .
- ^ Робинсон М.Дж., Мартин Б.А., Гутц Т.Д., МакГирк П.Р., Ошерофф Н. (апрель 1992 г.). «Влияние новых фторхинолонов на каталитическую активность эукариотической топоизомеразы II: влияние группы фтора C-8» . Антимикробные средства и химиотерапия . 36 (4): 751–756. дои : 10.1128/aac.36.4.751 . ЧВК 189387 . ПМИД 1323952 .
- ^ Перейти обратно: а б Сисси С., Палумбо М. (ноябрь 2003 г.). «Семейство хинолонов: от антибактериальных до противораковых средств». Современная медицинская химия. Противораковые агенты . 3 (6): 439–450. дои : 10.2174/1568011033482279 . ПМИД 14529452 .
В настоящем обзоре основное внимание уделяется структурным модификациям, ответственным за трансформацию антибактериального средства в противораковое средство. Действительно, отличительной особенностью препаратов на основе хинолоновой структуры является их замечательная способность воздействовать на различные ферменты топоизомеразы II типа. В частности, некоторые конгенеры этого семейства препаратов проявляют высокую активность не только в отношении бактериальных топоизомераз, но и в отношении эукариотических топоизомераз и токсичны для культивируемых клеток млекопитающих и моделей опухолей in vivo.
- ^ Хасси П., Маасс Г., Туммлер Б., Гросс Ф., Шомбург У. (июнь 1986 г.). «Влияние 4-хинолонов и новобиоцина на комплекс ДНК-полимеразы альфа-примазы тимуса теленка, топоизомераз I и II и рост лимфобластов млекопитающих» . Антимикробные средства и химиотерапия . 29 (6): 1073–1078. дои : 10.1128/AAC.29.6.1073 . ПМК 180502 . ПМИД 3015015 .
- ^ Хосоми Дж., Маэда А., Оомори Ю., Ирикура Т., Ёкота Т. (1988). «Мутагенность норфлоксацина и AM-833 в бактериях и клетках млекопитающих». Обзоры инфекционных болезней . 10 (Приложение 1): С148–9. JSTOR 4454399 .
- ^ Форсгрен А., Бредберг А., Парди А.Б., Шлоссман С.Ф., Теддер Т.Ф. (май 1987 г.). «Влияние ципрофлоксацина на биосинтез пиримидиннуклеотидов эукариот и рост клеток» . Антимикробные средства и химиотерапия . 31 (5): 774–779. дои : 10.1128/AAC.31.5.774 . ПМК 174831 . ПМИД 3606077 .
- ^ Гутц Т.Д., Барретт Дж.Ф., Сатклифф Дж.А. (январь 1990 г.). «Ингибирующее действие хинолоновых антибактериальных средств на эукариотические топоизомеразы и родственные тест-системы» . Антимикробные средства и химиотерапия . 34 (1): 8–12. дои : 10.1128/AAC.34.1.8 . ПМК 171510 . ПМИД 2158274 .
- ^ Лоуренс Дж.В., Даркин-Раттрей С., Се Ф., Нимс А.Х., Роу Т.С. (февраль 1993 г.). «4-Хинолоны вызывают избирательную потерю митохондриальной ДНК в клетках мышиной лейкемии L1210». Журнал клеточной биохимии . 51 (2): 165–174. дои : 10.1002/jcb.240510208 . ПМИД 8440750 . S2CID 41291987 .
- ^ Элси С.Х., Ошерофф Н., Нитисс Дж.Л. (июль 1992 г.). «Цитотоксичность хинолонов по отношению к эукариотическим клеткам. Идентификация топоизомеразы II как основной клеточной мишени для хинолона CP-115,953 в дрожжах» . Журнал биологической химии . 267 (19): 13150–13153. дои : 10.1016/S0021-9258(18)42185-0 . ПМИД 1320012 .
- ^ Суто М.Дж., Домагала Дж.М., Роланд Г.Е., Майу Г.Б., Коэн М.А. (декабрь 1992 г.). «Фторхинолоны: взаимосвязь между структурными вариациями, цитотоксичностью клеток млекопитающих и антимикробной активностью». Журнал медицинской химии . 35 (25): 4745–4750. дои : 10.1021/jm00103a013 . ПМИД 1469702 .
- ^ Энцманн Х., Виманн К., Ар Х.Дж., Шлютер Г. (апрель 1999 г.). «Повреждение митохондриальной ДНК, индуцированное хинолоном Bay y 3118 в эмбриональной печени индейки». Мутационные исследования . 425 (2): 213–224. дои : 10.1016/S0027-5107(99)00044-5 . ПМИД 10216214 .
- ^ Кашида Ю., Сасаки Ю.Ф., Осава К., Йокогама Н., Такахаши А., Ватанабэ Т., Мицумори К. (октябрь 2002 г.). «Механистическое исследование гепатоканцерогенности флумекина с упором на повреждение ДНК у мышей» . Токсикологические науки . 69 (2): 317–321. дои : 10.1093/toxsci/69.2.317 . ПМИД 12377980 .
- ^ Томас А., Точер Дж., Эдвардс Д.И. (май 1990 г.). «Электрохимические характеристики пяти хинолоновых препаратов и их влияние на повреждение и репарацию ДНК у Escherichia coli». Журнал антимикробной химиотерапии . 25 (5): 733–744. дои : 10.1093/jac/25.5.733 . ПМИД 2165050 .
- ^ «Фторхинолоны и хинолоны» . Американская академия оптометрии (Британское отделение) . Проверено 29 января 2009 г.
- ^ Аль-Суд Й.А., Аль-Масуди Н.А. (2003). «Новый класс дигалохинолонов, содержащий предшественники N'-альдегидогликозилгидразидов, меркапто-1,2,4-триазола, оксадиазолина и α-аминоэфиров: синтез и антимикробная активность» . Журнал Бразильского химического общества . 14 (5): 790–796. дои : 10.1590/S0103-50532003000500014 .
- ^ Даудон М., Протат М.Ф., Ревейо Р.Ж. (1983). «[Выявление и диагностика лекарственного литиаза]». Annales de Biologie Clinique (на французском языке). 41 (4): 239–249. ПМИД 6139048 .
- ^ Ринсе С., Даудон М., Моеш С., Ринсе М., Леру-Робер С. (май 1987 г.). «Идентификация флумекина в мочевых камнях». Журнал клинической химии и клинической биохимии . 25 (5): 313–314. ПМИД 3612030 .
- ^ Ревейо Р.Дж., Даудон М. (октябрь 1983 г.). «[Лекарственный литиаз мочевых путей]». Presse Médicale (на французском языке). 12 (38): 2389–2392. ПМИД 6138768 .
- ^ Арбуа Ф., Бессо Ж.К., ДеБлей Ф., Дитеманн А., Шарпантье С., Паули Дж. (январь 1997 г.). «Восемь случаев аллергии на хинолоны». Французский журнал аллергологии и клинической иммунологии . 37 (1): 15–19. дои : 10.1016/S0335-7457(97)80204-3 .
- ^ Информационный бюллетень о побочных реакциях 1996: 1. Архивировано 19 февраля 2012 г. в Wayback Machine, Сотрудничающем центре ВОЗ по международному мониторингу лекарственных средств.
- ^ Христос В. (октябрь 1990 г.). «Токсичность хинолонов на центральную нервную систему: данные о людях и животных». Журнал антимикробной химиотерапии . 26 (Приложение Б): 219–225. дои : 10.1093/jac/26.suppl_b.219 . ПМИД 2124211 .
- ^ Дефоин Ж.Ф., Дебонн Т., Рамбург М.О., Серафин Дж., Баффет М., Жоссо М. и др. (1990). «[Острый психиатрический синдром и хинолоны]». Журнал клинической и экспериментальной токсикологии (на французском языке). 10 (7–8): 469–472. ПМИД 2135062 .
- ^ Рампа С., Кэроли Ф (1991). «[Нейропсихические проявления и хинолоны. По поводу случая]». L'Encephale (на французском языке). 17 (6): 511–514. ПМИД 1666873 .
- ^ Вермеерш Г., Филали А., Марко Дж., Катто Дж.П., Кутюр А. (1990). «[Фотофизическая оценка фотосенсибилизации различными хинолонами]». Journal de Pharmacie de Belgique (на французском языке). 45 (5): 299–305. ПМИД 1964964 .
- ^ Ревуз Дж., Пуже Ф. (1983). «[Фотоонихолизис, вызванный апуроном]». Annales de Dermatology et de Venereologie (на французском языке). 110 (9): 765. PMID 6660786 .
- ^ Лакарель Б, Блин О, Одебер С, Окье П, Карсенти Х, Хоррьер Ф, Дюран А (1994). «Хинолон, флумекин, не влияет на фармакокинетику теофиллина». Европейский журнал клинической фармакологии . 46 (5): 477–478. дои : 10.1007/bf00191915 . ПМИД 7957547 . S2CID 97621 .
- ^ «Флумекин (антиотические противомикробные средства) производители и поставщики» . 88chem.com . Проверено 4 апреля 2010 г.
- ^ Фрэнсис П.Г., Уэллс Р.Дж. «Флюмекин» . Пимбл, Австралия: Аналитические лаборатории правительства Австралии.