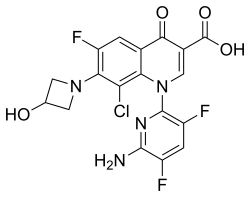
Делафлоксацин
 | |
| Клинические данные | |
|---|---|
| Торговые названия | Баксдела, Куофеникс, Делабакси |
| Другие имена | АБТ-492; RX-3341; WQ-3034 |
| AHFS / Drugs.com | Монография |
| Данные лицензии |
|
| Маршруты администрация | Внутрь , внутривенно. |
| код АТС | |
| Юридический статус | |
| Юридический статус |
|
| Идентификаторы | |
| Номер CAS |
|
| ПабХим CID | |
| Лекарственный Банк | |
| ХимическийПаук | |
| НЕКОТОРЫЙ | |
| КЕГГ | |
| ЧЕМБЛ | |
| Панель управления CompTox ( EPA ) | |
| Химические и физические данные | |
| Формула | С 18 Н 12 Cl F 3 N 4 О 4 |
| Молярная масса | 440.76 g·mol −1 |
| 3D model ( JSmol ) | |
Делафлоксацин, под торговой маркой Baxdela продаваемый, среди прочего, , представляет собой фторхинолоновый антибиотик, используемый для лечения острых бактериальных инфекций кожи и структур кожи . [1]
Медицинское использование
[ редактировать ]Делафлоксацин показан для лечения взрослых с острыми бактериальными инфекциями кожи и структур кожи (ABSSSI), вызванными определенными чувствительными бактериями, или взрослым с внебольничной бактериальной пневмонией (CABP), вызванной определенными чувствительными бактериями. [1]
Восприимчивыми к ABSSSI бактериями являются: [1]
- Грамположительные микроорганизмы: Staphylococcus aureus (включая метициллин-резистентные [MRSA] и метициллин-чувствительные изоляты [MSSA]), Staphylococcus haemolyticus , Staphylococcus lugdunensis , Streptococcus agalactiae , Streptococcus anginosus группу (включая Streptococcus anginosus , Streptococcus intermedius и Streptococcus cons ). теллатус), Streptococcus pyogenes и Enterococcus faecalis.
- Грамотрицательные микроорганизмы: Escherichia coli , Enterobacter cloacae , Klebsiella pneumoniae и Pseudomonas aeruginosa .
Восприимчивыми к CABP бактериями являются: [1] Streptococcus pneumoniae , Staphylococcus aureus (только изоляты, чувствительные к метициллину [MSSA]), Klebsiella pneumoniae , Escherichia coli , Pseudomonas aeruginosa , Haemophilus influenzae , Haemophilus parainfluenzae , Chlamydia pneumoniae , Legionella pneumophila и Mycoplasma pneumoniae .
Он не тестировался на беременных женщинах. [1]
В Европейском Союзе он показан для лечения острых бактериальных инфекций кожи и структур кожи (ABSSSI) у взрослых, когда считается нецелесообразным использование других антибактериальных средств, которые обычно рекомендуются для начального лечения этих инфекций. [2]
Побочные эффекты
[ редактировать ]Как и другие препараты класса фторхинолонов , делафлоксацин содержит предупреждение «черного ящика» о риске тендинита, разрыва сухожилия, периферической нейропатии, эффектов со стороны центральной нервной системы и обострения миастении гравис. Этикетка также предупреждает о риске реакций гиперчувствительности и диареи, связанной с Clostridium difficile . [1]
Побочные эффекты, возникшие у более чем 2% участников клинических исследований, включали тошноту, диарею, головную боль, повышение уровня трансаминаз и рвоту. [1]
Взаимодействия
[ редактировать ]Как и другие фторхинолоны, делафлоксацин хелатирует металлы, включая алюминий, магний, сукральфат, железо, цинк, а также двухвалентные и трехвалентные катионы, такие как диданозин; использование этого препарата с антацидами, некоторыми пищевыми добавками или препаратами, забуференными любым из этих ионов, будет мешать доступному количеству делафлоксацина. [1]
Фармакология
[ редактировать ]Период полувыведения составляет около 8 часов при обычных дозах. Экскреция составляет 65% с мочой, преимущественно в неметаболизированной форме, и 28% с калом. Клиренс снижается у людей с тяжелыми заболеваниями почек. [3]
Делафлоксацин более активен (более низкая МПК90 ), чем другие хинолоны, в отношении грамположительных бактерий, таких как метициллин-резистентный золотистый стафилококк (MRSA). В отличие от большинства одобренных фторхинолонов, которые являются цвиттер-ионными , делафлоксацин имеет анионный характер, что приводит к 10-кратному увеличению накопления делафлоксацина как в бактериях, так и в клетках при кислом pH. Считается, что это свойство дает делафлоксацину преимущество в уничтожении Staphylococcus aureus в кислой среде, включая внутриклеточные инфекции и биопленки. [3]
Химия
[ редактировать ]Химическое название: 1-дезокси-1-(метиламино)-D-глюцит, 1-(6-амино-3,5-дифторпиридин-2-ил)-8-хлор-6-фтор-7-(3-гидроксиазетидин- 1-ил)-4-оксо-1,4-дигидрохинолин-3-карбоксилат (соль). [1]
Инъекционная форма делафлоксацина продается в виде меглюминовой соли активного ингредиента, и это отражается в его принятом в США названии делафлоксацин меглюмин; состав для инъекций также включает ЭДТА и сульфобутиловый эфир-β-циклодекстрин. Таблетка состоит из делафлоксацина, безводной лимонной кислоты, кросповидона, стеарата магния, микрокристаллической целлюлозы, повидона, бикарбоната натрия и одноосновного моногидрата фосфата натрия. [1]
История
[ редактировать ]Делафлоксацин был известен как ABT-492, RX-3341 и WQ-3034, когда он находился в стадии разработки. [4]
Rib-X Pharmaceuticals приобрела делафлоксацин у Wakunaga Pharmaceutical в 2006 году. [5] Rib-X был переименован в Melinta Therapeutics в 2013 году. [6] Он был разработан и продан компанией Melinta Therapeutics (ранее Rib-X Pharmaceuticals). [1] которая впоследствии объединилась с Cempra. [7]
Компания Melinta провела ключевые клинические исследования делафлоксацина в отношении показаний к инфекциям кожи и структур кожи, а также осложненным бактериальным инфекциям и неосложненной гонорее. Испытание гонореи было прекращено до публикации данных. [8]
Делафлоксацин был одобрен FDA в июне 2017 года после того, как он не уступил ванкомицину плюс азтреонаму в двух исследованиях на 1042 пациентах с острой бактериальной инфекцией кожи и структур кожи. [9] Новые заявки на лекарства (NDA) для делафлоксацина (Baxdela) в таблетках по 450 мг и инъекциях по 300 мг были одобрены FDA в июне 2017 года. [10]
FDA обязало Melinta провести следующие исследования: [10]
- 5-летнее эпиднадзорное исследование для определения появления резистентности, окончательный отчет должен быть представлен в декабре 2022 г.
- исследование IV формы у беременных крыс для определения распространения в репродуктивном тракте, запланированное на июнь 2018 г., при этом в случае значительного распространения потребуются дальнейшие исследования.
Melinta объединилась с Cempra в августе 2017 года. [7]
Компания Melinta заключила соглашения о коммерциализации и распространении делафлоксацина как с Menarini Therapeutics (март 2017 г.), так и с Eurofarma Laboratorios (январь 2015 г.). Соглашение с Menarini позволяет им коммерциализировать и распространять продукцию в 68 странах, включая Европу, Китай и Южную Корею. Аналогичное соглашение с Eurofarma допускает коммерциализацию в Бразилии. [8]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г час я дж к «Бакдела-делафлоксацин меглумин таблетка Баксдела-делафлоксацин меглумин для инъекций, порошок, лиофилизированный, для приготовления раствора» . ДейлиМед . 12 февраля 2020 г. Проверено 12 мая 2020 г.
- ^ «Куофеникс ЭПАР» . Европейское агентство лекарственных средств (EMA) . 16 октября 2019 г. Проверено 12 мая 2020 г.
 В данную статью включен текст из этого источника, находящегося в свободном доступе .
В данную статью включен текст из этого источника, находящегося в свободном доступе . - ^ Jump up to: а б Кандел Ф.Дж., Пенуэлас М. (2017). «Делафлоксацин: дизайн, разработка и потенциальное место в терапии» . Дизайн, разработка и терапия лекарств . 11 : 881–891. дои : 10.2147/DDDT.S106071 . ПМЦ 5367733 . ПМИД 28356714 .
- ^ «Делафлоксацин» . АдисИнсайт . Проверено 10 июля 2017 г.
- ^ Картрайт Х. (12 июля 2011 г.). «Rib-X Pharmaceuticals подписывает соглашение о глобальном сотрудничестве в области исследований антибиотиков с Sanofi» . Обзор PharmaDeals . № 7. doi : 10.3833/pdr.v2011i7.1494 (неактивен 31 января 2024 г.). Архивировано из оригинала 25 апреля 2012 года.
{{cite news}}: CS1 maint: DOI неактивен по состоянию на январь 2024 г. ( ссылка ) - ^ Стернс Дж. (1 августа 2016 г.). «Melinta Therapeutics нацелена на смертельные бактерии, устойчивые к лекарствам» . Хартфордский деловой журнал .
- ^ Jump up to: а б «Cempra и Melinta объявляют о слиянии с целью создания ведущей вертикально интегрированной коммерческой компании по производству противоинфекционных препаратов» (пресс-релиз). Мелинта Терапевтикс. 9 августа 2017 года . Проверено 24 ноября 2022 г. - через GlobeNewswire.
- ^ Jump up to: а б Маркхэм А. (сентябрь 2017 г.). «Делафлоксацин: первое глобальное одобрение» . Наркотики . 77 (13): 1481–1486. дои : 10.1007/s40265-017-0790-5 . ПМК 6208769 . ПМИД 28748399 .
- ^ Осборн Р. (20 июня 2017 г.). «Пероральный препарат Мелинты для внутривенного введения делафлоксацина получил одобрение FDA при лечении кожных инфекций» . Биомир . Архивировано из оригинала 3 августа 2019 года . Проверено 10 июля 2017 г.
- ^ Jump up to: а б «Письмо об утверждении NDA: NDA 208610 и NDA 208611» (PDF) . FDA. 19 июня 2017 г.
Внешние ссылки
[ редактировать ]- «Делафлоксацин» . Информационный портал о наркотиках . Национальная медицинская библиотека США.
- «Делафлоксацин меглюмин» . Информационный портал о наркотиках . Национальная медицинская библиотека США.