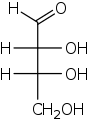
Тетроза
В органической химии тетроза — моносахарид . с 4 углерода атомами У них либо альдегид ( −CH=O ) функциональная группа в положении 1 ( альдотетрозы ) или кетон ( >C=O ) группа в положении 2 ( кетотетрозы ). [1] [2]
- D -Эритроза
- D -Троуз
- D -Эритрулоза
Альдотетрозы имеют два хиральных центра ( асимметричные атомы углерода 4 различных стереоизомера ), поэтому возможны . Существует два встречающихся в природе стереоизомера: энантиомеры эритрозы имеющие и треозы, D - конфигурацию , но не L- энантиомеры. Кетотетрозы имеют один хиральный центр и, следовательно, два возможных стереоизомера: эритрулозу ( L- и D -форму). Опять же, только D- в природе встречается энантиомер.
Биологические функции
[ редактировать ]Есть несколько известных способов использования тетрозы в природе. Некоторые из них наблюдаются в метаболических путях, а другие, как известно, влияют на определенные ферменты.
Промежуточные соединения пентозофосфатного пути
[ редактировать ]Одним из метаболических путей, в которых участвует тетроза, является пентозофосфатный путь . [3] Пентозофосфатный путь включает окислительную и неокислительную стадии. [4] Тетрозный сахар, D-эритроза , используется на неокислительной стадии, где D-рибулозо-5-фосфат превращается в 6-углеродный сахар ( фруктозо-6-фосфат ) и 3-углеродный сахар ( глицеральдегид-3-фосфат ). [4] Обе эти молекулы можно использовать в других частях тела.
D-эритрозо-4-фосфат образуется в результате реакции, называемой трансальдолированием. [5] В пентозофосфатном пути трансальдолаза удаляет первые 3 молекулы углерода седогептулозо-7-фосфата и помещает их на глицеральдегид-3-фосфат. [4] Трансальдолаза использует основание Шиффа для осуществления обратной альдольной реакции и прямой альдольной реакции в своем механизме, образуя эритрозо-4-фосфат и фруктозо-6-фосфат . [4] Эритрозо-4-фосфат является важным промежуточным продуктом пентозофосфатного пути, поскольку затем он используется на заключительном неокислительном этапе пути.
Последним неокислительным этапом пути является транскетолазная реакция. Транскетолаза или кофактор использует тиаминпирофосфат TPP, чтобы разорвать неблагоприятную связь между углеродом в карбониле и альфа-углеродом . [4] TPP атакует молекулу ксилулозо-5-фосфата и способствует разрыву связи между C2 (карбонильным углеродом) и C3 (альфа-углеродом), при этом высвобождается глицеральдегид-3-фосфат. [4] Затем C2 может атаковать эритрозо-4-фосфат, который образует фруктозо-6-фосфат. [4] Оба продукта этой реакции могут вступать в путь глюконеогенеза для регенерации глюкозы .
Ингибиторы ферментов
[ редактировать ]Было обнаружено, что молекула тетрозодифосфата, D-треозо-2,4-дифосфата, является ингибитором глицеральдегид-3-фосфатдегидрогеназы . [3] Глицеральдегид-3-фосфатдегидрогеназа является шестым ферментом, используемым в пути гликолиза , и его функция заключается в превращении глицеральдегид-3-фосфата в 1,3-бисфосфоглицерат . [6] Эта молекула тетрозодифосфата ингибирует катализ G3P-дегидрогеназы, поскольку она окисляет фермент, связываясь с ним в активном центре. [7] Когда тетрозодифосфат связывается с ферментом, активный центр фермента блокируется; поэтому фосфоролиз G3P не может произойти. Высокие концентрации тетрозодифосфата необходимо использовать, чтобы превзойти субстрат G3P и блокировать функцию дегидрогеназы G3P. При утрате функции глицеральдегид-3-фосфатдегидрогеназы гликолиз не может продолжаться. [6]
Было обнаружено, что D-эритрозо-4-фосфат является ингибитором фосфоглюкозоизомеразы . [8] Фосфоглюкозоизомераза является вторым ферментом пути гликолиза, и ее роль заключается в превращении глюкозо-6-фосфата во фруктозо-6-фосфат. [6]
В обоих этих случаях тетроза является ингибитором фермента пути гликолиза, препятствуя его дальнейшему развитию.
Ссылки
[ редактировать ]- ^ Линдхорст ТК (2007). Основы химии и биохимии углеводов (1-е изд.). Вайли-ВЧ. ISBN 978-3-527-31528-4 .
- ^ Робит Дж. Ф. (1997). Основы химии углеводов (1-е изд.). Спрингер. ISBN 0-387-94951-8 .
- ^ Jump up to: а б Батт Р.Д., Диккенс Ф., Уильямсон Д.Х. (ноябрь 1960 г.). «Метаболизм тетрозы. 2. Утилизация тетроз и тетритолов тканями крысы» . Биохимический журнал . 77 (2): 281–94. дои : 10.1042/bj0770281 . ПМК 1204983 . ПМИД 13687765 .
- ^ Jump up to: а б с д и ж г Гарретт Р.Х., Гришэм К.М. (2017). Биохимия . Бостон, Массачусетс: Cengage Learning. стр. 755–794. ISBN 978-1-305-57720-6 .
- ^ Хорекер Б.Л., Смирниотис П.З., Хиатт Х.Х., Маркс П.А. (февраль 1955 г.). «Тетрозофосфат и образование седогептулозодифосфата» . Журнал биологической химии . 212 (2): 827–36. дои : 10.1016/S0021-9258(18)71021-1 . ПМИД 14353884 .
- ^ Jump up to: а б с Гарретт Р.Х., Гришэм К.М. (2017). Биохимия . Бостон, Массачусетс: Cengage Learning. стр. 611–642. ISBN 978-1-305-57720-6 .
- ^ Ракер Э., Клибас В., Шрамм М. (октябрь 1959 г.). «Тетрозодифосфат, специфический ингибитор глицеральдегид-3-фосфатдегидрогеназы» . Журнал биологической химии . 234 (10): 2510–6. дои : 10.1016/S0021-9258(18)69730-3 . ПМИД 14435686 .
- ^ Граци Э., Де Флора А., Понтремоли С. (февраль 1960 г.). «Ингибирование фосфоглюкозоизомеразы D-эритрозо-4-фосфатом». Связь с биохимическими и биофизическими исследованиями . 2 (2): 121–5. дои : 10.1016/0006-291X(60)90201-1 .