УГТ2Б7
| УГТ2Б7 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Идентификаторы | |||||||||||||||||||||||||||||||||||||||||||||||||||
| Псевдонимы | UGT2B7 , UDPGT 2B9, UDPGT2B7, UDPGTH2, UGT2B9, член B7 семейства 2 глюкуронозилтрансфераз UDP, UDPGT 2B7, UDPGTh-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| Внешние идентификаторы | Опустить : 600068 ; МГИ : 3576103 ; Гомологен : 128251 ; Генные карты : UGT2B7 ; ОМА : UGT2B7 — ортологи | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| Викиданные | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
UGT2B7 (UDP-глюкуронозилтрансфераза-2B7) представляет собой метаболизма изофермент II фазы , который, как обнаружено, активен в печени , почках , эпителиальных клетках нижних отделов желудочно-кишечного тракта , а также в головном мозге . У человека УДФ-глюкуронозилтрансфераза-2В7 кодируется UGT2B7 геном . [ 5 ] [ 6 ]
Функция
[ редактировать ]UGT играют важную роль в конъюгации и последующем удалении потенциально токсичных ксенобиотиков и эндогенных соединений. UGT2B7 обладает уникальной специфичностью в отношении 3,4- катехиновых эстрогенов и эстриола , что позволяет предположить, что он может играть важную роль в регуляции уровня и активности этих мощных метаболитов эстрогена.
Этот фермент расположен на эндоплазматическом ретикулуме и ядерных мембранах клеток. Его функция — катализировать конъюгацию широкого спектра липофильных агликоновых субстратов с глюкуроновой кислотой с использованием уридиндифосфатглюкуроновой кислоты .
Вместе с UGT2B4 UGT2B7 способен глюкозидировать гиодезоксихолевую кислоту в печени, но, в отличие от изоформы 2B4, 2B7 способен также глюкуронидировать различные стероидные гормоны ( андростерон , эпитестостерон ) и жирные кислоты . [ 7 ] [ 8 ] Он также способен конъюгировать основные классы лекарств, таких как анальгетики ( морфин ), карбоновые нестероидные противовоспалительные препараты ( кетопрофен ) и антиканцерогены ( полностью транс- ретиноевая кислота ). [ 8 ] UGT2B7 является основной изоформой фермента, ответственной за метаболизм морфина , кодеина , норкодеина и других опиатов до соответствующих им 3- и 6-глюкуронидов. Например, в результате метаболизма морфина образуется морфин-3-глюкуронид (M3G), который не оказывает анальгезирующего эффекта, и морфин-6-глюкуронид (M6G). [ 9 ] который оказывает более сильное обезболивающее действие, чем морфин. [ 10 ] Как следствие, измененная активность UGT2B7 может существенно влиять как на эффективность, так и на побочные эффекты морфина, а также некоторых родственных опиатных препаратов. [ 11 ] [ 12 ] [ 13 ] [ 14 ] [ 15 ]
Структура
[ редактировать ]
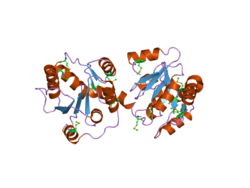
Структура полноценного фермента UGT человека еще не определена, однако Miley et al. разрешили частичную структуру C-концевой части UGT2B7, показывающую два димерных домена со складками, подобными Россману, в комплексе. [ 16 ] [ 17 ] Складка Россмана обычно связывает нуклеотидные субстраты, в данном случае кофактор UDP-глюкуроновой кислоты , участвующий в глюкуронидации с помощью UGT2B7. Как правило, С-конец ферментов UGT высококонсервативен и связывает кофактор UDP-глюкуроновой кислоты, тогда как N-конец (не разрешенный в этой структуре) отвечает за связывание субстрата. [ 18 ] Эта первая разрешенная структура указывала на то, что С-конец одного из двух димеров проецировался в сайт связывания УДФ-глюкуроновой кислоты второго димера, что делало второй димер неэффективным.
Дальнейшие исследования изучали димеризацию полиморфизмов ферментов UGT и обнаружили, что возможно образование как гомодимеров, так и гетеродимеров (с генетическим полиморфизмом UGT2B7 или других ферментов UGT, таких как UGT1A1), при этом некоторые комбинации оказывают влияние на активность фермента. [ 19 ]
Генетический полиморфизм
[ редактировать ]UGT2B7 считается высокополиморфным геном. [ 19 ] Различные исследовательские усилия изучали потенциальное влияние этих полиморфных вариантов на глюкуронидирующую активность UGT2B7 и особенно на его клиренс от вводимых лекарств , включая противораковую терапию. Снижение активности глюкуронирования генетическим вариантом UGT2B7 может привести к повышенной токсичности из-за повышенных уровней препарата, остающихся или накапливающихся в органах пациента, особенно в печени, тогда как повышенная активность может означать более низкую эффективность назначаемой терапии из-за более низких, чем ожидалось, уровней в организме.
Одно исследование показало, что рабочие ханьской красильной промышленности, подвергавшиеся воздействию бензидина, подвергались более высокому риску развития рака мочевого пузыря UGT2B7 C802T, кодирующий His268Tyr. , если у них был однонуклеотидный полиморфизм (SNP) [ 20 ] Мутация гистидина на тирозин в остатке 268 расположена в N-концевой части UGT2B7, которая связывает субстрат ксенобиотика, в отличие от C-конца, который связывает UDP-глюкуроновую кислоту. Предполагаемый механизм повышенного риска рака заключался в усилении глюкуронидации бензидина мутантом UGT2B7 с последующим расщеплением глюкуронидированного бензидина при уровнях pH мочи, высвобождая более высокие концентрации бензидина в мочевом пузыре. Другое исследование искало аналогичную связь варианта UGT2B7 G900A с риском колоректального рака , но не обнаружило значимой связи. [ 21 ]
Исследование клиренса эрлотиниба у пациентов с немелкоклеточным раком легких не выявило статистической значимости для SNP UGT2B7, который потенциально метаболизирует эрлотиниб, о чем свидетельствует ингибирование эрлотинибом UGT2B7. [ 22 ] Исследование клиренса диклофенака , нестероидного противовоспалительного препарата (НПВП), который может вызвать серьезное лекарственное повреждение печени , показало, что мутантный UGT2B7 с SNP C802T имел в 6 раз более низкий клиренс диклофенака, чем дикого типа UGT2B7 . возможно, способствуя повышению токсичности для печени у пациентов с этой мутацией. [ 23 ] Анализ генетического полиморфизма UGT2B7 при противотуберкулезном лекарственном повреждении печени (ATLI) не выявил связи между мутациями UGT2B7 и ATLI в исследуемой популяции. [ 24 ]
Также известно, что UGT2B7 участвует в метаболизме опиоидов посредством глюкуронидации, а исследование, изучающее влияние полиморфизмов на анальгетическую эффективность бупренорфина, показало, что мутация C802T значительно ухудшает обезболивающий ответ на бупренорфин после торакальной хирургии , особенно в более длительные сроки. точки (48 часов), в которых этот опиоид длительного действия должен оставаться эффективным. [ 25 ] Отдельно было обнаружено, что этот же вариант оказывает значительное влияние на в плазме крови концентрацию вальпроевой кислоты , назначаемой пациентам с эпилепсией , что может объяснять некоторую индивидуальную вариабельность, наблюдаемую при этом лечении с узким терапевтическим окном . [ 26 ] Оба этих случая указывают на снижение концентрации лекарственного соединения, вероятно, из-за повышенной глюкуронидирующей активности UGT2B7 с полиморфизмом C802T.

Поскольку UGT2B7 участвует в глюкуронидации многих ксенобиотических соединений, а полиморфизмы UGT2B7 преобладают, изучение потенциальных эффектов полиморфизма UGT2B7 на клиренс фармакологически значимых соединений часто представляет интерес, о чем свидетельствует разнообразие проведенных исследований. Например, полиморфизм C802T UGT2B7 был отмечен с распространенностью 73% у азиатов и 46% у представителей европеоидной расы; следовательно, эффекты этого полиморфизма могут повлиять на большую часть населения. [ 27 ] Однако не все исследования обнаруживают значительные изменения клиренса из-за этих генетических полиморфизмов. Не всегда ясно, связано ли это с особым полиморфизмом, не влияющим на ферментативную активность UGT2B7, или с тем, что интересующее соединение метаболизируется различными путями, которые могут маскировать любые различия, обусловленные изменениями активности UGT2B7.
Ссылки
[ редактировать ]- ^ Jump up to: а б с GRCh38: Версия Ensembl 89: ENSG00000171234 – Ensembl , май 2017 г.
- ^ Jump up to: а б с GRCm38: выпуск Ensembl 89: ENSMUSG00000070704 – Ensembl , май 2017 г.
- ^ «Ссылка на Human PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ «Ссылка на Mouse PubMed:» . Национальный центр биотехнологической информации, Национальная медицинская библиотека США .
- ^ Риттер Дж.К., Шин Ю.Ю., Оуэнс И.С. (май 1990 г.). «Клонирование и экспрессия УДФ-глюкуронозилтрансферазы печени человека в клетках COS-1. 3,4-катехиновые эстрогены и эстриол в качестве основных субстратов» . Журнал биологической химии . 265 (14): 7900–6. дои : 10.1016/S0021-9258(19)39016-7 . ПМИД 2159463 .
- ^ Монаган Г., Кларк Д.Дж., Пови С., См. К.Г., Боксер М., Берчелл Б. (сентябрь 1994 г.). «Выделение контига YAC человека, включающего кластер генов UGT2, и его региональная локализация на хромосоме 4q13». Геномика . 23 (2): 496–9. дои : 10.1006/geno.1994.1531 . ПМИД 7835904 .
- ^ Маккензи П., Литтл Дж. М., Радоминска-Пандья А. (февраль 2003 г.). «Глюкозидирование гидезоксихолевой кислоты УДФ-глюкуронозилтрансферазой 2B7». Биохимическая фармакология . 65 (3): 417–21. дои : 10.1016/S0006-2952(02)01522-8 . ПМИД 12527334 .
- ^ Jump up to: а б Барре Л., Фурнель-Жигле С., Финель М., Неттер П., Магдалу Дж., Уззин М. (март 2007 г.). «Субстратная специфичность человеческих UDP-глюкуронозилтрансфераз UGT2B4 и UGT2B7. Идентификация критического остатка ароматической аминокислоты в положении 33» . Журнал ФЭБС . 274 (5): 1256–64. дои : 10.1111/j.1742-4658.2007.05670.x . ПМИД 17263731 . S2CID 27151203 .
- ^ Коффман Б.Л., Риос Г.Р., Кинг К.Д., Тефли Т.Р. (январь 1997 г.). «Человеческий UGT2B7 катализирует глюкуронидацию морфина» . Метаболизм и распределение лекарств . 25 (1): 1–4. ПМИД 9010622 .
- ^ ван Дорп Э.Л., Ромберг Р., Сартон Э., Бовилл Дж.Г., Дахан А. (июнь 2006 г.). «Морфин-6-глюкуронид: преемник морфина для облегчения послеоперационной боли?» . Анестезия и анальгезия . 102 (6): 1789–97. дои : 10.1213/01.ane.0000217197.96784.c3 . ПМИД 16717327 . S2CID 18890026 .
- ^ Коллер Дж.К., Криструп Л.Л., Сомоджи А.А. (февраль 2009 г.). «Роль активных метаболитов в употреблении опиоидов». Европейский журнал клинической фармакологии . 65 (2): 121–39. дои : 10.1007/s00228-008-0570-y . ПМИД 18958460 . S2CID 9977741 .
- ^ Фудзита К, Андо Ю, Ямамото Ж, Мия Т, Эндо Х, Сунакава Ю, Араки К, Кодама К, Нагасима Ф, Итикава Ж, Нарабаяси М, Акияма Ю, Кавара К, Сиоми М, Огата Х, Иваса Х, Окадзаки Ю , Хиросе Т., Сасаки Ю (январь 2010 г.). «Связь генотипов UGT2B7 и ABCB1 с побочными реакциями на лекарства, вызванными морфином, у японских больных раком». Химиотерапия и фармакология рака . 65 (2): 251–8. дои : 10.1007/s00280-009-1029-2 . ПМИД 19466410 . S2CID 2712957 .
- ^ Абильдсков К., Уэлди П., Гарланд М. (апрель 2010 г.). «Молекулярное клонирование семейства генов УДФ-глюкуронозилтрансферазы 2B павиана и их активность в конъюгации морфина» . Метаболизм и распределение лекарств . 38 (4): 545–53. дои : 10.1124/dmd.109.030635 . ПМЦ 2845934 . ПМИД 20071451 .
- ^ Перголицци СП, Раффа РБ, Гулд Э (сентябрь 2009 г.). «Соображения по использованию оксиморфона у гериатрических пациентов». Экспертное заключение о безопасности лекарственных средств . 8 (5): 603–13. дои : 10.1517/14740330903153854 . ПМИД 19614559 . S2CID 12446624 .
- ^ Ругье К., Пикард Н., Соваж Ф.Л., Голье Ж.М., Марке П. (январь 2010 г.). «Вклад различных изоформ УДФ-глюкуронозилтрансферазы (УГТ) в метаболизм бупренорфина и норбупренорфина и связь с основными полиморфизмами УГТ в банке микросом печени человека». Метаболизм и распределение лекарств . 38 (1): 40–5. дои : 10.1124/dmd.109.029546 . ПМИД 19841060 . S2CID 17826299 .
- ^ Лампе Дж. Н. (2017). «Достижения в понимании белок-белковых взаимодействий в ферментах, метаболизирующих лекарства, с помощью биофизических методов» . Границы в фармакологии . 8 : 521. дои : 10.3389/fphar.2017.00521 . ПМК 5550701 . ПМИД 28848438 .
- ^ Майли М.Дж., Зелинска А.К., Кинан Дж.Э., Брэттон С.М., Радоминска-Пандья А., Рединбо М.Р. (июнь 2007 г.). «Кристаллическая структура кофактор-связывающего домена человеческого фермента фазы II метаболизма лекарств UDP-глюкуронозилтрансферазы 2B7» . Журнал молекулярной биологии . 369 (2): 498–511. дои : 10.1016/j.jmb.2007.03.066 . ЧВК 1976284 . ПМИД 17442341 .
- ^ Юань Л., Цянь С., Сяо Ю., Сунь Х., Цзэн С. (май 2015 г.). «Гомо- и гетеродимеризация человеческой UDP-глюкуронозилтрансферазы 2B7 (UGT2B7) дикого типа и ее аллельных вариантов влияют на активность глюкуронидации зидовудина». Биохимическая фармакология . 95 (1): 58–70. дои : 10.1016/j.bcp.2015.03.002 . ПМИД 25770680 .
- ^ Jump up to: а б Юань Л.М., Гао З.З., Сунь ХИ, Цянь С.Н., Сяо Ю.С., Сунь Л.Л., Цзэн С. (ноябрь 2016 г.). «Межизоформная гетеродимеризация человеческих UDP-глюкуронозилтрансфераз (UGT) 1A1, 1A9 и 2B7 и влияние на активность глюкуронидации» . Научные отчеты . 6 : 34450. Бибкод : 2016NatSR...634450Y . дои : 10.1038/srep34450 . ПМК 5114717 . ПМИД 27857056 .
- ^ Линь Г.Ф., Го В.К., Чен Дж.Г., Цинь Ю.К., Голка К., Сян К.К., Ма Ц.В., Лу Д.Р., Шен Дж.Х. (май 2005 г.). «Связь полиморфизма UDP-глюкуронозилтрансферазы 2B7 C802T (His268Tyr) с раком мочевого пузыря у рабочих, подвергшихся воздействию бензидина в Китае» . Токсикологические науки . 85 (1): 502–6. дои : 10.1093/toxsci/kfi068 . ПМИД 15615884 .
- ^ Фальковски С., Войлард Ж.Б., Постил Д., Тубиана-Матье Н., Терребонн Е., Парьенте А., Смит Д., Гимбо Р., Таламас С., Ругье-Малки К., Марке П., Пикард Н. (декабрь 2017 г.). «Распространенные варианты ферментов глюкуронидации и мембранных переносчиков как потенциальные факторы риска колоректального рака: исследование случай-контроль» . БМК Рак . 17 (1): 901. дои : 10.1186/s12885-017-3728-0 . ПМЦ 5745594 . ПМИД 29282011 .
- ^ Эндо-Цукудэ С, Сасаки Дзи, Саеки С, Ивамото Н, Инаба М, Ушидзима С, Киши Х, Фуджи С, Семба Х, Касивабара К, Цубата Ю, Хаяши М, Кай Ю, Сайто Х, Исобе Т, Кохроги Х, Хамада А (01 января 2018 г.). «Популяционная фармакокинетика и побочные эффекты эрлотиниба у японских пациентов с немелкоклеточным раком легких: влияние генетических полиморфизмов на метаболизирующие ферменты и переносчики» . Биологический и фармацевтический вестник . 41 (1): 47–56. дои : 10.1248/bpb.b17-00521 . ПМИД 29311482 .
- ^ Лазарска К.Э., Деккер С.Дж., Вермюлен Н.П., Командор Ю.Н. (март 2018 г.). «Влияние полиморфизмов UGT2B7*2 и CYP2C8*4 на метаболизм диклофенака» . Письма по токсикологии . 284 : 70–78. дои : 10.1016/j.toxlet.2017.11.038 . ПМИД 29203276 .
- ^ Чэнь Г, Ву С.К., Фэн М., Ван Ю, Ву Дж.К., Цзи Г.И., Чжан М.М., Лю QQ, Хэ JQ (декабрь 2017 г.). «Связь полиморфизмов UGT2B7 с риском поражения печени противотуберкулезными препаратами у китайских хань» . Международный журнал иммунопатологии и фармакологии . 30 (4): 434–438. дои : 10.1177/0394632017733638 . ПМЦ 5806809 . ПМИД 28934901 .
- ^ Састре Х.А., Варела Г., Лопес М., Мюриэль С., Гонсалес-Сармиенто Р. (январь 2015 г.). «Влияние вариантов уридиндифосфат-глюкуронилтрансферазы 2B7 (UGT2B7) на послеоперационную аналгезию бупренорфином». Болевая практика . 15 (1): 22–30. дои : 10.1111/папр.12152 . ПМИД 24256307 . S2CID 33996517 .
- ^ Сунь YX, Чжо WY, Линь Х, Пэн ZK, Ван HM, Хуан HW, Луо YH, Тан FQ (август 2015 г.). «Влияние генотипа UGT2B7 на фармакокинетику вальпроевой кислоты у китайских пациентов с эпилепсией». Исследования эпилепсии . 114 : 78–80. doi : 10.1016/j.eplepsyres.2015.04.015 . ПМИД 26088889 . S2CID 39744204 .
- ^ Лампе Дж.В., Биглер Дж., Буш А.К., Поттер Дж.Д. (март 2000 г.). «Распространенность полиморфизмов в семействе UDP-глюкуронозилтрансферазы человека 2B: UGT2B4 (D458E), UGT2B7 (H268Y) и UGT2B15 (D85Y)». Эпидемиология рака, биомаркеры и профилактика . 9 (3): 329–33. ПМИД 10750673 .
Дальнейшее чтение
[ редактировать ]- Квара А., Ларти М., Боама И., Резк Н.Л., Оливер-Комми Дж., Кену Э., Кашуба А.Д., Корт М.Х. (сентябрь 2009 г.). «Межиндивидуальная вариабельность фармакокинетики генерических нуклеозидных ингибиторов обратной транскриптазы у пациентов из Ганы с коинфекцией ТБ/ВИЧ: UGT2B7*1c связан с более быстрым клиренсом зидовудина и глюкуронидацией» . Журнал клинической фармакологии . 49 (9): 1079–90. дои : 10.1177/0091270009338482 . ПМК 2749505 . ПМИД 19628728 .
- Хван М.С., Ли С.Дж., Чон Х.Э., Ли С., Ю М.А., Шин Дж.Г. (2010). «Генетические вариации гена УДФ-глюкуронозилтрансферазы 2B7 (UGT2B7) в корейской популяции». Метаболизм лекарственных средств и фармакокинетика . 25 (4): 398–402. doi : 10.2133/dmpk.DMPK-10-SC-021 . ПМИД 20814162 .
- Роуз Дж.Э., Бем Ф.М., Дргон Т., Джонсон С., Уль Г.Р. (2010). «Персонализированное прекращение курения: взаимодействие между дозой никотина, зависимостью и оценкой генотипа успеха в отказе от курения» . Молекулярная медицина . 16 (7–8): 247–53. дои : 10.2119/molmed.2009.00159 . ПМЦ 2896464 . ПМИД 20379614 .
- Холмс М.В., Шах Т., Викери С., Смит Л., Хингорани А.Д., Касас Дж.П. (декабрь 2009 г.). «Выполнение обещаний персонализированной медицины? Систематический обзор и полевой обзор фармакогенетических исследований» . ПЛОС ОДИН . 4 (12): е7960. Бибкод : 2009PLoSO...4.7960H . дои : 10.1371/journal.pone.0007960 . ПМЦ 2778625 . ПМИД 19956635 .
- Квара А., Ларти М., Саго К.В., Кену Э., Корт М.Х. (октябрь 2009 г.). «Генетические полиморфизмы CYP2B6, CYP2A6 и UGT2B7 являются предикторами концентрации средней дозы эфавиренца у ВИЧ-инфицированных пациентов» . СПИД . 23 (16): 2101–6. дои : 10.1097/QAD.0b013e3283319908 . ПМЦ 2875867 . ПМИД 19779319 .
- Сетлур С.Р., Чен С.Х., Хоссейн Р.Р., Ха Дж.С., Ван Дорен В.Е., Стензель Б., Штайнер Е., Олдридж Д., Китабаяши Н., Банерджи С., Чен Ю.Й., Шефер Г., Хорнингер В., Ли С., Рубин М.А., Клокер Х., Демикелис Ф (январь 2010 г.). «Генетическая вариация генов, участвующих в метаболизме дигидротестостерона, и риск рака простаты» (PDF) . Эпидемиология рака, биомаркеры и профилактика . 19 (1): 229–39. doi : 10.1158/1055-9965.EPI-09-1018 . ПМИД 20056642 . S2CID 11725521 .
- Санчес МБ, Эрранс Х.Л., Лено С., Артеага Р., Отерино А., Валдисан Э.М., Николас Х.М., Адин Х., Армихо Х.А. (март 2010 г.). «Генетические факторы, связанные с лекарственной устойчивостью эпилепсии: актуальность возрастной стратификации пациентов и этология эпилепсии» . Захват . 19 (2): 93–101. дои : 10.1016/j.seizure.2009.12.004 . ПМИД 20064729 . S2CID 17525536 .
- Чен М., Ледюк Б., Керр С., Хоу Д., Уильямс Д.А. (март 2010 г.). «Идентификация человеческого UGT2B7 как основной изоформы, участвующей в O-глюкуронидации хлорамфеникола». Метаболизм и распределение лекарств . 38 (3): 368–75. дои : 10.1124/dmd.109.029900 . ПМИД 20008037 . S2CID 10438280 .
- Росс С.Дж., Кацов-Экерт Х., Дубе М.П., Брукс Б., Рассех С.Р., Бархдади А., Фероз-Зада Ю., Вишер Х., Браун А.М., Ридер М.Дж., Роджерс П.С., Филлипс М.С., Карлтон Б.С., Хайден М.Р. (декабрь 2009 г.). «Генетические варианты ТПМТ и КОМТ связаны с потерей слуха у детей, получающих химиотерапию цисплатином». Природная генетика . 41 (12): 1345–9. дои : 10.1038/ng.478 . ПМИД 19898482 . S2CID 21293339 .
- Тан Л, Йе Л, Сингх Р, Ву Б, Лев С, Чжао Дж, Лю З, Ху М (июнь 2010 г.). «Использование дактилоскопии глюкуронидации для описания и прогнозирования метаболизма моно- и дигидроксифлавонов с помощью рекомбинантных изоформ UGT и микросом кишечника и печени человека» . Молекулярная фармацевтика . 7 (3): 664–79. дои : 10.1021/mp900223c . ПМЦ 2941766 . ПМИД 20297805 .
- Войлард Дж.Б., Реролл Дж.П., Пикард Н., Руссо А., Друэ М., Мунтяну Э., Эссиг М., Марке П., Ле Мёр И. (июнь 2010 г.). «Риск диареи в долгосрочной когорте пациентов с трансплантацией почки, получающих микофенолата мофетил: значительная роль аллели варианта UGT1A8 2» . Британский журнал клинической фармакологии . 69 (6): 675–83. дои : 10.1111/j.1365-2125.2010.03625.x . ПМЦ 2883760 . ПМИД 20565459 .
- Ю Л, Цянь М, Лю Ю, Яо Т, Цзэн С (май 2010 г.). «Стереоселективный метаболизм глюкуронидации пропранолола человеческими УДФ-глюкуронозилтрансферазами 2B7 и 1A9». Хиральность . 22 (4): 456–61. дои : 10.1002/чир.20765 . ПМИД 19644937 .
- Ян Дж.В., Ли П.Х., Хатчинсон IV, Правица В., Шах Т., Мин Д.И. (октябрь 2009 г.). «Генетические полиморфизмы MRP2 и UGT2B7 и желудочно-кишечные симптомы у реципиентов почечного трансплантата, принимающих микофеноловую кислоту». Терапевтический лекарственный мониторинг . 31 (5): 542–8. дои : 10.1097/FTD.0b013e3181b1dd5e . ПМИД 19730281 . S2CID 6454841 .
- Ан Дж., Шумахер Ф.Р., Берндт С.И., Пфайффер Р., Альбанес Д., Андриоле Г.Л., Арданаз Е., Боинг Х., Буэно-де-Мескита Б., Чанок С.Дж., Клавель-Шапелон Ф., Дайвер В.Р., Фейгельсон Х.С., Газиано Х.М., Джованнуччи Е. , Хайман К.А., Хендерсон Б.Е., Гувер Р.Н., Колонел Л.Н., Крафт П., Ма Дж., Ле Маршан Л., Овервад К., Палли Д., Статтин П., Стампфер М., Страм Д.О., Томас Дж., Тун М.Дж., Трэвис Р.К., Трихопулос Д., Виртамо Дж., Вайнштейн С.Дж., Йегер М., Каакс Р., Хантер DJ, Хейс Р.Б. (октябрь 2009 г.). «Локусы количественных признаков, прогнозирующие уровень циркулирующих половых стероидных гормонов у мужчин из Консорциума когорты рака груди и простаты NCI (BPC3)» . Молекулярная генетика человека . 18 (19): 3749–57. дои : 10.1093/hmg/ddp302 . ПМЦ 2742399 . ПМИД 19574343 .
- Ху М, Луи С.С., Мак В.В., Чу Т.Т., Ли В.В., Пун Э.В., Цуй Т.К., Ко Г.Т., Баум Л., Там Л.С., Ли Е.К., Томлинсон Б. (октябрь 2010 г.). «Фармакогенетический анализ липидных реакций на розувастатин у китайских пациентов». Фармакогенетика и геномика . 20 (10): 634–7. дои : 10.1097/FPC.0b013e32833de489 . ПМИД 20679960 . S2CID 3475599 .
- Чжао В., Фахури М., Дешен Г., Русси Г., Брошар К., Ниоде П., Цимаратос М., Андре Ж.Л., Клоарек С., Коша П., Бенсман А., Азуга С., Жак-Эгрэн Е. (ноябрь 2010 г.). «Популяционная фармакокинетика и фармакогенетика микофеноловой кислоты после введения микофенолата мофетила детям, перенесшим трансплантацию почки de novo». Журнал клинической фармакологии . 50 (11): 1280–91. дои : 10.1177/0091270009357429 . ПМИД 20147615 . S2CID 22875166 .
- Бланка Санчес М., Херранс Х.Л., Лено С., Артеага Р., Отерино А., Валдисан Э.М., Николас Х.М., Адин Дж., Шуштариан М., Армихо Х.А. (апрель 2010 г.). «Полиморфизм UGT2B7_-161C>T связан с соотношением концентрации ламотриджина к дозе в многомерном исследовании». Терапевтический лекарственный мониторинг . 32 (2): 177–84. doi : 10.1097/FTD.0b013e3181ceecc6 . hdl : 10261/49808 . ПМИД 20216122 . S2CID 44807993 .
- Йонг М., Шварц С.М., Аткинсон С., Макар К.В., Томас С.С., Ньютон К.М., Айелло Боулз Э.Дж., Холт В.Л., Лейзенринг В.М., Лампе Дж.В. (февраль 2010 г.). «Связь между полиморфизмом ферментов глюкуронидации и сульфатации и маммографической плотностью груди у женщин в пременопаузе в Соединенных Штатах» . Эпидемиология рака, биомаркеры и профилактика . 19 (2): 537–46. doi : 10.1158/1055-9965.EPI-09-0898 . ПМК 2820123 . ПМИД 20142249 .
- Джой М.С., Бойетт Т., Ху Ю, Ван Дж., Ла М., Хоган С.Л., Стюарт П.В., Фальк Р.Дж., Дули М.А., Смит ПК (ноябрь 2010 г.). «Влияние фармакогеномики уридиндифосфатглюкуронозилтрансферазы 2B7 и 1A7 и клинических параметров пациентов на фармакокинетику микофеноловой кислоты в равновесном состоянии при гломерулонефрите» . Европейский журнал клинической фармакологии . 66 (11): 1119–30. дои : 10.1007/s00228-010-0846-x . ПМЦ 3739695 . ПМИД 20567810 .
Внешние ссылки
[ редактировать ]- human+UGT2B7 в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- UGT2B7 + белок, + человек в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)
- «ГТ2Б7» . ФармГКБ . Проверено 13 января 2009 г.



