Сенсорная стимуляционная терапия
Сенсорная стимуляционная терапия ( ССТ ) – это экспериментальная терапия, целью которой является использование механизмов нейронной пластичности для помощи в восстановлении соматосенсорной функции после инсульта или когнитивного старения . Инсульт и когнитивное старение являются хорошо известными источниками когнитивных потерь: первый из них — гибель нейронов , второй — ослабление нейронных связей . SST стимулирует определенное чувство на определенной частоте. Исследования показывают, что этот метод может обратить вспять когнитивное старение на срок до 30 лет и может выборочно улучшить или ухудшить двухточечный порог различения .
История и мотивация
[ редактировать ]По оценкам, к 2025 году 34 миллиона человек в Соединенных Штатах будут страдать деменцией. Поэтому чрезвычайно важно, чтобы мы разработали эффективное лечение для людей с такими симптомами, чтобы либо уменьшить, либо полностью уменьшить деменцию. В современном лечении, не связанном с фармакологическим лечением, психосоциальная терапия является отличным вмешательством. Благодаря психосоциальным методам лечения, таким как массаж, ароматерапия, мультисенсорная стимуляция, музыкальная терапия и ориентация в реальности, лечение деменции и связанных с ней заболеваний стало возможным в менее традиционной, но нефармакологической форме. [1] Когда-то считалось, что мозг практически не меняется и что его функция определяется в молодом возрасте. [2] В соответствии с этим ходом мыслей когнитивные потери в результате инсультов и старения считались невосполнимыми. Функциональная локализация — это теория, которая предполагает, что каждый отдел мозга выполняет определенную функцию и что потеря участка приравнивается к постоянной потере функции. Традиционные модели даже специализируются на полушариях мозга и описывают «художественные и логические отделы мозга». Этот фаталистический взгляд был резко брошен вызов недавней парадигме пластичности мозга .
Под пластичностью мозга понимают способность мозга реструктуризировать себя, формировать новые связи или регулировать силу существующих связей. [3] Современная парадигма позволяет концептуализировать мозг, способный меняться. Различные исследователи используют эту концепцию для разработки новых методов лечения состояний, которые ранее считались постоянными; например, Пол Бах-и-Рита работал над устройствами, которые давали зрение слепым людям и облегчали чувство падения у пациентов, потерявших функцию вестибулярного аппарата .
Было обнаружено, что многие чувства имеют пластическую природу. Было показано, что даже слуховое познание имеет некоторый потенциал для восстановления после инсульта. Недавнее исследование Саркамо и др. показали, что прослушивание музыки и аудиокниг на раннем этапе восстановления после инсульта может привести к улучшению когнитивных функций. [4]
Эта парадигма открыла двери в то, что раньше считалось невозможным; восстановление после инсультов, снижение когнитивного старения.
Гладить
[ редактировать ]
Инсульт может быть вызван несколькими различными ситуациями, но основной результат один и тот же. Приток крови к участку мозга прекращается, что приводит к быстрому истощению кислорода и других питательных веществ в голодающем отделе. Голодный участок мозговой ткани быстро начинает отмирать, что приводит к поражению мозга. В результате поражения прослеживается потеря различных когнитивных функций в зависимости от локализации и площади повреждения. [5]
Пациенты, перенесшие инсульт, часто страдают от мышечной слабости и потери мышечной функции . Наблюдалось некоторое естественное выздоровление, однако тренировки, основанные на достижениях нейробиологии, показали наиболее существенные улучшения. Эти исследовательские методы лечения сосредоточены на повторении основных задач с ограниченными придатками. Обычно обнаруживается, что более интенсивная коррекционная терапия приводит к лучшему восстановлению функции. [6] Исследования с помощью фМРТ и ПЭТ показали, что уже через 3 недели интенсивных программ тренировок наблюдаются статистические различия между экспериментальной группой и контрольной группой с заметным улучшением мышечного контроля. [7] Хотя эти методы открыли двери для улучшения качества жизни пациентов, перенесших инсульт, методы обучения требуют очень много времени и внимания . Это был бы мощный инструмент, если бы можно было найти систему, не требующую огромного внимания.
Когнитивное старение
[ редактировать ]С возрастом многие функции мозга ухудшаются, а некоторые теряются, это называется когнитивным старением. В самых крайних случаях можно подумать о катастрофических последствиях болезни Альцгеймера . Возраст является крупнейшим фактором риска развития болезни Альцгеймера. Однако из-за отсутствия знаний и успешных исследований в этой области мало что известно о темпах клинического ухудшения состояния и атрофии мозга. [1] Это заболевание связано с гибелью нейронов. Однако в более общем плане старение предполагает потерю синаптической силы вместо гибели нейронов. [8] При рассмотрении этой ситуации механизм правильного функционирования мозга все еще присутствует, но находится в беспорядке. Было показано, что дендритов на 46% по сравнению с участниками старшего возраста. у людей старше 50 лет может произойти снижение количества и плотности [9]
Соматосенсорная система
[ редактировать ]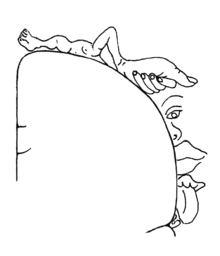
Кортикальный гомункулус, или визуальное представление того, как мозг видит ваше тело, был открыт Уайлдером Пенфилдом . всемирно известный нейрохирург. По окончании карьеры на медицинском факультете Макгилла он занимал должность директора Неврологического института.
Соматосенсорная система — это часть нашей сенсорной системы , отвечающая за осязание. Мы не смогли бы чувствовать температуру, боль, давление, вибрацию и кожную сыпь без непоколебимой помощи нашей соматосенсорной системы. [10] Периферическая нервная система способна воспринимать прикосновение, давление , вибрацию , положение конечностей , тепло , холод и боль . Эта информация передается через периферическую нервную систему в спинной мозг , где она окончательно обрабатывается головным мозгом . Одной из ключевых структур, обрабатывающих эту информацию, является первичная соматосенсорная кора , расположенная в теменной доле . Известно, что первичная соматосенсорная кора имеет подразделы, обрабатывающие информацию из разных отделов, причем площадь коры каждого отдела связана с его остротой зрения. Это наблюдение часто символически демонстрируется через гомункула . [11]
Сенсорная стимуляция
[ редактировать ]Сенсорная стимуляция использует быструю стимуляцию нервов на участке кожи, чтобы вызвать изменения в нейронах участника. Нервы электрически стимулируются способом, называемым коактивацией. [12] [13] В обоих случаях конечность участника, часто рука, фиксируется в устройстве, имеющем секцию, которая применяет стимуляцию. Участнику разрешено заниматься своими повседневными делами, и многие не возражают против наличия устройства. [12] Степень реорганизации часто измеряется с помощью двухточечных порогов дискриминации , которые измеряют наименьшее расстояние между двумя точками, которое может почувствовать субъект.
Было доказано, что использование этой техники может предотвратить потерю чувствительности на срок до 30 лет. [12] В исследовании Dinse et al. 28 пациентов в возрасте от 66 до 86 лет после лечения прошли такое же тестирование, как и участники на 30 лет моложе их самих. Эти участники подключали устройство на 3 часа во время стимуляции. В других исследованиях использовались более короткие периоды стимуляции и были достигнуты аналогичные результаты. [14]
Коактивация
[ редактировать ]Недавнее исследование, опубликованное в «Архивах физической медицины и реабилитации», показало, как четыре пациента выздоравливают после инсульта во время терапии электросенсорной стимуляцией. За их прогрессом следили с помощью нескольких различных тестов; Порог прикосновения, тактильная острота, тактильное распознавание объектов , колышки, помещенные в доску для колышков, и тесты на постукивание двигателем. Было обнаружено, что во время исследования у всех пациентов улучшилась работоспособность. Хотя в этом исследовании используется небольшая выборочная группа и не было контрольной группы, это исследование первого шага, которое предполагает будущие исследования. [13]
На основе этого исследования были разработаны будущие исследования, в которых кожу участников подвергали электрической стимуляции, чтобы вызвать сигналы, посылаемые в мозг.
Частотные исследования
[ редактировать ]В январе 2008 г. Ragert et al. исследовали влияние частоты стимуляции на методы сенсорной стимуляции, вызывающие пластические изменения. В ходе исследования изучалось, можно ли использовать изменение частоты для индукции долгосрочного потенцирования (LTP) или долгосрочной депрессии (LTD). LTP относится к процессам, посредством которых нейронные связи формируются и укрепляются посредством стимуляции и активности. И наоборот, LTD - это процесс, при котором нейронный путь уменьшается из-за низкого уровня стимуляции или из-за неиспользования. [15]
В исследовании Ragert et al. разделили своих участников на две группы, обе из которых прошли SS-терапию, но частота стимуляции в обеих группах была разной. Их анализ показал статистическое улучшение двухточечных тестов на дискриминацию для группы с высокой частотой и статистическое ухудшение того же теста в группе с низкой частотой. [15] Этот результат открывает интересную возможность для будущего этой техники; SS можно использовать не только для восстановления утраченных сенсорных функций, но и для притупления хронической боли .
Активно-зависимая пластическая терапия и сенсорная стимуляция
[ редактировать ]Зависимая от активности пластичность — это явление, при котором нейронные связи изменяются в результате повторяющегося использования. Эту форму пластичности использовали нейрореабилитационные клиники, чтобы помочь тем, кто восстанавливается после инсульта; например, клиника Taub Therapy Clinic использует терапию, вызванную ограничениями. [2] Эта терапия ориентирована на пациентов, перенесших инсульт, с ограниченной функцией конечности. Здоровая конечность пациента ограничивается, и пациенту приходится выполнять физические задачи возрастающей сложности, чтобы вызвать восстановление нейронных сетей.
Американская ассоциация инсульта опубликовала в 2005 году статью Саваки и др. о возможном использовании СС в качестве дополнения к терапии УДП. Они подозревали, что из-за важности соматосенсорной информации в движении усиление сенсорной обработки посредством SS также может улучшить UDP. В их эксперименте участвовали две экспериментальные группы; обеим группам было предложено совершить произвольные движения большим пальцем, а одна группа прошла 20-минутную SS перед направленными движениями большого пальца. Было обнаружено, что участники в паре восстанавливали функции лучше. [14]
Влияние на корковые карты
[ редактировать ]Кортикальные карты — это карты, на которых описаны части нашего мозга, такие как соматосенсорная система. Карты коры нашего мозга связаны не столько с нашими органами чувств, сколько с ощущением физического прикосновения. Установлено, что использование методов интенсивной тренировки можно использовать для увеличения корковых карт у пациентов, восстанавливающихся после инсульта. Исследования с использованием фМРТ и ПЭТ показали, что степень активации моторной коры увеличивается у пациентов, проходящих интенсивную терапию. [16] Это убедительно подтверждает идею о том, что пластические изменения в мозге являются механизмом, с помощью которого может произойти выздоровление.
Иглоукалывание и физиотерапия, улучшающие постуральный контроль
[ редактировать ]Пациенты, перенесшие гемипаретический инсульт [17] часто теряют способность стоять прямо и самостоятельно удерживать осанку. Не имея возможности контролировать свою осанку, мы теряем способность свободно и добровольно передвигаться, что необходимо для повседневной жизнедеятельности (ADL) . Были проведены исследования, чтобы выяснить, может ли сенсорная стимуляция улучшить функциональность после инсульта. В исследовании сравнивались две группы; группа, проходившая стандартную физиотерапию (группа 1), и группа, которой проводилась сенсорная стимуляция с помощью иглоукалывания , физиотерапии и тренировок ADL (группа 2). Обе группы начали исследование в течение десяти дней после первого инсульта. Группа 2 достигла стимуляции с помощью традиционной китайской акупунктуры (10 игл), помещенных в соответствии с традиционными китайскими точками акупунктуры и удерживаемых на месте в течение 30 минут. Наряду с ручной стимуляцией четырем из десяти игл подвергалась также электрическая стимуляция (от 2 до 5 Гц). Лечение продолжалось от четырех до десяти дней, в среднем шесть с половиной дней. Средний возраст двадцати одного пациента из группы 2 составил 74,2 года, а средний возраст группы 1 — 74,8 года. Из пациентов группы 2, у которых можно было провести постуральную запись, у 7 пациентов наблюдалось гемипаретическое поражение слева и у 10 - справа. Из больных 1-й группы у 4 было поражение левой стороны, у 3 — справа. Во время тестирования испытуемые стояли на платформе, сдвинув пятки вместе и скрестив руки на груди. Испытуемые подвергались возмущениям посредством вибрационной стимуляции икроножных мышц, вызывавшей переднезаднее движение, или гальванической стимуляции вестибулярных нервов, вызывавшей боковое движение. Было проведено три различных теста с открытыми и закрытыми глазами пациентов. [18] Результаты исследования показали, что существуют серьезные различия в группе 1 (контрольная группа) и группе 2 (группа лечения). Больше пациентов в экспериментальной группе, чем в контрольной группе, смогли сохранить здоровую позицию во время волнений. Поскольку обе группы лечились от симптомов после инсульта, считалось, что эти нарушения естественным образом улучшат их осанку и двигательные движения. Среди субъектов, которые выжили в течение 2 или более лет после гемипаретического инсульта, группа лечения (группа 2) не имела лучшего постурального контроля. Кроме того, при измерении постурального контроля пациенты, у которых была какая-либо дополнительная сенсорная стимуляция, имели сопоставимые приобретенные значения, приближающиеся к норме для здоровых субъектов того же возраста. Тесты сенсорной стимуляции способствовали, по крайней мере, частичному восстановлению постуральной функции на срок до 2 лет после инсульта и лечения. После тестирования был сделан вывод, что улучшение восстановления после сенсорной стимуляции может быть достигнуто за счет восстановления у пациентов почти нормальной динамики постурального контроля человека. Постуральный контроль является одним из наиболее важных вопросов реабилитации после инсульта, поэтому можно сделать вывод, что сенсорная стимуляция, полученная в результате этого исследования, может повысить функциональную пластичность мозга. [18]
Заключение
[ редактировать ]Терапия сенсорной стимуляции — это развивающаяся методика, направленная на восстановление потери чувствительности после инсульта и восстановления потерь, связанных со старением. Не доказано, что сенсорная стимуляция действительно может улучшить пластичность мозга или когнитивные функции. Парадигма пластичности мозга ознаменовала фундаментальное изменение в понимании мозга и его рассмотрении для будущих методов лечения. [2] SS использует эту парадигму и подвергает чувства простой стимуляции, вызывающей изменения внутри мозга. В этой конкретной ситуации участок кожи стимулируется либо электрическими, либо физическими средствами. Сигналы передаются через периферическую нервную систему в соматосенсорную кору. [12] [13] Эти сигналы затем становятся толчком к изменениям внутри мозга. Было показано, что регулировка частоты в этой технике может использоваться для индукции либо долговременного потенцирования, либо долговременной депрессии. [15] Было показано, что в случае ЛТП 30-летняя потеря чувствительности может быть восстановлена за относительно короткие периоды времени. [12] SS сочетался с системами обучения пластичности, зависящей от использования, и было показано, что такая комбинация обеспечивает более эффективное восстановление. [14] Одним из поразительных преимуществ этой техники является то, что участнику не обязательно обращать внимание на стимул, чтобы получить пользу от терапии. [12] Эта техника открывает много интересных дверей для будущих методов лечения. Потенциальная проблема этой техники заключается в том, что результаты практически не передаются с одного участка кожи на другой.
Было проведено множество исследований, большинство из которых дали положительные выводы, однако необходимо провести дальнейшие исследования сенсорной стимуляции при деменции, чтобы доказать или опровергнуть какие-либо теории. [19]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б Бут, Джонатан; Левин, Винсент; Беверли, Кэтрин; Бейтс, Джейн (2006). «Психосоциальные вмешательства для людей с умеренной и тяжелой деменцией: систематический обзор». Клиническая эффективность в сестринском деле . 9 : е1–е15. дои : 10.1016/j.cein.2006.06.002 . ISSN 1361-9004 .
- ^ Перейти обратно: а б с Норман Дойдж (2007). Мозг, который меняет сам себя: истории личного триумфа с передовых позиций науки о мозге . Нью-Йорк, штат Нью-Йорк: Викинг. ISBN 978-0-670-03830-5 . OCLC 71189897 .
- ^ Чжан Х; Пу ММ (март 2010 г.). «Прогресс в нейронной пластичности». Наука Китай Науки о жизни . 53 (3): 322–9. дои : 10.1007/s11427-010-0062-z . ПМИД 20596926 . S2CID 21508712 .
- ^ Саркямо Т., Пихко Э., Лайтинен С. и др. (декабрь 2010 г.). «Прослушивание музыки и речи ускоряет восстановление ранних сенсорных процессов после инсульта». J Cogn Neurosci . 22 (12): 2716–27. дои : 10.1162/jocn.2009.21376 . ПМИД 19925203 . S2CID 14758688 .
- ^ Халлетт М. (октябрь 2001 г.). «Пластичность моторной коры человека и восстановление после инсульта» . Мозговой Рес. Мозговой Рес. Преподобный . 36 (2–3): 169–74. дои : 10.1016/S0165-0173(01)00092-3 . ПМИД 11690613 . S2CID 15171827 .
- ^ Неллес Дж. (2004). «Корковая реорганизация - эффекты интенсивной терапии». Реставратор. Нейрол. Нейроски . 22 (3–5): 239–44. ПМИД 15502268 .
- ^ Лангхаммер Б; Стангелле Дж. К. (август 2000 г.). «Бобат или программа переобучения моторики? Сравнение двух различных подходов физиотерапии при реабилитации после инсульта: рандомизированное контролируемое исследование». Клин Реабилитация . 14 (4): 361–9. дои : 10.1191/0269215500cr338oa . hdl : 10852/28081 . ПМИД 10945420 . S2CID 42243092 .
- ^ Хоф PR; Моррисон Дж. Х. (октябрь 2004 г.). «Стареющий мозг: морфомолекулярное старение корковых цепей». Тенденции нейробиологии . 27 (10): 607–13. дои : 10.1016/j.tins.2004.07.013 . ПМИД 15374672 . S2CID 31680049 .
- ^ Джейкобс Б; Дрисколл Л; Шалл М. (октябрь 1997 г.). «Изменения дендритов и позвоночника в течение жизни в областях 10 и 18 коры головного мозга человека: количественное исследование Гольджи». Дж. Комп. Нейрол . 386 (4): 661–80. doi : 10.1002/(SICI)1096-9861(19971006)386:4<661::AID-CNE11>3.0.CO;2-N . ПМИД 9378859 . S2CID 25252374 .
- ^ Глевецкас-Мартенс, Н. «Анатомия соматосенсорной системы» . Проверено 13 августа 2012 г.
- ^ Дейл, Эд Первс (2011). Нейронаука . Сандерленд, Массачусетс: Sinauer Associates, Inc. ISBN 978-0-87893-695-3 . OCLC 794367770 .
- ^ Перейти обратно: а б с д и ж Динс HR; Клейбель Н; Калиш Т; Рагерт П; Вилимциг С; Тегентхофф М (июль 2006 г.). «Тактильная коактивация восстанавливает возрастное снижение тактильной дискриминации человека». Энн. Нейрол . 60 (1): 88–94. дои : 10.1002/ana.20862 . ПМИД 16685697 . S2CID 6778931 .
- ^ Перейти обратно: а б с Смит П.С.; Динс HR; Калиш Т; Джонсон М; Уокер-Бэтсон Д. (декабрь 2009 г.). «Эффекты повторяющейся электростимуляции для лечения потери чувствительности у людей после инсульта». Арх Физ Мед Реабилитация . 90 (12): 2108–11. дои : 10.1016/j.apmr.2009.07.017 . ПМИД 19969176 .
- ^ Перейти обратно: а б с Саваки Л; У CW; Кэлин-Ланг А; Коэн Л.Г. (январь 2006 г.). «Влияние соматосенсорной стимуляции на пластичность, зависящую от использования, при хроническом инсульте» . Гладить . 37 (1): 246–7. doi : 10.1161/01.STR.0000195130.16843.ac . ПМИД 16322491 .
- ^ Перейти обратно: а б с Рагерт П; Калиш Т; Блим Б; Францковяк С; Динсе HR (2008). «Дифференциальное влияние тактильной высокочастотной и низкочастотной стимуляции на тактильную дискриминацию у людей» . БМК Неврология . 9 :9. дои : 10.1186/1471-2202-9-9 . ПМК 2244613 . ПМИД 18215277 .

- ^ Тегентофф М., Рагерт П., Плегер Б. и др. (ноябрь 2005 г.). «Улучшение тактильной дискриминации и увеличение кортикальных соматосенсорных карт после рТМС 5 Гц» . ПЛОС Биол . 3 (11): е362. doi : 10.1371/journal.pbio.0030362 . ПМЦ 1255742 . ПМИД 16218766 .

- ^ компакт-диск Такахаси; Рейнкенсмейер DJ (март 2003 г.). «Гемипаретический инсульт ухудшает упреждающий контроль над движением руки». Exp Brain Res . 149 (2): 131–40. дои : 10.1007/s00221-002-1340-1 . ПМИД 12610680 . S2CID 18564943 .
- ^ Перейти обратно: а б Магнуссон М; Йоханссон К; Йоханссон Б.Б. (июнь 1994 г.). «Сенсорная стимуляция способствует нормализации постурального контроля после инсульта» (PDF) . Гладить . 25 (6): 1176–80. дои : 10.1161/01.STR.25.6.1176 . ПМИД 8202976 .
- ^ Кольер Л; Макферсон К; Эллис-Хилл С; Стаал Дж; Бакс Р. (декабрь 2010 г.). «Мультисенсорная стимуляция для улучшения функциональных показателей при умеренной и тяжелой деменции — промежуточные результаты» (PDF) . Am J Alzheimers Dis Other Demen . 25 (8): 698–703. дои : 10.1177/1533317510387582 . ПМИД 21131677 . S2CID 14720189 .