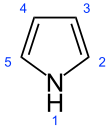
Пиррол
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное имя IUPAC
1 ч -пирроль [ 2 ] | |||
Другие имена
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| 1159 | |||
| Чеби | |||
| Химический | |||
| Chemspider | |||
| Echa Infocard | 100.003.387 | ||
| ЕС номер |
| ||
| 1705 | |||
PubChem CID
|
|||
| Rtecs номер |
| ||
| НЕКОТОРЫЙ | |||
| Номер | 1992, 1993 | ||
Comptox Dashboard ( EPA )
|
|||
| Характеристики | |||
| C 4 H 5 N | |||
| Молярная масса | 67.091 g·mol −1 | ||
| Плотность | 0,967 г см −3 | ||
| Точка плавления | −23 ° C (-9 ° F; 250 К) | ||
| Точка кипения | 129 до 131 ° C (от 264 до 268 ° F; 402 до 404 К) | ||
| Давление паров | 7 мм рт. Ст. При 23 ° C | ||
| Кислотность (p k a ) | 17.5 (для протона N - H) | ||
| Основность (P K B ) | 13,6 (P K A 0,4 для CA ) | ||
| −47.6 × 10 −6 см 3 мол −1 | |||
| Вязкость | 0,001225 Па с | ||
| Термохимия | |||
Теплоемкость ( с )
|
1.903 J K K −1 мол −1 | ||
Энтальпия STD
образование (Δ f h ⦵ 298 ) |
108,2 кДж раз −1 (газ) | ||
Энтальпия STD
сжигание (Δ c h ⦵ 298 ) |
2242 KJ раз −1 | ||
| Опасности | |||
| NFPA 704 (Огненная бриллиант) | |||
| точка возгорания | 33,33 ° C (91,99 ° F; 306,48 К) | ||
| 550 ° C (1022 ° F; 823 K) | |||
| Взрывные пределы | 3.1–14.8% | ||
| Лист данных безопасности (SDS) | Химические данные безопасности | ||
| Связанные соединения | |||
Связанные соединения
|
Фосфол , арсол , бисмоле , привязки | ||
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |||
Пиррола -это гетероциклическое , ароматическое , органическое соединение из пятичленных , кольцо с формулой C 4 H 4 NH . [ 3 ] Это бесцветная нестабильная жидкость, которая легко темнеет при воздействии воздуха. Заменяемые производные также называют пирролами, например, н -метилпиррол, C 4 H 4 NCH 3 . Porphobilinogen , трисубстационный пиррол, является биосинтетическим предшественником многих натуральных продуктов, таких как гем . [ 4 ]
Пирролы представляют собой компоненты более сложных макроциклов, в том числе и полученные из них продукты, включая порфирины гема порфириногены , хлорины , бактериохлорины и хлорофиллы . [ 5 ]
Свойства, структура, связь
[ редактировать ]Пиррола - это бесцветная летучая жидкость, которая легко темнеет при воздействии воздуха и обычно очищается путем дистилляции непосредственно перед использованием. [ 6 ] Пиррол имеет ореховый запах. гетероцикл из 5 человек Пиррол представляет собой ароматический , такой как Фуран и Тиофен . В отличие от Фурана и тиофена, он имеет диполь, в котором положительный конец находится на стороне гетероатома, с дипольным моментом 1,58 дня . В CDCL 3 он имеет химические сдвиги в 6,68 (H2, H5) и 6,22 (H3, H4). Пиррола является чрезвычайно слабым основанием для амина, с конъюгатной кислотой P k a −3,8. Наиболее термодинамически стабильный пирролийский катион (C 4 H 6 N + ) сформируется протонированием на 2 -м положении. Замена пиррола алкильными заместителями обеспечивает более базовую молекулу, например, тетраметилпиррол имеет конъюгатную кислоту P k a +3,7. Пиррола также слабо кислота в положении N - H, с AP K A 16,5. В качестве водородной связи кислоты он классифицируется как твердая кислота , а модель ECW перечисляет его кислотные параметры как e a = 1,38 и C a = 0,68.
Пиррол имеет ароматический характер, потому что пары электронов одинокие на атоме азота частично делокализуются в кольцо, создавая ароматическую систему 4 N + 2 (см. Правило Хюккеля ). С точки зрения его ароматичности, пиррола скромна по сравнению с бензолом , но сопоставим с родственными гетероциклами тиофена и фурана . Резонансные энергии бензола, пиррола, тиофена и фурана , соответственно, 152, 88, 121 и 67 кДж/моль (36, 21, 29 и 16 ккал/моль). [ 7 ] Молекула плоская.
История
[ редактировать ]Пиррол был впервые обнаружен Ф. Ф. Рунге в 1834 году в качестве составляющей угольной смолы . [ 8 ] В 1857 году он был выделен из пиролизата кости . Его название происходит от греческого пирроса ( πυρρός , «красноватый, огненный»), от реакции, используемой для его обнаружения - красного цвета, который он придает древесине при увлажнении со соляной кислотой . [ 9 ]
Появление в природе
[ редактировать ]
Сама пиррола не встречается в природе, но многие из его производных встречаются в различных кофакторах и натуральных продуктах . содержащие пирролы, включают витамин B 12 , желчные пигменты, такие как билирубин и биливердин , а также порфирины гема Обычно естественные продуцируемые молекулы , , хлорофилла , хлоринов , бактериохлоринов и порфириногенов. [ 5 ] Другие пирролевые вторичные метаболиты включают PQQ, Макалувамин М., Райанодин, Рэзинилам, Ламелларин, Продигиозин, Мирмикарин и Скептрин. Синтезы пирролевой гемины, синтезированные Гансом Фишером, были признаны Нобелевской премией.
Пиррола является составляющей табачного дыма и может способствовать его токсическим эффектам. [ 10 ]
Синтез
[ редактировать ]Пиррол готовится в промышленности путем обработки фурана с аммиаком в присутствии твердых кислотных катализаторов , таких как SIO 2 и AL 2 O 3 . [ 9 ]

Пиррол также может быть образована путем каталитического дегидрирования пирролидина. [ Цитация необходима ]
Было описано несколько синтезов пиррольского кольца. [ 11 ] Доминируют три маршрута, [ 12 ] Но существует много других методов.
Синтез Hantzsch Pyrrole
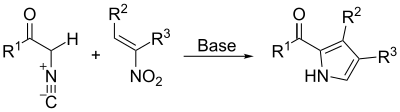
[ редактировать ]Синтез пиррола Ханцша-это реакция β-кетоэфиров ( 1 ) с аммиаком (или первичными аминами) и α-халокетонами ( 2 ), чтобы получить замещенные пирролы ( 3 ). [ 13 ] [ 14 ]

Синтез пиррола Кнорр
[ редактировать ]Синтез пиррола Knorr включает реакцию α-амино кетона или α-амино-β-кететер с активированным метиленовым соединением. [ 15 ] [ 16 ] [ 17 ] Метод включает реакцию α- амино кетона ( 1 ) и соединения, содержащего метиленовую группу α, с (связанным с следующим углеродом) карбонильной группой ( 2 ). [ 18 ]

Паал -Норр Синтез пиррола
[ редактировать ]В синтезе Paal-Knorr Pyrrole, 1,4-дикарбонильное соединение реагирует с аммиаком или первичным амином с образованием замещенного пиррола. [ 19 ] [ 20 ]

Другие методы
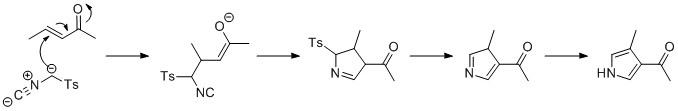
[ редактировать ]Реакция Ван Леузена пирролы продуцируются реакцией тозилметилзоцианида (Tosmic) с enone в присутствии основания, в добавлении Майкла . Затем 5- эндо- циклизация образует 5-членнее кольцо, которое реагирует на устранение тозильной группы. Последним шагом является таутомеризация к пирроле. [ Цитация необходима ]
Благодаря синтезу Бартон-Зарда изоцианоацетат реагирует с нитроалкеном в 1,4-аддиции, за которой следует 5 эндо- - циклизация DIG , устранение нитро и таутомеризации . [ 21 ]
Начальные материалы в синтезе пилота -Робинсона пиррола, названные в честь Гертруды и Роберта Робинсона и Оскара Пилота , являются двумя эквивалентами альдегида и гидразина . [ 22 ] [ 23 ] Продукт представляет собой пиррол с заместителями в 3 и 4 положениях. Альдегид реагирует с диамином на промежуточный ди-имин ( r- c = n- n = c-r). На втором этапе [3,3]- сигматропная перестройка происходит между. Добавление соляной кислоты приводит к закрытию кольца и потере аммиака с образованием пиррола. Механизм . был разработан Робинсоном
В одной модификации пропиональдегид обрабатывается сначала гидразином , а затем бензоилхлоридом при высоких температурах и помогает микроволновому облучению : [ 24 ]
![Piloty–Robinson reaction[24]](http://upload.wikimedia.org/wikipedia/commons/thumb/b/bd/Piloty-Robinson_reaction.png/400px-Piloty-Robinson_reaction.png)
Пирролы, несущие множественные заместители, были получены из реакции мюнхнонов и алкинов . Механизм реакции включает в себя 1,3-диполярную циклую , с последующей потерей углекислого газа процессом ретро -дилеров . Подобные реакции могут быть выполнены с использованием азалактонов.

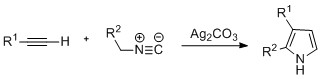
Пирролы также могут быть приготовлены с помощью серебряной циклизации алкинов с изонитрилами , где r 2 Электроно-гибкая группа, и r 1 Алкан, арильная группа или эфир. Также было замечено, что примеры дизамещенных алкинов образуют желаемый пиррол с значительным выходом. Реакция предлагается пройти через серебряный ацетилидный промежуток. Этот метод аналогичен химии Azide -Alkyne Click, используемой для формирования азолов.
Один синтетический путь к пирролу включает в себя декарбоксилирование муката аммония , аммония соли слизистой оболочки . Соль обычно нагревается в установке дистилляции с глицерином в качестве растворителя . [ 25 ]

Биосинтез
[ редактировать ]Биосинтез пиррол-колец начинается с аминолевулиновой кислоты (ALA), которая синтезируется из глицина и сукцинил-КоА . Аладегидратаза катализирует конденсацию двух молекул ALA посредством синтеза кольца типа KNORR с образованием порфобилиногена (PBG). Это более позднее реагирует, например, макроциклы гем и хлорофилл . [ 26 ]
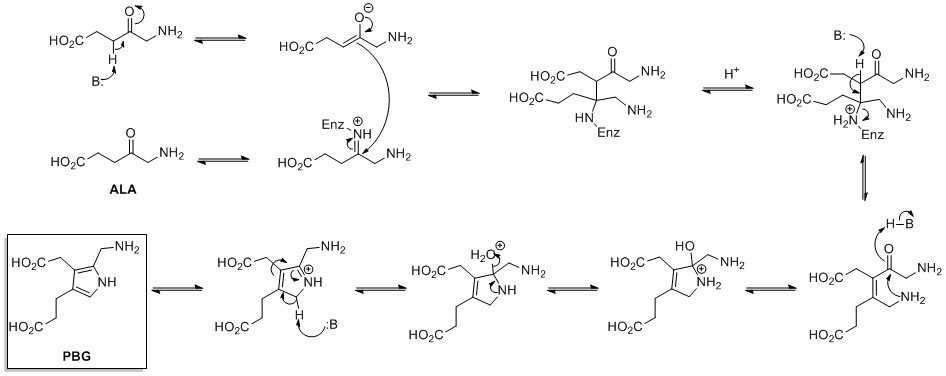
.
Пролин получен биосинтетически из аминокислоты L - глутамата . Глутамат-5-сиилдегид сначала образуется глютаматом 5-киназой (АТФ-зависимой) и глутамат-5-сиилдегиддегидрогеназой (которая требует NADH или NADPH). Затем это может либо спонтанно циклизировать с образованием 1-пирролино-5-карбоновой кислоты , которая снижается до пролина пирролин-5-карбоксилатредуктуктазой (с использованием NADH или NADPH), либо превращается в орнитин аминотрансферазой с орнитин-аминотрансферазой , а затем циклинараза с орнитином циклическим сформировать пролин. [ 27 ]

Пролин можно использовать в качестве предшественника ароматических пирролов в вторичных натуральных продуктах, как в прочигейозинах.

Биосинтез прочисьисана [ 28 ] [ 29 ] включает сходящуюся связь трех кольца типа пиррола (меченные A, B и C на рисунке 1) из L -пролин, L -серин, L -метионин, пируват и 2 -октатный.
Кольцо A синтезируется из L -пролин через нерибосомальный пептидсинтазу -синтазу (NRPS) (рис. 2), в котором пирролидиновое кольцо пролина дважды окисляется через FAD + Чтобы дать пиррол кольцо А.
Кольцо A затем расширяется через путь поликетидсинтазы, чтобы включить L -серину в кольцо B (рис. 3). Кольцо A фрагмент переносится из белка пептидилового носителя (PCP) в белок ацильного носителя (ACP) доменом KS с последующим переносом в малонил-ACP посредством декарбоксилирующей конденсации Claisen. Этот фрагмент затем способен реагировать с карбанином в масках, образованном из опосредованного PLP декарбоксилирование L -серина, которое циклирует в реакции дегидратации, чтобы получить второе пиррол -кольцо. Это промежуточное соединение затем модифицируется метилированием (которое включает метильную группу от L -метионина на спирт в 6 -м положении) и окислением первичного спирта до альдегида, чтобы получить кольцевые структуры сердечника A -B.
Реакции и реактивность
[ редактировать ]Благодаря своему ароматическому характеру пиррола трудно гидрировать , не легко реагировать в качестве диена в реакциях диель -альтер , и не подвергается обычным реакциям олефина . Его реакционная способность аналогична реактизации бензола и анилина , поскольку его легко алкилат и ацилат. В кислых условиях пирролы легко окисляются до полипиррола , [ 30 ] и, таким образом, многие электрофильные реагенты, которые используются в химии бензола, не применимы к пирролам. Напротив, замещенные пирролы (включая защищенные пирролы) использовались в широком диапазоне трансформаций. [ 11 ]
Реакция пиррола с электрофилами
[ редактировать ]Пирролы обычно реагируют с электрофилами в положении α (C2 или C5) из -за самой высокой степени стабильности протонированного промежуточного звена.

Пирролы легко реагируют с нитрусительными (например, HNO 3 / AC 2 O ), сульфонированием ( PY · SO 3 ) и галогенированием (например, NCS , NBS , BR 2 , SO 2 CL 2 и KI / H 2 O 2 ). [ 31 ] Галогенирование обычно обеспечивает полигалогенированные пирролы, но может быть выполнено моногалогенирование. Как типично для электрофильных добавлений к пирролам, галогенирование обычно происходит в 2-позиции, но также может происходить в 3-м положении путем силока азота. Это полезный метод для дальнейшей функционализации в целом менее реактивной 3-позиции. [ Цитация необходима ]
Ацилирование
[ редактировать ]Ацилирование обычно происходит в 2-за положении с помощью различных методов. Ацилирование кислотными ангидридами и кислотными хлоридами может происходить с или без катализатора или без. [ 32 ] 2-ацилпирролы также получают из реакции с нитрилами реакцией Houben-Hoesch . Пиррол альдегиды можно образовать с помощью реакции Vilsmeier -Haack . [ 33 ]

Реакция депротонированной пирролы
[ редактировать ]Протон NH в пирролах умеренно кислый с P K A 17,5. [ 34 ] Пиррол может быть депротонирован с сильными основаниями, такими как бутиллитий и гидрид натрия . [ 35 ] Полученный щелочной пирролид является нуклеофильным . Обработка этого конъюгатного основания с помощью электрофила, такого как йодометан, дает нметилпиррол .
N -Металяция пиррола может реагировать с электрофилами в положениях N или C, в зависимости от координирующего металла. Более ионные азотные связи (например, с литием, натрием и калием) и более сольватирующие растворители приводят к N -алкилированию. Нитрофильные металлы, такие как MGX, приводят к алкилированию при C (в основном C2) из -за более высокой степени координации с атомом азота. В случаях N -замещенных пирролов металлы углеродов более легкий. Алкильные группы могут быть введены в виде электрофилов или реакциями перекрестной связи. [ Цитация необходима ]
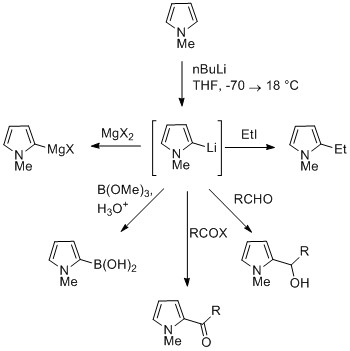
Замена на C3 может быть достигнута за счет использования n -замещенного 3 -бромпиррола, которое может быть синтезировано броминицией N -силилпиррола с NBS . [ Цитация необходима ]
Сокращение
[ редактировать ]Пирролы могут подвергаться восстановлению до пирролидинов и пирролинов . [ 36 ] Например, снижение березы эфиров пиррола и амидов, образующих пирролины, с региоселективностью в зависимости от положения группы электронов. [ Цитация необходима ]
Реакции циклизации
[ редактировать ]Пирролы с N -субстицией могут подвергаться реакциям циклов , таких как [4+2]-, [2+2]-и [2+1] -Cyclizations. Циклизации Diels-Alder могут происходить с пирролом, действующим в качестве диена, особенно в присутствии группы электронов на азоте. Винилпирролы также могут действовать как Диена. [ Цитация необходима ]
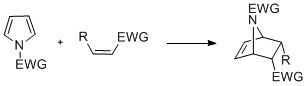
Пирролы могут реагировать с карбенами , такими как дихлорокарбен , в [2+1] -Cycloaddition. С дихлорокарбеном образуется дихлорциклопропановый промежуток, который разбивается с образованием 3-хлорпиридина (перестройка циаминика-деншедедта). [ 37 ] [ 38 ] [ 39 ]

Коммерческое использование
[ редактировать ]Полипирроль имеет некоторую коммерческую ценность. N -метилпирроль является предшественником N -метилпирролекарбоновой кислоты, блока здания в фармацевтической химии. [ 9 ] Пирролы также встречаются в нескольких препаратах, в том числе аторвастатин , кеторолак и сунитиниб . Пирролы используются в виде легких красных, алых и кармина. [ 40 ] [ 41 ]
Аналоги и производные
[ редактировать ]Структурные аналоги пиррола включают:
- Пирролин , частично насыщенный аналог с одной двойной связью
- Пирролидин , насыщенный гидрогенизированный аналог
Производные пиррола включают индол , производное с плавленовым бензольным кольцом.
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Уильям М. Хейнс (2016). Справочник по химии и физике CRC (97 -е изд.). Boca Raton: CRC Press. С. 3–478. ISBN 978-1-4987-5429-3 .
- ^ Международный союз чистой и прикладной химии (2014). Номенклатура органической химии: рекомендации IUPAC и предпочтительные названия 2013 . Королевское химическое общество . п. 141. doi : 10.1039/9781849733069 . ISBN 978-0-85404-182-4 .
- ^ Лоудон, Марк Г. (2002). «Химия нафталина и ароматических гетероциклов». Органическая химия (4 -е изд.). Нью -Йорк: издательство Оксфордского университета. С. 1135–1136. ISBN 978-0-19-511999-2 .
- ^ Кокс, Майкл; Lehninger, Albert L.; Нельсон, Дэвид Р. (2000). Лехнингер Принципы биохимии . Нью -Йорк: Стоит издатели. ISBN 978-1-57259-153-0 .
- ^ Jump up to: а беременный Jusélius, Jonas; Sundholm, Dage (2000). «Ароматические пути порфинов, хлоринов и бактериохлоринов» . Физический Химический Химический Физический 2 (10): 2145–2151. BIBCODE : 2000PCCP .... 2.2145J . doi : 10.1039/b000260g .

- ^ Армарего, Уилфред Л.Ф.; Чай, Кристина Л.Л. (2003). Очистка лабораторных химикатов (5 -е изд.). Elsevier. п. 346.
- ^ Смит, Майкл Б.; Март, Джерри (2007), Advanced Organic Chemistry: реакции, механизмы и структура (6-е изд.), Нью-Йорк: Wiley-Interscience, p. 62, ISBN 978-0-471-72091-1
- ^ Рунге, FF (1834). «О некоторых из продуктов распада угля» [о некоторых продуктах угля дистилляции]. Анналы физики и химии . 31 (5): 65–78. Bibcode : 1834anp ... 107 ... 65r . Doi : 10.1002/andp.18341070502 .
 См. Особенно страницы 67–68, где Рунге называет составной пиррол (огненное масло) или ротёль (красное масло).
См. Особенно страницы 67–68, где Рунге называет составной пиррол (огненное масло) или ротёль (красное масло).
- ^ Jump up to: а беременный в Харреус, Альбрехт Людвиг. "Пиррол". Энциклопедия промышленной химии Уллмана . Вейнхайм: Wiley-VCH. Doi : 10.1002/14356007.a22_453 . ISBN 978-3527306732 .
- ^ Фоулз, Джефферсон; Бейтс, Майкл; Нойтон, Доминик (март 2000 г.). «Химические компоненты в сигаретах и сигаретном дыме: приоритеты для снижения вреда» (PDF) . Порируа, Новая Зеландия: Министерство здравоохранения Новой Зеландии . С. 20, 49–65 . Получено 2012-09-23 .
- ^ Jump up to: а беременный Любелл, W.; Saint-Cyr, D.; Dufour-Gallant, J.; Hopewell, R.; Бутард, н.; Кассем, Т.; Dörr, A.; Зелли Р. (2013). «1 ч -пирролы (обновление 2013)» . Наука синтеза . 2013 (1): 157–388.
- ^ Гилкрист, Томас Л. (1997). Гетероциклическая химия (3 -е изд.). Ливерпуль: Лонгман. п. 194-196.
- ^ Ханцш, А. (1890). «Новый образовательный стиль Пирро -Рандивации» [новые методы формирования производных пирролов]. Отчеты немецкого химического общества . 23 : 1474–1476. Doi : 10.1002/cber.189002301243 .

- ^ Файст, Франц (1902). «Исследования в группе Фурана и Пиррола» [Исследования в группах Фурана и Пиррола]. Отчеты немецкого химического общества . 35 (2): 1537–1544. Doi : 10.1002/cber.19020350263 .

- ^ Кнорр, Людвиг (1884). «Синтез пирродролдериватов» [Синтез производных пирролов]. Отчеты немецкого химического общества . 17 (2): 1635–1642. Doi : 10.1002/cber.18840170220 .

- ^ Кнорр Л. (1886). «Синтетические попытки с ацетацитой» [Эксперимент с синтезом с [этил] эфиром ацетоуксусной кислоты]. Анналы химии . 236 (3): 290–332. Doi : 10.1002/jlac.18862360303 .

- ^ Knorr, L.; Ланге, Х. (1902). «О образовании пирролериватов из изонитрозокетонов» [о образовании производных пиррол из изонитросукетов]. Отчеты немецкого химического общества . 35 (3): 2998–3008. Doi : 10.1002/cber.19020350392 .

- ^ Корвин, Алсоф Генри (1950). «Глава 6: Химия Пирроле и его производных». В Elderfield Роберт Кули (ред.). Гетероциклические соединения . Тол. 1. Нью -Йорк, Нью -Йорк: Уайли. п. 287
- ^ Паал, С. (1884), «О производных гнезда ацетофенонацета и ацетонилацета» , сообщения о немецком химическом обществе , 17 (2): 2756–2767, doi : 10.1002/cber.18840170228

- ^ Кнорр, Людвиг (1884), «Синтез фюрсных индиватов из эфира диацееттбернштейновой кислоты» [синтез производных фурана из [диэтил] эфира 2,3-диацетил-сукцинической кислоты], сообщает Германское химическое общество , 17 (2 ): 2863–2870, doi : 10.1002/cber.188401702254

- ^ Ли, Цзе Джек (2013). Гетероциклическая химия при обнаружении лекарств . Нью -Йорк: Уайли. ISBN 9781118354421 .
- ^ Пилот, Оскар (1910). «Синтез модели пирро: пиррол из эфира сукцинилоберноновой кислоты, пиррола из азинов» [синтез производных пирролов: пиррол из тетилцитилцинилкцината, пиррол из азинов]. Отчеты немецкого химического общества . 43 (1): 489–498. Doi : 10.1002/cber.19100430182 .

- ^ Робинсон, Гертруда Мод; Робинсон, Роберт (1918). «Лив. Новый синтез тетрафенилпиррола». J. Chem. Соц 113 : 639–645. doi : 10.1039/ct9181300639 .
- ^ Jump up to: а беременный Милграм, Бенджамин С.; Эскильдсен, Катрин; Рихтер, Стивен М.; Шейдт, В. Роберт; Шейдт, Карл А. (2007). «Синтез пилота-Робинсона с помощью микроволновой печи 3,4-рассеянных пирролов» (примечание) . J. Org. Химический 72 (10): 3941–3944. doi : 10.1021/jo070389+ . PMC 1939979 . PMID 17432915 .
- ^ Фогель (1956). Практическая органическая химия (PDF) . п. 837.
- ^ Уолш, Кристофер Т.; Гарно-Зодикова, Сильви ; Ховард-Джонс, Аннализ Р. (2006). «Биологическое образование пирролов: природная логика и ферментативное оборудование». Отчеты о натуральных продуктах . 23 (4): 517–531. doi : 10.1039/b605245m . PMID 16874387 .
- ^ Lehninger, Albert L.; Нельсон, Дэвид Л.; Кокс, Майкл М. (2000). Принципы биохимии (3 -е изд.). Нью -Йорк: У. Х. Фриман. ISBN 1-57259-153-6 . .
- ^ Уолш, Коннектикут; Garneau-Tsodikova, S.; Ховард-Джонс, А.Р. (2006). «Биологическое образование пирролов: природная логика и ферментативное оборудование». НАТ Продлевать Репутация 23 (4): 517–531. doi : 10.1039/b605245m . PMID 16874387 .
- ^ Ху, Деннис X. (2016). «Структура, химический синтез и биосинтез натуральных продуктов провинции» . Химические обзоры . 116 (14): 7818–7853. doi : 10.1021/acs.chemrev.6b00024 . PMC 5555159 . PMID 27314508 .
- ^ Ван Джитао [Ван Джитао]; Органическая химия [ Органическая химия ] (на китайском языке) (2 -е изд.). Университет Тяньцзинь Нанкай. ISBN 978-7-310-00620-5 .
- ^ "Пиррол". Römpp Lexikon Chemie (на немецком языке). Это.
- ^ Бейли, Денис М.; Джонсон, Роберт Э.; Альбертсон, Ноэль Ф. (1971). «Этил пиррол-2-карбоксилат». Органические синтезы . 51 : 100. doi : 10.15227/orgsyn.051.0100 .
- ^ Сильверштейн, Роберт М.; Ryskiewicz, Edward E.; Уиллард, Констанс (1956). "2-пирролеалдегид". Органические синтезы . 36 : 74. doi : 10.15227/orgsyn.036.0074 .
- ^ Bird, C. W.; Cheeseman, G. W. H. (1984). Комплексная гетероциклическая химия . Пергамон. С. 39–88. ISBN 978-0-08-096519-2 , хотя обратите внимание, что Балон, М.; Кармона, М. С.; Муньос, М. А.; Hidalgo, J. (1989). «Кислотно-базовые свойства пиррола и его бензологов индолы и карбазола: повторное рассмотрение метода избыточной кислотности». Тетраэдр . 45 (23). Великобритания: Пергамон: 7501–7504. doi : 10.1016/s0040-4020 (01) 89212-7 предполагает, что ревизия фигуры на 17,3.
- ^ Франк, Хайнц-Жерхард; Стадельхофер, Юрген Уолтер (1987). Химия промышленной ароматики: сырье, процедуры, продукция [ Промышленная химия ароматики: сырье, процессы, продукты ] (на немецком языке). Берлин: Спрингер. С. ISBN 978-3-662-07876-1 .
- ^ Lyastukhin, Voronov [Ластухін, Воронов] (2006). Органическая химия [ Органическая химия ] (на украинском). С. 781–782. ISBN 966-7022-19-6 .
{{cite book}}: Cs1 maint: несколько имен: список авторов ( ссылка ) - ^ Ciamician, GL; ДУСстедт М. (1881). «О влиянии хлороформа на пиррол калия» [о реакции хлороформа с калиевым соединением пиррола]. Отчеты немецкого химического общества . 14 : 1153–1162. Doi : 10.1002/cber.188101401240 .
- ^ Корвин, Алсоф Генри (1950). Элдерфилд, Роберт Кули (ред.). Гетероциклические соединения . Тол. 1. Нью -Йорк, Нью -Йорк: Уайли. п. 309
- ^ Mosher, HS (1950). Элдерфилд, Роберт Кули (ред.). Гетероциклические соединения . Тол. 1. Нью -Йорк, Нью -Йорк: Уайли. п. 475.
- ^ «Пигменты DPP, дикетопирролопиррольные пигменты, пигменты DPP Оптовик, поставщики пигментов Diketopyrlopyrrole» . Dyes-figments.standardcon.com .
- ^ Каур, Матинер; Чой, Донг Хун (2015). «Дикетопирролопирроль: блестящие флуоресцентные зонды на основе красного пигментного красителя и их применение». Обзоры химического общества . 44 (1): 58–77. doi : 10.1039/c4cs00248b . PMID 25186723 .
Дальнейшее чтение
[ редактировать ]- Джонс, Р. Джонс, изд. (1990). Пирролы. Часть I. Синтез и физические и химические аспекты пиррольского кольца . Химия гетероциклических соединений. Тол. 48. Чичестер: Джон Вили и сыновья. п. 351. doi : 10.1002/recl.19911100712 . ISBN 978-0-471-62753-1 .
{{cite book}}:|journal=игнорируется ( помощь ) - Jolicoeur, Benoit; Чепмен, Эрин Э.; Томпсон, Элисон; Любелл, Уильям Д. (2006). «Защита пиррола». Тетраэдр . 62 (50): 11531–11563. doi : 10.1016/j.tet.2006.08.071 .