LSM
Эта статья может быть слишком технической для большинства читателей, чтобы понять . ( Август 2013 ) |

| LSM -домен | |||
|---|---|---|---|
 Кристаллическая структура белка, связанного с SM с р. Абиссии биологическая единица - гепамер | |||
| Идентификаторы | |||
| Символ | LSM | ||
| Pfam | PF01423 | ||
| InterPro | IPR001163 | ||
| Краткое содержание | 1d3b / scope / supfam | ||
| CDD | CD00600 | ||
| |||
В молекулярной биологии белки LSM представляют собой семейство РНК -связывающих белков, обнаруженных практически в каждом клеточном организме . LSM - это сокращение «как SM», потому что первыми идентифицированными членами семейства белков LSM были белки SM . Белки LSM определяются характерной трехмерной структурой и их сборкой в кольца из шести или семи отдельных молекул белка LSM и играют большое количество различных ролей в обработке и регуляции мРНК .
Белки SM были впервые обнаружены в виде антигенов, нацеленных на так называемые анти-SM-антитела у пациента с формой системной волчанки эритематозу (SLE), изнурительного аутоиммунного заболевания . Они были названы белками SM в честь Стефани Смит, пациента, которая страдала от СКВ. [ 1 ] Другие белки с очень похожими структурами были впоследствии обнаружены и названы LSM -белками. Новые члены семейства белков LSM продолжают идентифицировать и сообщать.
Белки со схожими структурами сгруппированы в иерархию семейств белков, суперсемей и складок. Структура белка LSM является примером небольшого бета -листа, сложенного в короткий ствол. Отдельные белки LSM собираются в кольцо до пончика из шести или семи членов (более правильно называемые тора ), которое обычно связывается с небольшой молекулой РНК с образованием комплекса рибонуклеопротеина . LSM Torus помогает молекуле РНК принять и поддерживать ее правильную трехмерную структуру. В зависимости от того, какие белки LSM и молекула РНК участвуют, этот комплекс рибонуклеопротеина облегчает широкий спектр обработки РНК, включая деградацию, редактирование, сплайсинг и регуляцию.
Альтернативными терминами для семейства LSM являются LSM-складка и SM-подобные складки , а альтернативные стили заглавных букв, такие как LSM , LSM и LSM , являются общими и одинаково приемлемыми.
История
[ редактировать ]Открытие антигена Смита
[ редактировать ]История открытия первых белков LSM начинается с молодой женщины, Стефани Смит, которой в 1959 году была диагностирована системная волчанка (SLE) , в конечном итоге уступив осложнениям заболевания в 1969 году в возрасте 22 лет. [ 1 ] В течение этого периода ее лечили в университетской больнице Рокфеллера в Нью -Йорке под уходом доктора Генри Кункеля и доктора Энг Тана. Как пациенты с аутоиммунным заболеванием , пациенты с СКВ производят антитела к антигенам в ядрах своих клеток , чаще всего к их собственной ДНК . Однако в 1966 году Кункель и Тан обнаружили, что Смит произвел антитела к набору ядерных белков, которые они назвали «Смит -антиген » ( SM AG ). [ 2 ] Около 30% пациентов с СКВ производят антитела к этим белкам, в отличие от ДНК с двойной страной. Это открытие улучшило диагностическое тестирование для SLE, но природа и функция этого антигена были неизвестны.
SM -белки, SNRNP, сплайсинг РНК сплайсосомы и мессенджера РНК
[ редактировать ]Исследования продолжались в 1970 -х и начале 1980 -х годов. Было обнаружено, что антиген Смита является комплексом молекул рибонуклеиновой кислоты ( РНК ) и множественных белков. Набор уридином ), богатых молекул малой ядерной РНК ( SNRNA (SNRNA ), был частью этого комплекса, и учитывая имена U1 , U2 , U4 , U5 и U6 . Было обнаружено, что четыре из этих SNRNAs (U1, U2, U4 и U5) тесно связаны с несколькими небольшими белками, которые были названы SMB , SMD, SME , SMF и SMG в порядке уменьшения размера. SMB есть альтернативно сплайсированный вариант, SMB ' и очень похожий белок, SMN , заменяет SMB'/B в определенных (в основном нервных) тканях. Позже был обнаружен SMD как смесь из трех белков, которые были названы SMD1 , SMD2 и SMD3 . Эти девять белков (SMB, SMB ', SMN, SMD1, SMD2, SMD3, SME, SMF и SMG) стали известны как белки SM Core или просто белки SM . SNRNAs комплексны с белками ядра SM и с другими белками с образованием частиц в ядре клетки, называемых небольшими ядерными рибонуклеопротеинами или SNRNP . К середине 1980-х годов стало ясно, что они SNRNPs помогают сформировать большой (4,8 МД- молекулярную массу ) комплекс, называемый сплайсосомой вокруг пре-мРНК , вырезая части пре-мРНК, называемую интронами и сплайсируют кодирующие части ( экзоны ) вместе. [ 3 ] После еще нескольких модификаций сплайсированная пре-мРНК становится РНК мессенджера (мРНК), которая затем экспортируется из ядра и транслируется в белок рибосомами .
Открытие белков, сходных с белками SM
[ редактировать ]SNRNA U6 (в отличие от U1, U2, U4 и U5) не связывается с белками SM, даже если U6 SNRNP является центральным компонентом в сплайсосоме . В 1999 году был обнаружен гетеромер белка, который связывается специфически с U6 и состоял из семи белков, четко гомологичных белков SM. Эти белки были обозначены белкам LSM (например, SM) ( LSM1 , LSM2 , LSM3 , LSM4 , LSM5 , LSM6 и LSM7 ), с аналогичным белком LSM8 идентифицировано позже. В бактерии Escherichia coli SM-подобный белок HF-I, кодируемый геном HFQ, описан в 1968 году как незаменимый актер был для РНК бактериофага Q репликации β. Геном ( Baker Saccharomyces cerevisiae 's дрожжи) был секвенирован в середине 1990-х годов, обеспечивая богатый ресурс для выявления гомологов этих человеческих белков. Впоследствии, поскольку больше геномов эукариот были секвенированы, стало ясно, что эукариоты, как правило, разделяют гомологи с тем же набором из семи SM и восьми белков LSM. [ 4 ] Вскоре после этого белки, гомологичные этим белкам Eukaryote LSM, были обнаружены в Archaea ( SM1 и SM2 ) и бактериях ( гомологи HFQ и YLXS ). [ 5 ] Архаальные белки LSM больше похожи на белки Eukaryote LSM, чем на бактериальные белки LSM. Описанные до сих пор описываемые белки LSM были довольно маленькие белки, варьирующиеся от 76 аминокислот 8,7 кД ( молекулярная масса ) для SMG человека до 231 аминокислот (29 кДа молекулярной массы) для SMB человека. Но в последнее время были обнаружены более крупные белки, которые включают структурный домен LSM в дополнение к другим структурным доменам белка (такие как LSM10 , LSM11 , LSM12 , LSM13 , LSM14 , LSM15 , LSM16 , атаксин-2 , а также Archaeal SM3 ).
Открытие сгиба LSM
[ редактировать ]Примерно в 1995 году сравнения различных гомологов LSM идентифицировали два мотива последовательности , длиной 32 нуклеиновых кислот (14 аминокислот), которые были очень похожи в каждом гомологе LSM и были разделены неконсервативной областью переменной длины. Это указывало на важность этих двух мотивов последовательности (названных SM1 и SM2 ) и предположило, что все гены белков LSM эволюционировали из одного гена предков. [ 6 ] кристаллы рекомбинантных В 1999 году были получены белков SM, что позволяет рентгеновской кристаллографии и определение их атомной структуры в трех измерениях. [ 7 ] Это продемонстрировало, что белки LSM имеют аналогичную трехмерную складку короткой альфа-спирали и пятицепочечный сложенный бета-лист , который впоследствии назвал LSM-складку . Другие исследования обнаружили, что белки LSM собираются в торус (кольцо в форме снута) из шести или семи белков LSM, и что РНК связывается с внутренней частью тора, с одним нуклеотидом, связанным с каждым белком LSM.
Структура
[ редактировать ]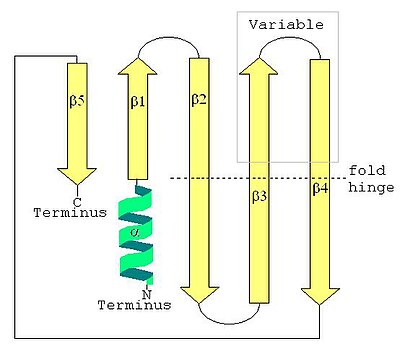

Фосфат уридина связывается в архейном SM1 между петлей β2B/β3A и петлей β4B/β5. Урацил остатками укладывается между остатками гистидина и аргинина , стабилизируется водородной связью с аспарагина , и водородной связью между остатками аспартата и рибозой . Белки LSM характеризуются бета -листом ( вторичная структура ), сложенные в складку LSM ( третичная структура ), полимеризацию в шесть или семь элементов ( четвертичная структура ) и связывание с РНК олигонуклеотиды . [ 8 ] Современная парадигма классифицирует белки на основе структуры белка полем в настоящее время, с тремя основными подходами: SCOP ( S Tructural C Protins и активным является ), Cath ( C Lass, Rchitecture , T Opology, Homologous Superfamily) , и FSSP/DALI ( F Amilies of S Tructurally Imilal Proteins ) .
Второстепенный
[ редактировать ]Вторичная структура белка LSM представляет собой небольшой пятицепочечный антипараллельный бета-лист , причем нити, идентифицированные с N-концевого конца до C-концевого конца как β1, β2, β3, β4, β5. Класс SCOP всех бета -белков и класс Cath в основном бета определяются как белковые структуры, которые в основном являются бета -листами, включая LSM. SM1 Мотив последовательности соответствует цепям β1, β2, β3 и мотиву последовательности SM2 соответствует цепям β4 и β5. Первые четыре бета -нить примыкают друг к другу, но β5 рядом с β1, превращая общую структуру в короткую стволу. Эта структурная топология описывается как 51234. Короткая (от двух до четырех видов) N-концевая альфа-спираль также присутствует в большинстве белков LSM. Цепы β3 и β4 короткие в некоторых белках LSM и разделены неструктурированной катушкой переменной длины. Цепы β2, β3 и β4 сильно изогнуты около 120 ° градусов в их средних точках. Изгибы в этих целях часто являются глицином , а боковые цепи, внутренние к бета -бочке, часто являются гидрофобными остатками Валин , лейцин , изолейцин и метионин .
Третичный
[ редактировать ]SCOP просто классифицирует структуру LSM как SM-подобную складку , одну из 149 различных белковых белков без каких-либо промежуточных групп. Бета -лист LSM резко согнут и описывается как архитектура рулона в CATH (одна из 20 различных белковых белковых архитектур в CATH). Один из бета -нитей (β5 в LSM) пересекает открытый край рулона, образуя небольшую топологию ствола типа SH3 (одна из 33 топологий бета -рулона в CATH). Кэт перечисляет 23 гомологичных суперсемейства с топологией ствола типа SH3, одной из которых является структура LSM ( РНК -связывающий белок в системе CATH). SCOP продолжает свою структурную классификацию после сгиба до суперсемейства, семьи и домена, в то время как Cath продолжает последовательно последовательно, но эти разделения более подходящим образом описаны в разделе «Эволюция и филогения».
ствола типа SH3-типа Третичная структура сгиба LSM образуется сильно изогнутыми (около 120 °) β2, β3 и β4, при этом структура ствола закрыта β5 цепью. Подчеркивая третичную структуру, каждая изогнутая бета -прядь может быть описана как две более короткие бета -пряди. Складки LSM можно рассматривать как восьмицепочечный антипараллельный бета-бутерброд , с пятью нитями в одной плоскости и тремя нитями в параллельной плоскости с углом шага при 45 ° между двумя половинками бета-сэндвича. Короткая (от двух до четырех видов) N-концевая альфа-спираль встречается на одном краю бета-бутерброда. Эта альфа-спираль и бета-ниши можно пометить (от N-концевого до C-конца ) α, β1, β2A, β2B, β3A, β3B, β4A, β4B, β5, где A и B относятся к любым 22-м изогнутой прядь в пяти цепочке или отдельных прядях в восьмицепочечном описании. Каждая прядь (в описании восьми цепи) образуется из пяти аминокислотных остатков. Включая изгибы и петли между нитями и альфа -спиралью, около 60 аминокислотных остатков способствуют складе LSM, но это варьируется между Гомологи из-за изменений в межтежковых петлях, альфа-спирали и даже длины цепей β3B и β4A.
Четвертичный
[ редактировать ]Белки LSM обычно собираются в кольцо LSM , шесть или семь членов , около 7 нанометров в диаметре с 2 нанометровым отверстием. Состояние наследственного - это гомогексамер или гомогепмер идентичных субъединиц LSM. Белки LSM у эукариот образуют гетерогептисты семи различных субъединиц LSM, таких как белки SM. Связывание между белками LSM лучше всего понимается с восьмицепочечным описанием сгиба LSM. The five-strand half of the beta sandwich of one subunit aligns with the three-strand half of the beta sandwich of the adjacent subunit, forming a twisted 8-strand beta sheet Aβ4a/Aβ3b/Aβ2a/Aβ1/Aβ5/Bβ4b/Bβ3a/ Bβ2B, где A и B относятся к двум различным субъединицам. В дополнение к водородным связям Bβ4B двух субъединиц белка LSM, существуют энергетически благоприятные контакты гидрофобными аминокислотны между между бета -цепь Aβ5 и Периферия области контакта.
РНК олигонуклеотидное связывание
[ редактировать ]Кольца LSM образуют рибонуклеопротеиновые комплексы с РНК -олигонуклеотидами , которые варьируются в силе связывания от очень стабильных комплексов (таких как SNRNP класса SM) к переходным комплексам. РНК -олигонуклеотиды обычно связываются внутри отверстия (просвет) LSM Torus, одного нуклеотида сообщалось о дополнительных сайтах связывания нуклеотидов на субъединицу LSM, но на верхней стороне кольца . Точная химическая природа этого связывания варьируется, но общие мотивы включают укладку гетероциклического основания (часто урацил ) между плоские боковые цепи двух аминокислот, водородную связь с гетероциклическим основанием и/или рибозой и солевыми мостами с фосфатной группой.
Функции
[ редактировать ]Различные виды колец LSM функционируют как каркасы или шапероны для РНК- олигонуклеотидов , помогая РНК принять и поддерживать надлежащую трехмерную структуру. В некоторых случаях это позволяет олигонуклеотидной РНК каталитически функционировать как рибозим . В других случаях это облегчает модификацию или деградацию РНК или сборки, хранения и внутриклеточного переноса комплексов рибонуклеопротеинов . [ 9 ]
SM Ring
[ редактировать ]Кольцо SM находится в ядре всех эукариот (около 2,5 × 10 6 копии на пролиферирующую человеческую клетку) и имеют наилучшие понятные функции. Кольцо SM - гетерогепмер . Молекула SM-класса SMRNA (в направлении от 5 до 3 ') попадает в просвет (отверстие для пончика) в субъединице МСП и последовательно проходит по часовой стрелке (глядя со стороны α-спирали) внутри просвета (дыра пончика) к SMG, SMD3, SMB, SMD1, SMD2, выходящие в субъединицу SMF. [ 10 ] (SMB может быть заменен вариантом SPLICE SMB 'и SMN в нервных тканях.) Кольцо SM постоянно связывается с SNRNAS U1, U2, U4 и U5, которые образуют четыре из пяти SNRNP , которые составляют основную сплайсосом . Кольцо SM также постоянно связывается с SNRNAS U11 , U12 и U4ATAC , которые образуют четыре из пяти SNRNP (включая U5 SNRNP), которые составляют незначительную сплайсосому . Оба эти сплицеосомы являются центральными РНК-обработчиками комплексов в созревании РНКсенджера из пре-мРНК . Также сообщалось, что белки SM являются частью рибонуклеопротеина компонента теломеразы . [ 11 ]
LSM2-8 Кольцо
[ редактировать ]Два SNRNP LSM2-8 (U6 и U6ATAC ) имеют ключевую каталитическую функцию в основных и незначительных сплайсосомах. Эти SNRNP не включают кольцо SM, а используют гетерогептимерное кольцо LSM2-8 . Кольца LSM примерно в 20 раз меньше, чем кольца SM. Порядок этих семи белков LSM в этом кольце не известен, но на основе гомологии аминокислотной последовательности с белками SM предполагается, что snRNA (в направлении от 5 до 3 ') может сначала связываться с LSM5 и предшествует Последовательно по часовой стрелке к LSM7, LSM4, LSM8, LSM2, LSM3 и выходу в субъединицу LSM6. Эксперименты с мутациями Saccharomyces cerevisiae (почкующихся дрожжей) предполагают, что кольцо LSM2-8 помогает восстановлению SNRNP U4 и U6 в U4/U6 DI-SNRNP . [ 12 ] (После завершения делеции экзона и сплайсинга интрона эти две SNRNP должны повторно восстановить для сплайсосомы, чтобы инициировать другой цикл сплайсинга экзона/интрона. В этой роли кольцо LSM2-8 действует как реперон РНК вместо РНК-каркаса.) -8 Кольцо также образует SNRNP с U8 небольшой нуклеолярной РНК (Snorna), которая локализуется в ядреве . Этот комплекс рибонуклеопротеина необходим для обработки рибосомной РНК и переноса РНК в их зрелые формы. [ 13 ] Сообщается, что кольцо LSM2-8 играет роль в обработке Pre-P в РНК -РНК-РНК . В отличие от кольца SM, кольцо LSM2-8 не постоянно связывается с его снурной и snorna.
SM10/SM11 Кольцо
[ редактировать ]Существует второй тип кольца SM, где LSM10 заменяет SMD1 и LSM11 заменяет SMD2. LSM11-это два доменного белка, а С-концевой домен-домен LSM. Это гетерогепмерное кольцо связывается со снурной U7 в U7 SNRNP . U7 SNRNP опосредует обработку 3 'UTR STEM-петли гистона мРНК в ядре . [ 14 ] Как и кольцо SM, оно собирается в цитоплазме на SnRNA U7 специализированным комплексом SMN.
LSM1-7 Кольцо
[ редактировать ]Второй тип кольца LSM-это кольцо LSM1-7 , которое имеет ту же структуру, что и кольцо LSM2-8, за исключением того, что LSM1 заменяет LSM8. В отличие от кольца LSM2-8, кольцо LSM1-7 локализуется в цитоплазме , где оно помогает разжигать РНКсенджер в комплексах рибонуклеопротеинов . Этот процесс контролирует оборот РНК мессенджера, так что рибосомная трансляция мРНК в белок быстро реагирует на изменения в транскрипции ДНК в РНК посланника клеткой. Было показано, что LSM1-7 вместе с PAT1 играет роль в формировании P-болей после дегенилирования. [ 15 ]
Gemin6 и Gemin7
[ редактировать ]Комплекс SMN (описанный в «Биогенезе SNRNP») состоит из белка SMN и Gemin2-8 . два из них, Gemin 6 и Gemin7, Было обнаружено, что имеют структуру LSM и образуют гетеродимер. Они могут иметь функцию шаперона в комплексе SMN, чтобы помочь образованию кольца SM на SM-класс SNRNAs . [ 16 ] Комплекс PRMT5 состоит из PRMT5 , PICLN , WD45 (MEP50) . Picln помогает сформировать SM -открытое кольцо на комплексе SMN. Комплекс SMN помогает в сборке SNRNP , где кольцо SM находится в открытой конформации на комплексе SMN, и это кольцо SM загружается на SNRNA комплексом SMN. [ 17 ]
LSM12-16 и другие многодоменные белки LSM
[ редактировать ]Белки LSM12-16 были описаны совсем недавно. Это двухдоменные белки с N-концевым доменом LSM и С-концевой домен метилтрансфераза. [ 18 ] Очень мало известно о функции этих белков, но, по-видимому, они являются членами кольца LSM-домен, которые взаимодействуют с РНК. Есть некоторые доказательства того, что LSM12, возможно, участвует в деградации мРНК, и LSM13-16 может играть роль в регуляции митоза . Неожиданно LSM12 недавно был вовлечен в передачу сигналов кальция , действуя как промежуточный белок связывания для нуклеотидного второго мессенджера, NAADP ( никотиновая кислота аденин-динуклеотидный фосфат ), который активирует эндолизосомный CA 2+ каналы TPCS ( двухпоровые каналы ). [ 19 ] Это произошло при связывании NAADP с доменом LSM, а не с доменом AD. [ 19 ] Большой белок неизвестной функции, атаксин-2 , связанный с нейродегенеративным заболеванием спиноцеребеллельной атаксии типа 2 , также имеет N-концевой домен LSM.
Архаальные SM кольца
[ редактировать ]Два белка LSM обнаружены во втором домене жизни, Archaea . Это белки SM1 и SM2 (не следует путать с мотивами последовательностей причине иногда идентифицируются как S M-подобные RCHAEAL Proteins этой SM1 и SM2), и иногда по SMAP1 и SMAP2 . [ 20 ] SM1 и SM2 обычно образуют кольца гомохептамеров , хотя наблюдались кольца гомогексамера. Кольца SM1 аналогичны кольцам Eukaryote LSM в том смысле, что они образуются в отсутствие РНК, в то время как кольца SM2 аналогичны кольцам эукариот -SM в том смысле, что им требуется уридино -рихская РНК для их формирования. Сообщалось, что им ассоциируется с РНК -РНК , предполагая роль в обработке передачи РНК , но их функция в археи в этом процессе (и, возможно, обработка других РНК, таких как рибосомная РНК ) в основном неизвестна. Один из двух основных ветвей археи, Crenarchaeotes имеет третий известный тип архейного белка LSM, SM3 . Это белок с двумя доменами с N-концевым доменом LSM, который образует гомогепмерное кольцо. Ничего не известно о функции этого белка LSM, но, по -видимому, он взаимодействует и, вероятно, помогает обрабатывать РНК в этих организмах.
Бактериальные кольца LSM
[ редактировать ]Несколько белков LSM были зарегистрированы в третьем домене жизни, бактериях . Белок HFQ образует гомогексамерные кольца и первоначально был обнаружен, как это необходимо для инфекции бактериофагом Qβ , хотя это явно не является нативной функцией этого белка в бактериях. Он не присутствует во всех бактериях, но был обнаружен в Pseudomonadota , Bacillota , Sporochaetota , Thermotogota , Aquificota и один вид археи . (Этот последний экземпляр, вероятно, является случаем горизонтального переноса генов .) HFQ является плейотропным с различными взаимодействиями, как правило, связанные с трансляции регуляцией . К ним относятся блокировка связывания рибосом с мРНК , маркировка мРНК для деградации путем связывания с их хвостами поли-а и ассоциация с бактериальными небольшими регуляторными РНК (такими как DSRA RNA), которые контролируют трансляцию путем связывания с определенными мРНК. [ 21 ] [ 22 ] Второй бактериальный белок LSM представляет собой YLXS (иногда также называемый YHBC), который был впервые идентифицирован в почвенной бактерии Bacillus subtilis . Это белок с двумя доменами с N-концевым доменом LSM. Его функция неизвестна, но гомологи аминокислотной последовательности обнаруживаются практически в каждом бактериальном геноме на сегодняшний день, и он может быть незаменимым белком. [ 23 ] Средний домен механочувствительных каналов MSCS в Escherichia Coli образует гомогептнерское кольцо. [ 24 ] Этот домен LSM не имеет очевидной РНК-связывающей функции, но гомогептамерный торус является частью центрального канала этого мембранного белка.
Эволюция и филогения
[ редактировать ]LSM Гомологи встречаются во всех трех областях жизни и могут даже быть найдены в каждом отдельном организме . Вычислительные филогенетические методы используются для вывода филогенетических отношений. Выравнивание последовательности между различными гомологами LSM является подходящим инструментом для этого, такого как выравнивание множественной последовательности первичной структуры (аминокислотная последовательность) и структурное выравнивание третичной структуры (трехмерная структура). Предполагается, что ген для белка LSM присутствовал в последнем универсальном предке всей жизни. [ 25 ] Основываясь на функциях известных белков LSM, этот оригинальный LSM -белок может иметь вспомогательные рибозимы в обработке РНК для синтезирования белков в рамках гипотезы мира РНК в раннем возрасте. Согласно этой точке зрения, этот ген был передан от предка к потомку, с частыми мутациями , дупликациями генов и случайными горизонтальными передачами генов . В принципе, этот процесс может быть обобщен в филогенетическом дереве с корнем в последнем универсальном предке (или ранее), и с советами, представляющими вселенную генов LSM, существующих сегодня.
Гомомерные кольца LSM в бактериях и археи
[ редактировать ]Основываясь на структуре, известные белки LSM делятся на группу, состоящую из бактериальных белков LSM (HFQ, YLXS и MSCS) и второй группы всех других белков LSM в соответствии с самыми последними опубликованными филогенетическими деревьями . [ 26 ] Три архейных белка LSM (SM1, SM2 и SM3) также кластер как группа, отличающиеся от белков Eukaryote LSM. Как бактериальные, так и архиальные белки LSM полимеризуются гомомерным кольцам, что является наследственным состоянием.
Гетеромерные кольца LSM у эукариот
[ редактировать ]Серия дупликаций генов одного гена Eukaryote LSM привела к большинству (если не все) известных генов Eukaryote LSM. Каждый из семи белков SM имеет большую гомологию аминокислотной последовательности с соответствующим белком LSM, чем для других белков SM. Это говорит о том, что наследственный ген LSM несколько раз дублировался, что привело к семи паралогам . Впоследствии они расходились друг от друга так, что кольцо LSM наследственного гомодептамера стало кольцом гетерогептамеров. Основываясь на известных функциях LSM-белков у эукариот и археи, предков, возможно, была обработка препибосомной РНК , предварительной РНК и предварительной РНК . Затем, согласно этой гипотезе, семь наследственных генов Eukaryote LSM снова дублировались до семи пар паралогов SM/LSM; LSM1/SMB, LSM2/SMD1, LSM3/SMD2, LSM4/SMD3, LSM5/SME, LSM6/SMF и LSM7/SMG. Эти две группы из семи генов LSM (и соответствующие два вида колец LSM) эволюционировали до кольца SM (требующая РНК) и кольцо LSM (которое образуется без РНК). Пара паралогов LSM1/LSM8 также, по -видимому, возникла до последнего общего предка эукариоте, в общей сложности не менее 15 генов белка LSM. Пара паралогов SMD1/LSM10 и пара паралогов SMD2/LSM11 существуют только в Животные , грибы и амебозоа (иногда идентифицируемые как клада Unikont ) и, по -видимому, отсутствуют в кладе биконта ( хромальвевеалаты , раскопки , растения и корневища ). Следовательно, эти два дупликации генов предшествовали этому фундаментальному расколу в линии эукариота. Пара паралогов SMB/SMN виден только у плацентарных млекопитающих , которые датируются дублированием этого гена LSM.
Биогенез SNRNP
[ редактировать ]Маленькие ядерные рибонуклеопротеины (SNRNPS) собираются в плотно организованном и регулируемом процессе, который включает как ядро клеток , так и цитоплазму . [ 27 ]
Ссылки
[ редактировать ]- ^ Jump up to: а беременный Ривз В.П., Нарайн С., Сато М. (2003). «Генри Кункель, Стефани Смит, Клиническая иммунология и разделенные гены». Волчанка . 12 (3): 213–7. doi : 10.1191/0961203303LU360XX . PMID 12708785 . S2CID 33112464 .
- ^ Тан Эм, Кункель Х.Г. (март 1966 г.). «Характеристики растворимого ядерного антигена, осаждающегося с сыворотой пациентов с системной волчанкой эритематозу» . J. Immunol . 96 (3): 464–71. doi : 10.4049/jimmunol.96.3.464 . PMID 5932578 . S2CID 30325463 .
- ^ Will Cl, Lührmann R (июнь 2001 г.). «Сплисосомный биогенез USNRNP, структура и функция». Карт Мнение Клеточная биол . 13 (3): 290–301. doi : 10.1016/s0955-0674 (00) 00211-8 . HDL : 11858/00-001M-0000-0012-F770-0 . PMID 11343899 .
- ^ Он W, Parker R (июнь 2000 г.). «Функции LSM -белков в деградации мРНК и сплайсинг». Карт Мнение Клеточная биол . 12 (3): 346–50. doi : 10.1016/s0955-0674 (00) 00098-3 . PMID 10801455 .
- ^ Törö I, Thore S, Mayer C, Basquin J, Séraphin B, Suck D (май 2001 г.). «Связывание РНК в домене ядра SM: рентгеновская структура и функциональный анализ белкового комплекса архаального SM» . Embo j . 20 (9): 2293–303. doi : 10.1093/emboj/20.9.2293 . PMC 125243 . PMID 11331594 .
- ^ Hermann H, Fabrizio P, Raker VA, Folalaki K, Hornig H, Brahms H, Lührmann R (май 1995). «Белки SNRNP SM имеют два эволюционно консервативных мотива последовательности, которые участвуют в взаимодействиях белка-белка SM» . Embo j . 14 (9): 2076–88. doi : 10.1002/j.1460-2075.1995.tb07199.x . PMC 398308 . PMID 7744013 .
- ^ Kambach C, Walke S, Young R, Avis JM, De La Fortelle E, Raker VA, Lührmann R, Li J, Nagai K (февраль 1999 г.). «Кристаллические структуры двух белковых комплексов SM и их последствия для сборки сплайсосомных SNRNP» . Клетка . 96 (3): 375–87. doi : 10.1016/s0092-8674 (00) 80550-4 . PMID 10025403 . S2CID 17379935 .
- ^ Национальный центр биотехнологической информации о структуре данных PDB Коды 1B34, 1D3B, 1I5L, 1KQ2, 1N9S, 1IB8.
- ^ Khusial P, Plaag R, Zieve GW (сентябрь 2005 г.). «Белки LSM образуют гептамерные кольца, которые связываются с РНК посредством повторяющихся мотивов». Тенденции Biochem. Наука 30 (9): 522–8. doi : 10.1016/j.tibs.2005.07.006 . PMID 16051491 .
- ^ Urlaub H, Raker Va, Kostka S, Lührmann R (январь 2001 г.). «SM-белок-SM-сайт РНК взаимодействия внутри внутреннего кольца сплайсосомной структуры ядра SNRNP» . Embo j . 20 (1–2): 187–96. doi : 10.1093/emboj/20.1.187 . PMC 140196 . PMID 11226169 .
- ^ Seto AG, Zaug AJ, Sobel SG, Wolin SL, Cech TR (сентябрь 1999 г.). «Saccharomyces cerevisiae теломераза - это SM малая ядерная частица рибонуклеопротеина». Природа . 401 (6749): 177–80. Bibcode : 1999Natur.401..177S . doi : 10.1038/43694 . PMID 10490028 . S2CID 4414530 .
- ^ Beggs JD (июнь 2005 г.). «LSM -белки и обработка РНК». Биохимия. Соц Транс . 33 (Pt 3): 433–8. doi : 10.1042/bst0330433 . PMID 15916535 .
- ^ Kufel J, Allmang C, Petfalski E, Beggs J, Tollervey D (январь 2003 г.). «Белки LSM необходимы для нормальной обработки и стабильности рибосомных РНК» . Дж. Биол. Химический 278 (4): 2147–56. doi : 10.1074/jbc.m208856200 . PMID 12438310 .
- ^ Schümperli D, Pillai RS (октябрь 2004 г.). «Специальная структура ядра SM SNRNP U7: далеко идущее значение небольшого ядерного рибонуклеопротеина» (PDF) . Клетка. Мол Life Sci . 61 (19–20): 2560–70. doi : 10.1007/s00018-004-4190-0 . PMID 15526162 . S2CID 5780814 .
- ^ Декер, CJ; Паркер Р. (2012-07-03). «P-Bodies и стрессовые гранулы: возможная роль в контроле трансляции и деградации мРНК» . Перспективы Cold Spring Harbor в биологии . 4 (9): A012286. doi : 10.1101/cshperspect.a012286 . ISSN 1943-0264 . PMC 3428773 . PMID 22763747 .
- ^ Ma Y, Dostie J, Dreyfuss G, Van Duyne GD (июнь 2005 г.). «Гетеродимер Gemin6-Gemin7 от выживания комплекса моторных нейронов имеет белкоподобную структуру SM» . Структура 13 (6): 883–92. doi : 10.1016/j.str.2005.03.014 . PMID 15939020 .
- ^ Chari A, Golas MM, Klingenhäger M, Neuenkirchen N, Sander B, Englbrecht C, Sickmann A, Stark H, Fischer U (2008-10-31). «Собрание шаперона сотрудничает с комплексом SMN для генерации сплайсосомных SNRNP». Клетка . 135 (3): 497–509. doi : 10.1016/j.cell.2008.09.020 . HDL : 11858/00-001M-0000-0010-93A3-A . PMID 18984161 . S2CID 119444 .
- ^ Альбрехт М., Ленгауэр Т (июль 2004 г.). «Новые SM-подобные белки с длинными С-концевыми хвостами и связанными метилтрансферазами» . Фебс Летт . 569 (1–3): 18–26. doi : 10.1016/j.febslet.2004.03.126 . PMID 15225602 . S2CID 37187215 .
- ^ Jump up to: а беременный Чжан, Джиюань; Гуань, Синь; Шах, Кунал; Ян, Джиушенг (2021-08-06). «LSM12-это рецептор NAADP и двухпорочный регуляторный белок, необходимый для мобилизации кальция из кислых органеллов» . Природная связь . 12 (1): 4739. Bibcode : 2021Natco..12.4739Z . doi : 10.1038/s41467-021-24735-z . ISSN 2041-1723 . PMC 8346516 . PMID 34362892 .
- ^ Мура С., Кожуховский А., Кингри М., Филлипс М., Эйзенберг Д (апрель 2003 г.). «Олигомеризация и лиганд-связывающие свойства SM-подобных архейных белков (SMAP)» . Белок Sci . 12 (4): 832–47. doi : 10.1110/ps.0224703 . PMC 2323858 . PMID 12649441 .
- ^ Шумахер М.А., Пирсон Р.Ф., Мёллер Т., Валентин-Хансен П., Бреннан Р.Г. (июль 2002 г.). «Структуры плейотропного трансляционного регулятора HFQ и комплекса HFQ-RNA: бактериальный SM-подобный белок» . Embo j . 21 (13): 3546–56. doi : 10.1093/emboj/cdf322 . PMC 126077 . PMID 12093755 .
- ^ Lease RA, Woodson SA (декабрь 2004 г.). «Велосипедная езда на SM-подобном белка HFQ на DSRA мелкой регуляторной РНК». J. Mol. Биол . 344 (5): 1211–23. doi : 10.1016/j.jmb.2004.10.006 . PMID 15561140 .
- ^ Ю. Л., Гунасекера А.Х., Мак Дж., Олейничзак И.Т., Чован Л.Е., Руан Х, Таун Д.Л., Лернер К.Г., Фесик С.В. (август 2001 г.). «Структура решения и функция консервативного белка SP14.3, кодируемого неотъемлемым геном Streptococcus pneumoniae». J. Mol. Биол . 311 (3): 593–604. doi : 10.1006/jmbi.2001.4894 . PMID 11493012 .
- ^ Басс Р.Б., Строп П., Барклай М., Рис, округ Колумбия (ноябрь 2002 г.). «Кристаллическая структура Escherichia coli MSCS, модулированный напряжением и механочувствительный канал» (PDF) . Наука . 298 (5598): 1582–7. Bibcode : 2002sci ... 298.1582b . doi : 10.1126/science.1077945 . PMID 12446901 . S2CID 15945269 .
- ^ Achsel T, Stark H, Lührmann R (март 2001 г.). «SM-домен-это древний РНК-связывающий мотив со специфичностью олиго (U)» . Прокурор Нат. Академический Наука США . 98 (7): 3685–9. Bibcode : 2001pnas ... 98.3685a . doi : 10.1073/pnas.071033998 . PMC 31112 . PMID 11259661 .
- ^ Ciccarelli FD, Doerks T, Von Mering C, Creevey CJ, Snel B, Bork P (март 2006 г.). «На пути к автоматической реконструкции высокоразрешенного дерева жизни». Наука . 311 (5765): 1283–7. Bibcode : 2006sci ... 311.1283c . Citeseerx 10.1.1.381.9514 . doi : 10.1126/science.1123061 . PMID 16513982 . S2CID 1615592 .
- ^ KISS T (декабрь 2004 г.). «Биогенез небольших ядерных РНП». J. Cell Sci . 117 (Pt 25): 5949–51. doi : 10.1242/jcs.01487 . PMID 15564372 . S2CID 10316639 .