Дигидроксифенилглицин
 | |
| Имена | |
|---|---|
| Название ИЮПАК ( S )-2-амино-2-(3,5-дигидроксифенил)уксусная кислота | |
| Другие имена 3,5-дигидроксифенилглицин, ДГПГ, С-ДГПГ | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
| МеШ | 3,5-дигидроксифенилглицин |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 8 Ч 9 НЕТ 4 | |
| Молярная масса | 183.05 g mol −1 |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
( S )-3,5-Дигидроксифенилглицин или DHPG является мощным агонистом группы I метаботропных глутаматных рецепторов (mGluRs) mGluR1 и mGluR5 .
DHPG был первым агонистом, который оказался селективным в отношении mGluR группы I. [1] Агонистическая активность обнаруживается только у ( S ) -изомера , а ( S )-DHPG может быть частичным агонистом mGluR группы I. [1]
( S )-DHPG исследовался на предмет терапевтических эффектов при лечении повреждений нейронов (например, связанных с ишемией или гипоксией ), улучшения когнитивных функций и болезни Альцгеймера . [1]
3,5-Дигидроксифенилглицин можно выделить из латекса Euphorbia helioscopia . [2]
DHGP также содержится в ванкомицине и родственных ему гликопептидах . Хотя (S) стереоизомер синтезируется ферментами DpgA-D, [3] именно (R)-стереоизомер используется в ванкомицине и других родственных соединениях. DHPG образуется ферментативно по пути поликетидсинтазы .
Биосинтез
[ редактировать ]При синтезе в бактериях DHPG для синтеза требуется 5 ферментов: DpgA-D и 4-гидроксифенилглицинтрансфераза (Pgat). [4] DpgA представляет собой поликетидсинтазу III типа и инициирует синтез путем конденсации ацетил-КоА с тремя молекулами малонил-КоА . Тетракарбонильное соединение затем циклизуется с образованием промежуточного соединения C8. Затем DpgB/D обезвоживает промежуточное соединение, используя енолятную химию, чтобы способствовать потере воды. DpgB/D изомеризует продукт с ароматизацией кольца.

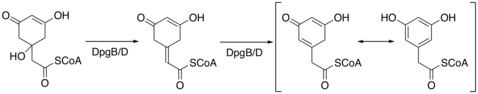
DpgC окисляет ароматическое промежуточное соединение по бензильному углероду с помощью кислорода до альфа-кетосоединения. DpgC выполняет это окисление в отсутствие каких-либо кофакторов железа, гема, флавина или птерина. Chen и соавт. предлагают следующий механизм реакции для объяснения реакционной способности DpgC. [5] Этот механизм подтверждается данными, опубликованными Widboom et al в 2007 году. [6] Наконец, молекула трансаминируется 4-гидроксифенилглицинтрансферазой с использованием тирозина и превращается в DHPG.

4-Гидроксифенилглицинтрансфераза синтезирует (S)-стереоизомер DHPG, однако эпимераза переключает стереоцентр на (R)-конфигурацию после того, как DHPG включается в нерибосомальный полипептид ванкомицина .
Ссылки
[ редактировать ]- ^ Jump up to: а б с Вишневский К.; Автомобиль, Х. (2002). «( S )-3,5-ДГПГ: обзор» . Препараты для ЦНС. Ред. 8 (1): 101–116. дои : 10.1111/j.1527-3458.2002.tb00218.x . ПМК 6741645 . ПМИД 12070529 .
- ^ Мюллер, П.; Шютте, HR (май 1968 г.). « М -Гидроксифенилглицин и 3,5-дигидроксифенилглицин, 2 новые аминокислоты из латекса Euphorbia helioscopia » . З. Натурфорш. Б (на немецком языке). 23 (5): 659–663. дои : 10.1515/znb-1968-0516 . ПМИД 4385921 . S2CID 94822221 .
- ^ Йим, Г., Такер, М.Н., Котева, К., Райт, Г. «Биосинтез гликопептидных антибиотиков». Журнал антибиотиков , 2017 , 67 , 31-41.
- ^ Пфайфер, В., Николсон, Г.Дж., Райс, Дж., Ректенволк, Дж., Шефер, А.Б., Шоуки, Р.М., Шредер, Дж., Воллебен, В., Пельцер, С. «Поликетидсинтаза в биосинтезе гликопептидов: Биосинтез непротеогенной аминокислоты (S)-3,5-дигидроксифенилглицина». Журнал биологической химии , 2001 , 276 (42/19), 38370-38377.
- ^ Чен, Х., Ценг, К.С., Хаббард, Б.К., Уолш, К.Т. «Биосинтез гликопептидных антибиотиков: ферментативная сборка выделенной аминокислотной мономии (S)-3,5-дигидроксифенилглицина». ПНАС , 2001 , 98 (26), 14901-14906.
- ^ Видбум, П.Ф., Филдинг, Э.Н., Лю, Ю., Брунер, С.Д. «Структурная основа независимого от кофактора диоксигенирования при биосинтезе ванкомицина». Природа , 2007 , 447 , 342-345.