Газовая хроматография
Эта статья нуждается в дополнительных цитатах для проверки . ( ноябрь 2020 г. ) |
 Газовый хроматограф с парофазным пробоотборником | |
| Акроним | ГК |
|---|---|
| Классификация | Хроматография |
| Аналиты |
|
| Другие методы | |
| Связанный | |
| через дефис | Газовая хроматография-масс-спектрометрия |
Газовая хроматография ( ГХ ) – распространенный тип хроматографии, используемый в аналитической химии для разделения и анализа соединений, которые могут испаряться без разложения . Типичное использование ГХ включает проверку чистоты определенного вещества или разделение различных компонентов смеси. [1] В препаративной хроматографии ГХ можно использовать для получения чистых соединений из смеси. [2] [3]
Газовую хроматографию также иногда называют парофазной хроматографией ( VPC ) или газожидкостной распределительной хроматографией ( GLPC ). Эти альтернативные названия, а также соответствующие им сокращения часто используются в научной литературе. [2]
Газовая хроматография — это процесс разделения соединений в смеси путем введения газообразного или жидкого образца в подвижную фазу, обычно называемую газом-носителем, и пропускания газа через неподвижную фазу. Подвижная фаза обычно представляет собой инертный газ или нереакционноспособный газ, такой как гелий , аргон , азот или водород . [1] Неподвижная фаза может быть твердой или жидкой, хотя сегодня в большинстве систем ГХ используется полимерная жидкая неподвижная фаза. [4] Неподвижная фаза содержится внутри разделительной колонны. Сегодня большинство колонок ГХ представляют собой капилляры из плавленого кварца с внутренним диаметром 100–320 микрометров (0,0039–0,0126 дюйма) и длиной 5–60 метров (16–197 футов). Колонка ГХ расположена внутри печи, где можно контролировать температуру газа, а выходной поток, выходящий из колонки, контролируется подходящим детектором. [1]
Принцип работы
[ редактировать ]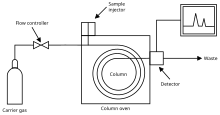
Газовый хроматограф состоит из узкой трубки, известной как колонка , через которую проходит испаренный образец, увлекаемый непрерывным потоком инертного или нереакционноспособного газа. Компоненты пробы проходят через колонку с разной скоростью, в зависимости от их химических и физических свойств и возникающих в результате взаимодействий с футеровкой или наполнителем колонки, называемой стационарной фазой . Колонку обычно помещают в печь с контролируемой температурой. Когда химические вещества выходят из конца колонны, они обнаруживаются и идентифицируются электронным способом. [1]
История
[ редактировать ]
Фон
[ редактировать ]Хроматография датируется 1903 годом в работе русского учёного Михаила Семеновича Цветта . [5] которые разделяли растительные пигменты с помощью жидкостной колоночной хроматографии.
Изобретение
[ редактировать ]Изобретение газовой хроматографии обычно приписывают Энтони Т. Джеймсу и Арчеру Дж. П. Мартину . [6] [7] использовалась распределительная хроматография В их газовом хроматографе в качестве принципа разделения , а не адсорбционная хроматография . Популярность газовой хроматографии быстро возросла после разработки пламенно-ионизационного детектора. [8] Мартин и еще один из их коллег, Ричард Синдж , с которым он разделил Нобелевскую премию по химии 1952 года , отметили в более ранней статье [9] что хроматографию можно также использовать для разделения газов. Синг занимался другой работой, а Мартин продолжал работать с Джеймсом.
Прекурсоры для газоадсорбционной хроматографии
[ редактировать ]Немецкий физико-химик Эрика Кремер в 1947 году вместе с австрийским аспирантом Фрицем Прайором разработал то, что можно считать первым газовым хроматографом, который состоял из газа-носителя, колонки, наполненной силикагелем, и детектора по теплопроводности. Хроматограф выставляли на выставке ACHEMA во Франкфурте, но он никого не заинтересовал. [10] Н. К. Тернер вместе с корпорацией Burrell представил в 1943 году массивный прибор, в котором использовалась угольная колонка и пары ртути. Стиг Клаэссон из Уппсальского университета опубликовал в 1946 году свою работу об угольной колонне, в которой также использовалась ртуть. [10] Герхард Гессе, будучи профессором Марбургского университета в Лане, решил проверить распространенное среди немецких химиков мнение о том, что молекулы не могут быть разделены в движущемся газовом потоке. Он установил простую стеклянную колонку, наполненную крахмалом, и успешно разделил бром и йод, используя азот в качестве газа-носителя. Затем он построил систему, которая пропускала инертный газ через стеклянный конденсатор, заполненный силикагелем, и собирала элюированные фракции. [10] Кортни С.Г. Филлипс из Оксфордского университета исследовала разделение в колонке с углем с помощью детектора по теплопроводности. Он посоветовался с Клаэссоном и решил использовать смещение в качестве принципа разделения. Узнав о результатах Джеймса и Мартина, он перешел на распределительную хроматографию. [10]
Колонная технология
[ редактировать ]В ранней газовой хроматографии использовались насадочные колонки, состоящие из блоков длиной 1–5 м и диаметром 1–5 мм, заполненные частицами. Разрешение насадочных колонок было улучшено благодаря изобретению капиллярной колонки, в которой неподвижная фаза нанесена на внутреннюю стенку капилляра. [6]
Физические компоненты
[ редактировать ]Автосамплеры
[ редактировать ]Автосамплер . позволяет автоматически вводить пробу во впускные отверстия Вставка образца вручную возможна, но больше не используется. Автоматическая вставка обеспечивает лучшую воспроизводимость и оптимизацию времени.

Существуют различные типы автосамплеров. Автосамплеры можно классифицировать по вместимости проб (автоинжекторы и автосамплеры, где автоинжекторы могут работать с небольшим количеством проб), по роботизированным технологиям (робот XYZ). [11] против вращающегося робота – наиболее распространенного) или для анализа:
- Жидкость
- Статическое свободное пространство с помощью шприцевой технологии
- Динамическое свободное пространство благодаря технологии конвейерной линии
- Твердофазная микроэкстракция (ТФМЭ)
Впускные отверстия
[ редактировать ]
Входное отверстие колонки (или инжектор) обеспечивает возможность введения пробы в непрерывный поток газа-носителя. Входное отверстие представляет собой деталь, прикрепленную к головке колонны.
Распространенные типы входов:
- Инжектор S/SL (разделенный/неразделенный) – образец вводится в нагретую небольшую камеру с помощью шприца через перегородку – тепло способствует испарению образца и матрицы образца. Затем газ-носитель переносит всю пробу (режим без разделения) или часть (режим разделения) в колонку. В раздельном режиме часть смеси пробы и газа-носителя из инжекционной камеры выбрасывается через разделенное вентиляционное отверстие. Разделенный ввод предпочтителен при работе с образцами с высокими концентрациями аналитов (>0,1%), тогда как ввод без разделения лучше всего подходит для анализа следов с низкими количествами аналитов (<0,01%). В режиме без разделения разделения клапан открывается через заранее установленное время, чтобы удалить более тяжелые элементы, которые в противном случае могли бы загрязнить систему. Это предварительно установленное (без разделения) время должно быть оптимизировано: более короткое время (например, 0,2 минуты) обеспечивает меньшее запаздывание, но потери в ответе, более длительное время (2 минуты) увеличивает запаздывание, но также и сигнал. [12]
- Вход на колонке – здесь образец вводится непосредственно в колонку целиком без нагрева или при температуре ниже точки кипения растворителя. Низкая температура конденсирует образец в узкую зону. Затем колонку и вход можно нагреть, переводя пробу в газовую фазу. Это обеспечивает минимально возможную температуру для хроматографии и предотвращает разложение образцов выше точки кипения.
- Инжектор PTV. Введение пробы с программированием температуры было впервые описано Фогтом в 1979 году. [ нужна ссылка ] Первоначально Фогт разработал эту методику как метод введения больших объемов проб (до 250 мкл) в капиллярную ГХ. Фогт вводил образец в хвостовик с контролируемой скоростью впрыска. Температура лайнера была выбрана несколько ниже температуры кипения растворителя. Низкокипящий растворитель непрерывно испаряли и выпускали через разделительную линию. На основе этой технологии Пой разработал испарительный инжектор с программируемой температурой; ПТВ. Вводя образец при низкой начальной температуре футеровки, можно обойти многие недостатки классических методов горячего впрыска. [ нужна ссылка ]
- Входное отверстие источника газа или клапан переключения газа – газообразные пробы в бутылях для сбора подключаются к шестиходовому переключающему клапану. Поток газа-носителя не прерывается, пока пробу можно расширить в ранее вакуумированную петлю для проб. При переключении содержимое петли отбора проб вводится в поток газа-носителя.
- Система P/T (очистка и улавливание). Инертный газ барботируется через водную пробу, вызывая удаление нерастворимых летучих химикатов из матрицы. Летучие вещества «улавливаются» на абсорбирующей колонке (известной как ловушка или концентратор) при температуре окружающей среды. Затем ловушку нагревают, и летучие вещества направляют в поток газа-носителя. Образцы, требующие предварительного концентрирования или очистки, можно вводить через такую систему, обычно подключаемую к порту S/SL.
Выбор газа-носителя (подвижной фазы) имеет важное значение. Водород имеет диапазон скоростей потока, который по эффективности сравним с гелием. Однако гелий может быть более эффективным и обеспечивать лучшее разделение, если скорость потока оптимизирована. Гелий негорюч и работает с большим количеством детекторов и старых инструментов. Поэтому гелий является наиболее распространенным используемым газом-носителем. Однако за последние годы цена на гелий значительно выросла, в результате чего все большее число хроматографистов переходят на газообразный водород. Историческое использование, а не рациональное рассмотрение, может способствовать продолжению преимущественного использования гелия.
Детекторы
[ редактировать ]Обычно используемыми детекторами являются пламенно-ионизационный детектор (FID) и детектор теплопроводности (TCD). Хотя ТЦД выгодны тем, что они неразрушающие, их низкий предел обнаружения для большинства аналитов препятствует их широкому использованию. [1] ПИД чувствительны в первую очередь к углеводородам и более чувствительны к ним, чем ТЦД. [4] ПИД не могут обнаруживать воду или углекислый газ, что делает их идеальными для анализа органических веществ в окружающей среде. [1] ПИД в два-три раза более чувствителен к обнаружению аналита, чем ТЦД. [1]
ТПД основан на теплопроводности вещества, проходящего вокруг тонкой проволоки из вольфрама и рения, по которому течет ток. [4] В этой установке гелий или азот служат газом-носителем из-за их относительно высокой теплопроводности, которая сохраняет нить накала холодной и поддерживает однородное удельное сопротивление и электрический КПД нити. [4] [13] Когда молекулы аналита элюируются из колонки, смешиваясь с газом-носителем, теплопроводность снижается, а температура нити и удельное сопротивление увеличиваются, что приводит к колебаниям напряжения, что в конечном итоге приводит к срабатыванию детектора. [4] [13] Чувствительность детектора пропорциональна току накала и обратно пропорциональна непосредственной температуре окружающей среды этого детектора, а также скорости потока газа-носителя. [4]
В пламенно-ионизационном детекторе (ПИД) электроды размещаются рядом с пламенем, питаемым водородом/воздухом, вблизи выхода из колонны, и когда углеродсодержащие соединения выходят из колонны, они пиролизуются пламенем. [4] [13] Этот детектор работает только для органических/углеводородсодержащих соединений из-за способности углерода образовывать катионы и электроны при пиролизе, который генерирует ток между электродами. [4] [13] Увеличение тока транслируется и проявляется в виде пика на хроматограмме. ПИД имеют низкие пределы обнаружения (несколько пикограмм в секунду), но они не способны генерировать ионы из карбонилсодержащих углеродов. [4] Совместимые с ПИД газы-носители включают гелий, водород, азот и аргон. [4] [13]
В ПИД иногда поток модифицируется перед входом в детектор. Метанизатор преобразует окись углерода и диоксид углерода в метан , чтобы его можно было обнаружить. Другая технология — это полидуга от Activated Research Inc, которая преобразует все соединения в метан.
Детектор щелочного пламени (AFD) или щелочной пламенно-ионизационный детектор (AFID) имеет высокую чувствительность к азоту и фосфору, подобно АФД. Однако ионы щелочных металлов подаются вместе с газообразным водородом, а не каплями над пламенем. По этой причине AFD не испытывает «усталости» NPD, но обеспечивает постоянную чувствительность в течение длительного периода времени. Кроме того, когда ионы щелочных металлов не добавляются в пламя, AFD работает как стандартный FID. Каталитический детектор горения (CCD) измеряет содержание горючих углеводородов и водорода. Разрядно-ионизационный детектор (DID) использует электрический разряд высокого напряжения для производства ионов.
Пламенно-фотометрический детектор (FPD) использует фотоумножительную трубку для обнаружения спектральных линий соединений, когда они сгорают в пламени. Соединения, элюируемые из колонки, переносятся в водородное пламя, которое возбуждает определенные элементы в молекулах, а возбужденные элементы (P, S, галогены, некоторые металлы) излучают свет определенных характеристических длин волн. [13] Излучаемый свет фильтруется и детектируется фотоумножителем. [4] [13] В частности, эмиссия фосфора составляет около 510–536 нм, а эмиссия серы — 394 нм. [4] [13] При использовании атомно-эмиссионного детектора (АЭД) образец, элюируемый из колонки, поступает в камеру, которая возбуждается микроволнами, индуцирующими плазму. [13] Плазма вызывает разложение образца аналита, а некоторые элементы генерируют спектры атомной эмиссии. [13] Спектры атомной эмиссии преломляются на дифракционной решетке и регистрируются серией фотоумножителей или фотодиодов. [13]
Детектор электронного захвата (ДЗЭ) использует источник радиоактивных бета-частиц (электронов) для измерения степени захвата электронов. ДЭЗ используются для обнаружения молекул, содержащих электроотрицательные/акцепторные элементы и функциональные группы, такие как галогены, карбонил, нитрилы, нитрогруппы и металлоорганические соединения. [4] [13] В детекторах этого типа в качестве газа-носителя подвижной фазы используется азот или 5% метан в аргоне. [4] [13] Газ-носитель проходит между двумя электродами, расположенными в конце колонны, а рядом с катодом (отрицательным электродом) находится радиоактивная фольга, например 63Ni. [4] [13] Радиоактивная фольга испускает бета-частицу (электрон), которая сталкивается с газом-носителем и ионизирует его, генерируя больше ионов, в результате чего возникает ток. [4] [13] Когда молекулы аналита с электроотрицательными/акцепторными элементами или функциональными группами захватывают электроны, что приводит к уменьшению тока, вызывающего отклик детектора. [4] [13]
Азотно-фосфорный детектор (АФД), разновидность термоэмиссионного детектора, в котором азот и фосфор изменяют работу выхода на шарике со специальным покрытием, и измеряется результирующий ток.
Детектор сухой электролитической проводимости (DELCD) использует воздушную фазу и высокую температуру (по Колсену) для измерения хлорированных соединений.
Масс-спектрометр (МС), также называемый ГХ-МС ; высокоэффективный и чувствительный даже в небольшом количестве образца. Этот детектор можно использовать для идентификации аналитов на хроматограммах по их масс-спектру. [14] Некоторые ГХ-МС подключены к ЯМР-спектрометру, который действует как резервный детектор. Эта комбинация известна как ГХ-МС-ЯМР . [ нужна ссылка ] Некоторые системы ГХ-МС-ЯМР подключены к инфракрасному спектрофотометру , который действует как резервный детектор. Эта комбинация известна как ГХ-МС-ЯМР-ИК. Однако следует подчеркнуть, что это случается очень редко, поскольку большинство необходимых анализов можно выполнить исключительно с помощью ГХ-МС. [ нужна ссылка ]
Вакуумный ультрафиолет (ВУФ) представляет собой новейшую разработку детекторов газовой хроматографии. Большинство химических веществ поглощают и имеют уникальные сечения поглощения в газовой фазе в контролируемом диапазоне длин волн ВУФ примерно 120–240 нм. Если сечения поглощения аналитов известны, ВУФ-детектор способен абсолютно определить (без калибровки) количество молекул, присутствующих в проточной ячейке, в отсутствие химических помех. [15]
Ольфактометрический детектор , также называемый GC-O, использует человека-оценщика для анализа запаховой активности соединений. С помощью порта для запаха или порта для обнюхивания можно оценить качество запаха, интенсивность запаха и продолжительность запаховой активности соединения.
Другие детекторы включают детектор электролитической проводимости Холла (ElCD), детектор ионизации гелия (HID), инфракрасный детектор (IRD), детектор фотоионизации (PID), детектор ионизации импульсным разрядом (PDD) и термоэлектронный детектор ионизации (TID). [16]
Методы
[ редактировать ]
Метод представляет собой совокупность условий, в которых работает ГХ для данного анализа. Разработка метода – это процесс определения того, какие условия являются адекватными и/или идеальными для требуемого анализа.
Условия, которые можно изменять для проведения необходимого анализа, включают температуру на входе, температуру детектора, температуру колонки и температурную программу, газ-носитель и скорость потока газа-носителя, стационарную фазу колонки, диаметр и длину, тип входа и скорость потока, размер образца и способ ввода. техника. В зависимости от детектора(ов) (см. ниже), установленных на ГХ, может существовать ряд условий работы детектора, которые также можно изменять. Некоторые ГХ также оснащены клапанами, которые могут изменять маршрут потока пробы и носителя. Время открытия и закрытия этих клапанов может иметь важное значение для разработки метода.
Выбор газа-носителя и скорости потока
[ редактировать ]Типичные газы-носители включают гелий , азот , аргон и водород . [4] [1] Какой газ использовать, обычно определяется используемым детектором, например, для DID в качестве газа-носителя требуется гелий. [1] При анализе проб газа носитель также выбирают исходя из матрицы пробы, например, при анализе смеси в аргоне предпочтительным является аргоновый носитель, поскольку аргон в пробе не проявляется на хроматограмме. Безопасность и доступность также могут влиять на выбор перевозчика.
Чистота газа-носителя также часто определяется детектором, хотя необходимый уровень чувствительности также может играть значительную роль. Обычно используют чистоту 99,995% или выше. Наиболее распространенной степенью чистоты, требуемой современными приборами для большинства чувствительности, является степень 5,0 или чистота 99,999 %, что означает, что в газе-носителе содержится в общей сложности 10 частей на миллион примесей, которые могут повлиять на результаты. Обычно используются самые высокие степени чистоты - 6,0, но необходимость обнаружения на очень низких уровнях в некоторых судебно-медицинских и экологических приложениях привела к необходимости использования газов-носителей с чистотой 7,0, и теперь они коммерчески доступны. Торговые названия типичной чистоты включают «Нулевой класс», «Класс сверхвысокой чистоты (UHP)», «Класс 4,5» и «Класс 5,0».
Линейная скорость газа-носителя влияет на анализ так же, как и температура (см. выше). Чем выше линейная скорость, тем быстрее анализ, но тем меньше разделение между аналитами. Таким образом, выбор линейной скорости представляет собой такой же компромисс между уровнем разделения и продолжительностью анализа, как и выбор температуры колонки. Линейная скорость будет реализована посредством скорости потока газа-носителя относительно внутреннего диаметра колонны.
В ГХ, выпущенных до 1990-х годов, скорость потока носителя контролировалась косвенно, контролируя давление на входе носителя, или «давление в головке колонки». Фактическая скорость потока измерялась на выходе колонки или детектора с помощью электронного расходомера или пузырькового расходомера, и это могло быть сложным, трудоемким и утомительным процессом. Невозможно было изменять настройку давления во время анализа, и поэтому поток во время анализа был практически постоянным. Связь между расходом и давлением на входе рассчитывается с помощью уравнения Пуазейля для сжимаемых жидкостей .
Однако многие современные ГХ измеряют скорость потока электронным способом и электронно контролируют давление газа-носителя для установки скорости потока. Следовательно, давление носителя и скорость потока можно регулировать во время работы, создавая программы давления/расхода, аналогичные температурным программам.
Выбор стационарного соединения
[ редактировать ]Полярность . растворенного вещества имеет решающее значение для выбора стационарного соединения, которое в оптимальном случае будет иметь такую же полярность, как и растворенное вещество Обычными стационарными фазами в открытых трубчатых колоннах являются цианопропилфенилдиметилполисилоксан, карбовакс-полисилоксан, бисцианопропилцианопропилфенилполисилоксан и дифенилдиметилполисилоксан. Для упакованных столбцов доступны дополнительные параметры. [4]
Типы входов и скорости потока
[ редактировать ]Выбор типа входа и метода ввода зависит от того, находится ли образец в жидкой, газовой, адсорбированной или твердой форме, а также от того, присутствует ли матрица растворителя, которую необходимо испарить. Растворенные образцы можно вводить непосредственно в колонку через COC-инжектор, если условия хорошо известны; если матрицу растворителя необходимо испарить и частично удалить, используется инжектор S/SL (наиболее распространенный метод впрыска); газообразные пробы (например, воздушные баллоны) обычно вводятся с использованием системы газовых клапанов; адсорбированные образцы (например, на адсорбентных трубках) вводятся с использованием либо внешнего (действующего или автономного) десорбционного устройства, такого как система продувки и улавливания, либо десорбируются в инжекторе (приложения ТФМЭ).
Размер образца и техника инъекции
[ редактировать ]Впрыск образца
[ редактировать ]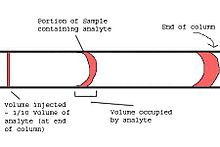
Настоящий хроматографический анализ начинается с внесения образца в колонку. Развитие капиллярной газовой хроматографии привело к возникновению множества практических проблем, связанных с техникой инжекции. Техника введения в колонку, часто используемая с насадочными колонками, обычно невозможна для капиллярных колонок. В системе ввода капиллярного газового хроматографа вводимое количество не должно перегружать колонку иширина впрыскиваемой пробки должна быть небольшой по сравнению с растеканием вследствие хроматографического процесса. Несоблюдение последнего требования приведет к снижению разделительной способности колонны. Как правило, впрыскиваемый объем V inj и объем детекторной ячейки V det должны составлять примерно 1/10 объема, занимаемого частью образца, содержащей интересующие молекулы (аналиты), когда они выходят из столбец.
Некоторые общие требования, которым должна соответствовать хорошая методика ввода, заключаются в том, что должна быть возможность получить оптимальную эффективность разделения колонки, она должна обеспечивать точные и воспроизводимые инъекции небольших количеств репрезентативных проб, она не должна вызывать изменений в составе пробы, она не должна демонстрируют различение, основанное на различиях в температуре кипения, полярности, концентрации или термической/каталитической стабильности, и это должно быть применимо для анализа следов, а также для неразбавленных образцов.
Однако существует ряд проблем, присущих использованию шприцев для инъекций. Даже самые лучшие шприцы заявляют о точности всего в 3%, а в неквалифицированных руках ошибки гораздо больше. Игла может отрезать небольшие кусочки резины от перегородки при введении через нее образца. Они могут заблокировать иглу и помешать наполнению шприца при следующем использовании. Возможно, не очевидно, что это произошло. Часть образца может попасть в резину и высвободиться при последующих инъекциях. Это может привести к появлению фантомных пиков на хроматограмме. Возможна избирательная потеря наиболее летучих компонентов пробы в результате испарения с кончика иглы. [17]
Выбор столбца
[ редактировать ]Выбор колонки зависит от образца и измеряемого активного вещества. Основным химическим признаком, который учитывается при выборе колонки, является полярность смеси, однако функциональные группы могут играть большую роль при выборе колонки. Полярность образца должна точно соответствовать полярности неподвижной фазы колонки, чтобы повысить разрешение и разделение при одновременном сокращении времени анализа. Время разделения и работы также зависит от толщины пленки (неподвижной фазы), диаметра колонки и длины колонки.
Температура колонки и температурная программа
[ редактировать ]
Колонка(и) ГХ находится в печи, температура которой точно контролируется электроникой. (Обсуждая «температуру колонки», аналитик технически имеет в виду температуру термостата колонки. Однако это различие не важно и впоследствии не будет проводиться в этой статье.)
Скорость прохождения образца через колонку прямо пропорциональна температуре колонки. Чем выше температура колонки, тем быстрее образец движется по колонке. Однако чем быстрее проба движется по колонке, тем меньше она взаимодействует с неподвижной фазой и тем меньше разделяются аналиты.
Обычно температура колонки выбирается таким образом, чтобы обеспечить компромисс между продолжительностью анализа и уровнем разделения.
Метод, при котором колонка поддерживается при одной и той же температуре на протяжении всего анализа, называется «изотермическим». Однако большинство методов повышают температуру колонки во время анализа, начальную температуру, скорость повышения температуры («линейное изменение температуры») и конечную температуру называют температурной программой.
Температурная программа позволяет аналитам, которые элюируются на ранних стадиях анализа, адекватно разделяться, одновременно сокращая время, необходимое для прохождения через колонку аналитов, элюирующихся позже.
Обработка и анализ данных
[ редактировать ]Качественный анализ
[ редактировать ]Обычно хроматографические данные представляются в виде графика зависимости отклика детектора (ось Y) от времени удерживания (ось X), который называется хроматограммой. Это обеспечивает спектр пиков образца, представляющий аналиты , присутствующие в образце, элюируемые из колонки в разное время. Время удерживания можно использовать для идентификации аналитов, если условия метода постоянны. Кроме того, характер пиков будет постоянным для образца в постоянных условиях и может идентифицировать сложные смеси аналитов. Однако в большинстве современных приложений ГХ подключается к масс-спектрометру или аналогичному детектору, который способен идентифицировать аналиты, представленные пиками.
Количественный анализ
[ редактировать ]Площадь под пиком пропорциональна количеству аналита, присутствующего на хроматограмме. Рассчитав площадь пика с помощью математической функции интегрирования , можно определить концентрацию аналита в исходном образце. Концентрацию можно рассчитать с помощью калибровочной кривой, созданной путем нахождения отклика для ряда концентраций аналита или путем определения относительного коэффициента отклика аналита. Относительный коэффициент отклика представляет собой ожидаемое соотношение аналита к внутреннему стандарту (или внешнему стандарту ) и рассчитывается путем нахождения отклика известного количества аналита и постоянного количества внутреннего стандарта (химического вещества, добавленного к образцу с постоянной концентрации с четким временем удерживания аналита).
В большинстве современных ГХ-МС систем компьютерное программное обеспечение используется для рисования и интегрирования пиков, а также сопоставления спектров МС со спектрами библиотеки.
Приложения
[ редактировать ]В общем, вещества, которые испаряются при температуре ниже 300 °C (и, следовательно, стабильны до этой температуры), можно измерить количественно. Образцы также не должны содержать соли ; они не должны содержать ионы . Могут быть измерены очень незначительные количества вещества, но часто требуется, чтобы образец измерялся по сравнению с образцом, содержащим чистое подозрительное вещество, известное как эталонный стандарт .
Для повышения значимости показаний можно использовать различные температурные программы; например, чтобы различать вещества, которые ведут себя одинаково во время процесса ГХ.
Специалисты, работающие с ГХ, анализируют состав химического продукта, например, при обеспечении качества продукции в химической промышленности; или измерение химических веществ в почве, воздухе или воде, таких как почвенные газы . [18] ГХ очень точен при правильном использовании и может измерять пикомоли вещества в жидкой пробе объемом 1 мл или концентрации в миллиардных долях в газообразных пробах.
На практических курсах в колледжах студенты иногда знакомятся с ГК, изучая содержание лавандового масла или измеряя уровень этилена , который выделяют растения Nicotiana benthamiana после искусственного повреждения их листьев. Эти ГХ анализируют углеводороды (C2-C40+). В типичном эксперименте насадочная колонка используется для отделения легких газов, которые затем обнаруживаются с помощью ТЗД . Углеводороды помощью отделяются с помощью капиллярной колонки и обнаруживаются с ПИД . Сложность при анализе легких газов, включающих H 2 , заключается в том, что He, который является наиболее распространенным и наиболее чувствительным инертным носителем (чувствительность пропорциональна молекулярной массе), имеет почти идентичную теплопроводность с водородом (это разница в теплопроводности между двумя отдельные нити в виде мостика Уитстона, который показывает, когда компонент элюируется). По этой причине широко распространены приборы с двойным ТПД, используемые с отдельным каналом для водорода, в котором в качестве носителя используется азот. Аргон часто используется при анализе химических реакций в газовой фазе, таких как синтез ФТ, так что можно использовать один газ-носитель, а не два отдельных. Чувствительность снижается, но это компромисс ради простоты подачи газа.
Газовая хроматография широко применяется в судебной медицине . Такие разнообразные дисциплины, как идентификация и количественная оценка дозы твердых наркотиков (в форме перед употреблением), расследование поджогов, анализ сколов краски и токсикологические дела, используют ГХ для идентификации и количественной оценки различных биологических образцов и улик с места преступления.
См. также
[ редактировать ]- Аналитическая химия
- Хроматография
- Газовая хроматография-масс-спектрометрия
- Газовая хроматография-ольфактометрия
- Высокоэффективная жидкостная хроматография
- Обратная газовая хроматография
- Масс-спектрометрия реакции переноса протона
- Вторичная ионизация электрораспылением
- Масс-спектрометрия с проточной трубкой выбранных ионов
- Стандартное дополнение
- Тонкослойная хроматография
- Неразрешенная сложная смесь
Ссылки
[ редактировать ]- ^ Перейти обратно: а б с д и ж г час я Харви, Дэвид (2000). Современная аналитическая химия . Бостон: МакГроу-Хилл. ISBN 0-07-237547-7 . OCLC 41070677 .
- ^ Перейти обратно: а б Павия, Л.; Гэри М. Лэмпман; Джордж С. Криц; Рэндалл Г. Энгель (2006). Введение в органические лабораторные методы (4-е изд.). Томсон Брукс/Коул. стр. 797–817. ISBN 978-0-495-28069-9 .
- ^ «Газовая хроматография» . Линде АГ. Архивировано из оригинала 3 марта 2012 года . Проверено 11 марта 2012 г.
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п д р с Харрис, Дэниел С.; Чарльз А. Люси (2016). Количественный химический анализ (Девятое изд.). Нью-Йорк: WH Freeman & Company. ISBN 978-1-4641-3538-5 . OCLC 915084423 .
- ^ «Отчеты Немецкого ботанического общества т.24 1906 г.» . ХатиТраст . 1883 год . Проверено 19 апреля 2019 г.
- ^ Перейти обратно: а б Бартл, Кейт Д.; Майерс, Питер (10 сентября 2002 г.). «История газовой хроматографии». TrAC Тенденции в аналитической химии . 21 (9): 547–557. дои : 10.1016/S0165-9936(02)00806-3 .
- ^ Джеймс, AT; Мартин, AJP (1 марта 1952 г.). «Газожидкостная распределительная хроматография: разделение и микрооценка летучих жирных кислот от муравьиной до додекановой кислоты» . Биохимический журнал . 50 (5): 679–690. дои : 10.1042/bj0500679 . ПМЦ 1197726 . ПМИД 14934673 .
- ^ Р. А. Дьюар; Маквильям, ИГ (март 1958 г.). «Пламенно-ионизационный детектор для газовой хроматографии» . Природа . 181 (4611): 760. Бибкод : 1958Natur.181..760M . дои : 10.1038/181760a0 . ISSN 1476-4687 . S2CID 4175977 .
- ^ Мартин, AJP; Synge, RLM (1 декабря 1941 г.). «Новая форма хроматограммы с использованием двух жидких фаз: теория хроматографии. 2. Применение к микроопределению высших моноаминокислот в белках» . Биохимический журнал . 35 (12): 1358–1368. дои : 10.1042/bj0351358 . ПМЦ 1265645 . ПМИД 16747422 .
- ^ Перейти обратно: а б с д Эттре, Лесли С. (2008). Главы эволюции хроматографии . Лондон: Издательство Имперского колледжа. ISBN 978-1860949432 .
- ^ Карвалью, Матеус (2018). «Osmar, микрошприцевый автосамплер с открытым исходным кодом» . Аппаратное обеспечениеX . 3 : 10–38. дои : 10.1016/j.ohx.2018.01.001 .
- ^ Честин, Томас Г. «Газовые хроматографические инжекторы с разделением/без разделения и на колонке» . Проверено 6 октября 2019 г.
- ^ Перейти обратно: а б с д и ж г час я дж к л м н тот п Хигсон, С. (2004). Аналитическая химия. Издательство ОКСФОРДСКОГО университета ISBN 978-0-19-850289-0
- ^ Скуг, Дуглас А.; Уэст, Дональд М.; Джеймс Холлер, Ф.; Крауч, Стэнли Р. (1 января 2013 г.). Скуг, Дуглас А.; Уэст, Дональд М.; Холлер, Ф. Джеймс; Крауч, Стэнли Р. (ред.). Основы аналитической химии (Девятое изд.). Бельмонт, Калифорния: Брукс/Коул. ISBN 9780495558286 . OCLC 824171785 .
- ^ Шуг, Кевин А.; Савицкий, Ян; Карлтон, Дуг Д.; Фань, Хуэй; Макнейр, Гарольд М.; Ниммо, Джон П.; Кролл, Питер; Смэтс, Джонатан; Уолш, Филипп; Харрисон, Дейл (1834). «Вакуумный ультрафиолетовый детектор для газовой хроматографии». Аналитическая химия . 86 (16): 8329–35. дои : 10.1021/ac5018343 . ПМИД 25079505 .
- ^ Пул, Колин Ф. (20 ноября 2015 г.). «Ионизационные детекторы для газовой хроматографии». Журнал хроматографии А. 1421 : 137–153. дои : 10.1016/j.chroma.2015.02.061 . ПМИД 25757823 .
- ^ Гроб, Роберт Л.; Барри, Юджин Ф. (2004). Современная практика газовой хроматографии (4-е изд.) . Джон Уайли и сыновья. ISBN 978-0-471-22983-4 .
- ^ Ким, Д; Варгас, Р; Бонд-Ламберти, Б; Турецкий, М (2012). «Влияние повторного увлажнения и оттаивания почвы на потоки почвенных газов: обзор современной литературы и предложения для будущих исследований» . Биогеонауки . 9 (7): 3459–3483. Бибкод : 2012BGeo....9.2459K . дои : 10.5194/bg-9-2459-2012 .
Внешние ссылки
[ редактировать ]![]() СМИ, связанные с газовой хроматографией, на Викискладе?
СМИ, связанные с газовой хроматографией, на Викискладе?
- Хроматографические колонки в библиотеке Chemistry LibreTexts
- Газовая хроматография в Керли