Порфирин
Порфирины ( / ˈ p ɔːr f ər ɪ n / POR -fər-in ) — группа гетероциклических , макроциклических , органических соединений , состоящих из четырех модифицированных пиррольных субъединиц, соединенных между собой у своих α-атомов углерода посредством метиновых мостиков ( =СН- ). У позвоночных существенным членом группы порфиринов является гем , входящий в состав гемопротеинов , в функции которых входит перенос кислорода в кровоток . У растений важным производным порфирина является хлорофилл , который участвует в сборе света и переносе электронов при фотосинтезе .
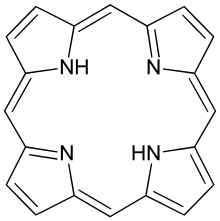
Родителем порфиринов является порфин , редкое химическое соединение, представляющее исключительно теоретический интерес. Замещенные порфины называются порфиринами. [ 1 ] Структура порфиринового кольца, состоящая в общей сложности из 26 π-электронов, из которых 18 π-электронов образуют плоский непрерывный цикл, часто описывается как ароматическая . [ 2 ] [ 3 ] Одним из результатов использования большой сопряженной системы является то, что порфирины обычно сильно поглощают в видимой области электромагнитного спектра, т.е. они имеют глубокую окраску. Название «порфирин» происходит от греческого πορφύρα (порфира) «пурпурный». [ 4 ]
Структура
[ редактировать ]Порфириновые комплексы состоят из плоского квадратного ядра MN 4 . Периферия порфиринов, состоящая из sp 2 -гибридизированные углероды обычно имеют небольшие отклонения от планарности. «Гофрированные» или седловидные порфирины обусловлены взаимодействием системы с окружающей средой. [ 5 ] Кроме того, металл часто не центрируется в плоскости N 4 . [ 6 ] В свободных порфиринах два пиррольных протона взаимно трансформируются и выступают из плоскости N 4 . [ 7 ] Эти неплоские искажения связаны с изменением химических и физических свойств. Хлорофилловые кольца более отчетливо неплоские, но они более насыщены, чем порфирины. [ 8 ]
Комплексы порфиринов
[ редактировать ]Одновременно со смещением двух протонов N- H порфирины связывают ионы металлов в «кармане» N4. металла Ион обычно имеет заряд 2+ или 3+. Показано схематическое уравнение этих синтезов, где M = ион металла и L = лиганд :
- H 2 порфирин + [ML n ] 2+ → M(порфиринат)L n −4 + 4 L + 2 H +
- Типичные порфирины и производные
-
В природе широко распространены производные протопорфирина IX , предшественника гема .
-
Октаэтилпорфирин (H 2 OEP) – синтетический аналог протопорфирина IX. В отличие от природных порфириновых лигандов, ОЭП 2− является высокосимметричным.
-
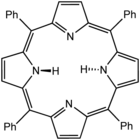
Тетрафенилпорфирин (H 2 TPP) – еще один синтетический аналог протопорфирина IX. В отличие от природных порфириновых лигандов, TPP 2− является высокосимметричным. Другое отличие состоит в том, что его метиновые центры заняты фенильными группами.
-
Упрощенный вид гема , комплекса протопорфирина IX.
-
Макроцикл из 40 молекул порфирина, модель
-
Макроцикл из 40 молекул порфирина, СТМ-изображение
Древние порфирины
[ редактировать ]Геопорфирин, также известный как петропорфирин, представляет собой порфирин геологического происхождения. [ 9 ] Они могут встречаться в сырой нефти , сланце , угле или осадочных породах. [ 9 ] [ 10 ] Абельсонит, возможно, единственный минерал геопорфирина, поскольку порфирины редко встречаются изолированно и образуют кристаллы. [ 11 ]
Область органической геохимии зародилась с выделения порфиринов из нефти. [ нужна ссылка ] Это открытие помогло установить биологическое происхождение нефти. Нефть иногда «отпечатки пальцев» определяют путем анализа следовых количеств никеля и ванадилпорфиринов . [ нужна ссылка ]
Биосинтез
[ редактировать ]У нефотосинтезирующих эукариот , таких как животные, насекомые, грибы и простейшие , а также у бактерий группы α-протеобактерий, обязательным этапом порфиринов биосинтеза является образование δ-аминолевулиновой кислоты (δ-АЛК, 5-АЛК или dALA) в результате реакции аминокислоты глицина с сукцинил -КоА из цикла лимонной кислоты . В растениях , водорослях , бактериях (кроме группы α-протеобактерий) и археях он вырабатывается из глутаминовой кислоты посредством глутамил-тРНК и глутамат-1-полуальдегида . Ферментами, участвующими в этом пути, являются глутамил-тРНК-синтетаза , глутамил-тРНК-редуктаза и глутамат-1-полуальдегид-2,1-аминомутаза . Этот путь известен как путь C5 или путь Била.
Затем две молекулы dALA объединяются порфобилиногенсинтазой с образованием порфобилиногена (PBG), который содержит пиррольное кольцо. Затем четыре PBG объединяются путем дезаминирования в гидроксиметилбилан (HMB), который гидролизуется с образованием кольцевого тетрапиррола уропорфириногена III . Эта молекула претерпевает ряд дальнейших модификаций. Промежуточные соединения используются у разных видов для образования определенных веществ, но у человека основной конечный продукт протопорфирин IX соединяется с железом с образованием гема. Желчные пигменты являются продуктами распада гема.
На следующей схеме обобщен биосинтез порфиринов со ссылками по номеру EC и базе данных OMIM . Также показана порфирия , связанная с дефицитом каждого фермента:

Лабораторный синтез
[ редактировать ]
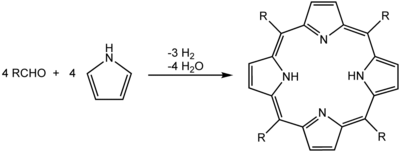
Обычным синтезом порфиринов является реакция Ротемунда , о которой впервые сообщили в 1936 году. [ 12 ] [ 13 ] что также является основой для более поздних методов, описанных Адлером и Лонго. [ 14 ] Общая схема представляет собой процесс конденсации и окисления , начиная с пиррола и альдегида .
Возможные применения
[ редактировать ]Фотодинамическая терапия
[ редактировать ]Порфирины были оценены в контексте фотодинамической терапии (ФДТ), поскольку они сильно поглощают свет, который затем преобразуется в тепло в освещенных областях. [ 15 ] Этот метод был применен при дегенерации желтого пятна с использованием вертепорфина . [ 16 ]
ФДТ считается неинвазивным методом лечения рака, включающим взаимодействие света определенной частоты, фотосенсибилизатора и кислорода. Это взаимодействие приводит к образованию высокореактивных форм кислорода (АФК), обычно синглетного кислорода, а также супероксидного аниона, свободного гидроксильного радикала или перекиси водорода. [ 17 ] Эти высокоактивные формы кислорода реагируют с чувствительными клеточными органическими биомолекулами, такими как; липиды, ароматические аминокислоты и гетероциклические основания нуклеиновых кислот производят окислительные радикалы, которые повреждают клетку, возможно, вызывая апоптоз или даже некроз. [ 18 ]
Молекулярная электроника и сенсоры
[ редактировать ]Соединения на основе порфиринов представляют интерес как возможные компоненты молекулярной электроники и фотоники. [ 19 ] Синтетические порфириновые красители были включены в прототипы сенсибилизированных красителями солнечных элементов . [ 20 ] [ 21 ]
Биологические применения
[ редактировать ]Порфирины исследовались как возможные противовоспалительные средства. [ 22 ] и оценены их противораковая и антиоксидантная активность. [ 23 ] Было обнаружено, что несколько конъюгатов порфирин-пептид обладают противовирусной активностью против ВИЧ in vitro . [ 24 ]
Токсикология
[ редактировать ]Биосинтез гема используется в качестве биомаркера в исследованиях экологической токсикологии. В то время как избыточное производство порфиринов указывает на воздействие хлорорганических соединений , свинец ингибирует фермент дегидратазу АЛК . [ 25 ]
Галерея
[ редактировать ]-
Структура Льюиса мезо -тетрафенилпорфирина
-
Показания УФ-ВИД для мезо -тетрафенилпорфирина
-
Светоактивируемый порфирин. Одноатомный кислород. Клеточное старение
Родственные виды
[ редактировать ]На природе
[ редактировать ]В природе встречается несколько гетероциклов, родственных порфиринам, почти всегда связанных с ионами металлов. К ним относятся
| N4-макроцикл | Имя кофактора | металл | комментарий |
|---|---|---|---|
| хлор | хлорофилл | магний | существует несколько версий хлорофилла (боковая цепь; исключением является хлорофилл c ) |
| бактериохлорин | бактериохлорофилл (частично) | магний | существует несколько версий бактериохлорофилла (боковая цепь; некоторые используют обычное хлориновое кольцо) |
| сирогидрохлорин (изобактериохлорин) | Мне жаль | железо | Важный кофактор в ассимиляции серы. |
| промежуточный продукт биосинтеза на пути к кофактору F430 и B12 | |||
| Коррин | витамин В12 | кобальт | существует несколько вариантов B12 (сайдчейн) |
| корфин | Кофактор F430 | никель | сильно сокращенный макроцикл |
Синтетический
[ редактировать ]Бензопорфирин представляет собой порфирин с бензольным кольцом, конденсированным с одним из пиррольных звеньев. например, вертепорфин представляет собой производное бензопорфирина. [ 26 ]
Неприродные изомеры порфирина
[ редактировать ]
О первом синтетическом изомере порфирина сообщили Эмануэль Фогель и его коллеги в 1986 году. [ 27 ] Этот изомер [18]порфирина-(2.0.2.0) называется порфиценом , а центральная полость N 4 образует прямоугольную форму, как показано на рисунке. [ 28 ] Порфицены продемонстрировали интересное фотофизическое поведение и нашли универсальное соединение для фотодинамической терапии . [ 29 ] Это вдохновило Фогеля и Сесслера взяться за задачу получения [18]порфирина-(2.1.0.1) и назвать его коррфиценом или порфицерином . [ 30 ] О третьем порфирине, [18]порфирин-(2.1.1.0), сообщили Калло и Фогель-Сесслер. Фогель и его коллеги сообщили об успешном выделении [18]порфирина-(3.0.1.0) или изопорфицена . [ 31 ] Японский учёный Фурута [ 32 ] и польский учёный Латос-Гражиньский. [ 33 ] почти одновременно сообщили о N-конфузных порфиринах . Инверсия одной из пиррольных субъединиц в макроциклическом кольце привела к тому, что один из атомов азота был обращен наружу от ядра макроцикла.

См. также
[ редактировать ]- Заболевание, связанное с порфирином: порфирия.
- Порфирин, связанный с железом: гем
- Гемсодержащая группа ферментов: Цитохром P450.
- Порфирин, связанный с магнием: хлорофилл
- Аналоги с коротким атомом углерода: корролы , в том числе витамин B 12 , координированный с кобальтом.
- Корфины, сильно восстановленный порфирин, координированный с никелем, который связывает активный сайт кофактора F430 в метилкоферменте М-редуктазе (MCR).
- Азотзамещенные порфирины: фталоцианин.
Ссылки
[ редактировать ]- ^ Раяти С., Малекмохаммади С. (2016). «Каталитическая активность многостенных углеродных нанотрубок, нанесенных на порфирин марганца (III): эффективный, селективный и многоразовый катализатор окисления алкенов и алканов мочевиной и перекисью водорода» . Журнал экспериментальной нанонауки . 11 (11): 872. Бибкод : 2016JENan..11..872R . дои : 10.1080/17458080.2016.1179802 .
- ^ Иванов А.С., Болдырев А.И. (август 2014 г.). «Расшифровка ароматичности порфириноидов с помощью адаптивного разделения по естественной плотности». Органическая и биомолекулярная химия . 12 (32): 6145–6150. дои : 10.1039/C4OB01018C . ПМИД 25002069 .
- ^ Лэш ТД (2011). «Происхождение ароматического характера в порфириноидных системах». Журнал порфиринов и фталоцианинов . 15 (11н12): 1093–1115. дои : 10.1142/S1088424611004063 .
- ^ Харпер Д., Бульоне, округ Колумбия. «порфирия (сущ.)» . Интернет-словарь этимологии . Проверено 14 сентября 2014 г.
- ^ Сенге М.О., Макгоуэн С.А., О'Брайен Дж.М. (декабрь 2015 г.). «Конформационный контроль кофакторов в природе - влияние индуцированных белками искажений макроциклов на биологическую функцию тетрапирролов». Химические коммуникации . 51 (96): 17031–17063. дои : 10.1039/C5CC06254C . hdl : 2262/75305 . ПМИД 26482230 .
- ^ Уокер Ф.А., Симонис Ю (2011). «Химия железопорфиринов». Энциклопедия неорганической и бионеорганической химии . дои : 10.1002/9781119951438.eibc0104 . ISBN 9781119951438 .
- ^ Дженцен В., Ма Дж.Г., Шелнатт Дж.А. (февраль 1998 г.). «Сохранение конформации порфиринового макроцикла в гемопротеинах» . Биофизический журнал . 74 (2 ч. 1): 753–763. Бибкод : 1998BpJ....74..753J . дои : 10.1016/S0006-3495(98)74000-7 . ПМК 1302556 . ПМИД 9533688 .
- ^ Сенге М.О., Райан А.А., Летчфорд К.А., Макгоуэн С.А., Мильке Т. (2014). «Хлорофиллы, симметрия, хиральность и фотосинтез» . Симметрия . 6 (3): 781–843. Бибкод : 2014Symm....6..781S . дои : 10.3390/sym6030781 . hdl : 2262/73843 .
- ^ Перейти обратно: а б Кадиш К.М., изд. (1999). Справочник по порфиринам . Эльзевир . п. 381. ИСБН 9780123932006 .
- ^ Чжан Б., Lash TD (сентябрь 2003 г.). «Полный синтез порфиринового минерала абельсонита и родственных ему петропорфиринов с пятичленными экзоциклическими кольцами». Буквы тетраэдра . 44 (39): 7253. doi : 10.1016/j.tetlet.2003.08.007 .
- ^ Мейсон Г.М., Труделл Л.Г., Брантавер Дж.Ф. (1989). «Обзор стратиграфического распространения и диагенетической истории абельсонита». Органическая геохимия . 14 (6): 585. Бибкод : 1989OrGeo..14..585M . дои : 10.1016/0146-6380(89)90038-7 .
- ^ Ротемунд П. (1936). «Новый синтез порфиринов. Синтез порфина». Дж. Ам. хим. Соц. 58 (4): 625–627. дои : 10.1021/ja01295a027 .
- ^ Ротемунд П. (1935). «Образование порфиринов из пиррола и альдегидов». Дж. Ам. хим. Соц . 57 (10): 2010–2011. дои : 10.1021/ja01313a510 .
- ^ Адлер А.Д., Лонго Ф.Р., Финарелли Дж.Д., Гольдмахер Дж., Ассур Дж., Корсаков Л. (1967). «Упрощенный синтез мезо -тетрафенилпорфина». Дж. Орг. хим. 32 (2): 476. doi : 10.1021/jo01288a053 .
- ^ Джунтини Ф., Бойл Р., Сибриан-Васкес М., Висенте М.Г. (2014). «Порфириновые конъюгаты для терапии рака». В Кадиш К.М., Смит К.М., Гилард Р. (ред.). Справочник по порфириновой науке . Том. 27. С. 303–416.
- ^ Вормальд Р., Эванс Дж., Смит Л., Хеншоу К. (июль 2007 г.). «Фотодинамическая терапия неоваскулярной возрастной макулярной дегенерации» (PDF) . Кокрейновская база данных систематических обзоров (3): CD002030. дои : 10.1002/14651858.CD002030.pub3 . ПМИД 17636693 .
- ^ Прайс М., Терлеки С.Р., Кессель Д. (2009). «Роль перекиси водорода в проапоптотических эффектах фотодинамической терапии» . Фотохимия и фотобиология . 85 (6): 1491–1496. дои : 10.1111/j.1751-1097.2009.00589.x . ПМЦ 2783742 . ПМИД 19659920 .
- ^ Сингх С., Аггарвал А., Бхупатираджу Н.В., Арианна Г., Тивари К., Дрен СМ (сентябрь 2015 г.). «Гликозилированные порфирины, фталоцианины и другие порфириноиды для диагностики и терапии» . Химические обзоры . 115 (18): 10261–10306. doi : 10.1021/acs.chemrev.5b00244 . ПМК 6011754 . ПМИД 26317756 .
- ^ Льютак Дж.П., Грико Д.Т. (октябрь 2012 г.). «Синтез π-растянутых порфиринов посредством внутримолекулярного окислительного сочетания». Химические коммуникации . 48 (81): 10069–10086. дои : 10.1039/c2cc31279d . ПМИД 22649792 .
- ^ Уолтер М.Г., Рудин А.Б., Вамсер CC (2010). «Порфирины и фталоцианины в солнечных фотоэлектрических элементах». Журнал порфиринов и фталоцианинов . 14 (9): 759–792. дои : 10.1142/S1088424610002689 .
- ^ Йелла А., Ли Х.В., Цао Х.Н., Йи С., Чандиран А.К., Назируддин М.К. и др. (ноябрь 2011 г.). «Сенсибилизированные порфирином солнечные элементы с окислительно-восстановительным электролитом на основе кобальта (II/III) превышают 12-процентную эффективность». Наука . 334 (6056): 629–634. Бибкод : 2011Sci...334..629Y . дои : 10.1126/science.1209688 . ПМИД 22053043 . S2CID 28058582 .
- ^ Алонсо-Кастро А.Дж., Сапата-Моралес-младший, Эрнандес-Мюниве А, Кампос-Ксолальпа Н., Перес-Гутьеррес С., Перес-Гонсалес К. (май 2015 г.). «Синтез, антиноцицептивное и противовоспалительное действие порфиринов». Биоорганическая и медицинская химия . 23 (10): 2529–2537. дои : 10.1016/j.bmc.2015.03.043 . ПМИД 25863493 .
- ^ Баджу Г.Д., Ахмед А., Деви Дж. (декабрь 2019 г.). «Синтез и биологическая активность тетра(4-метоксифенил)порфиринсалицилатов оксованадия(IV)» . БМК Химия . 13 (1): 15. дои : 10.1186/s13065-019-0523-9 . ПМК 6661832 . ПМИД 31384764 .
- ^ Мендонса Д.А., Баккер М., Круз-Оливейра С., Невес В., Хименес М.А., Дефаус С. и др. (июнь 2021 г.). «Проникновение через гематоэнцефалический барьер с помощью новых конъюгатов пептид-порфирин, обладающих анти-ВИЧ-активностью» . Биоконъюгатная химия . 32 (6): 1067–1077. doi : 10.1021/acs.bioconjchem.1c00123 . ПМЦ 8485325 . ПМИД 34033716 .
- ^ Уокер Ч., Силби Р.М., Хопкин С.П., Пикалл Д.Б. (2012). Принципы экотоксикологии . Бока-Ратон, Флорида: CRC Press. п. 182. ИСБН 978-1-4665-0260-4 .
- ^ Скотт Л.Дж., Гоа КЛ (февраль 2000 г.). «Вертепорфин». Наркотики и старение . 16 (2): 139–146, обсуждение 146–8. дои : 10.2165/00002512-200016020-00005 . ПМИД 10755329 . S2CID 260491296 .
- ^ Фогель Э., Колчан М. (март 1986 г.). «Порфицен — новый изомер порфина». Прикладная химия . 25 (3): 257. doi : 10.1002/anie.198602571 .
- ^ Нагамайя Дж., Дутта А., Пати Н.Н., Саху С., Соман Р., Панда П.К. (март 2022 г.). «3,6,13,16-Тетрапропилпорфицен: рациональный синтез, комплексообразование и галогенирование». Журнал органической химии . 87 (5): 2721–2729. дои : 10.1021/acs.joc.1c02652 . ПМИД 35061396 . S2CID 246165814 .
- ^ Догерти Ти Джей (2001). «Основные принципы фотодинамической терапии». Журнал порфиринов и фталоцианинов . 5 (2): 105. дои : 10.1002/jpp.328 .
- ^ Фогель Э., Гилард Р. (ноябрь 1993 г.). «Новые порфиценовые лиганды: октаэтил- и этиопорфицен (OEPc и EtioPc) - тетра- и пентакоординированные цинковые комплексы OEPc». Angewandte Chemie, международное издание . 32 (11): 1600. doi : 10.1002/anie.199316001 .
- ^ Фогель Э., Шольц П., Демут Р., Эрбен С., Бреринг М., Шмиклер Х. и др. (октябрь 1999 г.). «Изопорфицен: четвертый конституционный изомер порфирина с ядром N (4) E/Z-изомерии». Ангеванде Хеми . 38 (19): 2919–2923. doi : 10.1002/(SICI)1521-3773(19991004)38:19<2919::AID-ANIE2919>3.0.CO;2-W . ПМИД 10540393 .
- ^ Хироюки Ф (1994). « «N-путанный порфирин»: новый изомер тетрафенилпорфирина». Дж. Ам. хим. Соц . 116 (2): 767. doi : 10.1021/ja00081a047 .
- ^ Хмелевский П.Я., Латос-Гражинский Л., Рахлевич К., Гловяк Т. (18 апреля 1994 г.). «Тетра-п-толилпорфирин с перевернутым пиррольным кольцом: новый изомер порфирина». Angewandte Chemie, международное издание . 33 (7): 779. doi : 10.1002/anie.199407791 .