Дигидроксифенилглицин

| |
| Имена | |
|---|---|
| Имя IUPAC
( S ) -2-амино-2- (3,5-дигидроксифенил) уксусная кислота
| |
| Другие имена
3,5-дигидроксифенилглицин, DHPG, S-DHPG
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Chemspider | |
| Сетка | 3,5-дигидроксифенилглицин |
PubChem CID
|
|
| НЕКОТОРЫЙ | |
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 8 H 9 № 4 | |
| Молярная масса | 183.05 g mol −1 |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
( S ) -3,5-дигидроксифенилглицин или DHPG является мощным агонистом группы I метаботропных глутаматных рецепторов (MGLURS) MGLUR1 и MGLUR5 .
DHPG был первым агонистом, который, как показано, был селективным для MGLURS группы. [ 1 ] Агонистская активность обнаруживается только в ( S ) -изомере , и ( S ) -DHPG может быть частичным агонистом Mglurs группы I. [ 1 ]
( S ) -DHPG был исследован на предмет терапевтических эффектов при лечении повреждения нейронов (таких как те, которые связаны с ишемией или гипоксией ), когнитивным усилением и болезнью Альцгеймера . [ 1 ]
3,5-дигидроксифенилглицин может быть выделен из латекса эйфхорбийской гелиоскопии . [ 2 ]
DHGP также обнаружен в ванкомицине и связанных с ним гликопептидах . Хотя (S) стереоизомер синтезируется ферментами DPGA-D, [ 3 ] Это (R) стереоизомер, который используется в ванкомицине и других связанных соединениях. DHPG является ферментативно полученным из пути поликетида -синтазы.
Биосинтез
[ редактировать ]При синтезировании в бактериях DHPG требует 5 ферментов, DPGA-D и 4-гидроксифенилглицинетрансферазы (PGAT), чтобы быть синтезированным. [ 4 ] DPGA представляет собой поликетид-синтазу типа III и инициирует синтез путем конденсации ацетил-КоА с тремя молекулами малонил-КоА . Тетра-карбонильное соединение затем циклирует, чтобы сформировать промежуточное соединение C8. DPGB/D затем обезвоживает промежуточное соединение, используя химию enalt для стимулирования потери воды. DPGB/D изомеризует продукт для ароматизации кольца.

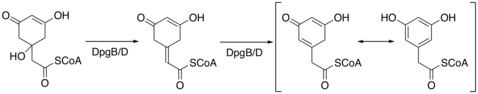
DPGC окисляет ароматическое промежуточное соединение в бензиловом углероде с использованием кислорода в альфа-кето. DPGC выполняет это окисление при отсутствии каких -либо кофакторов железа, гема, флавина или птерина. Чен и др. Предлагают следующий механизм реакции, чтобы объяснить реакционную способность DPGC. [ 5 ] Этот механизм подтверждается результатами, представленными в Widboom et al. В 2007 году. [ 6 ] Наконец, молекула трансхизируется 4-гидроксифенилглицином трансферазой с использованием тирозина, чтобы стать DHPG.

4-гидроксифенилглицин-трансфераза синтезирует (S) стереоизомер DHPG, однако эпимераза переключает стереоцентр на (R) конфигурацию после DHPG, включенной в нерибосомный полипептид ванкомицина .
Ссылки
[ редактировать ]- ^ Jump up to: а беременный в Wiśniewski K.; Car, H. (2002). «( S ) -3,5-DHPG: обзор» . CNS препарат Rev. 8 (1): 101–116. doi : 10.1111/j.1527-3458.2002.tb00218.x . PMC 6741645 . PMID 12070529 .
- ^ Мюллер, П.; Schütte, HR (май 1968 г.). « М -гидроксифенилглицин и 3,5 -дигидроксифенилглицин, 2 новых аминокислоты из латекса эйфхорбийской гелиоскопии » . Z. Naturforsch. Б (на немецком языке). 23 (5): 659–663. doi : 10.1515/Znb-1968-0516 . PMID 4385921 . S2CID 94822221 .
- ^ Yim, G., Thaker, MN, Koteva, K., Wright, G. «Гликопептидный биосинтез антибиотиков». Журнал антибиотиков , 2017 , 67 , 31-41.
- ^ Pfeifer, V., Nicholson, GJ, Ries, J., Recktenwalk, J., Schefer, AB, Shawky, RM, Schröder, J., Wohlleben, W., Pelzer, S. Биосинтез небетратогенной аминокислоты (S) -3,5-дигидроксифенилглицин ". Журнал биологической химии , 2001 , 276 (42/19), 38370-38377.
- ^ Chen, H., Tseng, CC, Hubbard, BK, Walsh, CT "Биосинтехсис антибиотиков гликопептида: ферментативная сборка специальной аминокислотной мономии (ы) -3,5-дигидроксифенилглицин". PNAS , 2001 , 98 (26), 14901-14906.
- ^ Widboom, PF, Fielding, EN, Liu, Y., Bruner, SD «Структурная основа для кофактор-независимой диоксигенации в биосинтезе ванкомицина». Nature , 2007 , 447 , 342-345.