Фикоднавирусиды
| Фикоднавирусиды | |
|---|---|
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область : | Вариднавирия |
| Королевство: | Бэмфордвире |
| Тип: | Нуклеоцитовирикота |
| Сорт: | Мегавирицеты |
| Заказ: | Альгавиралес |
| Семья: | Фикоднавирусиды |
| Роды | |
Phycodnaviridae — семейство крупных (100–560 т.п.н.) двухцепочечных ДНК-вирусов , поражающих морские или пресноводные эукариотические водоросли . Вирусы этого семейства имеют схожую морфологию с икосаэдрическим капсидом (многогранником с 20 гранями). По состоянию на 2014 год в этом семействе насчитывалось 33 вида, разделенных на 6 родов. [ 1 ] [ 2 ] Это семейство принадлежит к супергруппе крупных вирусов, известных как нуклеоцитоплазматические большие ДНК-вирусы . В 2014 году были опубликованы данные, свидетельствующие о том, что определенные штаммы Phycodnaviridae могут заражать людей, а не только виды водорослей, как считалось ранее. [ 3 ] Большинство родов этого семейства проникают в клетку-хозяина путем эндоцитоза клеточных рецепторов и реплицируются в ядре. Фикоднавирусы играют важную экологическую роль, регулируя рост и продуктивность своих водорослей-хозяев. Виды водорослей, такие как Heterosigma akashiwo и род Chrysochromulina, могут образовывать густое цветение, что может нанести ущерб рыболовству и привести к потерям в аквакультуре. [ 4 ] Вирус Heterosigma akashiwo (HaV) был предложен для использования в качестве микробного агента для предотвращения повторения токсичных красных приливов, вызываемых этим видом водорослей. [ 5 ] Фикоднавирусы вызывают гибель и лизис пресноводных и морских видов водорослей, выделяя в воду органический углерод, азот и фосфор, обеспечивая питательные вещества для микробного цикла. [ 6 ]
Таксономия
[ редактировать ]Группа: ДНК двухцепочечная
Таксономия этого семейства изначально основывалась на круге хозяев: хлоровирусы заражают хлореллоподобные зеленые водоросли из пресных вод; тогда как представители остальных пяти родов заражают морские микроводоросли и некоторые виды бурых макроводорослей. Впоследствии это было подтверждено анализом их ДНК-полимераз B-семейства, который показал, что представители Phycodnaviridae более тесно связаны друг с другом по сравнению с другими вирусами с двухцепочечной ДНК, образуя монофилетическую группу. [ 7 ] [ 8 ] [ 9 ] Фикоднавирусы включают шесть родов: Coccolithovirus , Chlorovirus , Phaeovirus , Prasinovirus , Prymnesiovirus и Raphidovirus . Роды можно отличить друг от друга, например, по различиям в жизненном цикле и содержании генов. [ 8 ]
Структура
[ редактировать ]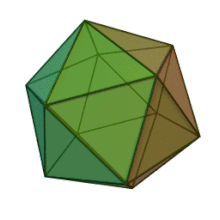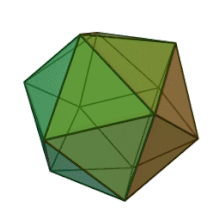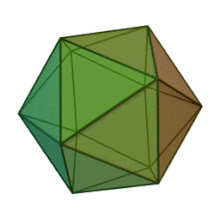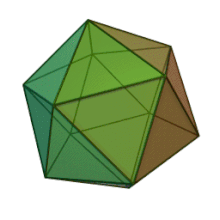
Все шесть родов семейства Phycodnaviridae имеют сходную структуру и морфологию вирионов. Это крупные вирионы, диаметр которых может составлять от 100 до 220 нм. Они имеют двухцепочечный ДНК-геном и белковое ядро, окруженное липидным бислоем и икосаэдрическим капсидом. [ 10 ] Капсид имеет 2-, 3- и 5-кратную ось симметрии с 20 равносторонними треугольными гранями, состоящими из белковых субъединиц. У всех известных представителей Phycodnaviridae капсид состоит из упорядоченных субструктур с 20 трисимметронами и 12 пентасимметронами, состоящими из тримерных капсомеров пончикообразной формы, где каждый капсид состоит из трех мономеров основного капсидного белка. Если все тримерные капсомеры идентичны по структуре, то капсид вириона содержит в общей сложности 5040 копий основного капсидного белка с числом триангуляции 169. В пятикратных вершинах находится 12 пентамеров-капсомеров, состоящих из разных белков. Белок(ы), который находится под осевым каналом каждого пентамера, может отвечать за переваривание стенки клетки-хозяина во время вирусной инфекции. Вид вируса Phaeocystis puchetii из рода Prymnesiovirus имеет самую крупную структуру капсида в семействе Phycodnaviridae . [ 11 ]
Липидная двухслойная мембрана фикоднавирусов недостаточно изучена и изучена. Некоторые исследования показали, что мембрана происходит из эндоплазматической сети, а также может быть получена непосредственно из мембраны клетки-хозяина во время сборки вируса. Хотя члены семейства Phycodnaviridae очень разнообразны, они имеют очень консервативные гены, связанные с морфологией или структурой вирионов. [ нужна ссылка ] Несмотря на сходство структуры капсида фикоднавирусов, недавние эксперименты выявили морфологические различия среди членов этого семейства. Вирус Emiliania huxleyi 86 (EhV-86), штамм кокколитовируса, отличается от своих аналогов водорослевого вируса тем, что его капсид покрыт липидной мембраной. [ 12 ] Кроме того, недавние эксперименты по 3D-реконструкции показали, что вирус хлореллы PBCV-1 имеет цилиндрический шип длиной 250 А, отходящий от одной из его вершин. EhV-86 также может иметь структуру шипа или хвоста. [ 13 ]
Геном
[ редактировать ]Фикоднавирусы известны своими большими геномами двухцепочечной ДНК размером от 100 КБ до более 550 КБ с содержанием GC от 40% до 50%. [ 8 ] В настоящее время доступны полные последовательности генома нескольких членов семейства Phycodnaviridae (включая шесть хлоровирусов, два феовируса, несколько празиновирусов и кокколитовирус), а также имеются некоторые частичные последовательности для другого кокколитовируса. [ 14 ] [ 15 ] [ 16 ] [ 17 ]
Структуры генома фикоднавирусов существенно различаются. Хлоровирус PBCV-1 имеет линейный геном размером 330 т.п.н. с непермутированной двухцепочечной ДНК, ковалентно замкнутой шпильками на концах. Точно так же феовирус EsV-1 имеет линейный геном из двухцепочечной ДНК с инвертированными повторами, которые имеют почти идеальную гомологию. Эти инвертированные повторы могут способствовать эффективной циркуляризации генома, и в течение некоторого времени предполагалось, что EsV-1 имеет кольцевой геном. [ 15 ] Предполагается, что кокколитовирус EhV-86 имеет как линейные, так и кольцевые геномы на разных стадиях упаковки ДНК. ПЦР-амплификация выявляет случайные выступы A/T, обнаружение ДНК-лигаз и эндонуклеаз, намекая на то, что линейный геном может быть упакован и образует циркулярную форму во время репликации ДНК. [ 16 ] [ 18 ] Фикоднавирусы имеют компактные геномы для эффективности репликации: примерно один ген на 900–1000 п.н. последовательностей генома. [ 16 ] Феовирус EsV-1 является исключением: у него 231 ген, кодирующий белок, что означает, что у него есть один ген примерно на 1450 п.н. Несмотря на компактные геномы, обычно встречающиеся у вирусов, геномы Phycodnaviridae имеют повторяющиеся области, обычно вблизи концевых концов, и определенные тандемные повторы, расположенные по всему геному. Предполагается, что эти повторяющиеся последовательности могут играть роль в рекомбинации генов, которая позволяет вирусу обмениваться генетической информацией с другими вирусами или клеткой-хозяином. [ 19 ]
Филогения
[ редактировать ]![Эволюционная история была выведена с использованием метода максимального правдоподобия, основанного на модели на основе матрицы JTT [1]. Дерево консенсуса начальной загрузки, полученное на основе 100 повторов, представляет собой эволюционную историю анализируемых таксонов. Ветви, соответствующие разделам, воспроизведенным менее чем в 50% загрузочных репликах, сворачиваются. Процент повторяющихся деревьев, в которых связанные таксоны сгруппированы вместе в бутстреп-тесте (100 повторов), показан размером красного узла на каждой ветви. Исходные деревья для эвристического поиска были получены автоматически путем применения алгоритмов Neighbor-Join и BioNJ к матрице парных расстояний, оцененных с использованием модели JTT, а затем выбора топологии с превосходным значением логарифмического правдоподобия. В анализе приняли участие 26 аминокислотных последовательностей. Всего в окончательном наборе данных было 2599 позиций. Эволюционный анализ проводился в MEGA7.](http://upload.wikimedia.org/wikipedia/commons/thumb/4/48/Molecular_Phylogenetic_analysis_of_NCLDV_members_by_Maximum_Likelihood_method.png/274px-Molecular_Phylogenetic_analysis_of_NCLDV_members_by_Maximum_Likelihood_method.png)
Вирусы, принадлежащие к Phycodnaviridae, содержат геномы двухцепочечной ДНК размером несколько 100 тыс. пар оснований, которые вместе с другими мегавирусами (например, Iridoviridae , Pandoraviridae и Mimiviridae ) называются ядерно-цитоплазматическими большими ДНК-вирусами . Из-за большого размера генома и различных кодируемых белков вирусы Phycodnaviridae бросают вызов традиционным представлениям о том, что вирусы — это маленькие и простые «организмы на грани жизни». Филогенетический анализ основных генов на основе конкатенации генов, [ 21 ] отдельные филогении ДНК-полимеразы, [ 22 ] и основной белок капсида, [ 23 ] указывают на тесные эволюционные связи между представителями Phycodnaviridae , а также между Phycodnaviridae и другими семействами ядерно-цитоплазматических крупных ДНК-вирусов.
Жизненный цикл
[ редактировать ][ нужна ссылка ]
| Род | Сведения о хосте | Тканевой тропизм | Детали входа | Подробности выпуска | Сайт репликации | Монтажный участок | Передача инфекции |
|---|---|---|---|---|---|---|---|
| Рафидовирус [ 24 ] | Алга | Никто | Эндоцитоз клеточных рецепторов | Лизис | Ядро | Цитоплазма | Пассивная диффузия |
| Кокколитовирус | Алга | Никто | Эндоцитоз клеточных рецепторов | зарождающийся | Ядро | Цитоплазма | Пассивная диффузия |
| феовирус | Алга | Никто | Эндоцитоз клеточных рецепторов | Лизис | Ядро | Цитоплазма | Пассивная диффузия |
| хлоровирус | Алга | Никто | Эндоцитоз клеточных рецепторов | Лизис | Ядро | Цитоплазма | Неизвестный |
| Примнезиовирус | Алга | Никто | Эндоцитоз клеточных рецепторов | Лизис | Ядро | Цитоплазма | Пассивная диффузия |
| Празиновирус | Алга | Никто | Эндоцитоз клеточных рецепторов | Лизис и почкование | Ядро | Цитоплазма | Пассивная диффузия |
Рафидовирус
[ редактировать ]В Рафидовирусе (вероятно, Рафидовирус с ошибкой ) существует только один вид, вирус Heterosigma akashiwo (HaV), который заражает одноклеточную водоросль Heterosigma akashiwo . H. akashiwo является представителем класса Raphidophyceae , вида, образующего цветение, и широко распространен в умеренных и неритических водах. [ 21 ] Были выделены несколько других типов вирусов, инфицирующих H. akashiwo , и их не следует путать с HaV, например, H. akashiwo РНК-вирус (HaRNAV). [ 25 ] и H. akashiwo (HaNIV). вирус ядерного включения [ 26 ] [ 4 ] Поскольку HaV был впервые выделен и охарактеризован в 1997 г., [ 4 ] информация о жизненном цикле ограничена.
HaV специфически инфицирует H. akashiwo и не заражает другие морского фитопланктона . протестированные виды [ 4 ] Механизмы, определяющие специфичность вируса к хозяину, недостаточно изучены. Томару и др. (2008) [ 4 ] предполагают, что специфичность вируса к хозяину может быть вызвана уникальными взаимодействиями между вирусным лигандом и рецептором хозяина. В исследовании Нагаски и др. вирусные частицы были обнаружены внутри цитоплазмы хозяина через 24 часа после заражения. Латентный период или лизогенный цикл оценивался в 30–33 часа со средним размером вспышки (количество вирусов, образующихся после лизиса) 770 на клетку. Вирусные частицы обнаружены в подповерхностной области и в вироплазмы . области [ 5 ]
Кокколитовирус
[ редактировать ]
В 2009 году Маккиндер и др. выяснил механизм проникновения рода Coccolithovirus . [ 12 ] Используя конфокальную и электронную микроскопию , исследователи продемонстрировали, что штамм вируса EhV-86 использует уникальный механизм заражения, который отличается от других вирусов водорослей и демонстрирует большее сходство со стратегиями входа и выхода, наблюдаемыми в большой двухцепочечной нуклеоцитоплазматической ДНК животных. вирусы (нуклеоцитоплазматические крупные ДНК-вирусы). EhV-86 отличается от своих водорослевых аналогов тем, что его капсид покрыт липидной мембраной. EhV-86 проникает в клетки путем эндоцитоза (процесс, при котором частицы пищи или жидкости попадают в клетку посредством пузырька) или прямого слияния (оболочка вируса сливается с мембраной хозяина). Проникновение EhV-86 путем эндоцитоза приводит к образованию дополнительной мембранной оболочки, окружающей инкапсулированный в капсид геном. Независимо от механизма проникновения капсид попадает в цитоплазму в неизмененном виде. После проникновения в клетку вирусный капсид разбирается, и ДНК высвобождается в цитоплазму хозяина или непосредственно в ядро. EhV-86 уникален среди других фикоднавирусов, поскольку кодирует шесть субъединиц РНК-полимеразы. Например, ни PBCV-1, ни ESV-1 не кодируют компоненты РНК-полимеразы. [ 8 ] Гены вирусной РНК-полимеразы не транскрибируются в течение как минимум 2 часов после заражения (pi). На 3–4 пи вирионы собираются в цитоплазме с помощью АТФазы (белка, упаковывающего ДНК) и транспортируются к плазматической мембране, где они высвобождаются из хозяина посредством механизма почкования. В этом механизме почкования EhV-86 получает внешнюю мембрану от мембраны хозяина. [ 12 ] Размер всплеска колеблется от 400 до 1000 частиц на ячейку. [ 8 ]
кластер генов, продуцирующих сфинголипиды У EhV-86 идентифицирован . Исследователи обнаружили, что производство вирусных сфинголипидов, вырабатываемых на литической стадии, участвует в запрограммированной гибели клеток в популяциях кокколитофоров. Была обнаружена высокая корреляция между продукцией гликосфинголипидов (ГСЛ) и активностью каспаз на литической стадии инфицированных клеток. Каспазы — это семейство ферментов протеаз, участвующих в запрограммированной гибели клеток. Исследователи также обнаружили, что для инициации лизиса клеток необходима критическая концентрация GSL (>0,06 мг/мл). Таким образом, авторы предполагают, что продукция GSL до критической концентрации может быть частью механизма синхронизации литического цикла. Авторы также предполагают, что эти биомолекулы могут быть способны индуцировать запрограммированную гибель клеток в других непораженных клетках, тем самым служа сигналом прекращения цветения водорослей. [ 27 ]
феовирус
[ редактировать ]кокколитовирусы и феовирусы Было описано, что имеют противоположные жизненные стратегии. Кокколитовирус обладает стратегией острого жизненного цикла, характеризующейся высокой скоростью размножения и мутаций, а также большей зависимостью передачи вируса от плотной популяции хозяев. Феовирусы обладают устойчивой стратегией жизни, при которой инфекция может вызывать или не вызывать заболевание, а геном передается от родителя к потомству. [ 28 ]
Феовирусы поражают бурые водоросли Ectocarpales , которые относятся к отряду нитчатых бурых водорослей. Одним из наиболее изученных феовирусов является вирус Ectocarpus siliculosus , наиболее известный как EsV-1. [ 28 ] Вирус EsV-1 инфицирует только одноклеточные гаметы или споры E. siliculosus . Вегетативные клетки невосприимчивы к инфекции, так как защищены жесткой клеточной стенкой. [ 29 ] После заражения одна копия вирусной ДНК включается в геном хозяина. Затем вирусный геном EsV-1 реплицируется, и вирионы собираются в спорангиях или гаметангиях инфицированных растений. [ 30 ] Вирусы впоследствии высвобождаются в результате лизиса репродуктивных клеток, стимулируемого изменениями условий окружающей среды, например повышением температуры. [ 31 ] У здоровых растений стимулы окружающей среды синхронизируют выброс гамет и зооспор в окружающую воду. [ 31 ] Свободные вирусные частицы могут затем повторно заразить свободно плавающие гаметы или споры здоровых растений. Зараженные гаметы или споры подвергаются митозу, образуя зараженные растения, и все клетки потомства растения содержат вирусную ДНК. Однако вирусные частицы производятся только в репродуктивных клетках водорослей, а вирусы остаются латентными в вегетативных клетках. В инфицированных спорофитах клетки подвергаются мейозу и образуют гаплоидные споры. Геном EsV передается по менделевскому принципу, при котором половина потомства содержит вирусную ДНК. Часто водоросли из зараженных спор неотличимы от водорослей, полученных из здоровых спор, но частично или полностью неспособны к размножению. [ 29 ] [ 30 ]
хлоровирус
[ редактировать ]Хлоровирусы — единственные охарактеризованные на сегодняшний день вирусы, поражающие пресноводные водоросли. [ 32 ] Хозяевами хлорвирусов являются зоохлореллы, эндосимбиотические зеленые водоросли, обычно ассоциированные с хозяевами Paramecium bursaria , кишечнополостными Hydra viridis или солнечниками Acanthocystis turfacea . [ 33 ] Например, у инфузории Paramecium bursaria водоросли живут внутри клеток хозяина, обеспечивая питательные вещества посредством фотосинтеза. Жизнь внутри клеток инфузории обеспечивает водорослям защиту и способ передвижения. Зоохлореллы устойчивы к инфекции в симбиотическом состоянии. При нарушении взаимоотношений водоросли с хозяином, например, при выпасе веслоногими ракообразными, допускается заражение хлоровирусами. [ 34 ]
жизненный цикл хлоровируса, поражающего Paramecium bursaria , известного как PBCV-1. Подробно изучен [ нужна ссылка ] . Криоэлектронная микроскопия и 3D-реконструкция вирусного капсида показывают, что существует длинная структура-шип, которая сначала контактирует с клеточной стенкой и, вероятно, служит для прокола клеточной стенки хозяина. Вирус PBCV-1 специфичен для своего хозяина, и распознавание опосредовано взаимодействием поверхностных белков вируса с поверхностными углеводами водорослей. После прикрепления вируса к клеточной стенке хозяина гликолитические ферменты, связанные с капсидом, разрушают клеточную стенку. Вирусная мембрана, вероятно, сливается с мембраной хозяина, позволяя вирусной ДНК проникать в цитоплазму, оставляя снаружи пустой капсид. Поскольку у PBCV-1 отсутствует ген РНК-полимеразы, вирусу приходится использовать механизмы клетки-хозяина для производства вирусной РНК. Таким образом, вирусная ДНК быстро перемещается в ядро, где через 5–10 минут после заражения начинается ранняя транскрипция. В течение нескольких минут после заражения происходит хромосомная деградация хозяина, подавляющая транскрипцию хозяина. Через 20 минут после заражения большая часть мРНК в инфицированной клетке представляет собой вирусные мРНК. Белки, транслируемые с ранней стадии транскрипции, участвуют в инициации репликации вирусной ДНК, происходящей через 60–90 минут после заражения. Вторая фаза белков транслируется в цитоплазме, и сборка капсидов вируса начинается примерно через 2–3 часа после заражения. Зрелые вирионы образуются при добавлении вновь реплицированной вирусной ДНК из ядра хозяина, чему, вероятно, способствует кодируемая вирусом ДНК-упаковочная АТФаза. Примерно через 5–6 часов после заражения PBCV-1 цитоплазма заполняется вирионами, а через 6–8 часов после заражения происходит лизис, в результате чего на клетку высвобождается примерно 1000 частиц. [ 32 ] [ 35 ]
Примнезиовирус
[ редактировать ]Род Prymnesiovirus в настоящее время содержит только один вид, известный как вирус Chrysochromulina brevifilum PW1 (CbV-PW1). CbV-PW1 заражает два вида морского фитопланктона, Chrysochromulina brevifilum и C. strobilus , принадлежащие к роду Chrysochromulina . [ 36 ] [ 37 ] По данным базы данных AlgaeBase, в настоящее время в этом роде насчитывается 63 названия морских и пресноводных видов, из которых 48 признаны таксономически приемлемыми названиями. [ 38 ] Chrysochromulina — особенно важный род, поскольку он может составлять более 50% фотосинтезирующих нанопланктонных клеток в океане. [ 36 ]
Мало что известно о жизненном цикле вируса, заражающего планктонные виды, содержащие жгутиконосцы, Chrysochromulina brevifilum и C. strobilus . Саттл и Чан (1995) были первыми, кто выделил вирусы, поражающие примнезиофиты или гаптофиты. В этом исследовании ультратонкие срезы вирусов Chyrsochromulina brevifilum были приготовлены и просмотрены с помощью трансмиссионной электронной микроскопии. [ 36 ] Электронные микрофотографии на ранней стадии инфекции позволяют предположить, что репликация вируса происходит в цитоплазме внутри вироплазмы . Вироплазма — это локализованная область в цитоплазме или вокруг ядра клетки, которая служит «фабрикой репликации вируса». Вироплазма содержит такие компоненты, как генетический материал вируса, белки-хозяева и рибосомы, необходимые для репликации. Виросомы часто окружены мембраной; В ходе исследования было обнаружено, что мембрана, окружающая виросому, содержащуюся в инфицированных клетках, состоит из фибриллярного матрикса. [ 36 ] Вирионы высвобождаются из инфицированных клеток после разрушения органелл и лизиса мембраны клетки-хозяина. Саттл и Чан (1995) насчитали более 320 вирусов в ультратонком срезе инфекционной клетки. [ 36 ] Оценки размеров пакетов варьируются от 320 до 600 вирусов на клетку. [ 39 ]
Празиновирус
[ редактировать ]Представители рода Prasinovirus заражают небольшие одноклеточные зеленые водоросли отряда Mamiellales , обычно встречающиеся в прибрежных морских водах. [ 40 ] Разновидностью рода Prasinovirus является вирус Micromonas pusilla SP1 (MpV-SP1), [ 41 ] который был выделен из пробы воды, собранной в Сан-Диего. [ 42 ] Празиновирус MpV-SP1 инфицирует Micromonas pusilla , который является доминирующим фотосинтезирующим морским пикоукариотом. [ 43 ] и который заражает Micromonas pusilla (UTEX 991, Plymouth 27). Обычными хозяевами празиновирусов являются представители родов Ostreococcus и Micromonas . три потенциальных вида Ostreococcus , которые различаются в зависимости от их требований к освещению. Были идентифицированы [ 44 ] Один из наиболее широко изученных празиновирусов, штамм OtV5, геном которого полностью секвенирован, инфицирует Ostreococcus tauri , самые маленькие из известных в настоящее время свободноживущих эукариотов . [ 45 ]
Празиновирусы используют стратегию ядерно-цитоплазматической репликации, при которой вирионы прикрепляются к поверхности клетки-хозяина с последующей инъекцией ДНК в цитоплазму хозяина. [ 45 ] Исследователи обнаружили, что «пустые» вирусы OtV5 или вирусы, у которых только капсид прикреплен к мембране хозяина, редко наблюдались на любой стадии инфекции, что позволяет предположить, что вирионы отделяются от мембраны хозяина после инъекции их ДНК. Авторы также обнаружили, что значительная часть вирусов не прикрепляется к клеткам после инокуляции, и предполагают, что прикрепление вируса может быть ограничивающим этапом инфекции. Вирусная ДНК затем реплицируется внутри ядра с помощью механизмов клетки-хозяина. Вирусные частицы собираются в цитоплазме, обычно занимая пространство вблизи внутренней поверхности ядра. Из-за чрезвычайно малого размера клеток водорослей средний размер вспышки составил 25 вирусных частиц на клетку. [ 45 ]
наблюдалось производство вируса без лизиса клеток Недавно в клетках O. tauri . Томас и др. (2011) обнаружили, что в резистентных клетках-хозяевах вирусный геном реплицируется, и вирусы высвобождаются посредством механизма почкования. [ 46 ] Такая низкая скорость высвобождения вируса при почковании обеспечивает длительную выживаемость хозяина и потомства вируса, что приводит к стабильному сосуществованию. [ 47 ]
Кодируемые белки
[ редактировать ]Вирус Ectocarpus siliculosus (EsV-1), принадлежащий к роду Phaeovirus , и вирус Paramecium bursaria chromella (PBCV-1), принадлежащий к роду Chlorovirus , представляют собой два хорошо изученных вируса, чьи геномы, как было обнаружено, кодируют множество белков. Эти белки участвуют в обеспечении стабильности вируса, синтезе ДНК, транскрипции и других важных взаимодействиях с хозяином. [ нужна ссылка ]
Ферменты гликозилирования
[ редактировать ]PBCV-1 содержит гликозилированный основной капсидный белок массой 54 кДа, который составляет около 40% общего вирусного белка. [ 12 ] В отличие от большинства структурных белков вируса, которые гликозилируются в эндоплазматическом ретикулуме (ЭР) и аппарате Гольджи , кодируемых хозяином с помощью гликозилтрансфераз . [ 48 ] PBCV-1 независимо гликозилирует свой основной капсидный белок, кодируя большинство ферментов, необходимых для построения сложных олигосахаридов, которые затем прикрепляются к основному капсидному белку PBCV-1 с образованием гликопротеина. Следовательно, гликозилирование основного капсидного белка PBCV-1 происходит независимо от ЭР и аппарата Гольджи в клетках-хозяевах. [ 49 ]
Белки ионных каналов
[ редактировать ]Первый известный вирусный белок, который действует как калий-селективный ионный канал, был обнаружен в PBCV-1. [ 50 ] Белок (называемый Kcv) состоит из 94 аминокислот и кодируется небольшой открытой рамкой считывания ( ORF ) (ORF A250R) в PBCV-1, которая может производить калий-селективную и чувствительную к напряжению проводимость в Xenopus ооцитах . [ 50 ] Предполагаемый белок PBCV-1 имеет короткий цитоплазматический N-конец (12 аминокислот), содержащий один консенсусный сайт протеинкиназы C, и два трансмембранных домена. Различные аминокислотные последовательности и отсутствие COOH-концевого цитоплазматического хвоста отличают белок Kcv от других калиевых каналов. [ 50 ] [ 29 ]
EsV-1 кодирует ORF из 124 кодонов, которая имеет значительное аминокислотное сходство с PBCV-1 Kcv (41% идентичности аминокислот). [ 29 ] Однако белок EsV-1 имеет более длинный N-конец (35 аминокислот), содержащий два консенсусных сайта протеинкиназы C, и три трансмембранных домена. [ 29 ] Неизвестно, может ли белок EsV-1 образовывать функциональный канал в гетерологичных клетках. Геном EsV-1 также кодирует несколько белков с богатыми гидрофобными аминокислотами областями, которые напоминают спиральные трансмембранные домены. Среди этих белков входной домен предполагаемой гибридной His-киназы 186 и ORF 188 напоминают белки ионных каналов. [ 45 ]
Белки, связанные с репликацией ДНК
[ редактировать ]И EsV-1, и PBCV-1 кодируют ДНК-полимеразу , принадлежащую к семейству ДНК-полимераз-δ, и все они содержат корректирующий 3'-5' экзонуклеазный домен. [ 51 ] Кроме того, как PBCV-1, так и EsV-1 кодируют белок фактора процессивности скользящего зажима (PCNA), который взаимодействует с белками, участвующими в репликации ДНК, а также с белками, участвующими в репарации ДНК и пострепликативном процессинге (например, ДНК-метилазами и ДНК-транспозазами). [ 52 ]
Гетеропентамерный фактор репликации C (RFC) представляет собой комплекс, который отвечает за АТФ-зависимую загрузку PCNA на ДНК; [ 53 ] [ 54 ] EsV-1 кодирует пять белков, которые могут образовывать комплекс RFC. PBCV-1 кодирует единственный белок, который напоминает белок, обнаруженный в комплексе Archae RFC. [ 45 ] PBCV-1 также кодирует другие белки, участвующие в репликации ДНК, включая АТФ-зависимую ДНК-лигазу . [ 55 ] типа II ДНК-топоизомераза и РНКаза H. [ 29 ] Хотя и EsV-1, и PBCV-1 обладают генами основных элементов системы репликации эукариот, ни один из них не имеет полных репликативных генов, поскольку у них всех отсутствуют гены примазы. [ 12 ] [ 29 ]
Связанные с транскрипцией белки
[ редактировать ]Ни EsV-1, ни PBCV-1 не кодируют полную РНК-полимеразу , но они продуцируют несколько белков, подобных фактору транскрипции, для помощи транскрипционной системе хозяина. [ нужна ссылка ]
EsV-1 кодирует два небольших полипептида (ORF 193 и ORF 196) для регуляции транскрипции; белки напоминают домен α/β/α субъединицы TFIID -18. [ 45 ] Комплекс TFIID необходим для транскрипции эукариот, поскольку он связывается с ТАТА-боксом в основном промоторе гена, чтобы инициировать сборку РНК-полимеразы. Кроме того, полипептиды напоминают домены SET, BTB/POZ (т.е. Broad Complex, Tramtrack и Bric-a-brac/poxvirus и цинковый палец) (ORF 40) и BAF60b (ORF 129) также кодируются ESV-1 для регулируют ремоделирование хроматина и репрессию транскрипции. [ 45 ] [ 12 ] [ 56 ]
В PBSV-1 были обнаружены четыре белка, подобные фактору транскрипции, включая TFIIB (A107L), TFIID (A552R), TFIIS (A125L) и фактор транскрипции типа VLTF-2 (A482R). [ 29 ] Кроме того, PBCV-1 также кодирует два фермента, участвующих в формировании кэп-структуры мРНК: РНК-трифосфатазу. [ 57 ] и мРНК гуанилилтрансфераза . [ 58 ] Ферменты PBCV-1 более тесно связаны с ферментами дрожжей, чем с многофункциональными РНК-кэпирующими ферментами поксвируса по размеру, аминокислотной последовательности и биохимическим свойствам. [ 59 ] [ 58 ] PBCV-1 также кодирует РНКазу III , которая участвует в процессинге мРНК вируса. [ 29 ]
Белки, связанные с нуклеотидным метаболизмом
[ редактировать ]Чтобы обеспечить дезоксинуклеотиды для производства вирусов в низкопролиферирующих клетках-хозяевах, крупные ДНК-вирусы обладают генами, кодирующими сами ферменты синтеза дезоксинуклеотидов. [ 29 ] В PBCV-1 обнаружено тринадцать нуклеотидных метаболических ферментов, два из которых включают пирофосфатазу dUTP и деаминазу dCMP , которые могут продуцировать dUMP (т.е. субстрат для тимидилатсинтетазы). [ 60 ] Для сравнения, EsV-1 кодирует только АТФазу (ORF 26), а также обе субъединицы рибонуклеотидредуктазы (ORF 128 и 180), которая является ключевым ферментом в синтезе дезоксинуклеотидов. [ 45 ]
Другие ферменты
[ редактировать ]Другие ферменты, такие как метилтрансферазы , эндонуклеазы рестрикции ДНК и интеграза , также были обнаружены в PBCV-1. [ 12 ] [ 29 ] PBCV-1 также кодирует белок, состоящий из 187 аминокислот, который напоминает Cu-Zn SOD со всеми консервативными аминокислотными остатками для связывания меди и цинка, который может разлагать быстро накопленный супероксид в клетках-хозяевах во время инфекции, тем самым улучшая репликацию вируса. . [ 61 ]
Экологические последствия
[ редактировать ]Рафидовирус
[ редактировать ]
Heterosigma akashiwo образует густое вредоносное цветение в водах умеренного и субарктического пояса с плотностью до 5 × 10. 6 клеток/мл. [ 62 ] Цветение водорослей может быть чрезвычайно вредным для водной флоры и фауны, вызывая гибель дикой и культивируемой рыбы, такой как лосось, желтохвост и морской лещ. [ 5 ] Интенсивность и продолжительность этого цветения варьируются в зависимости от года, а ущерб аквакультуре от H.akashiwo увеличивается. В 1989 году ядовитое цветение водорослей у побережья Новой Зеландии привело к потере чавычи на сумму семнадцать миллионов новозеландских долларов. В 1995 и 1997 годах в прибрежных водах Японии в заливе Кагосимо было убито рыбы на сумму 1 090 миллионов и 327 миллионов иен соответственно. [ 5 ]
вирус HaV, инфицирующий H. akashiwo, Было показано, что является фактором прекращения цветения. Саттл и др. (1990) предположили, что вирусная инфекция водорослей может играть роль в регулировании плотности популяций сообществ фитопланктона, тем самым играя значительную роль в их динамике в океанах. [ 63 ] Более ранние исследования, такие как исследование Nagasaki et al. (1993) исследовали динамику между HaV и H. akashiwo . Образцы водорослей были получены на средней или последней стадии красного прилива в заливе Хиросима , Япония. Используя просвечивающую электронную микроскопию , Нагаски и др. идентифицировали вирус HaV внутри и вокруг ядерной области клеток H. akashiwo . [ 63 ] Дальнейшее подтверждение роли вируса HaV в прекращении цветения было предоставлено исследованием, проведенным Nagaski et al. (1994). Нагаски и др. (1994) обнаружили, что доля вируссодержащих клеток быстро увеличивалась перед окончанием красного прилива; за три дня до окончания красного прилива вируссодержащие клетки не обнаружены, а в пробе, собранной в последний день, выявлена высокая частота (11,5%) вируссодержащих клеток. [ 64 ]
Дальнейшие исследования Тарутани и др. (2000) также обнаружили связь между уменьшением плотности клеток H. akashiwo и увеличением численности HaV. Исследователи обнаружили, что HaV не только играет важную роль в контроле биомассы, но также влияет на клональный состав или характеристики клеток H. akashiwo . Исследователи обнаружили, что большинство изолятов после прекращения цветения были устойчивы к клональным изолятам HaV, тогда как во время формирования цветения устойчивые клетки были второстепенным компонентом. Авторы предполагают, что вирусная инфекция в период окончания цветения влияет на свойства доминантных клеток в H. akashiwo . популяциях [ 65 ] Селективное давление, оказываемое вирусами на более поздней стадии заражения, может способствовать генетическому разнообразию, позволяя популяции H. akashiwo процветать после прекращения цветения. [ нужна ссылка ]
Как уже упоминалось, цветение H. akashiwo губительно для популяций рыб в умеренных и субарктических водах и продолжает представлять серьезную угрозу для аквакультуры. Нагасаки и др. (1999) изучили характеристики роста HaV и предположили, что HaV можно использовать в качестве микробного агента против красных приливов H. akashiwo . Преимущество использования HaV заключается в том, что он специфически заражает H. akashiwo, даже когда присутствуют другие микроорганизмы. Кроме того, он имеет высокую скорость роста и может производиться с низкой себестоимостью. Использование HaV в качестве микробного агента является многообещающим решением для ликвидации красных приливов и защиты рыболовства и морской жизни, но, как пришли к выводу авторы, влияние различных клонов HaV на популяции H. akashiwo необходимо изучить более подробно, прежде чем вирус будет использоваться для широкомасштабные приложения. [ 5 ]
Кокколитовирус
[ редактировать ]
Кокколитовирус ) (EhV) поражает кокколитофор Emiliania huxleyi ( E. huxleyi . Кокколитофоры — морские гаптофиты , окруженные микроскопическими пластинками из карбоната кальция . [ 66 ] Они обитают в верхних слоях мирового океана и представляют третью по численности группу фитопланктона, насчитывающую около 300 видов. [ 67 ] E. huxleyi признан наиболее известным и экологически важным из кокколитофоров. E. huxleyi имеет глобальное распространение от тропиков до субарктических вод и иногда образует густое цветение, которое может покрывать территорию в 100 000 квадратных километров. [ 67 ] Эти триллионы кокколитофоров производятся, затем умирают и опускаются на дно океанов, способствуя образованию отложений, и являются крупнейшими производителями кальцита в океанах. [ 66 ] Таким образом, кокколиты играют важную роль в глобальной фиксации углерода и углеродном цикле, а также в круговороте серы. [ 67 ] Со временем кокколитофоры сформировали геологические особенности нашей планеты. Например, Белые скалы Дувра образовались из белого мела или карбоната кальция, вырабатываемого кокколитофорами в течение миллионов лет. [ нужна ссылка ]
Цветение кокколитофор обычно не вредно для морской жизни в океане. Поскольку эти организмы процветают в условиях скудных питательных веществ, кокколитофоры служат источником питания для мелкой рыбы и зоопланктона . [ 66 ] E. huxylei вирусы ( EhV Было показано, что ) связаны с прекращением этого цветения. О завершении стадии цветения свидетельствует изменение цвета воды. Когда большое количество кокколитов (карбонатная оболочка, окружающая E. huxylei ) выделяется из клеток E. huxylei в результате гибели или лизиса клеток, вода становится белой или бирюзовой. В районах прекращения интенсивного цветения белый цвет является отражающим и его можно увидеть на спутниковых снимках. [ 67 ] Уилсон и др. (2002) использовали аналитическую проточную цитометрию для измерения численности вирусов в различных местах в зоне цветения и вокруг нее. Исследователи обнаружили, что концентрации вирусов были выше внутри «области с высокой отражательной способностью», что позволяет предположить, что индуцированный вирусом лизис клеток E. huxleyi приводит к отслоению кокколита. [ 68 ] Другие исследования Martinez et al. (2007) и Братбак и др. (1993) обнаружили более высокие концентрации вирусов EhV по мере снижения цветения E. huxleyi , что указывает на то, что литическая вирусная инфекция была основной причиной прекращения цветения. [ 69 ] [ 70 ] Таким образом, вирусы EhV играют важную роль в регулировании производства биомассы в морской среде и экологической преемственности. Таким образом, такое регулирование популяций кокколитофоров вирусами EhV оказывает значительное влияние на биогеохимические циклы , особенно на углеродный цикл . [ нужна ссылка ]
феовирус
[ редактировать ]
Один из наиболее изученных феовирусов, EsV-1, поражает мелкие нитчатые бурые водоросли E. siliculosus , имеющие космополитическое распространение (встречающиеся в большинстве океанов мира). [ 29 ] Ectocarpales , которые являются наиболее экономически важной тесно связаны с группой бурых водорослей Laminariales группой бурых водорослей, имеющей широкий спектр применения в косметической и пищевой промышленности. [ 71 ]
Мюллер и др. (1990) были одними из первых, кто исследовал причины дефектов гаметангиев у E. siliculosus, происходящего из Новой Зеландии. Исследователи идентифицировали репродуктивные клетки E. siliculosus, наполненные гексагональными частицами, которые затем высвобождались в культуральную среду, когда клетки лопались. После высвобождения этих частиц спорофиты заразились, о чем свидетельствуют патологические симптомы, позволяющие предположить, что эти частицы являются вирусами. [ 72 ] Такие исследования позволили оценить инфекционный потенциал вирусов E. siliculosus . Используя ПЦР-амплификацию фрагмента вирусного гена, Muller et al. (2005) отслеживали уровни заражения патогенами в образцах Ectocarpus с острова Гран-Канария, в Северной Атлантике и на юге Чили. Исследователи обнаружили высокий уровень распространенности патогенов; 40–100% экземпляров Ectocarpus содержали вирусную ДНК. [ 73 ] Аналогичные оценки были даны Sengco et al. (1996), которые подсчитали, что по крайней мере 50% растений Ectocarpus в мире содержат вирусную ДНК. [ 74 ] Такая высокая частота вирусных инфекций среди глобально распространенных растений Ectocarpus имеет экологические последствия. Вирусная инфекция EsV-1 растений E. siliculosus , как уже упоминалось, ограничивает репродуктивный успех инфицированных растений. Таким образом, вирус EsV-1 играет ключевую роль в регулировании популяций E. siliculosus , оказывая дальнейшее влияние на динамику местной экосистемы. [ нужна ссылка ]
хлоровирус
[ редактировать ]
Представители рода Chlorovirus встречаются в пресноводных источниках по всему миру и заражают симбионты зеленых водорослей зоохлореллы. Информации о роли хлоровирусов в экологии пресной воды недостаточно. [ 75 ] Несмотря на это, хлорвирусы обнаруживаются в природных водах в концентрации 1–100 бляшкообразующих единиц (БОЕ)/мл, а измерения достигают 100 000 БОЕ/мл природной воды. [ 8 ] Единица образования бляшек — это количество частиц, способных образовывать видимые структуры внутри клеточной культуры, известные как бляшки. [ нужна ссылка ] Численность хлоровирусов варьируется в зависимости от сезона, при этом самая высокая численность приходится на весну. [ 8 ] Хлоровирусы, такие как PBCV-1, играют роль в регулировании популяции зоохлореллы-хозяина. Как уже говорилось ранее, заражение зоохлореллой происходит только при нарушении симбиотических отношений с хозяином. Заражение водорослей на этой стадии независимости хозяина/водорослей будет препятствовать восстановлению отношений между хозяином и водорослями, тем самым снижая выживаемость эндосимбиотических хозяев зоохлорелл, таких как Paramecium bursaria. Таким образом, хлоровирусы играют важную роль в пресноводных экосистемах, регулируя не только популяции своих хозяев, зоохлорелл, но и в некоторой степени регулируя и популяции хозяев-зоохлорелл. Хлоровирусы и вирусы в целом вызывают гибель и лизис своих хозяев, выделяя в воду растворенный органический углерод, азот и фосфор. Эти питательные вещества затем могут быть поглощены бактериями, тем самым внося свой вклад в микробный цикл. Высвобождение растворенных органических материалов обеспечивает рост бактерий, а бактерии являются важным источником питания для организмов на более высоких трофических уровнях. Следовательно, хлорвирусы оказывают значительное воздействие на потоки углерода и питательных веществ, влияя на динамику пресноводных экосистем. [ 6 ]
Примнезиовирус
[ редактировать ]Примнезиовирус, CbV-PW1, как уже упоминалось, инфицирует водоросли рода Chyrsochromulina . Хирсохромулина , встречающаяся в пресных и морских водах по всему миру, иногда образует густое цветение, которое может выделять вредные токсины, оказывая негативное воздействие на рыболовство. [ 36 ] Особо токсичный вид C.polylepis нанес огромный ущерб коммерческому рыболовству в Скандинавии. В 1988 году это цветение привело к потере 500 тонн рыбы в клетках на сумму 5 миллионов долларов США. [ 76 ] Учитывая, что Chyrsochromulina является широко распространенным видом и имеет важное экологическое значение, вирусная инфекция и лизис представителей рода, вероятно, окажут существенное влияние на биогеохимические циклы, такие как рециркуляция питательных веществ в водной среде. Саттл и Чен предполагают, что присутствие вирусов должно оказывать сильное регулирующее воздействие на популяции Chyrsochromulina , тем самым предотвращая образование цветения или обеспечивая прекращение цветения, что объясняет, почему стойкое цветение является необычным явлением в природе. [ 36 ]
Празиновирус
[ редактировать ]Как уже упоминалось, широко изучаемый празиновирус OtV5 инфицирует самый маленький из известных в настоящее время эукариот, Ostreococcus tauri . O. tauri имеет диаметр около 0,8 микрометра и находится в пределах пикоразмерной фракции (0,2–2 микрометра). Пикоукариоты, такие как Ostreococcus tauri, широко распространены и вносят значительный вклад в микробную биомассу и общую первичную продуктивность. В олиготрофных средах морской пикофитопланктон составляет до 90% автотрофной биомассы и, таким образом, является важным источником пищи для нанопланктонных и фаготрофных простейших. [ 77 ] Поскольку пикоэукариоты служат основой морских микробных пищевых сетей, они необходимы для выживания более высоких трофических уровней. Ostreococcus tauri имеет быструю скорость роста, и густое цветение наблюдалось у берегов Лонг-Айленда и Калифорнии. [ 77 ] Было обнаружено, что образцы, собранные в заливе Лонг-Айленд, содержат множество вирусоподобных частиц, что, вероятно, является причиной прекращения цветения. [ 78 ] Несмотря на большое количество пикоэукариот, число этих одноклеточных организмов превосходит вирусы примерно в десять раз. [ 79 ] Вирусы, такие как OtV5, играют важную роль в регуляции популяций фитопланктона и посредством лизиса клеток способствуют возврату питательных веществ обратно в сторону других микроорганизмов, что также известно как вирусный шунт . [ 80 ]
Как уже упоминалось, празиновирус MpV-SP1 поражает Micromonas pusilla , который является основным компонентом пикофитопланктона мирового океана. M. pusilla обитает в тропических и полярных морских экосистемах. [ 81 ] Коттрелл и Саттл (1995) обнаружили, что 2–10% популяции M. pusilla в прибрежной среде подвергались лизису в день, в среднем 4,4%. [ 43 ] Более высокие оценки были даны Evans et al. (2003), которые предполагают, что вирусы M. pusilla могут лизировать до 25% популяции Micromonas в день. [ 82 ] Это предполагает, что вирусы ответственны за умеренную смертность в популяциях M. pusilla . [ 43 ] В более широком масштабе вирусная инфекция M. pusilla отвечает за рециркуляцию питательных веществ и энергии в водных пищевых цепях, количественную оценку которой еще предстоит определить. [ нужна ссылка ]
Патология
[ редактировать ]До недавнего времени считалось, что фикоднавирусы заражают исключительно виды водорослей. Недавно ДНК, гомологичная вирусу хлоровируса Acanthocystis turfacea 1 (ATCV-1), была выделена с поверхностей слизистой оболочки носоглотки человека. Присутствие ATCV-1 в микробиоме человека было связано с ухудшением когнитивных функций. Инокуляция ATCV-1 экспериментальным животным была связана со снижением производительности памяти и сенсомоторной системы, а также с изменением экспрессии генов в гиппокампе, связанных с синаптической пластичностью , обучением, формированием памяти и вирусным иммунным ответом. [ 3 ]
Ссылки
[ редактировать ]- ^ «Вирусная зона» . ЭксПАСи . Проверено 15 июня 2015 г.
- ^ Jump up to: а б ICTV. «Таксономия вирусов: выпуск 2014 г.» . Проверено 15 июня 2015 г.
- ^ Jump up to: а б Ёлкен, Р.Х.; и др. (2014). «Хлоровирус ATCV-1 является частью орофарингеального вирома человека и связан с изменениями когнитивных функций у людей и мышей» . Proc Natl Acad Sci США . 111 (45): 16106–16111. Бибкод : 2014PNAS..11116106Y . дои : 10.1073/pnas.1418895111 . ПМЦ 4234575 . ПМИД 25349393 .
- ^ Jump up to: а б с д и Томару, Юджи; Шираи, Йоко; Нагасаки, Кейзо (1 августа 2008 г.). «Экология, физиология и генетика фикоднавируса, поражающего ядовитый цветущий рафидофит Heterosigma akashiwo ». Рыболовная наука . 74 (4): 701–711. Бибкод : 2008FisSc..74..701T . дои : 10.1111/j.1444-2906.2008.01580.x . S2CID 23152411 .
- ^ Jump up to: а б с д и Нагасаки, Кейзо; Тарутани, Кенджи; Ямагучи, Минео (1 марта 1999 г.). «Характеристики роста вируса Heterosigma akashiwo и его возможное использование в качестве микробиологического агента для борьбы с красным приливом» . Прикладная и экологическая микробиология . 65 (3): 898–902. Бибкод : 1999ApEnM..65..898N . дои : 10.1128/АЕМ.65.3.898-902.1999 . ПМК 91120 . ПМИД 10049839 .
- ^ Jump up to: а б Сиги, Дэвид (27 сентября 2005 г.). Пресноводная микробиология: биоразнообразие и динамические взаимодействия микроорганизмов в водной среде . Джон Уайли и сыновья. ISBN 9780470026472 .
- ^ Аноним (2012) Таксономия вирусов: IX отчет международного комитета по таксономии вирусов. Амстердам: Академическая пресса, стр. 261.
- ^ Jump up to: а б с д и ж г Дуниган, Дэвид Д.; Фицджеральд, Лиза А.; Ван Эттен, Джеймс Л. (2006). «Фикоднавирусы: взгляд на генетическое разнообразие» . Вирусные исследования . 117 (1): 119–132. doi : 10.1016/j.virusres.2006.01.024 . ПМИД 16516998 . S2CID 11532538 .
- ^ Чен, Фэн; Саттл, Кертис А. (1996). «Эволюционные взаимоотношения между крупными двухцепочечными ДНК-вирусами, которые заражают микроводоросли и другие организмы, на основании генов ДНК-полимеразы» . Вирусология . 219 (1): 170–178. дои : 10.1006/виро.1996.0234 . ПМИД 8623526 .
- ^ Бейкер, Тимоти С.; Ян, Сяодун; Олсон, Норман Х.; Эттен, Джеймс Л. Ван; Бергуан, Макс; Россманн, Майкл Г. (2000). «Цитирование природы» . Структурная биология природы . 7 (2): 101–103. дои : 10.1038/72360 . ПМК 4167659 . ПМИД 10655609 .
- ^ Ян, Х.; Чипман, PR; Кастберг, Т.; Братбак, Г.; Бейкер, Т.С. (2005). «Вирус морских водорослей PpV01 имеет икосаэдрический капсид с квазисимметрией T = 219» . Журнал вирусологии . 79 (14): 9236–9243. doi : 10.1128/JVI.79.14.9236-9243.2005 . ПМЦ 1168743 . ПМИД 15994818 .
- ^ Jump up to: а б с д и ж г Маккиндер, Люк CM; Достойно, Шарлотта А.; Бигги, Гайя; Холл, Мэтью; Райан, Кейт П.; Варсани, Арвинд; Харпер, Гленн М.; Уилсон, Уильям Х.; Браунли, Колин (1 января 2009 г.). «Одноклеточный вирус водорослей, Emiliania huxleyivirus 86, использует стратегию заражения, подобную животной» . Журнал общей вирусологии . 90 (9): 2306–2316. дои : 10.1099/vir.0.011635-0 . ПМИД 19474246 .
- ^ Вирусы, Международный комитет по таксономии; Кинг, Эндрю MQ (2012). «Фикоднавирусы». Таксономия вирусов . стр. 249–262. дои : 10.1016/B978-0-12-384684-6.00024-0 . ISBN 9780123846846 .
- ^ Ли, Ю; Лу, Чжицян; Сунь, Лянву; Ропп, Сьюзен; Кутиш, Джеральд Ф.; Рок, Дэниел Л.; Ван Эттен, Джеймс Л. (1997). «Анализ ДНК размером 74 КБ, расположенной на правом конце генома вируса хлореллы PBCV-1 размером 330 КБ» . Вирусология 237 (2): 360–377. дои : 10.1006/virus.1997.8805 . ПМИД 9356347 .
- ^ Jump up to: а б Деларок, Николя; Мюллер, Дитер Герхард; Боте, Гордана; Пол, Томас; Книпперс, Рольф; Боланд, Вильгельм (2001). «Полная последовательность ДНК генома EsV-1 вируса Ectocarpus siliculosus» . Вирусология . 287 (1): 112–132. дои : 10.1006/виро.2001.1028 . ПМИД 11504547 .
- ^ Jump up to: а б с Уилсон, Вашингтон; Шредер, округ Колумбия; Аллен, MJ; Холден, Монтана; Паркхилл, Дж.; Баррелл, Б.Г.; Черчер, К.; Хэмлин, Н.; Мунгалл, К.; Норбертчак, Х.; Перепел, Массачусетс; Прайс, К.; Раббинович, Э.; Уокер, Д.; Крейгон, М.; Рой, Д.; Газаль, П. (2005). «Полная последовательность генома и профиль транскрипции литической фазы кокколитовируса». Наука . 309 (5737): 1090–1092. Бибкод : 2005Sci...309.1090W . дои : 10.1126/science.1113109 . ПМИД 16099989 . S2CID 6710771 .
- ^ Финке, Ян; Вингет, Даниэль; Чан, Эми; Саттл, Кертис (2017). «Изменения в генетическом репертуаре вирусов, инфицирующих Micromonas pusilla, отражают горизонтальный перенос генов и связи с их распространением в окружающей среде» . Вирусы . 9 (5): 116. дои : 10.3390/v9050116 . ПМК 5454428 . ПМИД 28534829 .
- ^ Аллен, MJ; Шредер, округ Колумбия; Уилсон, Вашингтон (1 марта 2006 г.). «Предварительная характеристика семейств повторов в геноме EhV-86, вируса гигантских водорослей, поражающего морские микроводоросли Emiliania huxleyi ». Архив вирусологии . 151 (3): 525–535. дои : 10.1007/s00705-005-0647-1 . ПМИД 16195784 . S2CID 10421212 .
- ^ Аллен, Майкл Дж.; Шредер, Деклан К.; Донкин, Эндрю; Кроуферд, Кэтрин Дж.; Уилсон, Уильям Х. (2006). «Сравнение геномов двух кокколитовирусов» . Вирусологический журнал . 3:15 . дои : 10.1186/1743-422X-3-15 . ПМЦ 1440845 . ПМИД 16553948 .
- ^ Кумар, Судхир; Стечер, Глен; Тамура, Коитиро (2016). «MEGA7: Молекулярно-эволюционно-генетический анализ, версия 7.0 для больших наборов данных» . Молекулярная биология и эволюция . 33 (7): 1870–1874. дои : 10.1093/molbev/msw054 . ПМК 8210823 . ПМИД 27004904 .
- ^ Jump up to: а б Маруяма, Фумито; Уэки, Сёко (2016). «Эволюция и филогения крупных ДНК-вирусов, мимивирусов и фикоднавирусов, включая недавно охарактеризованный вирус Heterosigma akashiwo» . Границы микробиологии . 7 : 1942. doi : 10.3389/fmicb.2016.01942 . ПМК 5127864 . ПМИД 27965659 .
- ^ Фишер, МГ; Аллен, MJ; Уилсон, Вашингтон; Саттл, Калифорния (2010). «Гигантский вирус с замечательным набором генов поражает морской зоопланктон» . Труды Национальной академии наук . 107 (45): 19508–19513. Бибкод : 2010PNAS..10719508F . дои : 10.1073/pnas.1007615107 . ПМК 2984142 . ПМИД 20974979 .
- ^ Яу, С.; Лауро, FM; Демере, МЗ; Браун, М.В.; Томас, Т.; Рафтери, MJ; Эндрюс-Пфанкох, К.; Льюис, М.; Хоффман, Дж. М.; Гибсон, Дж.А.; Кавиччиоли, Р. (2011). «Вирофаговый контроль динамики вируса-хозяина антарктических водорослей» . Труды Национальной академии наук . 108 (15): 6163–6168. Бибкод : 2011PNAS..108.6163Y . дои : 10.1073/pnas.1018221108 . ПМК 3076838 . ПМИД 21444812 .
- ^ Халл, Роджер (2014). «Вирусы растений и их классификация». Вирусология растений . стр. 15–68. дои : 10.1016/B978-0-12-384871-0.00002-9 . ISBN 9780123848710 .
- ^ Тай, Вера; Лоуренс, Дженис Э; Ланг, Эндрю С; Чан, Эми М; Калли, Александр I; Саттл, Кертис А. (2003). «Характеристика HaRNAV, вируса с одноцепочечной РНК, вызывающего лизис Heterosigma akashiwo (Raphidophyceae)». Журнал психологии . 39 (2): 343–352. дои : 10.1046/j.1529-8817.2003.01162.x . S2CID 86464306 .
- ^ Лоуренс, Дженис Э; Чан, Эми М; Саттл, Кертис А. (2001). «Новый вирус (HaNIV) вызывает лизис токсичной водоросли Heterosigma akashiwo (Raphidophyceae), образующей цветение». Журнал психологии . 37 (2): 216–222. Бибкод : 2001JPcgy..37..216L . дои : 10.1046/j.1529-8817.2001.037002216.x . S2CID 86563435 .
- ^ Варди, А.; Ван Мой, BAS; Фредрикс, ХФ ; Попендорф, К.Дж.; Оссолински, Дж. Э.; Харамати, Л.; Бидле, К.Д. (2009). «Вирусные гликосфинголипиды вызывают литическую инфекцию и гибель клеток в морском фитопланктоне». Наука . 326 (5954): 861–865. Бибкод : 2009Sci...326..861V . дои : 10.1126/science.1177322 . ПМИД 19892986 . S2CID 40102053 .
- ^ Jump up to: а б Стивенс, Ким; Вейнберг, Карен; Беллас, Кристофер; Браун, Соня; Браунли, Колин; Браун, Мюррей Т.; Шредер, Деклан К. (2014). «Новая эволюционная стратегия, раскрытая в феовирусах» . ПЛОС ОДИН . 9 (1): e86040. Бибкод : 2014PLoSO...986040S . дои : 10.1371/journal.pone.0086040 . ПМЦ 3897601 . ПМИД 24465858 .
- ^ Jump up to: а б с д и ж г час я дж к л Кляйн, М.; Ланка, Южная Каролина; Книпперс, Р.; Мюллер, генеральный директор (10 января 1995 г.). «Оболочечный белок вируса Ectocarpus siliculosus » . Вирусология . 206 (1): 520–526. дои : 10.1016/s0042-6822(95)80068-9 . ПМИД 7831806 .
- ^ Jump up to: а б Шарье, Бенедикт; Коэльо, Сусана М.; Ле Бэйль, Од; Тонон, Тьерри; Мишель, Гурван; Потен, Филипп; Клоарег, Бернард; Бойен, Кэтрин; Питерс, Акира Ф.; Кок, Дж. Марк (2007). «Развитие и физиология бурой водоросли Ectocarpus siliculosus: два столетия исследований» (PDF) . Новый фитолог . 177 (2): 319–332. дои : 10.1111/j.1469-8137.2007.02304.x . ПМИД 18181960 . S2CID 43432914 .
- ^ Jump up to: а б Мюллер, Д.Г. (1991). «Морской вириопланктон, продуцируемый инфицированным Ectocarpus siliculosus (Phaeophyceae)» . Серия «Прогресс в области морской экологии» . 76 : 101–102. Бибкод : 1991MEPS...76..101M . дои : 10.3354/meps076101 .
- ^ Jump up to: а б Сиги, Дэвид (27 сентября 2005 г.). Пресноводная микробиология: биоразнообразие и динамические взаимодействия микроорганизмов в водной среде . Джон Уайли и сыновья. ISBN 9780470026472 .
- ^ Эттен, Джеймс Л. Ван; Дуниган, Дэвид Д. (18 августа 2016 г.). «Гигантские хлоровирусы: пять простых вопросов» . ПЛОС Патогены . 12 (8): e1005751. дои : 10.1371/journal.ppat.1005751 . ПМЦ 4990331 . ПМИД 27536965 .
- ^ Делонг, Джон П.; Аль-Амели, Зейна; Дункан, Гарри; Ван Эттен, Джеймс Л.; Дуниган, Дэвид Д. (2016). «Хищники катализируют рост числа хлорвирусов, питаясь симбиотическими хозяевами зоохлорелл» . Труды Национальной академии наук . 113 (48): 13780–13784. Бибкод : 2016PNAS..11313780D . дои : 10.1073/pnas.1613843113 . ПМК 5137705 . ПМИД 27821770 .
- ^ Ван Эттен, Джеймс Л.; Дуниган, Дэвид Д. (2012). «Хлоровирусы: необычный растительный вирус» . Тенденции в науке о растениях . 17 (1): 1–8. doi : 10.1016/j.tplants.2011.10.005 . ПМК 3259250 . ПМИД 22100667 .
- ^ Jump up to: а б с д и ж г Саттл, Калифорния; Чан, AM (1995). «Вирусы, поражающие морские Prymnesiophyte Chrysochromulina spp.: Выделение, предварительная характеристика и естественная распространенность» . Серия «Прогресс в области морской экологии» . 118 : 275–282. Бибкод : 1995MEPS..118..275S . дои : 10.3354/meps118275 .
- ^ Саттл, Кертис А.; Чан, Эми М. (2002). «Примнезиовирус». Индекс вирусов Спрингера . стр. 741–743. дои : 10.1007/3-540-31042-8_128 . ISBN 978-3-540-67167-1 .
- ^ «Хризохромулина Лакей, 1939 :: Algaebase» . www.algaebase.org . Проверено 28 февраля 2017 г.
- ^ Кинг, Эндрю MQ (1 января 2012 г.). Таксономия вирусов: Классификация и номенклатура вирусов: Девятый отчет Международного комитета по таксономии вирусов . Эльзевир. ISBN 9780123846846 .
- ^ Клерисси, Камилла; Дедевиз, Ив; Гримсли, Найджел (2012). «Празиновирусы морской зеленой водоросли Ostreococcus tauri преимущественно видовоспецифичны» . Журнал вирусологии . 86 (8): 4611–4619. дои : 10.1128/JVI.07221-11 . ПМК 3318615 . ПМИД 22318150 .
- ^ «История таксономии ICTV: вирус Micromonas pusilla SP1» . ICTV. 8 марта 1998 года . Проверено 25 июня 2017 г.
- ^ Коттрелл, Монтана; Саттл, Калифорния (1991). «Широко распространенное распространение и клональные вариации вирусов, вызывающих лизис космополитного эукариотического морского фитопланктера Micromonas pusilla» . Серия «Прогресс в области морской экологии» . 78 : 1–9. Бибкод : 1991MEPS...78....1C . дои : 10.3354/meps078001 .
- ^ Jump up to: а б с Коттрелл, Мэтью Т.; Саттл, Кертис А. (1995). «Динамика литического вируса, заражающего фотосинтезирующие морские пикофлагелляты Micromonas pusilla» . Лимнология и океанография . 40 (4): 730–739. Бибкод : 1995LimOc..40..730C . дои : 10.4319/lo.1995.40.4.0730 .
- ^ «Домашний Ostreococcus lucimarinus » . genome.jgi.doe.gov . Проверено 28 февраля 2017 г.
- ^ Jump up to: а б с д и ж г час Дерелл, Эвелин; Феррас, Кончита; Эсканд, Мари-Лайн; Эйшени, Софи; Кук, Ричард; Пигано, Гвенаэль; Дедевиз, Ив; Беллек, Лора; Моро, Эрве (28 мая 2008 г.). «Жизненный цикл и геном OtV5, большого ДНК-вируса пелагической морской одноклеточной зеленой водоросли Ostreococcus tauri » . ПЛОС ОДИН . 3 (5): е2250. Бибкод : 2008PLoSO...3.2250D . дои : 10.1371/journal.pone.0002250 . ПМК 2386258 . ПМИД 18509524 .
- ^ Томас, Розенн; Гримсли, Найджел; Эсканд, Мари-Лайн; Субирана, Люси; Дерелл, Эвелин; Моро, Эрве (2011). «Приобретение и поддержание устойчивости к вирусам в популяциях эукариотического фитопланктона». Экологическая микробиология . 13 (6): 1412–1420. Бибкод : 2011EnvMi..13.1412T . дои : 10.1111/j.1462-2920.2011.02441.x . ПМИД 21392198 .
- ^ Симе-Нгандо, Телесфор (2014). «Экологические бактериофаги: Вирусы микробов в водных экосистемах» . Границы микробиологии . 5 : 355. дои : 10.3389/fmicb.2014.00355 . ПМК 4109441 . ПМИД 25104950 .
- ^ Сигвард Олофссон, Джон-Эрик с. Ганс (1998). «Гликозилирование вирусных гликопротеинов в клетке-хозяине - поле битвы за защиту хозяина и устойчивость к вирусам». Скандинавский журнал инфекционных заболеваний . 30 (5): 435–440. дои : 10.1080/00365549850161386 . ПМИД 10066039 .
- ^ Маркине-Горяйнов Н.; Жилле, Л.; Ван Эттен, JL; Коррес, Х.; Верма, Н.; Вандерплашен, А. (2004). «Гликозилтрансферазы, кодируемые вирусами» . Журнал общей вирусологии . 85 (10): 2741–2754. дои : 10.1099/vir.0.80320-0 . ПМИД 15448335 .
- ^ Jump up to: а б с Плагге, Б.; Газзаррини, С.; Нельсон, М.; Серана, Р.; Ван Эттен, JL; Дерст, К.; Дифранческо, Д.; Мороний, А.; Тиль, Г. (2000). «Белок калиевого канала, кодируемый вирусом хлореллы PBCV-1» . Наука . 287 (5458): 1641–1644. Бибкод : 2000Sci...287.1641P . дои : 10.1126/science.287.5458.1641 . ПМИД 10698737 . S2CID 17411728 .
- ^ Хюбшер, Ульрих; Нашер, Хайнц-Петер; Сюваоя, Юхани Э. (2000). «Эукариотические ДНК-полимеразы, растущее семейство». Тенденции биохимических наук . 25 (3): 143–147. дои : 10.1016/S0968-0004(99)01523-6 . ПМИД 10694886 .
- ^ Уорбрик, Э. (2000). «Загадка многих партнеров PCNA». Биоэссе . 22 (11): 997–1006. doi : 10.1002/1521-1878(200011)22:11<997::AID-BIES6>3.0.CO;2-# . ПМИД 11056476 . S2CID 196597356 .
- ^ Эллисон, Виола; Стиллман, Брюс (2001). «Открытие зажима» . Клетка . 106 (6): 655–660. дои : 10.1016/S0092-8674(01)00498-6 . ПМИД 11572772 . S2CID 17575635 .
- ^ Мосси, Ромина; Хубшер, Ульрих (1998). «Устранение зажимов и загрузчиков зажимов. Фактор репликации эукариот C» . Европейский журнал биохимии . 254 (2): 209–216. дои : 10.1046/j.1432-1327.1998.2540209.x . ПМИД 9660172 .
- ^ Хо, СК; Ван Эттен, JL; Шуман, С. (1997). «Характеристика АТФ-зависимой ДНК-лигазы, кодируемой вирусом хлореллы PBCV-1» . Журнал вирусологии . 71 (3): 1931–7. doi : 10.1128/JVI.71.3.1931-1937.1997 . ЧВК 191272 . ПМИД 9032324 .
- ^ Девайндт, К.; Альбагли, О.; Бернардин, Ф.; Дордайн, П.; Квиф, С.; Лантуан, Д.; Керкарт, JP; Лепринс, Д. (1995). «Онкоген LAZ3/BCL6 кодирует специфичный для последовательности ингибитор транскрипции: новая функция домена BTB/POZ как автономного репрессирующего домена» . Рост и дифференцировка клеток . 6 (12): 1495–503. ПМИД 9019154 .
- ^ Хо, СК; Гонг, К.; Шуман, С. (2001). «Компонент РНК-трифосфатазы аппарата для кэпирования мРНК вируса хлореллы 1 Paramecium bursaria» . Журнал вирусологии . 75 (4): 1744–1750. doi : 10.1128/JVI.75.4.1744-1750.2001 . ПМК 114083 . ПМИД 11160672 .
- ^ Jump up to: а б Хо, СК; Ван Эттен, JL; Шуман, С. (1996). «Экспрессия и характеристика фермента, кэпирующего РНК, кодируемого вирусом хлореллы PBCV-1» . Журнал вирусологии . 70 (10): 6658–64. doi : 10.1128/JVI.70.10.6658-6664.1996 . ПМК 190707 . ПМИД 8794301 .
- ^ Шуман, С. (2001). «Структура, механизм и эволюция аппарата кэпирования мРНК». Прогресс в исследованиях нуклеиновых кислот и молекулярной биологии . 66 : 1–40. дои : 10.1016/s0079-6603(00)66025-7 . ISBN 9780125400664 . ПМИД 11051760 .
- ^ Ван Эттен, Джеймс Л.; Мейнц, Рассел Х. (1999). «Гигантские вирусы, поражающие водоросли» . Ежегодный обзор микробиологии . 53 : 447–494. дои : 10.1146/аннурев.микро.53.1.447 . ПМИД 10547698 . S2CID 7346326 .
- ^ Канг, М.; Дункан, Джорджия; Кушинский, К.; Ойлер, Г.; Чжэн, Дж.; Беккер, Д.Ф.; Ван Эттен, JL (2014). «Хлоровирус PBCV-1 кодирует активную супероксиддисмутазу меди-цинка» . Журнал вирусологии . 88 (21): 12541–12550. дои : 10.1128/JVI.02031-14 . ПМЦ 4248938 . ПМИД 25142578 .
- ^ Лоуренс, Дженис Э.; Брюссаард, Корина П.Д.; Саттл, Кертис А. (1 марта 2017 г.). «Вирус-специфические реакции Heterosigma akashiwo на инфекцию» . Прикладная и экологическая микробиология . 72 (12): 7829–7834. Бибкод : 2006ApEnM..72.7829L . дои : 10.1128/АЕМ.01207-06 . ПМЦ 1694243 . ПМИД 17041155 .
- ^ Jump up to: а б Нагасаки, К.; Андо, М.; Имаи, И.; Итакура, С.; Исида, Ю. (1994). «Вирусоподобные частицы в Heterosigma akashiwo (Raphidophyceae): возможный механизм распада красного прилива». Морская биология . 119 (2): 307–312. Бибкод : 1994ВтЧт.119..307N . дои : 10.1007/BF00349570 . S2CID 85350528 .
- ^ Нагасаки, Кейзо; Андо, Масаси; Итакура, Сигэру; Имаи, Ичиро; Исида, Юзабуро (1994). «Вирусная смертность на финальной стадии красного прилива Heterosigma akashiwo (Raphidophyceae)». Журнал исследований планктона . 16 (11): 1595–1599. дои : 10.1093/планкт/16.11.1595 .
- ^ Тарутани, К.; Нагасаки, К.; Ямагучи, М. (2000). «Вирусное воздействие на общую численность и клональный состав вредного цветущего фитопланктона Heterosigma akashiwo» . Прикладная и экологическая микробиология . 66 (11): 4916–4920. Бибкод : 2000ApEnM..66.4916T . дои : 10.1128/АЕМ.66.11.4916-4920.2000 . ПМЦ 92399 . ПМИД 11055943 .
- ^ Jump up to: а б с Джон, Вейер (26 апреля 1999 г.). «Что такое кокколитофор? Информационный бюллетень: Тематические статьи» . Earthobservatory.nasa.gov . Проверено 3 марта 2017 г.
- ^ Jump up to: а б с д «Дом — Эмилиания Хаксли» . genome.jgi.doe.gov . Проверено 3 марта 2017 г.
- ^ Уилсон, Уильям Х.; Тарран, Глен А.; Шредер, Деклан; Кокс, Майкл; Хорошо, Джоанн; Малин, Джиллиан (2002). «Выделение вирусов, ответственных за гибель цветения Emiliania huxleyi в Ла-Манше» (PDF) . Журнал Морской биологической ассоциации Великобритании . 82 (3): 369–377. Бибкод : 2002JMBUK..82..369W . дои : 10.1017/S002531540200560X . S2CID 85219045 .
- ^ Мартинес, Дж. М.; Шредер, округ Колумбия; Ларсен, А.; Братбак, Г.; Уилсон, WH (2007). «Молекулярная динамика Emiliania huxleyi и сопутствующих вирусов в ходе двух отдельных исследований мезокосма» . Прикладная и экологическая микробиология . 73 (2): 554–562. Бибкод : 2007ApEnM..73..554M . дои : 10.1128/АЕМ.00864-06 . ПМК 1796978 . ПМИД 17098923 .
- ^ Братбак, Г.; Эгге, Дж. К.; Хелдал, М. (1993). «Вирусная смертность морской водоросли Emiliania huxleyi (Haptophyceae) и прекращение цветения водорослей» . Серия «Прогресс в области морской экологии» . 93 : 39–48. Бибкод : 1993MEPS...93...39B . дои : 10.3354/meps093039 .
- ^ «Ectocarpus siliculosus — генетический и геномный модельный организм бурых водорослей» . Институт биологии Франсуа Жакоба. 21 июня 2018 г.
- ^ Мюллер, генеральный директор; Каваи, Х.; Сташ, Б.; Ланка, С. (1990). «Вирусная инфекция морской бурой водоросли Ectocarpus siliculosus (Phaeophyceae)». Ботаника Акта 103 (1): 72–82. дои : 10.1111/j.1438-8677.1990.tb00129.x .
- ^ Мюллер, Д.Г.; Вестермайер, Р.; Моралес, Дж.; Рейна, Дж. Гарсия; Дель Кампо, Э.; Корреа, Дж. А.; Ромеча, Э. (2000). «Массовое распространение вирусной ДНК у эктокарпусов (Phaeophyceae, Ectocarpales) из двух мест обитания в Северной Атлантике и южной части Тихого океана». Морская ботаника . 43 (2). дои : 10.1515/БОТ.2000.016 . hdl : 10553/73463 . S2CID 84166193 .
- ^ Сенгко, MR; Бротигам, М.; Капп, М.; Мюллер, генеральный директор (1 февраля 1996 г.). «Обнаружение ДНК вируса у Ectocarpus siliculosus и E. fasciculatus (Phaeophyceae)». Европейский журнал психологии . 31 (1): 73–78. Бибкод : 1996EJPhy..31...73S . дои : 10.1080/09670269600651221 .
- ^ Дуниган, Дэвид Д.; Черни, Рональд Л.; Бауман, Эндрю Т.; Роуч, Джаред К.; Лейн, Лесли С.; Агаркова Ирина В.; Вулсер, Курт; Янаи-Бальсер, Джана М.; Гурнон, Джеймс Р.; Витек, Джейсон С.; Кроншнабель, Бернард Дж.; Жаньяр, Адриан; Блан, Гийом; Аптон, Крис; Дункан, Гарри А.; МакКлунг, О. Уильям; Ма, Фангруй; Ван Эттен, Джеймс Л. (2012). «Протеом вируса хлореллы 1 Paramecium bursaria раскрывает новые архитектурные и регуляторные особенности гигантского вируса» . Журнал вирусологии . 86 (16): 8821–8834. дои : 10.1128/JVI.00907-12 . ПМЦ 3421733 . ПМИД 22696644 .
- ^ «Токсическое цветение водорослей в скандинавских водах, май – июнь 1988 г. | Океанография» . Океанография . 2 (1): 9–14. 1989. дои : 10.5670/oceanog.1989.24 . Проверено 1 марта 2017 г.
- ^ Jump up to: а б Дерелл, Э.; Ферраз, К.; Ромбоутс, С.; Рузе, П.; Уорден, Аризона; Роббенс, С.; Партенский Ф.; Дегроев, С.; Эчейни, С.; Кук, Р.; Саис, Ю.; Вуйтс, Дж.; Джаббари, К.; Боулер, К.; Пано, О.; Пьегу, Б.; Болл, С.Г.; Рал, Ж.-П.; Буже, Ф.-Ю.; Пигано, Г.; Де Баетс, Б.; Пикард, А.; Дельсени, М.; Демайль, Ж.; Ван Де Пер, Ю.; Моро, Х. (2006). «Анализ генома самого маленького свободноживущего эукариота Ostreococcus tauri раскрывает множество уникальных особенностей» . Труды Национальной академии наук . 103 (31): 11647–11652. Бибкод : 2006PNAS..10311647D . дои : 10.1073/pnas.0604795103 . ПМЦ 1544224 . ПМИД 16868079 .
- ^ О'Келли, Чарльз Дж.; Сераки, Майкл Э.; Тьер, Эдвард К.; Хобсон, Илана К. (2003). «Переходное цветение Ostreococcus (Chlorophyta, Prasinophyceae) в заливе Вест-Нек, Лонг-Айленд, Нью-Йорк». Журнал психологии . 39 (5): 850–854. Бибкод : 2003JPcgy..39..850O . дои : 10.1046/j.1529-8817.2003.02201.x . S2CID 84541779 .
- ^ Яу, Шери; Хемон, Клэр; Дерелл, Эвелин; Моро, Эрве; Пигано, Гвенаэль; Гримсли, Найджел (2016). «Хромосома вирусного иммунитета у морских пикоукариот, Ostreococcus tauri» . ПЛОС Патогены . 12 (10): e1005965. дои : 10.1371/journal.ppat.1005965 . ПМК 5082852 . ПМИД 27788272 .
- ^ Вайц, Джошуа С.; Вильгельм, Стивен В. (1 июля 2013 г.). «Океан вирусов» . Ученый .
- ^ Уорден, Аризона; Ли, Дж.-Х.; Мок, Т.; Рузе, П.; Симмонс, член парламента; Аэртс, Алабама; Аллен, А.Е.; Кувелье, ML; Дерелл, Э.; Эверетт, М.В.; Фулон, Э.; Гримвуд, Дж.; Гундлах, Х.; Генриссат, Б.; Наполи, К.; Макдональд, С.М.; Паркер, Миссисипи; Ромбоутс, С.; Саламов А.; фон Дассов, П.; Бэджер, Дж. Х.; Коутиньо, премьер-министр; Демир, Э.; Дубчак И.; Гентеманн, К.; Эйкрем, В.; Гриди, Дж. Э.; Джон, У.; Ланье, В.; и др. (2009). «Зеленая эволюция и динамические адаптации, выявленные по геномам морских пикоукариот Micromonas» . Наука . 324 (5924): 268–272. Бибкод : 2009Sci...324..268W . дои : 10.1126/science.1167222 . ПМИД 19359590 . S2CID 206516961 .
- ^ Эванс, К.; Арчер, SD; Жаке, С.; Уилсон, WH (2003). «Прямые оценки вклада вирусного лизиса и выпаса микрозоопланктона в сокращение популяции видов Micromonas» . Водная микробная экология . 30 : 207–219. дои : 10.3354/ame030207 .
Дальнейшее чтение
[ редактировать ]- Ван Эттен, Джеймс Л. (2003). «Необычный образ жизни гигантских вирусов хлореллы» . Ежегодный обзор генетики . 37 : 153–195. дои : 10.1146/annurev.genet.37.110801.143915 . ПМИД 14616059 .
- Ван Эттен, Джеймс Л.; Мейнц, Рассел Х. (1999). «Гигантские вирусы, поражающие водоросли» . Ежегодный обзор микробиологии . 53 : 447–494. дои : 10.1146/аннурев.микро.53.1.447 . ПМИД 10547698 . S2CID 7346326 .
- Айер, Лакшминараян М.; Баладжи, С.; Кунин Евгений Владимирович; Аравинд, Л. (2006). «Эволюционная геномика ядерно-цитоплазматических крупных ДНК-вирусов» . Вирусные исследования . 117 (1): 156–184. doi : 10.1016/j.virusres.2006.01.009 . ПМИД 16494962 .
- Рауль, Д.; Аудик, Стефан; Роберт, Кэтрин; Абергель, Шанталь; Ренесто, Патрисия; Огата, Хироюки; ЛаСкола, Бернар; Сьюзан, Мари; Клавери, Жан-Мишель (2004). «Геномная последовательность мимивируса размером 1,2 мегабазы». Наука . 306 (5700): 1344–1350. Бибкод : 2004Sci...306.1344R . дои : 10.1126/science.1101485 . ПМИД 15486256 . S2CID 84298461 .
- Домашняя страница вирусов хлореллы