Ретровирус
| Ретровирусиды | |
|---|---|
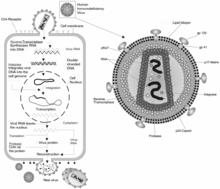 | |
| Схема ретровируса ВИЧ клеточной инфекции, продукции вируса и структуры вируса | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область : | Рибовирия |
| Королевство: | Паранавиры |
| Тип: | Артвервирикота |
| Сорт: | Ревтравирицеты |
| Заказ: | Ортервирусы |
| Семья: | Ретровирусиды |
| Подсемейства и роды [1] | |
Ретровирус , — это тип вируса который встраивает ДНК-копию своего РНК- генома в ДНК клетки- хозяина , в которую он проникает, изменяя таким образом геном этой клетки. [2] клетки-хозяина После проникновения в цитоплазму вирус использует свой собственный фермент обратной транскриптазы для производства ДНК из своего РНК-генома, что является противоположностью обычной схемы, то есть ретро (назад). Затем новая ДНК встраивается в геном клетки-хозяина с помощью фермента интегразы , после чего ретровирусная ДНК называется провирусом . Затем клетка-хозяин рассматривает вирусную ДНК как часть своего собственного генома, транскрибируя и транслируя вирусные гены вместе с собственными генами клетки, производя белки, необходимые для сборки новых копий вируса. Многие ретровирусы вызывают серьезные заболевания у человека, других млекопитающих и птиц. [3]
Ретровирусы имеют множество подсемейств в трех основных группах.
- Онкоретровирусы (ретровирусы, вызывающие рак) включают Т-лимфотропный вирус человека (HTLV), вызывающий тип лейкемии у людей, и вирусы мышиного лейкоза (MLV) у мышей. [4]
- Лентивирусы (медленные вирусы) включают ВИЧ-1 и ВИЧ-2 , вызывающие синдром приобретенного иммунодефицита ( СПИД ) у людей.
- Спумавирусы (пенистые вирусы) доброкачественны и не вызывают каких-либо заболеваний у людей или животных. [5]
Специализированные ферменты ДНК-инфильтрации ретровирусов делают их ценными исследовательскими инструментами в молекулярной биологии, и они успешно используются в системах доставки генов. [6]
Данные об эндогенных ретровирусах (наследуемая ДНК провирусов в геномах животных) позволяют предположить, что ретровирусы заражают позвоночных уже по меньшей мере 450 миллионов лет. [7]
Структура
[ редактировать ]Вирионы , вирусы в виде самостоятельных частиц ретровирусов, состоят из оболочек около 100 нм диаметром . Наружная липидная оболочка состоит из гликопротеина. [8] Вирионы также содержат две идентичные одноцепочечные молекулы РНК 7–10 тыс. нуклеотидов длиной . Две молекулы присутствуют в виде димера, образованного спариванием оснований между комплементарными последовательностями. Места взаимодействия между двумя молекулами РНК были идентифицированы как « целующаяся стебель-петля ». [3] Хотя вирионы разных ретровирусов не имеют одинаковой морфологии и биологии, все компоненты вириона очень похожи. [9]
Основными компонентами вириона являются:
- Оболочка хозяина : состоит из липидов (полученных из плазматической мембраны во время процесса почкования ), а также гликопротеина, кодируемого геном env . Оболочка ретровируса выполняет три различные функции: защиту от внеклеточной среды через липидный бислой , позволяющую ретровирусу проникать в клетки-хозяева и выходить из них посредством перемещения через эндосомальную мембрану , а также способность напрямую проникать в клетки путем слияния с их мембранами.
- РНК : состоит из димерной РНК. Он имеет кепку на 5'- конце и поли(А)-хвост на 3'-конце. Геномная РНК (гРНК) образуется в результате активности РНК-полимеразы II хозяина (Pol II) и путем добавления 5'-метилового кэпа и 3'-поли-А-хвоста обрабатывается как мРНК хозяина. [10] Геном РНК также имеет терминальные некодирующие области, которые важны для репликации, и внутренние области, которые кодируют белки вириона для экспрессии генов . 5'-конец включает четыре региона: R, U5, PBS и L. Район R представляет собой короткую повторяющуюся последовательность на каждом конце генома, используемую во время обратной транскрипции для обеспечения правильного сквозного переноса в растущем геноме. цепь. U5, с другой стороны, представляет собой короткую уникальную последовательность между R и PBS. PBS (сайт связывания праймера) состоит из 18 оснований, комплементарных 3'-концу праймера тРНК. L-область представляет собой нетранслируемую лидерную область, которая дает сигнал для упаковки геномной РНК. 3'-конец включает три области: PPT (полипуриновый тракт), U3 и R. PPT представляет собой праймер для синтеза плюс-цепи ДНК во время обратной транскрипции . U3 представляет собой последовательность между PPT и R, которая служит сигналом, который провирус может использовать в транскрипции . R представляет собой терминальную повторяющуюся последовательность на 3'-конце.
- Белки : состоят из белков gag, протеазы (PR), белков pol и белков env.
- Белки группоспецифического антигена (gag) являются основными компонентами вирусного капсида , их количество составляет около 2000–4000 копий на вирион. Gag обладает двумя доменами, связывающими нуклеиновые кислоты, включая матрикс (MA) и нуклеокапсид (NC). Специфическое распознавание, связывание и упаковка ретровирусной геномной РНК для сборки вирионов является одной из важных функций белка Gag. Взаимодействия Gag с клеточными РНК также регулируют аспекты сборки. [11] Экспрессия gag сама по себе приводит к сборке незрелых вирусоподобных частиц, которые отпочковываются от плазматической мембраны. Во всех ретровирусах белок Gag является предшественником внутреннего структурного белка. [12]
- Протеаза (про) экспрессируется по-разному у разных вирусов. Он участвует в протеолитическом расщеплении во время созревания вириона с образованием зрелых белков gag и pol. Ретровирусные белки Gag отвечают за координацию многих аспектов сборки вирионов.
- Белки Pol отвечают за синтез вирусной ДНК и интеграцию в ДНК хозяина после заражения.
- Белки Env играют роль в ассоциации и проникновении вирионов в клетку-хозяина. [13] Наличие функциональной копии гена env отличает ретровирусы от ретроэлементов . [14] Способность ретровируса связываться с клеткой-мишенью с помощью специфических рецепторов на клеточной поверхности обеспечивается поверхностным компонентом (SU) белка Env, тогда как способность ретровируса проникать в клетку посредством слияния мембран обеспечивается мембраной. -закрепленный трансмембранный компонент (ТМ). Таким образом, именно белок Env делает ретровирус инфекционным.
- Несколько видов белков связаны с РНК вириона ретровируса. Белок нуклеокапсида (NC) является наиболее распространенным белком, который покрывает РНК; в то время как другие белки присутствуют в гораздо меньших количествах и обладают ферментативной активностью. Некоторые ферментные активности, присутствующие в вирионе ретровируса, включают РНК-зависимую ДНК-полимеразу (обратную транскриптазу; RT), ДНК-зависимую ДНК-полимеразу, интегразу рибонуклеазы H (РНКаза H) и протеазу. [15] Было продемонстрировано, что ретровирусные РНКазы H, кодируемые всеми ретровирусами, включая ВИЧ, демонстрируют три различных способа расщепления: внутренний, направленный по 3'-концу ДНК и направленный по 5'-концу РНК. Все три способа расщепления играют роль в обратной транскрипции. Следовательно, активность РНКазы H важна в нескольких аспектах обратной транскрипции. Использование активности РНКазы H во время репликации ретровируса демонстрирует уникальную стратегию копирования генома одноцепочечной РНК в двухцепочечную ДНК, поскольку минусцепочечная ДНК комплементарна и образует пару оснований с геномом ретровируса в первом цикле ДНК. синтез. [16] Активность рибонуклеазы РНКазы H также необходима в жизненном цикле ретровирусов, поскольку она генерирует и удаляет праймеры, необходимые обратной транскриптазе (RT) для инициации синтеза ДНК. Ретровирусы, лишенные активности РНКазы H, неинфекционны. [17]

Геномная структура
[ редактировать ]Ретровирусный геном упакован в виде вирусных частиц. Эти вирусные частицы представляют собой димеры одноцепочечных линейных молекул РНК с положительным смыслом. [10]
Ретровирусы (и ортервирусы в целом) следуют схеме 5'- gag - pro - pol - env -3' в геноме РНК. gag и pol кодируют полипротеины, каждый из которых управляет капсидом и репликацией. Область pol кодирует ферменты, необходимые для репликации вируса, такие как обратная транскриптаза, протеаза и интеграза. [19] В зависимости от вируса гены могут перекрываться или сливаться в более крупные полипротеиновые цепи. Некоторые вирусы содержат дополнительные гены. Род лентивирусов, род спамавирусов, род HTLV/вируса лейкемии крупного рогатого скота (BLV) и недавно интродуцированный род рыбных вирусов относятся к ретровирусам, классифицируемым как сложные. Эти вирусы имеют гены, называемые дополнительными генами, в дополнение к генам gag, pro, pol и env. Акцессорные гены расположены между pol и env, ниже env, включая область U3 LTR, или в env и перекрывающихся частях. Хотя вспомогательные гены выполняют вспомогательную роль, они также координируют и регулируют экспрессию вирусных генов.Кроме того, некоторые ретровирусы могут нести гены, называемые онкогенами, или гены onc из другого класса. Ретровирусы с этими генами (их еще называют трансформирующими вирусами) известны своей способностью быстро вызывать опухоли у животных и переводить клетки в культуре в онкогенное состояние. [20]
Полипротеины расщепляются на более мелкие белки, каждый из которых выполняет свою функцию. Нуклеотиды, кодирующие их, известны как субгены . [18]
Умножение
[ редактировать ]
Когда ретровирусы интегрируют свой собственный геном в зародышевую линию , их геном передается следующему поколению. Эти эндогенные ретровирусы (ERV), в отличие от экзогенных , сейчас составляют 5–8% генома человека. [21] Большинство вставок не имеют известной функции, и их часто называют « мусорной ДНК ». Однако многие эндогенные ретровирусы играют важную роль в биологии хозяина, например, контроль транскрипции генов, слияние клеток во время плаценты в ходе прорастания эмбриона развития и устойчивость к экзогенной ретровирусной инфекции. Эндогенным ретровирусам также уделяется особое внимание при исследовании патологий, связанных с иммунологией , таких как аутоиммунные заболевания, такие как рассеянный склероз , хотя еще не доказано, что эндогенные ретровирусы играют какую-либо причинную роль в этом классе заболеваний. [22]
Традиционно считалось, что транскрипция происходит только от ДНК к РНК, но обратная транскриптаза транскрибирует РНК в ДНК. Термин «ретро» в ретровирусе относится к такому изменению (преобразованию ДНК из РНК) обычного направления транскрипции. Он по-прежнему подчиняется центральной догме молекулярной биологии , которая гласит, что информация может передаваться от нуклеиновой кислоты к нуклеиновой кислоте, но не может быть передана обратно от белка ни к белку, ни к нуклеиновой кислоте. Активность обратной транскриптазы за пределами ретровирусов была обнаружена почти у всех эукариот , что позволяет генерировать и вставлять новые копии ретротранспозонов в геном хозяина. Эти вставки транскрибируются ферментами хозяина в новые молекулы РНК, попадающие в цитозоль. Затем некоторые из этих молекул РНК транслируются в вирусные белки. Белки, кодируемые генами gag и pol, транслируются с мРНК длиной в геном в полипротеины Gag и Gag-Pol. Например, для гена gag ; он транслируется в молекулы капсидного белка, а для ген pol ; он транслируется в молекулы обратной транскриптазы. Ретровирусам нужно гораздо больше белков Gag, чем белков Pol, и они разработали усовершенствованные системы для синтеза необходимого количества каждого из них. Например, после синтеза Gag почти 95 процентов рибосом прекращают трансляцию, в то время как другие рибосомы продолжают трансляцию, синтезируя Gag-Pol. В шероховатой эндоплазматической сети начинается гликозилирование, и ген env транслируется со сплайсированных мРНК в шероховатой эндоплазматической сети в молекулы белка оболочки. Когда молекулы белка оболочки переносятся в комплекс Гольджи, они разделяются на поверхностный гликопротеин и трансмембранный гликопротеин с помощью протеазы хозяина. Эти два гликопротеиновых продукта остаются в тесной связи и после дальнейшего гликозилирования транспортируются к плазматической мембране. [3]
Важно отметить, что ретровирус должен «внести» в свой капсид собственную обратную транскриптазу , иначе он не сможет использовать ферменты инфицированной клетки для выполнения задачи из-за необычной природы производства ДНК из РНК. [ нужна ссылка ]
Промышленные лекарства, разработанные как ингибиторы протеаз и обратной транскриптазы, производятся таким образом, что они воздействуют на определенные сайты и последовательности в соответствующих ферментах. Однако эти препараты могут быстро стать неэффективными из-за того, что последовательности генов, кодирующие протеазу и обратную транскриптазу, быстро мутируют. Эти изменения в основаниях приводят к изменению определенных кодонов и сайтов ферментов и, таким образом, позволяют избежать нацеливания лекарства за счет потери сайтов, на которые оно фактически нацелено. [ нужна ссылка ]
Поскольку в обратной транскрипции отсутствует обычная корректура репликации ДНК, ретровирус мутирует очень часто . Это позволяет вирусу быстро стать устойчивым к противовирусным препаратам и препятствует разработке эффективных вакцин и ингибиторов ретровируса. [23]
Одна из трудностей, с которой сталкиваются некоторые ретровирусы, такие как ретровирус Молони, связана с необходимостью активного деления клеток для трансдукции. В результате клетки, такие как нейроны, очень устойчивы к инфекции и трансдукции ретровирусами. Это вызывает опасения, что инсерционный мутагенез вследствие интеграции в геном хозяина может привести к раку или лейкемии. В этом отличие от лентивирусов , рода Retroviridae , которые способны интегрировать свою РНК в геном неделящихся клеток-хозяев. [ нужна ссылка ]
Рекомбинация
[ редактировать ]В каждую ретровирусную частицу упакованы два РНК генома , но после заражения каждый вирус генерирует только один провирус . [24] После заражения происходит обратная транскрипция и этот процесс сопровождается рекомбинацией . Рекомбинация включает переключение цепи матрицы между двумя копиями генома (рекомбинация выбора копии) во время обратной транскрипции. В каждом цикле репликации происходит от 5 до 14 событий рекомбинации на геном. [25] Генетическая рекомбинация, по-видимому, необходима для поддержания целостности генома и как механизм восстановления поврежденных геномов. [24]
Передача инфекции
[ редактировать ]- От ячейки к ячейке [26]
- Жидкости
- Передается воздушно-капельным путем, как ретровирус овец Яагсекте .
Провирус
[ редактировать ]ДНК, образующаяся после обратной транскрипции (провирус), длиннее генома РНК, поскольку на каждом из концов имеются последовательности U3-R-U5, называемые длинным терминальным повтором (LTR). Таким образом, 5'-конец имеет дополнительную последовательность U3, а другой терминал имеет последовательность U5. [15] LTR способны посылать сигналы для выполнения жизненно важных задач, таких как инициация производства РНК или управление скоростью транскрипции. Таким образом, LTR могут контролировать репликацию и, следовательно, весь ход вирусного цикла. [27] Несмотря на то, что неинтегрированная ретровирусная кДНК расположена в ядре, она является очень слабым субстратом для транскрипции. По этой причине интегрированный провирус необходим для постоянной и эффективной экспрессии ретровирусных генов. [10]
Эта ДНК может быть включена в геном хозяина в виде провируса, который может передаваться клеткам-потомкам. ДНК ретровируса случайным образом вставляется в геном хозяина. Из-за этого его можно внедрить в онкогены . Таким образом, некоторые ретровирусы могут превращать нормальные клетки в раковые. Некоторые провирусы остаются латентными в клетке в течение длительного периода времени, прежде чем активируются при изменении клеточной среды. [ нужна ссылка ]
Ранняя эволюция
[ редактировать ]Исследования ретровирусов привели к первому продемонстрированному синтезу ДНК из матриц РНК — фундаментальному способу передачи генетического материала, который происходит как у эукариот , так и у прокариот . Было высказано предположение, что процессы транскрипции РНК в ДНК, используемые ретровирусами, возможно, впервые привели к использованию ДНК в качестве генетического материала. В этой модели, гипотезе мира РНК , клеточные организмы переняли более химически стабильную ДНК, когда ретровирусы эволюционировали, чтобы создавать ДНК из шаблонов РНК . [ нужна ссылка ]
По оценкам даты эволюции пенообразных эндогенных ретровирусов, время существования самого недавнего общего предка составило > 450 миллионов лет назад . [28]
Генная терапия
[ редактировать ]гаммаретровирусные и лентивирусные векторы для генной терапии Разработаны , которые обеспечивают стабильную генетическую модификацию обработанных клеток путем хромосомной интеграции перенесенных векторных геномов. Эта технология может быть использована не только в исследовательских целях, но и для клинической генной терапии, направленной на долгосрочную коррекцию генетических дефектов, например, в стволовых клетках и клетках-предшественниках. Созданы ретровирусные векторные частицы, обладающие тропизмом к различным клеткам-мишеням. Гаммаретровирусные и лентивирусные векторы на данный момент использовались в более чем 300 клинических испытаниях, посвященных вариантам лечения различных заболеваний. [6] [29] Ретровирусные мутации могут быть разработаны для создания моделей трансгенных мышей для изучения различных видов рака и их метастатических моделей . [ нужна ссылка ]
Рак
[ редактировать ]Ретровирусы, вызывающие рост опухоли, включают вирус саркомы Рауса и вирус опухоли молочной железы мышей . Рак может быть вызван протоонкогенами, которые были ошибочно включены в провирусную ДНК, или разрушением клеточных протоонкогенов. Вирус саркомы Рауса содержит ген src , который запускает образование опухоли. Позже было обнаружено, что в передаче клеточного сигнала участвует аналогичный ген в клетках, который, скорее всего, был вырезан из провирусной ДНК. Нетрансформирующие вирусы могут случайным образом вставлять свою ДНК в протоонкогены, нарушая экспрессию белков, регулирующих клеточный цикл. Промотор ДНК провируса также может вызывать чрезмерную экспрессию регуляторных генов.Ретровирусы могут вызывать такие заболевания, как рак и иммунодефицит. Если вирусная ДНК интегрируется в хромосомы хозяина, это может привести к необратимым инфекциям. Поэтому важно выяснить реакцию организма на ретровирусы. Экзогенные ретровирусы особенно связаны с патогенными заболеваниями. Например, у мышей есть вирус опухоли молочной железы мышей (MMTV), который является ретровирусом. Этот вирус передается новорожденным мышам через грудное молоко. В возрасте 6 месяцев мыши, несущие вирус, заболевают раком молочной железы из-за ретровируса. Кроме того, вирус лейкемии I (HTLV-1), обнаруженный в Т-клетках человека, уже много лет обнаруживается у людей. Подсчитано, что этот ретровирус вызывает лейкемию в возрасте от 40 до 50 лет. [30] Он имеет воспроизводимую структуру, которая может вызывать рак. Помимо обычной последовательности генов ретровирусов, HTLV-1 содержит четвертую область — PX. Эта область кодирует регуляторные белки Tax, Rex, p12, p13 и p30. Белок Tax инициирует лейкемический процесс и организует транскрипцию всех вирусных генов в интегрированной провирусной ДНК HTLV. [31]
Классификация
[ редактировать ]
Экзогенный
[ редактировать ]Этот раздел может потребовать очистки Википедии , чтобы соответствовать стандартам качества . Конкретная проблема заключается в следующем: это не таксон «Retroviridae», о котором говорится в статье; предложить перейти к Балтиморской классификации #Вирусы с обратной транскрипцией или Revtraviricetes . ( февраль 2021 г. ) |
Экзогенные ретровирусы — это инфекционные РНК- или ДНК-содержащие вирусы, которые передаются от одного организма к другому. В системе классификации Балтимора , которая объединяет вирусы в зависимости от способа синтеза информационной РНК , они подразделяются на две группы: группа VI: вирусы с одноцепочечной РНК с промежуточной ДНК в их жизненном цикле, и группа VII: двухцепочечные РНК-вирусы. ДНК-вирусы с промежуточной РНК в жизненном цикле. [ нужна ссылка ]
Вирусы группы VI
[ редактировать ]Все члены группы VI используют кодируемую вирусом обратную транскриптазу , РНК-зависимую ДНК-полимеразу, для производства ДНК из исходного РНК-генома вириона. Эта ДНК часто интегрируется в геном хозяина, как в случае ретровирусов и псевдовирусов , где она реплицируется и транскрибируется хозяином.
В группу VI входят:
- Заказать Ортервирусалес
- Семейство Belpaoviridae .
- Семейство Метавирусиды
- Семейство псевдовирусиды
- Семейство Retroviridae - ретровирусы, например ВИЧ.
- Семейство Caulimoviridae – семейство вирусов VII группы (см. ниже).
Семейство Retroviridae ранее было разделено на три подсемейства ( Oncovirinae , Lentivirinae и Spumavirinae ), но теперь разделено на два: Orthoretrovirinae и Spumaretrovirinae . Термин «онковирус» в настоящее время широко используется для описания вируса, вызывающего рак. В настоящее время в это семейство входят следующие роды:
- Подсемейство Орторетровиринае :
- Род Альфаретровирус ; включая вирус птичьего лейкоза и вирус саркомы Рауса
- Род Бетаретровирус ; включая вирус опухоли молочной железы мыши
- Род Гаммаретровирус ; включая вирус мышиного лейкоза и вирус кошачьего лейкоза
- Род Дельтаретровирус ; включая вирус лейкоза крупного рогатого скота и вызывающий рак Т-лимфотропный вирус человека.
- Род Эпсилонретровирус.
- Род Лентивирус ; включая вирус иммунодефицита человека 1 и обезьян и кошек . вирусы иммунодефицита
- Подсемейство Spumaretrovirinae :
- Род Бовиспумавирус.
- Род Equispumavirus.
- Род Felispumavirus
- Род Prosimiispumavirus.
- Род Симииспумавирус.
Обратите внимание, что согласно ICTV 2017, род Spumavirus был разделен на пять родов, а его прежний типовой вид Simian Foamy Virus теперь повышен до рода Simiispumavirus с не менее чем 14 видами, включая новый типовой вид Eastern шимпанзе, обезьяний пенистый вирус . [32]
Вирусы группы VII
[ редактировать ]Оба семейства в группе VII имеют геномы ДНК, содержащиеся в вторгающихся вирусных частицах. Геном ДНК транскрибируется как в мРНК для использования в качестве транскрипта при синтезе белка, так и в прегеномную РНК для использования в качестве матрицы во время репликации генома. кодируемая вирусом, Обратная транскриптаза, использует прегеномную РНК в качестве матрицы для создания геномной ДНК.
В группу VII входят:
- Семейство Caulimoviridae - например, вирус мозаики цветной капусты.
- Семейство Hepadnaviridae — например, вирус гепатита B.
Последнее семейство тесно связано с недавно предложенным
- Семейство Nackednaviridae — например, Nackednavirus африканских цихлид (ACNDV), ранее называвшийся вирусом гепатита B африканских цихлид (ACHBV). [33]
в то время как семейства Belpaoviridae , Metaviridae , Pseudoviridae , Retroviridae и Caulimoviridae составляют порядок Ortervirales . [34]
Эндогенный
[ редактировать ]Эндогенные ретровирусы формально не включены в эту классификационную систему и в целом подразделяются на три класса на основе родства с экзогенными родами:
- Класс I наиболее похож на гаммаретровирусы.
- Класс II наиболее похож на бетаретровирусы и альфаретровирусы.
- Класс III наиболее похож на спамавирусы.
Споры
[ редактировать ]Ретровирусы оказались в центре внимания нескольких недавних заявлений и утверждений, которые были в значительной степени дискредитированы научным сообществом. Первоначальное исследование, проведенное в 2009 году, казалось, позволило сделать новые выводы, которые могут изменить некоторые устоявшиеся знания по этой теме. Однако, хотя более поздние исследования опровергли некоторые утверждения о ретровирусах, есть несколько противоречивых фигур, которые продолжают делать заявления, которые в целом считаются не имеющими веских оснований или консенсуса в поддержку этих утверждений. [35] [36] [37]
Уход
[ редактировать ]Антиретровирусные препараты — это препараты для лечения инфекций, вызванных ретровирусами, в первую очередь ВИЧ . Различные классы антиретровирусных препаратов действуют на разных стадиях жизненного цикла ВИЧ . Комбинация нескольких (обычно трех или четырех) антиретровирусных препаратов известна как высокоактивная антиретровирусная терапия (ВААРТ). [38]
Лечение ветеринарных ретровирусов
[ редактировать ]Вирус лейкемии кошек и инфекции, вызванные вирусом иммунодефицита кошек, лечат биологическими препаратами , включая единственный иммуномодулятор, лицензированный в настоящее время для продажи в США, модулятор иммунитета Т-лимфоцитов (LTCI). [39]
Ссылки
[ редактировать ]- ^ «Таксономия вирусов: выпуск 2018b» . Международный комитет по таксономии вирусов (ICTV) . Март 2019 года . Проверено 16 марта 2019 г.
- ^ «ретровирус» . Оксфордский словарь английского языка . Архивировано из оригинала 26 сентября 2018 года . Проверено 25 сентября 2018 г.
- ^ Перейти обратно: а б с Картер Дж.Б., Сондерс В.А. (2007). Вирусология: принципы и приложения (1-е изд.). Чичестер, Англия: Джон Уайли и сыновья. п. 191. ИСБН 978-0-470-02386-0 . OCLC 124160564 .
- ^ Гроб Дж.М., Хьюз С.Х., Вармус Х.Э., ред. (1997). Ретровирусы . Лаборатория Колд-Спринг-Харбор. ISBN 978-0-87969-571-2 .
- ^ {Миллер, AD (2006). Ретровирусные векторы в генной терапии. Энциклопедия наук о жизни. doi:10.1038/npg.els.0005741}
- ^ Перейти обратно: а б Курт Р., Баннерт Н., ред. (2010). Ретровирусы: молекулярная биология, геномика и патогенез . Горизонт Научный. ISBN 978-1-904455-55-4 .
- ^ Чжэн, Цзялу; Вэй, Ютун; Хан, Гуань-Чжу (1 февраля 2022 г.). «Разнообразие и эволюция ретровирусов: перспективы вирусных «окаменелостей» » . Вирусология Синика . 37 (1): 11–18. дои : 10.1016/j.virs.2022.01.019 . ISSN 1995-820Х . ПМЦ 8922424 . ПМИД 35234634 .
- ^ Гроб, Джон М.; Хьюз, Стивен Х.; Вармус, Гарольд Э. (1997). Место ретровирусов в биологии . Лабораторный пресс Колд-Спринг-Харбор.
- ^ Гроб Дж. М. (1992). «Структура и классификация ретровирусов». В Леви Дж.А. (ред.). Ретровирусиды . Том. 1 (1-е изд.). Нью-Йорк: Пленум. п. 20. ISBN 978-0-306-44074-8 .
- ^ Перейти обратно: а б с Художник Марк М.; Коллинз, Кэтлин Л. (1 января 2019 г.), «ВИЧ и ретровирусы» , в Шмидте, Томасе М. (редактор), Энциклопедия микробиологии (четвертое издание) , Academic Press, стр. 613–628, doi : 10.1016/b978 -0-12-801238-3.66202-5 , ISBN 978-0-12-811737-8 , S2CID 188750910 , получено 3 мая 2020 г.
- ^ Олсон Э.Д., Мюзье-Форсайт К. (февраль 2019 г.). «Взаимодействие ретровирусного белка Gag с РНК: значение для упаковки специфической геномной РНК и сборки вириона» . Семинары по клеточной биологии и биологии развития . СИ: Дендритные клетки человека. 86 : 129–139. дои : 10.1016/j.semcdb.2018.03.015 . ПМК 6167211 . ПМИД 29580971 .
- ^ Гроб Дж. М., Хьюз С.Х., Вармус Х.Э. (1997). Вирионные белки . Лабораторный пресс Колд-Спринг-Харбор. ISBN 978-0-87969-571-2 .
- ^ Гроб 1992 , стр. 26–34.
- ^ Ким Ф.Дж., Баттини Дж.Л., Манель Н., Ситбон М. (январь 2004 г.). «Появление ретровирусов позвоночных и захват оболочки» . Вирусология . 318 (1): 183–91. дои : 10.1016/j.virol.2003.09.026 . ПМИД 14972546 .
- ^ Перейти обратно: а б Картер Дж.Б., Сондерс В.А. (2007). Вирусология: принципы и приложения . Чичестер, Англия: Джон Уайли и сыновья. ISBN 978-0-470-02386-0 . OCLC 124160564 .
- ^ Шампу Дж.Дж., Шульц С.Дж. (июнь 2009 г.). «Активность РНКазы H: структура, специфичность и функции в обратной транскрипции» . Журнал ФЭБС . 134 (1–2): 86–103. doi : 10.1016/j.virusres.2007.12.007 . ПМЦ 2464458 . ПМИД 18261820 .
- ^ Моеллинг К., Брокер Ф., Керриган Дж.Э. (2014). «РНКаза H: специфичность, механизмы действия и противовирусная мишень». Ретровирусы человека . Методы молекулярной биологии. Том. 1087. стр. 71–84. дои : 10.1007/978-1-62703-670-2_7 . ISBN 978-1-62703-669-6 . ПМИД 24158815 .
- ^ Перейти обратно: а б Варджиу Л., Родригес-Томе П., Спербер Г.О., Кадедду М., Гранди Н., Бликстад В. и др. (январь 2016 г.). «Классификация и характеристика эндогенных ретровирусов человека; распространены мозаичные формы» . Ретровирусология . 13 :7. дои : 10.1186/s12977-015-0232-y . ПМЦ 4724089 . ПМИД 26800882 .
- ^ Питерс, П.Дж., Марстон, Б.Дж., Вейдл, П.Дж., и Брукс, Дж.Т. (2013). Инфекция, вызванная вирусом иммунодефицита человека. Тропическая медицина Хантера и новые инфекционные заболевания, 217–247. doi:10.1016/b978-1-4160-4390-4.00027-8
- ^ Гроб Дж. М., Хьюз С.Х., Вармус Х.Э. (1997). «Генетическая организация» . Ретровирусы . Лабораторный пресс Колд-Спринг-Харбор. ISBN 978-0-87969-571-2 .
- ^ Белшоу Р., Перейра В., Кацуракис А., Талбот Дж., Пейс Дж., Берт А., Тристем М. (апрель 2004 г.). «Длительное реинфицирование генома человека эндогенными ретровирусами» . Труды Национальной академии наук Соединенных Штатов Америки . 101 (14): 4894–9. Бибкод : 2004PNAS..101.4894B . дои : 10.1073/pnas.0307800101 . ПМЦ 387345 . ПМИД 15044706 .
- ^ Медстранд П., ван де Лагемаат Л.Н., Данн К.А., Лэндри Дж.Р., Свенбак Д., Магер Д.Л. (2005). «Влияние мобильных элементов на эволюцию регуляции генов млекопитающих». Цитогенетические и геномные исследования . 110 (1–4): 342–52. дои : 10.1159/000084966 . ПМИД 16093686 . S2CID 25307890 .
- ^ Сваровская Е.С., Чеслок С.Р., Чжан В.Х., Ху В.С., Патхак В.К. (январь 2003 г.). «Уровень ретровирусных мутаций и точность обратной транскриптазы» . Границы бионауки . 8 (1–3): d117–34. дои : 10.2741/957 . ПМИД 12456349 .
- ^ Перейти обратно: а б Роусон Дж.М., Николаичик О.А., Кил Б.Ф., Патак В.К., Ху В.С. (ноябрь 2018 г.). «Рекомбинация необходима для эффективной репликации ВИЧ-1 и поддержания целостности вирусного генома» . Исследования нуклеиновых кислот . 46 (20): 10535–10545. дои : 10.1093/nar/gky910 . ПМК 6237782 . ПМИД 30307534 .
- ^ Кромер Д., Гримм А.Дж., Шлуб Т.Э., Мак Дж., Давенпорт, член парламента (январь 2016 г.). «Оценка скорости переключения и рекомбинации матрицы ВИЧ in vivo» . СПИД . 30 (2): 185–92. дои : 10.1097/QAD.0000000000000936 . ПМИД 26691546 . S2CID 20086739 .
- ^ Джолли С (март 2011 г.). «Передача ретровирусов от клетки к клетке: врожденный иммунитет и факторы рестрикции, индуцированные интерфероном» . Вирусология . 411 (2): 251–9. дои : 10.1016/j.virol.2010.12.031 . ПМК 3053447 . ПМИД 21247613 .
- ^ Маклахлан, Н. Джеймс; Дубови, Эдвард Дж. (2011). Ветеринарная вирусология Феннера (Четвертое изд.). Академическая пресса. п. 250. ИСБН 978-0-12-375159-1 . Проверено 6 мая 2020 г.
- ^ Айевсакун П., Кацуракис А. (январь 2017 г.). «Морское происхождение ретровирусов в раннем палеозое» . Природные коммуникации . 8 : 13954. Бибкод : 2017NatCo...813954A . дои : 10.1038/ncomms13954 . ПМЦ 5512871 . ПМИД 28071651 .
- ^ Депорт М, изд. (2010). Лентивирусы и макрофаги: молекулярные и клеточные взаимодействия . Кайстер Академик. ISBN 978-1-904455-60-8 .
- ^ Росс, СР (2018). Клеточные иммунные ответы на ретровирусы. Во взаимодействии ретровирусов и клеток (стр. 401–420). Эльзевир. https://doi.org/10.1016/B978-0-12-811185-7.00011-X
- ^ Баррелл, CJ, Ховард, CR, и Мерфи, FA (2017). Ретровирусы. В «Медицинской вирусологии Феннера и Уайта» (стр. 317–344). Эльзевир. https://doi.org/10.1016/b978-0-12-375156-0.00023-0
- ^ таксономии ICTV Браузер
- ^ Лаубер С., Зейтц С., Маттеи С., Су А., Бек Дж., Херштейн Дж. и др. (сентябрь 2017 г.). «Расшифровка происхождения и эволюции вирусов гепатита В с помощью семейства вирусов рыб без оболочки» . Клетка-хозяин и микроб . 22 (3): 387–399.e6. дои : 10.1016/j.chom.2017.07.019 . ПМК 5604429 . ПМИД 28867387 . и PDF
- ^ Крупович М., Бломберг Дж., Коффин Дж.М., Дасгупта И., Фан Х., Гиринг А.Д. и др. (июнь 2018 г.). «Ортервирусы: новый порядок вирусов, объединяющий пять семейств вирусов с обратной транскрипцией» . Журнал вирусологии . 92 (12). дои : 10.1128/JVI.00515-18 . ПМЦ 5974489 . ПМИД 29618642 .
- ↑ Проверка фактов Джуди Миковиц, скандальный вирусолог, нападающая на Энтони Фаучи в видеоролике о вирусном заговоре , Мартин Энсеринк, Джон Коэн, 8 мая 2020 г., доступ 17 июня 2022 г., веб-сайт science.org.
- ^ Нил, Стюарт Джей Ди; Кэмпбелл, Эдвард М. (2020). «Ложная наука: XMRV, COVID-19 и токсичное наследие доктора Джуди Миковиц» . Исследования СПИДа и ретровирусы человека . 36 (7): 545–549. дои : 10.1089/aid.2020.0095 . ПМЦ 7398426 . ПМИД 32414291 .
- ↑ «Вирусные заговорщики выдвигают нового чемпиона» , Дэйви Альба , 9 мая 2020 г., nytimes.com
- ^ Резерфорд Г.В., Сангани П.Р., Кеннеди Дж.Е. (2003). «Схемы поддерживающей антиретровирусной терапии с использованием трех или четырех препаратов по сравнению с двумя препаратами при ВИЧ-инфекции». Кокрейновская база данных систематических обзоров (4): CD002037. дои : 10.1002/14651858.CD002037 . ПМИД 14583945 .
- ^ Джинджерич Д.А. (2008). «Иммуномодулятор Т-лимфоцитов (LTCI): обзор иммунофармакологии нового биологического препарата» (PDF) . Международный журнал прикладных исследований в ветеринарной медицине . 6 (2): 61–68. ISSN 1559-470X .
Дальнейшее чтение
[ редактировать ]- Гроб Дж. М., Хьюз С.Х., Вармус Х.Э. (1997). Гроб Дж.М., Хьюз С.Х., Вармус Х.Э. (ред.). Ретровирусы . Лаборатория Колд-Спринг-Харбор. ISBN 978-0-87969-571-2 . ПМИД 21433340 . НБК19376.
- Призрак М (3 декабря 2007 г.). «Анналы науки: сюрприз Дарвина» . Житель Нью-Йорка .
- Досталкова, А; Воката, Б; Кауфман, Ф; Ульбрих, П; Рамл, Т; Румлова, М (2021). «Влияние малых полианионов на сборку in vitro избранных членов альфа-, бета- и гаммаретровирусов» . Вирусы . 13 (1): 129. дои : 10.3390/v13010129 . ПМЦ 7831069 . ПМИД 33477490 .
Внешние ссылки
[ редактировать ]- ViralZone Ресурс Швейцарского института биоинформатики для всех семейств вирусов, предоставляющий общую молекулярную и эпидемиологическую информацию (перейдите по ссылкам «Вирусы с ретро-транскрипцией» ).
- Ретровирусная анимация (требуется Flash)
- Ретровирусология Научный журнал
- Глава о жизненном цикле ретровирусов Кимбалла» из «Биологии (страницы онлайн-учебника по биологии)
