Герпесвирус, ассоциированный с саркомой Капоши
| Гаммагерпесвирус человека 8 | |
|---|---|
| |
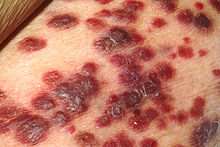
| саркома Капоши | |
| Классификация вирусов | |
| (без рейтинга): | Вирус |
| Область : | Дуплоднавирия |
| Королевство: | Хынггунвирэ |
| Тип: | Пепловирикота |
| Сорт: | Гервивирицеты |
| Заказ: | Герпесвирусные инфекции |
| Семья: | Ортогерпесвирусиды |
| Род: | Радиновирус |
| Разновидность: | Гаммагерпесвирус человека 8
|
Герпесвирус, ассоциированный с саркомой Капоши ( KSHV ), является девятым известным вирусом герпеса человека ; его официальное название, согласно Международному комитету по таксономии вирусов (ICTV), — гаммагерпесвирус человека 8 , или ВГЧ-8 . сокращенно [ 1 ] Как и у других герпесвирусов, его неофициальные названия используются как синонимы официального названия ICTV. Этот вирус вызывает саркому Капоши — рак, часто встречающийся у больных СПИДом . [ 2 ] а также первичная выпотная лимфома , [ 3 ] Мультицентрическая болезнь Кастлемана, ассоциированная с HHV-8, и синдром воспалительных цитокинов KSHV . [ 4 ] Это один из семи известных в настоящее время вирусов рака человека, или онковирусов . [ 2 ] Даже спустя много лет после открытия KSHV/HHV8 не существует известного лечения онкогенеза, связанного с KSHV.
История
[ редактировать ]В 1872 году Мориц Капоши описал опухоль кровеносного сосуда. [ 5 ] (первоначально называемая «идиопатическая множественная пигментированная саркома кожи»), которая с тех пор получила одноименное название саркома Капоши (КС). Сначала считалось, что СК является редкой опухолью среди еврейского и средиземноморского населения, пока позже не было установлено, что она чрезвычайно распространена среди населения Африки к югу от Сахары. Это привело к первым предположениям в 1950-х годах о том, что эта опухоль может быть вызвана вирусом. С началом эпидемии СПИДа в начале 1980-х годов произошло внезапное возобновление СК, поражающего больных СПИДом, при этом до 50% зарегистрированных больных СПИДом имели эту опухоль – необычайный уровень предрасположенности к раку. [ 6 ]
Тщательный анализ эпидемиологических данных Валери Берал, Томаса Петермана и Гарольда Яффе . [ 7 ] побудили этих исследователей предположить, что СК вызван неизвестным вирусом, передающимся половым путем, который редко вызывает опухоли, если только у хозяина не наблюдается иммуносупрессия , как при СПИДе. [ нужна ссылка ]

Еще в 1984 году ученые сообщили о том, что видели структуры, подобные вирусу герпеса, в опухолях СК, исследованных под электронной микроскопией . Ученые искали агент, вызывающий СК, и в качестве возможной причины было предложено более 20 агентов, включая цитомегаловирус и сам ВИЧ . В конечном итоге возбудитель был идентифицирован в 1994 году Юанем Чангом и Патриком С. Муром , командой жены и мужа из Колумбийского университета , посредством выделения фрагментов ДНК из вируса герпеса, обнаруженного в опухоли СК у пациента со СПИДом. [ 8 ] [ 9 ] [ 10 ] Чанг и Мур использовали анализ репрезентативных различий , или RDA, чтобы найти KSHV, сравнивая опухолевую ткань KS пациента со СПИДом с его собственной непораженной тканью. Идея этого эксперимента заключалась в том, что если вирус вызывает СК, геномная ДНК в двух образцах должна быть абсолютно идентична, за исключением ДНК, принадлежащей вирусу. В своем первоначальном эксперименте с RDA они выделили два небольших фрагмента ДНК, которые составляли менее 1% фактического вирусного генома. Эти фрагменты были похожи (но все же отличались от) известных последовательностей герпевируса, что указывало на присутствие нового вируса. На основе этих фрагментов исследовательская группа менее чем через два года смогла секвенировать весь геном вируса. [ нужна ссылка ]
Открытие этого герпесвируса вызвало серьезные споры и научную борьбу, пока не было собрано достаточно данных, чтобы показать, что KSHV действительно был возбудителем саркомы Капоши. [ 11 ] В настоящее время известно, что этот вирус широко распространен среди людей, живущих в странах Африки к югу от Сахары; промежуточные уровни инфекции наблюдаются в популяциях Средиземноморья (включая Ливан, Саудовскую Аравию, Италию и Грецию), а низкие уровни инфекции наблюдаются в большинстве популяций Северной Европы и Северной Америки. Геи и бисексуальные мужчины более восприимчивы к заражению (пока неизвестные пути передачи половым путем), тогда как в развивающихся странах вирус передается несексуальным путем. [ нужна ссылка ]
Вирусология
[ редактировать ]KSHV — это вирус герпеса , большой двухцепочечный ДНК-вирус с белковой оболочкой, упаковывающей его нуклеиновые кислоты, называемый капсидом , который затем окружен аморфным белковым слоем, называемым тегументом , и, наконец, заключен в липидную оболочку, полученную из часть клеточной мембраны. KSHV имеет геном , длина которого составляет примерно 165 000 оснований нуклеиновых кислот. Вирусный геном состоит из уникальной области длиной ~145 тыс. оснований, кодирующей все экспрессируемые вирусные гены, фланкированной ~20-30 тыс. оснований концевых повторяющихся последовательностей. [ 12 ] Каждая терминальная единица повтора имеет длину 801 п.н., содержит 85% G+C и ориентирована повторяющимся образом «голова к хвосту». KSHV — это радиновирус , род Herpes, примечательный тем, что он украл множество генов из клеток-хозяев, включая, в случае KSHV, гены, которые кодируют белок, связывающий комплемент , IL-6 , BCL-2 , циклин -D, G-белок. -связанный рецептор , регуляторный фактор интерферона и белок, ингибирующий Flice ( FLIP ), а также белки синтеза ДНК, включая дигидрофолатредуктазу , тимидин. киназа , тимидилатсинтетаза , ДНК- полимераза и многие другие. Хотя ни один другой опухолевый вирус человека не обладает такими же генами, другие опухолевые вирусы нацелены на одни и те же клеточные пути, иллюстрируя, что на базовом уровне все опухолевые вирусы, по-видимому, атакуют одни и те же пути клеточного контроля, так называемые пути супрессора опухоли. [ нужна ссылка ]
Решающее значение для проникновения KSHV в клетки [ 13 ] являются рецептором EPH A2 , [ 14 ] Час, [ 15 ] ТСГ101 , [ 16 ] и несколько интегринов (идентичность которых еще не подтверждена). [ 17 ] После заражения вирус проникает в лимфоциты через макропиносомы . [ нужна ссылка ] Как только вирус вновь заражает клетку, липидная мембрана сбрасывается, и вирион перемещается в ядро. Вирусный геном высвобождается там, где он превращается в эписому посредством плохо изученного процесса, который, по-видимому, включает гомологичную рекомбинацию концевых повторов. [ нужна ссылка ] Вирусная эписома хроматинизируется при попадании в ядро клетки-хозяина. [ 18 ]
После проникновения вирус обычно остается в латентном («тихом») состоянии. Только подмножество генов, которые кодируются в области, связанной с латентностью KSHV (KLAR), экспрессируются во время латентного периода, включая ядерный антиген, связанный с латентностью (LANA), vFLIP, vCyclin и 12 микроРНК. Латентный период является отличительной чертой всех известных на сегодняшний день этиологий, связанных с KSHV, включая все онкогенезы, связанные с KSHV. Было показано, что как гены, кодирующие белок, такие как LANA, так и некодирующие гены (микроРНК), кодируемые в KLAR, важны для канцерогенеза, связанного с KSHV. Для изучения функций микроРНК был создан подробный протокол мутагенеза бакмид и полный набор клеточных линий, несущих делеционные мутанты микроРНК, которые доступны исследователям в качестве ресурса. [ 19 ] Кроме того, было показано, что vFLIP и vCyclin косвенно вмешиваются в сигнальный путь TGF-β, индуцируя онкогенный кластер mir17-92 хозяина. [ 20 ] Эти наблюдения представляют собой новый механизм, который может быть важен для онкогенеза и ангиогенеза KSHV, что является отличительной чертой СК. [ нужна ссылка ]
В латентный период LANA является единственным вирусным белком, необходимым для репликации вируса, которая осуществляется механизмом репликации хозяина. LANA привязывает вирусную ДНК к клеточным хромосомам, ингибирует р53 и белок ретинобластомы , а также подавляет вирусные гены, необходимые для полноценного производства и сборки вируса («литическая репликация»). Почему в латентный период экспрессируется только часть вирусных генов, до конца не понятно. Но было показано, что экспрессия генов, связанная с латентным периодом, может быть частично объяснена характерным эпигенетическим состоянием, которое эписома KSHV приобретает во время латентного периода. LANA играет важную роль во время латентного периода, регулируя транскрипты как хозяина, так и вируса, а также связываясь с несколькими активными промоторами; он также связывается с белком-хозяином hSET1, который создает метки H3K4me3 в хроматине. [ 21 ]
Различные сигналы, такие как воспаление, могут спровоцировать вступление вируса в литическую репликацию. Первичный вирусный белок, ответственный за переключение между латентной и литической репликацией, известен как активатор трансактивации репликации ORF50 (RTA). Когда условия клеточной сигнализации активируют выработку RTA, это, в свою очередь, активирует синтез стереотипного каскада вторичных и третичных вирусных белков, которые в конечном итоге составляют компоненты вирусного капсида, а также ферменты синтеза ДНК, необходимые для репликации вирусного генома. [ 22 ] Считается, что во время литической репликации геном вируса реплицируется как непрерывная линейная молекула, отделенная от эписомы (так называемая модель катящегося круга ). По мере репликации каждой единицы генома она разрезается внутри области терминального повтора, а затем упаковывается в вирусную частицу (вирион). Затем вирус покрывается липидной мембраной, проходя через ядро и цитоплазму и выходя из клетки. Таким образом, хотя геном KSHV имеет кольцевую форму в ядре латентно инфицированных клеток, в инфекционных вирусах он упакован в виде линейной молекулы. Когда вирус вступает в литическую репликацию, из одной клетки могут образовываться тысячи вирусных частиц, что обычно приводит к гибели инфицированной клетки. [ нужна ссылка ]
COVID-19 и КШВ
[ редактировать ]В 2020 году было обнаружено, что заражение вирусом SARS-CoV-2 , вирусом, вызывающим COVID-19 , может индуцировать литическую реактивацию KSHV в организме человека, в результате чего вирус герпеса прекращает латентный период и начинает образование раковых клеток. . Кроме того, было обнаружено, что некоторые лекарства, используемые для лечения инфекции SARS-CoV-2, а именно нафамостат и азитромицин , в конечном итоге способствуют выработке зрелых вирионов, «... потенциально индуцируя литическую реактивацию KSHV». [ 23 ]
Патофизиология
[ редактировать ]Механизмы заражения вирусом недостаточно изучены. Здоровые люди могут заразиться вирусом и не проявлять никаких признаков или симптомов из-за способности иммунной системы сдерживать инфекцию. Инфекция вызывает особую тревогу у людей с ослабленным иммунитетом . Больные раком, получающие химиотерапию, больные СПИДом и пациенты, перенесшие трансплантацию органов, подвергаются высокому риску проявления признаков инфекции. [ нужна ссылка ] .
Недавние достижения в области технологий секвенирования показали, что вирус хроматинируется в латентном периоде. Также было показано, что микроРНК, кодируемая вирусом, манипулирует и взаимодействует не только с мРНК хозяина, но также дерегулирует длинную некодирующую РНК хозяина (днРНК). [ 24 ] Совсем недавно кольцевые РНК (циркулярные РНК) были обнаружены как при EBV, так и при KSHV. [ 25 ] [ 26 ] [ 27 ]
Считается, что заражение этим вирусом происходит на протяжении всей жизни, но здоровая иммунная система будет держать вирус под контролем. У многих людей, инфицированных KSHV, никогда не проявляются никакие симптомы. Саркома Капоши возникает, когда у человека, инфицированного KSHV, снижается иммунитет из-за СПИДа, лечения или, очень редко, старения.
КШВ является известным возбудителем четырех заболеваний: [ 4 ] [ 28 ]
- Саркома Капоши – ангиопролиферативная опухоль, которая может поражать кожу (чаще всего), лимфатические узлы или внутренние органы.
- ВГЧ-8-ассоциированная мультицентрическая болезнь Кастлемана – лимфопролиферативное заболевание .
- Первичная выпотная лимфома – KSHV-ассоциированная агрессивная лимфома с участием В-клеток, которые представляют собой незрелые плазматические клетки , называемые плазмобластами и рассматриваемые как один тип лимфоидных новообразований с плазмобластной дифференцировкой .
- Синдром воспалительных цитокинов KSHV – синдром с MCD-подобными симптомами, но без сопутствующей патологии.
Эпидемиология
[ редактировать ]В 1970-е годы глобальная распространенность ВГЧ-8 составляла от 2 до 10%. [ 29 ] Серораспространенность ВГЧ-8 значительно варьируется в зависимости от географического положения, а уровень инфицирования в странах Северной Европы, Юго-Восточной Азии и Карибского бассейна составляет 2-4%. [ 30 ] в странах Средиземноморья - примерно 10%, а в странах Африки к югу от Сахары - примерно 40%. [ 31 ] В Южной Америке уровень заражения в целом низкий, но высок среди индейцев . [ 32 ] Даже внутри отдельных стран в разных регионах можно наблюдать значительные различия: уровень заражения составляет около 19,2% в Синьцзяне по сравнению с примерно 9,5% в Хубэе , Китай. [ 33 ] Хотя было показано, что серологическая распространенность линейно увеличивается с возрастом, [ 33 ] [ 34 ] [ 35 ] [ 36 ] в странах с высоким уровнем инфицирования может наблюдаться более высокая серологическая распространенность в более молодых возрастных группах. [ 37 ] Уровень образования показал обратную корреляцию с уровнем заражения. [ 34 ] [ 35 ] Лица, инфицированные ВИЧ-1 или генитальными бородавками, обычно более склонны к коинфекции ВГЧ-8. [ 31 ] [ 33 ] [ 38 ]
В странах с низкой серологической распространенностью ВГЧ-8 преимущественно встречается у больных СПИДом и СК. [ 39 ] В странах с высокой серологической распространенностью инфекция часто встречается в детском возрасте. [ 40 ] что указывает на вероятную передачу вируса от матери ребенку через слюну. [ 41 ] [ 42 ] По данным исследования в Замбии , у всех детей с СК матери были положительными на ВГЧ-8, тогда как не все дети, чьи матери были больны СК, были положительными по ВГЧ-8. [ 43 ] По данным другого исследования в Замбии, 13,8% детей были серопозитивными к ВГЧ-8 к 4 годам. [ 44 ] Не было показано, что серораспространенность существенно различается в зависимости от пола или семейного положения. [ 36 ]
Эволюция
[ редактировать ]По оценкам, самый последний общий предок этого вируса в Средиземноморье, Иране и Синьцзяне (Китай) появился 29 872 года (95% наивысшая плотность вероятности 26 851–32 760 лет) назад. [ 45 ] Самый последний общий предок вирусов, выделенных в Синьцзяне, произошел 2037 лет назад (95% наивысшая плотность вероятности 1843–2229 лет) назад. Учитывая исторические связи между Средиземноморьем и Синьцзяном в римский период, вполне вероятно, что этот вирус был занесен в Синьцзян по Шелковому пути . Частота мутаций оценивалась в 3,44 × 10 −6 замен на сайт в год (95% наивысшая плотность вероятности 2,2 × 10 −6 до 4,71 × 10 −6 ). Однако глобальное распространение различных генотипов KSHV и потенциальный путь передачи требуют дальнейшего изучения. [ нужна ссылка ]
Типирование изолятов основано на вариабельном мембранном белке К1. Признаны шесть типов (A – F). [ 46 ]
Профилактика
[ редактировать ]Поскольку люди, инфицированные KSHV, передают вирус бессимптомно, половым партнерам следует проявлять осторожность при незащищенном сексе и действиях, при которых во время сексуальной активности может произойти обмен слюной. Разумный совет — использовать презервативы , когда это необходимо, и избегать глубоких поцелуев с партнерами, инфицированными КШВ и ВИЧ или чей статус неизвестен.
Уход
[ редактировать ]Саркома Капоши обычно представляет собой локализованную опухоль, которую можно лечить хирургическим путем или местным облучением. химиотерапия такими препаратами, как липосомальные антрациклины или паклитаксел Может использоваться , особенно при инвазивном заболевании. Противовирусные препараты, такие как ганцикловир , которые нацелены на репликацию герпесвирусов, таких как KSHV, используются для успешного предотвращения развития саркомы Капоши. [ 47 ] хотя при развитии опухоли эти препараты практически бесполезны или бесполезны. Для больных СПИД-КС наиболее эффективной терапией является высокоактивная антиретровирусная терапия, направленная на снижение ВИЧ-инфекции. [ 48 ] У пациентов со СПИДом, получающих адекватное лечение против ВИЧ, частота возникновения саркомы Капоши может снизиться до 90%.
Хотя KSHV влияет на иммунную систему хозяина, существует большая вероятность того, что клиническое вмешательство восстановит это изменение. Одной из проблем является подавление сверхэкспрессии клеток-мишеней, подавляющих иммунитет. При длительной стимуляции воспаления клетка-мишень становится неспособной реагировать, что приводит к истощению фенотипа. Активационная иммунотерапия может оживить и улучшить функцию иммунных клеток. По сравнению с другими видами иммунотерапии, методы лечения, нацеленные на белок 1, препятствующий запрограммированной гибели клеток ( PD-1 )/лиганд запрограммированной смерти 1 ( PD-L1 ), имели большой успех. Из-за инфекции KSHV моноциты увеличивают экспрессию PD-1, которая является ингибирующей молекулой, и вызывают ускользание иммунитета при многих типах опухолей. В NK-клетках пациентов с КС-ВИЧ наблюдается высокая экспрессия PD-1, что приводит к истощению фенотипа. Антитело против PD-1 ( ниволумаб или пембролизумаб ) продемонстрировало значительный противоопухолевый эффект. Ниволумаб в настоящее время находится в I фазе клинических исследований, а пембролизумаб показал свою эффективность при лечении пациентов с ВИЧ и СК в I фазе и находится во II фазе клинических исследований. Аналог талидомида – Помалидомид также был одобрен FDA в 2011 году. Было показано, что помалидомид восстанавливает экспрессию MHC-1 , который помогает клеткам отображать внутриклеточные белки цитотоксическим Т-клеткам, а также может подавлять экспрессию PD-L1 и увеличивать количество CD8+ Т-клеток. убийство. [ 49 ]
гены КШВ
[ редактировать ]KSHV кодирует около 90 генов и множество некодирующих РНК, таких как микроРНК. [ 50 ] Гены «ORF» названы в зависимости от положения в геноме гомологичных генов первого описанного радиновируса, герпесвируса саймири. Гены «K» уникальны для KSHV. Некоторые гены KSHV имеют хорошо изученные функции, тогда как другие остаются неохарактеризованными. [ нужна ссылка ]
ORF2 – дигидрофолатредуктаза
ORF8 – gB – гликопротеин оболочки , участвующий в проникновении вируса.
ORF9 – Pol8 – ДНК-полимераза, необходимая для репликации вирусной ДНК.
ORF10 – регулирует экспорт РНК и реакцию на IFN типа I.
ORF16 – v Bcl2
ORF18, ORF24, ORF30, ORF31, ORF34, ORF66 – факторы вирусной транскрипции, необходимые для экспрессии поздних генов.
ORF21 – вТК – тимидинкиназа
ORF22 – gH – гликопротеин оболочки , участвующий в проникновении вируса.
ORF23 – нехарактерный
ORF25, ORF26 и ORF65 – капсидные белки
ORF33 – участвует в образовании вирусных частиц.
ORF34 – неясная функция
ORF35 – неясная функция, мутант не экспрессирует ранние вирусные гены.
ORF36 – vPK – вирусная протеинкиназа, выполняющая множество ролей в цикле репликации.
ORF37 - SOX - белок с двойной функцией - активность ДНКазы необходима для упаковки генома, а активность РНКазы регулирует экспрессию гена хозяина.
ORF38 – участвует в образовании вирусных частиц.
ORF39 – gM – гликопротеин оболочки
ORF40 и ORF41 – геликаза и примаза – репликация ДНК
ORF42 – нехарактерный
ORF45 - белок тегумента , связывает и предотвращает дефосфорилирование рибосомальных киназ S6 p90 (RSK) и ERK для модуляции ERK/RSK MAPK. сигнального пути
ORF47 – gL – гликопротеин оболочки, участвующий в проникновении вируса.
ORF49 - может потребоваться для экспрессии вирусных генов.
ORF50 – RTA, активатор репликации и транскрипции – основной фактор транскрипции, управляющий литической реактивацией KSHV.
ORF52 - KicGAS - тегументный белок, необходимый для образования вирионов и ингибирования cGAS. восприятия ДНК
ORF53 – gN – гликопротеин оболочки
ORF55 – неохарактеризованный
ORF57 – MTA – регулирует стабильность РНК, экспорт и трансляцию вирусных генов.
ORF59 – PF–8 – фактор процессивности полимеразы, дополнительная субъединица вирусной ДНК-полимеразы.
ORF67 и ORF69 – ядерный выход
ORF70 – тимидилатсинтаза
ORF72 – против Циклина
ORF73 – LANA , латентно-ассоциированный ядерный антиген – привязывает геном к хромосоме во время латентного периода, а также регулирует экспрессию генов хозяина. Цитоплазматическая форма LANA может ингибировать активацию иммунных ответов.
ORF74 – vGPCR
ORF75 – ФГАРАТ
ПАН, полиаденилированная ядерная РНК – некодирующие линейные и кольцевые РНК.
микроРНК (mirKs) – вирусные микроРНК, экспрессируемые в латентный период для регуляции пролиферации и гибели клеток.
К1 – участвует в онкогенезе
K2 - интерлейкина 6 гомолог , Q2HRC7
К3 и К5 – убиквитин Е3-лигазы – регулируют презентацию антигена.
K4 – vCCL2 – хемокин
K4.1 – vCCL3 – хемокин
K8 - репрессор транскрипции - модулирует хроматин.
К8.1 – гликопротеин оболочки
K9 – v IRF 1, фактор регуляции вирусного интерферона 1
K10 – v IRF кольцевая РНК ( circRNA также генерируется 4. Из этого локуса ) .
K10.5-v IRF 3 (первоначально обозначенный LANA2) экспрессируется в латентном периоде в клеточных линиях PEL, но также является настоящим литическим фактором, как и все vIRF. [ 51 ]
К11 – v ИРФ 2
К12 – капосин
К13 – v ФЛИП
См. также
[ редактировать ]- Онковирус (вирус рака)
- Парадокс курильщика
Ссылки
[ редактировать ]- ^ «Основной список видов ICTV 2018b.v2» . Международный комитет по таксономии вирусов . Архивировано из оригинала 30 марта 2019 года . Проверено 13 июня 2019 г.
- ^ Jump up to: а б Бошофф, К.; Вайс, Р. (2002). «Злокачественные новообразования, связанные со СПИДом». Обзоры природы Рак . 2 (5): 373–382. дои : 10.1038/nrc797 . ПМИД 12044013 . S2CID 13513517 .
- ^ Сезарман, Э.; Чанг, Ю.; Мур, PS; Саид, JW; Ноулз, DM (1995). «Связанные с саркомой Капоши герпесвирусоподобные последовательности ДНК в лимфомах полостей тела, связанных со СПИДом» . Медицинский журнал Новой Англии . 332 (18): 1186–1191. дои : 10.1056/NEJM199505043321802 . ПМИД 7700311 .
- ^ Jump up to: а б Гонсалвес, Присцила Х.; Зигельбауэр, Йозеф; Ульдрик, Томас С.; Ярчоан, Роберт (2017). «Рак, связанный с герпесвирусом саркомы Капоши, и связанные с ним заболевания» . Curr Opin ВИЧ СПИД . 12 (1): 47–56. дои : 10.1097/COH.0000000000000330 . ПМК 6311702 . ПМИД 27662501 .
- ^ Капоши, М. (1872). «Идиопатическая множественная пигментная саркома кожи» . Архив дерматологии и сифилиса . 4 (2): 265–273. дои : 10.1007/BF01830024 . S2CID 31438763 .
Переведено на Капоши, М. (2008). «Идиопатическая множественная пигментированная саркома кожи» . CA: Журнал рака для врачей . 32 (6): 342–347. дои : 10.3322/canjclin.32.6.342 . S2CID 72037330 . - ^ Ла Ферла, Л.; Пинцоне, MR; Пелликано, Г.Ф.; Нуннари, Г. (01 апреля 2016 г.). «Саркома Капоши у ВИЧ-инфицированных больных: обзор литературы» . Инфекционные болезни и тропическая медицина. п. 2 . Проверено 21 февраля 2023 г.
- ^ Берал В., Петерман Т.А., Беркельман Р.Л., Джаффе Х.В. (1990). «Саркома Капоши у больных СПИДом: инфекция, передающаяся половым путем?» . Ланцет (Представлена рукопись). 335 (8682): 123–8. дои : 10.1016/0140-6736(90)90001-L . ПМИД 1967430 . S2CID 35639169 .
- ^ Чанг, Ю.; Цезарьман, Э.; Пессин, М.С.; Ли, Ф.; Калпеппер, Дж.; Ноулз, DM; Мур, PS (1994). «Идентификация герпесвирусоподобных последовательностей ДНК в саркоме Капоши, связанной со СПИДом» . Наука 266 (5192): 1865–1869. Бибкод : 1994Sci... 266.1865C дои : 10.1126/science.7997879 . ПМИД 7997879 .
- ^ Мур П.С., Чанг И (май 1995 г.). «Обнаружение герпевирусоподобных последовательностей ДНК в саркоме Капоши у больных с ВИЧ-инфекцией и без нее» . Медицинский журнал Новой Англии . 332 (18): 1181–5. дои : 10.1056/NEJM199505043321801 . ПМИД 7700310 . S2CID 13465834 .
- ^ Антман, К.; Чанг, Ю. (2000). «Саркома Капоши». Медицинский журнал Новой Англии . 342 (14): 1027–1038. дои : 10.1056/NEJM200004063421407 . ПМИД 10749966 .
- ^ Бошофф С., Вайс Р.А. (май 2000 г.). «Разрешение споров по поводу саркомы Капоши» . Журнал Национального института рака . 92 (9): 677–679. дои : 10.1093/jnci/92.9.677 . ПМИД 10793096 .
- ^ Руссо Дж.Дж., Бохенцки Р.А., Чиен М.С. и др. (декабрь 1996 г.). «Нуклеотидная последовательность герпесвируса, ассоциированного с саркомой Капоши (HHV8)» . Труды Национальной академии наук Соединенных Штатов Америки . 93 (25): 14862–7. Бибкод : 1996PNAS...9314862R . дои : 10.1073/pnas.93.25.14862 . ПМК 26227 . ПМИД 8962146 .
- ^ Кумар, Бинод; Чандран, Бала (14 ноября 2016 г.). «Проникновение и перемещение KSHV в клетках-мишенях: перехват клеточных сигнальных путей, актина и динамики мембран» . Вирусы . 8 (11): 305. дои : 10.3390/v8110305 . ISSN 1999-4915 . ПМК 5127019 . ПМИД 27854239 .
- ^ Нейпель Ф., Флекенштейн Б., Хан А. и др. (июнь 2012 г.). «Тирозинкиназа А2 рецептора эфрина является клеточным рецептором герпесвируса, ассоциированного с саркомой Капоши» . Природная медицина . 18 (6): 961–968. дои : 10.1038/нм.2805 . ПМЦ 3645317 . ПМИД 22635007 .
- ^ Веттил, Моханан Валия; Кумар, Бинод; Ансари, Майрадж Ахмед; Дутта, Дипанджан; Икбал, Джавед; Гъйши, Олси; Боттеро, Вирджиния; Чандран, Bullet (апрель 2016 г.). «Компонент ESCRT-0 Hrs способствует макропиноцитозу герпесвируса, ассоциированного с саркомой Капоши, в дермальных микрососудистых эндотелиальных клетках человека» . Журнал вирусологии . 90 (8): 3860–3872. дои : 10.1128/JVI.02704-15 . ISSN 1098-5514 . ПМЦ 4810545 . ПМИД 26819309 .
- ^ Кумар, Бинод; Дутта, Дипанджан; Икбал, Джавед; Ансари, Майрадж Ахмед; Рой, Арунава; Чикоти, Лила; Пизано, Джина; Веттил, Моханан Валия; Чандран, Бала (октябрь 2016 г.). «Белок ESCRT-I Tsg101 играет роль в постмакропиноцитарном трафике и инфицировании эндотелиальных клеток герпесвирусом, ассоциированным с саркомой Капоши» . ПЛОС Патогены . 12 (10): e1005960. дои : 10.1371/journal.ppat.1005960 . ISSN 1553-7374 . ПМК 5072609 . ПМИД 27764233 .
- ^ Кампаделли-Фьюме Дж., Коллинз-МакМиллен Д. и др. (июль 2016 г.). «Интегрины как рецепторы герпервируса и медиаторы сигналосомы хозяина». Ежегодный обзор вирусологии . 3 (1): 215–236. doi : 10.1146/annurev-virology-110615-035618 . hdl : 11585/593080 . ПМИД 27501260 .
- ^ Пурушотаман и др. (февраль 2016 г.). «Репликация и обслуживание генома KSHV» . Границы микробиологии . 7:54 . дои : 10.3389/fmicb.2016.00054 . ПМЦ 4740845 . ПМИД 26870016 .
- ^ Джайн, Вайбхав; Плезанс-Бонстафф, Карли; Сангани, Раджникумар; Ланье, Кертис; Дольче, Александр; Ху, Цзяньхун; Брюлуа, Кевин; Хекер, Ирина; Тернер, Питер; Ренне, Рольф; Крюгер, Брайан (19 февраля 2016 г.). «Набор инструментов для исследования микроРНК герпесвируса: создание полного набора делеционных мутантов микроРНК KSHV» . Вирусы . 8 (2): 54. дои : 10.3390/v8020054 . ISSN 1999-4915 . ПМЦ 4776209 . ПМИД 26907327 .
- ^ Чой, Х.С.; Джайн, В; Крюгер, Б; Маршалл, В.; Ким, Швейцария; Шислер, Дж.Л.; Уитби, Д; Ренне, Р. (2015). «Герпесвирус, ассоциированный с саркомой Капоши (KSHV), индуцирует онкогенный кластер миР-17-92 и подавляет передачу сигналов TGF-β» . ПЛОС Патогены . 11 (11): e1005255. doi : 10.1371/journal.ppat.1005255 . ПМЦ 4636184 . ПМИД 26545119 .
- ^ Бу В., Палмери Д., Кришнан Р. и др. (ноябрь 2008 г.). «Идентификация прямых транскрипционных мишеней белка литического переключателя Rta, ассоциированного с саркомой Капоши, путем условной ядерной локализации» . Журнал вирусологии . 82 (21): 10709–23. дои : 10.1128/JVI.01012-08 . ПМК 2573185 . ПМИД 18715905 .
- ^ Анжела Бетсаида Б. Лагипо (6 октября 2020 г.). «Препараты против SARS-CoV-2 и анти-COVID-19 активируют герпесвирус, связанный с саркомой Капоши » Новости Медицинские науки о жизни.
- ^ Сетураман, С; Гей, Луизиана; Джайн, В; Хеккер, я; Ренне, Р. (июль 2017 г.). «микроРНК-зависимая и независимая дерегуляция длинных некодирующих РНК онкогенным герпесвирусом» . ПЛОС Патогены . 13 (7): e1006508. doi : 10.1371/journal.ppat.1006508 . ПМЦ 5531683 . ПМИД 28715488 .
- ^ Топтан, Т; Абере, Б; Налесник, М.А.; Свердлов, С.Х.; Ранганатан, С; Ли, Н; Шаир, К.Х.; Мур, PS; Чанг, Ю (11 сентября 2018 г.). «Опухолевые вирусы с кольцевой ДНК образуют кольцевые РНК» . Труды Национальной академии наук Соединенных Штатов Америки . 115 (37): Е8737–Е8745. Бибкод : 2018PNAS..115E8737T . дои : 10.1073/pnas.1811728115 . ПМК 6140489 . ПМИД 30150410 .
- ^ Тагава, Т; Гао, С; Копарде, В.Н.; Гонсалес, М; Спудж, Дж.Л.; Серкинья, AP; Люрен, К; Рамасвами, Р; Ульдрик, Т.С.; Ярчоан, Р; Зигельбауэр, Дж. М. (11 декабря 2018 г.). «Открытие кольцевых РНК, кодируемых вирусом герпеса саркомы Капоши, и человеческой противовирусной кольцевой РНК» . Труды Национальной академии наук Соединенных Штатов Америки . 115 (50): 12805–12810. Бибкод : 2018PNAS..11512805T . дои : 10.1073/pnas.1816183115 . ПМК 6294913 . ПМИД 30455306 .
- ^ Унгерлейдер, Северная Каролина; Джайн, В; Ван, Ю; Мэнесс, Нью-Джерси; Блэр, Р.В.; Альварес, X; Мидкифф, К; Колсон, Д; Бай, С; Робертс, К; Мосс, Западная Нью-Йорк; Ван, X; Серфец, Дж; Седдон, М; Леман, Т; Ма, Т; Донг, Ю; Ренне, Р; Тиббетс, ЮАР; Флемингтон, Великобритания (15 марта 2019 г.). «Сравнительный анализ репертуаров кольцевых РНК гаммагерпесвируса: консервативные и уникальные вирусные кольцевые РНК» . Журнал вирусологии . 93 (6). дои : 10.1128/JVI.01952-18 . ПМК 6401440 . ПМИД 30567979 .
- ^ Чен Би Джей, Чуан СС (март 2020 г.). «Лимфоидные новообразования с плазмабластической дифференцировкой: комплексный обзор и диагностические подходы» . Достижения анатомической патологии . 27 (2): 61–74. дои : 10.1097/PAP.0000000000000253 . ПМИД 31725418 .
- ^ Галло, Роберт К. (4 декабря 1998 г.). «Загадки саркомы Капоши» . Наука . 282 (5395): 1837–1839. дои : 10.1126/science.282.5395.1837 . ISSN 0036-8075 . ПМИД 9874635 . S2CID 29362584 .
- ^ Чжан, Тецзюнь; Ван, Линдинг (2016). «Эпидемиология герпесвируса, ассоциированного с саркомой Капоши, в Азии: проблемы и возможности». Журнал медицинской вирусологии . 89 (4): 563–570. дои : 10.1002/jmv.24662 . ISSN 0146-6615 . ПМИД 27531516 . S2CID 1145299 .
- ^ Jump up to: а б Чатлинн, LG; Аблаши, Д.В. (1999). «Сероэпидемиология герпесвируса, ассоциированного с саркомой Капоши (KSHV)». Семинары по биологии рака . 9 (3): 175–85. дои : 10.1006/scbi.1998.0089 . ПМИД 10343069 .
- ^ Моханна, С; Мако, В; Браво, Ф; Готуццо, Э (2005). «Эпидемиология и клинические характеристики классической саркомы Капоши, серологическая распространенность и варианты вируса герпеса человека 8 в Южной Америке: критический обзор старой болезни» . Международный журнал инфекционных заболеваний . 9 (5): 239–50. дои : 10.1016/j.ijid.2005.02.004 . ПМИД 16095940 .
- ^ Jump up to: а б с Фу, Б; Солнце, Ф; Ли, Б; Ян, Л; Цзэн, Ю; Солнце, Х; Сюй, Ф; Рейнер, С; Гуадалупе, М; Гао, С.Дж.; Ван, Л. (2009). «Серораспространенность герпесвируса, связанного с саркомой Капоши, и факторы риска в Синьцзяне, Китай» . Журнал медицинской вирусологии . 81 (8): 1422–31. дои : 10.1002/jmv.21550 . ПМЦ 2755560 . ПМИД 19551832 .
- ^ Jump up to: а б Пельсер, К; Витале, Ф; Уитби, Д; Граубар, BI; Мессина, А; Гафа, Л; Браун, Э.Э.; Андерсон, Луизиана; Романо, Н; Лаурия, К; Гедерт, Джей Джей (2009). «Социально-экономические и другие корреляты серологической распространенности герпесвируса, связанного с саркомой Капоши, среди пожилых людей на Сицилии» . Журнал медицинской вирусологии . 81 (11): 1938–44. дои : 10.1002/jmv.21589 . ПМЦ 2784645 . ПМИД 19777527 .
- ^ Jump up to: а б Ван, Х; Лю, Дж; Дилимулати; Ли, Л; Рен, З; Вэнь, Х; Ван, X (2011). «Серораспространенность и факторы риска герпесвирусной инфекции, связанной с саркомой Капоши, среди общего уйгурского населения южного и северного региона Синьцзяна, Китай» . Вирусологический журнал . 8 : 539. дои : 10.1186/1743-422X-8-539 . ПМЦ 3266657 . ПМИД 22168313 .
- ^ Jump up to: а б Олсен, С.Дж.; Чанг, Ю; Мур, PS; Биггар, Р.Дж.; Мелби, М. (1998). «Увеличение распространенности серовируса герпеса, связанного с саркомой Капоши, с возрастом в регионе с высокой эндемичностью саркомы Капоши, Замбия, 1985 год» . СПИД . 12 (14): 1921–5. дои : 10.1097/00002030-199814000-00024 . ПМИД 9792393 . S2CID 1734745 .
- ^ Вавер, MJ; Энг, С.М.; Сервадда, Д; Севанкамбо, Северная Каролина; Киванука, Н; Ли, С; Грей, Р.Х. (2001). «Распространенность герпесвируса, связанного с саркомой Капоши, по сравнению с некоторыми заболеваниями, передающимися половым путем, у подростков и молодых людей в сельском районе Ракаи, Уганда» . Заболевания, передающиеся половым путем . 28 (2): 77–81. дои : 10.1097/00007435-200102000-00003 . ПМИД 11234789 . S2CID 7592869 .
- ^ Класкала, Ж; Брейфилд, BP; Канкаса, К; Бхат, Г; Уэст, Джей Ти; Митчелл, CD; Вуд, К. (2005). «Эпидемиологические характеристики инфекции вируса герпеса человека-8 у большой популяции беременных женщин в Замбии» . Журнал медицинской вирусологии . 75 (1): 93–100. дои : 10.1002/jmv.20242 . ПМИД 15543582 . S2CID 9051177 .
- ^ Кури, В; Энг, С.М.; Родригес, МЭ; Резик, С; Оррака, Орегон; Мур, PS; Чанг, Ю. (2004). «Серораспространенность герпесвируса, ассоциированного с саркомой Капоши, в различных популяциях на Кубе» . Revista Panamericano de Salud Pública . 15 (5): 320–5. дои : 10.1590/s1020-49892004000500006 . ПМИД 15231079 .
- ^ Шульц, ТФ (2000). «Герпесвирус, ассоциированный с саркомой Капоши (герпесвирус человека 8): эпидемиология и патогенез» . Журнал антимикробной химиотерапии . 45 Приложение T3 (90004): 15–27. дои : 10.1093/jac/45.suppl_4.15 . ПМИД 10855768 .
- ^ Месри, Генри А.; Цезарьман, Этель; Бошофф, Крис (октябрь 2010 г.). «Герпесвирус саркомы Капоши/герпесвирус человека-8 (KSHV/HHV8) и онкогенез саркомы Капоши» . Обзоры природы. Рак 10 (10): 707–19. дои : 10.1038/nrc2888 . ПМЦ 4721662 . ПМИД 20865011 .
- ^ Брейфилд, BP; Фири, С; Канкаса, К; Муянга, Дж; Мантина, Х; Квенда, Г; Уэст, Джей Ти; Бхат, Г; Маркс, Д.Б.; Класкала, Ж; Митчелл, CD; Вуд, К. (2003). «Постнатальная инфекция вирусом герпеса человека 8 и вирусом иммунодефицита человека типа 1 у матерей и младенцев из Замбии» . Журнал инфекционных болезней . 187 (4): 559–68. дои : 10.1086/367985 . ПМИД 12599072 .
- ^ Он, Дж; Бхат, Г; Канкаса, К; Чинту, К; Митчелл, К; Дуань, Вт; Вуд, К. (1998). «Серораспространенность вируса герпеса человека 8 среди замбийских женщин детородного возраста без саркомы Капоши (СК) и пар мать-ребенок с СК» . Журнал инфекционных болезней . 178 (6): 1787–90. дои : 10.1086/314512 . ПМИД 9815235 .
- ^ Минхас, В; Крэбтри, КЛ; Чао, А; м'Сока, Ти Джей; Канкаса, К; Бултерис, М; Митчелл, CD; Вуд, К. (2008). «Инфекция раннего детства вирусом герпеса человека 8 в Замбии и роль коинфекции вируса иммунодефицита человека типа 1 в высокоэндемичном районе» . Американский журнал эпидемиологии . 168 (3): 311–20. дои : 10.1093/aje/kwn125 . ПМК 2727264 . ПМИД 18515794 .
- ^ Лю З, Фанг Кью, Цзо Дж, Минхас В, Вуд С, Хэ Н, Чжан Т (2017) Был ли герпесвирус, связанный с саркомой Капоши, занесен в Китай через древний Шелковый путь? Эволюционный взгляд. Арка Вирол
- ^ Жари А, Ледюк В, Дезире Н, Пети Х, Палич Р, Жоли В, Канестри А, Готланд А, Ламберт-Никлот С, Сергерс Л, Амиэль С, Декамп Д, Спано Дж. П., Катлама С, Кальвес В, Марселин А.Г. (2020)Новый вариант герпесвируса, ассоциированный с саркомой Капоши, у мужчин, практикующих секс с мужчинами, связанный с тяжелыми патологиями. J заразить дис
- ^ Мартин Д.Ф., Купперманн Б.Д., Волиц Р.А., Палестина А.Г., Ли Х, Робинсон К.А. (апрель 1999 г.). «Пероральный ганцикловир для пациентов с цитомегаловирусным ретинитом, получающих имплантат ганцикловира. Исследовательская группа по изучению ганцикловира компании Roche» . Медицинский журнал Новой Англии . 340 (14): 1063–70. дои : 10.1056/NEJM199904083401402 . ПМИД 10194235 .
- ^ Ярчоан, Р.; Тосато, Г.; Литтл, РФ (2005). «Понимание терапии: злокачественные новообразования, связанные со СПИДом – влияние противовирусной терапии на патогенез и лечение» . Природная клиническая практика онкологии . 2 (8): 406–415, викторина 415. doi : 10.1038/ncponc0253 . ПМИД 16130937 . S2CID 23476060 .
- ^ Бруссард, Грант; Дамания, Цветение (07.02.2020). «КШВ: Иммунная модуляция и иммунотерапия» . Границы в иммунологии . 10 : 3084. дои : 10.3389/fimmu.2019.03084 . ISSN 1664-3224 . ПМК 7025529 . ПМИД 32117196 .
- ^ Самолс М.А., Ху Дж., Скальски Р.Л., Ренне Р. (июль 2005 г.). «Клонирование и идентификация кластера микроРНК в латентно-ассоциированной области герпевируса, ассоциированного с саркомой Капоши» . Журнал вирусологии . 79 (14): 9301–5. doi : 10.1128/JVI.79.14.9301-9305.2005 . ПМЦ 1168752 . ПМИД 15994824 .
- ^ Голас, Г.; Джанг, С.Дж.; Наик, Н.Г.; Алонсо, доктор юридических наук; Папп, Б.; Тот, З. (2020). «Сравнительный анализ вирусных факторов регуляции интерферона КШВ на предмет их необходимости для продукции вируса и ингибирования пути интерферона I типа» . Вирусология . 541 : 160–173. дои : 10.1016/j.virol.2019.12.011 . ПМК 7024068 . ПМИД 32056714 .
Дальнейшее чтение
[ редактировать ]- Эдельман, округ Колумбия (2005). «Вирус герпеса человека 8 – новый человеческий патоген» . Вирусологический журнал . 2:78 . дои : 10.1186/1743-422X-2-78 . ПМЦ 1243244 . ПМИД 16138925 .
Внешние ссылки
[ редактировать ]- Вирус герпеса человека-8: сопутствующие ресурсы ВИЧ InSite
- Ежегодный семинар KSHV, 22-й международный семинар по герпесвирусу саркомы Капоши (KSHV) и связанным с ним агентам, 30 июня – 3 июля 2019 г., Нью-Йорк, США