Пентафторид висмута

| |

| |
| Имена | |
|---|---|
| Другие имена
фторид висмута(V)
| |
| Идентификаторы | |
3D model ( JSmol )
|
|
| КЭБ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.029.205 |
ПабХим CID
|
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA )
|
|
| Характеристики | |
| БиФ 5 | |
| Молярная масса | 303.97 g mol −1 |
| Появление | длинные белые иглы, [ 1 ] бесцветное кристаллическое твердое вещество [ 2 ] |
| Плотность | 5,40 г см −3 [ 1 ] |
| Температура плавления | 151,4 ° С (304,5 ° F; 424,5 К), [ 2 ] 154,4 °С [ 1 ] |
| Точка кипения | 230 ° С (446 ° F; 503 К) [ 1 ] [ 2 ] |
| Структура | |
| октаэдрический Би | |
| Опасности | |
| СГС Маркировка : | |
 
| |
| Опасность | |
| Х272 , Х314 | |
| P210 , P220 , P221 , P260 , P264 , P280 , P301+P330+P331 , P303+P361+P353 , P304+P340 , P305+P351+P338 , P310 , P321 , P363 , П370+П378 , П405 , П501 | |
| NFPA 704 (огненный алмаз) | |
| точка возгорания | негорючий |
| Паспорт безопасности (SDS) | Паспорт безопасности |
| Родственные соединения | |
Другие анионы
|
трихлорид висмута , трибромид висмута , трийодид висмута , пентаметилвисмут |
Другие катионы
|
пентафторид фосфора , пентафторид мышьяка , пентафторид сурьмы |
Родственные соединения
|
трифторид висмута |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |
Пентафторид висмута — неорганическое соединение формулы BiF 5 . Это белое твердое вещество, обладающее высокой реакционной способностью. Соединение представляет интерес для исследователей, но не представляет особой ценности.
Структура
[ редактировать ]BiF 5 является полимерным и состоит из линейных цепочек трансмостиковых угловых октаэдров, разделяющих BiF 6 . [ 1 ] [ 3 ] Это та же структура, что и у α -UF 5 . [ 1 ]
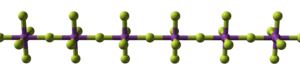  |
 
|
| (BiF 5 ) ∞ цепочка | упаковка цепей |
Подготовка
[ редактировать ]BiF 5 можно получить обработкой BiF 3 F 2 при 500°C. [ 2 ]
- БиФ 3 + Ф 2 → БиФ 5
В альтернативном синтезе ClF 3 является фторирующим агентом при 350°C. [ 4 ]
- BiF 3 + ClF 3 → BiF 5 + ClF
Реакции
[ редактировать ]Пентафторид висмута — наиболее реакционноспособный из пентафторидов пиктогена и чрезвычайно сильный фторирующий агент . Он бурно реагирует с водой с образованием озона и дифторида кислорода , а также с йодом или серой при комнатной температуре. BiF 5 фторирует парафиновое масло ( углеводороды ) до фторуглеродов при температуре выше 50 °C и окисляет UF 4 до UF 6 при температуре 150 °C. 180°C пентафторид Br2 висмута до BrF3 ClF и Cl2 до При фторирует . [ 1 ]
BiF 5 также реагирует с фторидами щелочных металлов MF с образованием гексафторвисмутатов M[BiF 6 ], содержащих гексафторвисмутат-анион [BiF 6 ] − . [ 2 ] Пентафторуд висмута в растворителе плавиковой кислоты также реагирует с фторидом никеля с образованием никелевой соли этого аниона, которая может включаться в комплекс с ацетонитрилом. [ 5 ]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж г Гринвуд, Норман Н .; Эрншоу, Алан (1997). Химия элементов (2-е изд.). Баттерворт-Хайнеманн . стр. 561–563. ISBN 978-0-08-037941-8 .
- ^ Jump up to: а б с д и Холлеман, Арнольд Фредерик; Виберг, Эгон (2001), Виберг, Нильс (ред.), Неорганическая химия , перевод Иглсона, Мэри; Брюэр, Уильям, Сан-Диего/Берлин: Academic Press/De Gruyter, стр. 769–770, ISBN 0-12-352651-5
- ^ К. Хебекер (1971). «О кристаллической структуре пентафторида висмута». З. неорг. общая хим. 384 (2): 111–114. дои : 10.1002/zaac.19713840204 .
- ^ А.И. Попов; А.В. Шарабарин; В.Ф. Суховерхов; Н. А. Чумаевский (1989). «Синтез и свойства фторидов пятивалентной сурьмы и висмута». З. Анорг. Аллг. Хим . 576 (1): 242–254. дои : 10.1002/zaac.19895760128 .
- ^ Роланд Бугон; Пьеретта Шарпен; Карл О. Кристе; Жак Изабе; Моник Лэнс; Мартина Нирлих; Жюльен Винье; Уильям В. Уилсон (1988). «Получение и характеристика гексафторвисмутата(1-) никеля(2+) и тройных аддуктов [Ni(CH3CN)6](BiF6)2 и [Ni(CH3CN)6](SbF6)2. Кристаллическая структура гексакис(ацетонитрила) -d3)гексафторантимонат никеля(2+). Неорганическая химия . 27 (8): 1389–1393. дои : 10.1021/ic00281a018 .
