Ремонт несоответствия ДНК
| Часть серии на |
| Генетика |
|---|
 |
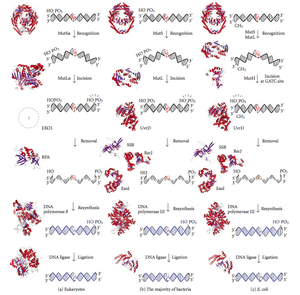
Реконструкция несоответствия ДНК ( MMR )-это система распознавания и восстановления ошибочной вставки, делеции и неправильной инкорпорации оснований , которые могут возникать во время репликации ДНК и рекомбинации , а также восстанавливать некоторые формы повреждения ДНК . [ 1 ] [ 2 ]
Ремонт несоответствия является специфичным для пряди. Во время синтеза ДНК вновь синтезированная (дочь) Strand обычно включает ошибки. Чтобы начать ремонт, механизм ремонта несоответствия отличает недавно синтезированную прядь от шаблона (родительский). У грамотрицательных бактерий переходное гемиметилирование различает пряди (родительский состав метилирован , а дочь-нет). Однако у других прокариот и эукариот точный механизм не ясен. Предполагается, что у эукариот вновь синтезированная ДНК с отставанием напряженно содержит ники (перед герметизацией ДНК-лигазы) и дает сигнал, который направляет несоответствующие системы корректуры в соответствующую цепь. Это подразумевает, что эти ники должны присутствовать в ведущей стенде, и недавно были найдены доказательства этого. [ 3 ] Недавняя работа [ 4 ] показал, что NICS-это сайты для RFC-зависимой нагрузки репликационного скользящего зажима, пролиферирующего ядерного антигена клеток (PCNA), специфичным для ориентации, так что одна лицо белка в форме пончика сопоставлено в сторону 3'-OH закончить на ник. Загруженная PCNA направляет действие эндонуклеазы Mutlalpha [ 5 ] дочери Страйт в присутствии несоответствия и Мутсальфа или Мутсбета.
Любое мутационное событие, которое нарушает супергелическую структуру ДНК , несет с собой потенциал для компромисса генетической стабильности клетки. Тот факт, что системы обнаружения и ремонта ущерба столь же сложны, как и сама механизм репликации, подчеркивает важность эволюции, связанную с точностью ДНК.
Примеры несоответствующих оснований включают спаривание G/T или A/C (см. Репарацию ДНК ). Несоответствия обычно связаны с таутомеризацией оснований во время репликации ДНК. Ущерб восстанавливается путем распознавания деформации, вызванной несоответствием, определением шаблона и ницевой прядью, а также исключения неправильно включенного основания и замены его правильным нуклеотидом . Процесс удаления включает в себя не только сам несовпадающий нуклеотид. Несколько или до тысячи пар оснований вновь синтезированной пряди ДНК могут быть удалены.
Несоответствие восстановления белков
[ редактировать ]В этом разделе нужны дополнительные цитаты для проверки . ( Май 2024 ) |
| ДНК-несоответствующий белок, С-концевой домен | |||
|---|---|---|---|
 HPMS2-ATPGS | |||
| Идентификаторы | |||
| Символ | DNA_MIS_REPAIR | ||
| Pfam | PF01119 | ||
| PFAM клан | CL0329 | ||
| InterPro | IPR013507 | ||
| PROSITE | PDOC00057 | ||
| Краткое содержание | 1bkn / scope / supfam | ||
| |||
Ремонт несоответствия - это высококонсервативный процесс от прокариот до эукариот . Первое доказательство восстановления несоответствия было получено от S. pneumoniae HEXA и HEXB ( гены ). Последующая работа над E. coli выявила ряд генов, которые, когда мутационно инактивируются, вызывают гиперманируемые штаммы. Следовательно, генные продукты называются белками «mut» и являются основными активными компонентами системы восстановления несоответствия. Три из этих белков необходимы для обнаружения несоответствия и направления на его репарацию: MUTS , MUTH и MUTL (MUTS - гомолог HEXA и MUTL HEXB).
MUTS образует димер (MUTS 2 ), который распознает несоответствующее основание на дочери и связывает мутированную ДНК. MUTH связывается в гемиметилированных сайтах вдоль дочерней ДНК, но ее действие скрыто, активируется только при контакте с помощью DIMER MUTL (MUTL 2 ), который связывает комплекс MUTS-ДНК и действует как медиатор между MUTS 2 и MUTH, активируя последний. ДНК зациклена, чтобы найти ближайший участок метилирования D (GATC) к несоответствию, что может быть до 1 КБ. После активации комплекса MUTS-ДНК Мут пробивает дочернюю прядь возле гемиметилированного участка. MUTL набирает UVRD Helicase (DNA Helicase II), чтобы отделить две нити с определенной полярностью от 3 до 5 '. Весь комплекс Mutshl затем скользит вдоль ДНК в направлении несоответствия, освобождая цепь, которая будет вырезана по мере ее поступления. Экзонуклеаза запускает комплекс и переваривает хвост SS-ДНК. Набранная экзонуклеаза зависит от того, какая сторона несоответствия Muth разжигает прядь - 5 'или 3'. Если ник, сделанный MUTH, находится на 5 'конце несоответствия, используется либо RecJ, либо ExoVII (оба' от 5 до 3 'экзонуклеазы). Если, однако, ник находится на 3 -м конце несоответствия, Используется EXOI (фермент от 3 до 5 ').
Весь процесс заканчивается мимо сайта несоответствия - т.е. как сам сайт, так и окружающие его нуклеотиды полностью вырезаны. Одноцепочечный разрыв, созданный экзонуклеазой, может затем быть восстановлен ДНК-полимеразой III (с помощью одноцепочечного связывающего белка), которая использует другую цепь в качестве матрицы и, наконец, запечатана ДНК-лигазой. Затем ДНК метилаза быстро метилирует дочернюю прядь.
MUTS гомологичный
[ редактировать ]При гранике димер MUTS 2 сгибает спираль ДНК и щиты приблизительно 20 пар оснований. Он обладает слабой активностью АТФазы, а связывание АТФ приводит к образованию третичных структур на поверхности молекулы. Кристаллическая структура MUT показывает, что она исключительно асимметрична, и, хотя его активная конформация является димером, только одна из двух половинок взаимодействует с сайтом несоответствия.
У эукариот Mt S H Omologs образуют два основных гетеродимера: MSH2 /MSH6 (MUTSα) и MSH2 /MSH3 (MUTSβ). Путь MUTSα участвует в основном в замене основания и восстановлении несоответствия малого петли. Путь MUTSβ также участвует в восстановлении малого петли, в дополнение к восстановлению большой петли (~ 10 нуклеотидных петлей). Тем не менее, MUTSβ не восстанавливает замены базы.
Mutl -гомологи
[ редактировать ]MUTL также обладает слабой активностью АТФазы (использует АТФ для целей движения). Он образует комплекс с MUTS и MUTH, увеличивая след MUTS на ДНК.
Тем не менее, процессивность (расстояние, которое фермент может перемещаться по ДНК перед диссоциацией) UVRD составляет всего ~ 40–50 п.н. Поскольку расстояние между ником, созданным MUTH и несоответствием, может в среднем ~ 600 п.н., если нет другого UVRD, загруженного, размахивая секция может быть свободно повторно в ее дополнительную прядь, заставляя процесс начать все сначала. Однако, когда помогает MUTL, скорость нагрузки UVRD значительно увеличивается. В то время как процессивность (и использование АТФ) отдельных молекул UVRD остается неизменной, общее влияние на ДНК значительно повышается; ДНК не имеет шансов повторно аннуляции, поскольку каждый UVRD раскрывает 40-50 п.н. ДНК, диссоциирует, а затем немедленно заменяется другим UVRD, повторяя процесс. Это обнажает большие участки ДНК для пищеварения экзонуклеазы , что позволяет быстро удалить (и более позднюю замену) неправильной ДНК.
У эукариот есть пять мкт omologs , h обозначенных как MLH1, MLH2, MLH3, PMS1 и PMS2. Они образуют гетеродимеры, которые имитируют Mutl в E. coli . Человеческие гомологи прокариотического Mutl образуют три комплекса, называемые mutlα, mutlβ и mutlγ. Комплекс Mutlα изготовлен из субъединиц MLH1 и PMS2, гетеродимер Mutlβ изготовлен из MLH1 и PMS1, тогда как MutLγ изготовлен из MLH1 и MLH3. MUTLα действует как эндонуклеаза, которая вводит разрывы нити в дочерней цепи при активации с помощью несоответствия и других требуемых белков, MUTSα и PCNA. Эти перерывы пряди служат точками входа для экзонуклеазной активности, которая удаляет несоответствующую ДНК. Роли, сыгранные mutlβ и mutlγ в восстановлении несоответствия, менее понятны.
Muth: эндонуклеаза, присутствующая в E. coli и Salmonella
[ редактировать ]Muth - это очень слабая эндонуклеаза , которая активируется однажды, связанной с MUTL (который сам связан с MUT). Это забрасывает неметилированную ДНК и неметилированную цепь гемиметилированной ДНК, но не проклевает полностью метилированную ДНК. Эксперименты показали, что восстановление несоответствия является случайным, если ни одна цепь не метилирован. [ Цитация необходима ] Такое поведение привело к предложению, которое Мут определяет, какая Strand содержит несоответствие. Мут не имеет эукариотического гомолога. Его функция эндонуклеазы занимается гомологами Mutl, которые имеют некоторую специализированную экзонуклеазующую активность 5'-3 '. Смещение цепочки для удаления несоответствий из вновь синтезированной дочери Странд у эукариот может быть предоставлена свободными 3 'концами фрагментов Оказаки в новой пряди, созданной во время репликации.
PCNA β-привязанный зажим
[ редактировать ]PCNA и β-слюневый зажим связаны с MUTSα/β и MUT, соответственно. Хотя первоначальные сообщения свидетельствуют о том, что комплекс PCNA-MUTSα может усилить распознавание несоответствия, [ 6 ] недавно было продемонстрировано [ 7 ] что нет очевидных изменений в аффинности MUTSα для несоответствия в присутствии или отсутствии PCNA. Кроме того, мутанты MUTSα, которые не могут взаимодействовать с PCNA in vitro, демонстрируют способность осуществлять распознавание несоответствия и несоответствие иссечения до почти диких уровней. Такие мутанты являются дефектными в реакции восстановления, направленной на 5-'цепочку, впервые предполагая функцию MUTSα MUTSα на стадии реакции после удаления.
Клиническое значение
[ редактировать ]Унаследованные дефекты в восстановлении несоответствия
[ редактировать ]Мутации в человеческих гомологах мутных белков влияют на стабильность генома, что может привести к нестабильности микросателлитов (MSI), вовлеченной в некоторые раковые заболевания человека. В специфике наследственный неполипоз колоректальный рак ( HNPCC или синдром Линча) объясняется повреждением вариантов зародышевой линии в генах, кодирующих MUTS и Mutl -гомологи MSH2 и MLH1 соответственно, которые классифицируются как гены подавляющих опухоли. Один подтип HNPCC, синдром Muir-Torre (MTS), связан с опухолями кожи. Если оба унаследованные копии (аллели) гена MMR, наносящих ущерб генетическим вариантам, это приводит к очень редкому и тяжелому состоянию: синдром восстановления несоответствия рака (или дефицит восстановления конституционного несоответствия, CMMR-D), проявляясь как множественные случаи опухолей в ранний возраст, часто опухоли толстой кишки и головного мозга . [ 8 ]
Эпигенетическое молчание генов восстановления несоответствия
[ редактировать ]Спорадический рак с дефицитом репарации ДНК лишь редко имеет мутацию в гене репарации ДНК, но вместо этого они имеют тенденцию иметь эпигенетические изменения, такие как метилирование промотора, которые ингибируют экспрессию генов ДНК. [ 9 ] Около 13%колоректальных раковых заболеваний дефицит при восстановлении несоответствия ДНК, обычно из -за потери MLH1 (9,8%), а иногда и MSH2, MSH6 или PMS2 (все ≤1,5%). [ 10 ] Для большинства спорадических колоректальных раковых заболеваний с дефицитом MLH1 дефицит был вызван метилированием промотора MLH1. [ 10 ] Другие типы рака имеют более высокие частоты потери MLH1 (см. Таблицу ниже), которые снова в значительной степени являются результатом метилирования промотора гена MLH1 . Другой эпигенетический механизм, лежащий в основе дефицита MMR, может включать в себя чрезмерную экспрессию микроРНК, например, уровни miR-155 обратно коррелирует с экспрессией MLH1 или MSH2 при колоректальном раке. [ 11 ]
| Тип рака | Частота дефицита при раке | Частота дефицита в смежном дефекте поля |
|---|---|---|
| Желудок | 32% [ 12 ] [ 13 ] | 24%-28% |
| Желудок (опухоли типа Foveolar) | 74% [ 14 ] | 71% |
| Желудок в кашмирской долине с высоким содержанием | 73% [ 15 ] | 20% |
| Пищевод | 73% [ 16 ] | 27% |
| Голова и шековая плоскоклеточная карцинома (HNSCC) | 31%-33% [ 17 ] [ 18 ] | 20%-25% |
| Немелкоклеточный рак легкого (NSCLC) | 69% [ 19 ] | 72% |
| Колоректальный | 10% [ 10 ] |
Отказы MMR в полевых дефектах
[ редактировать ]Полевой дефект (полевая рака) - это область эпителия, которая была предварительно кондиционирована эпигенетическими или генетическими изменениями, предрасполагая его к развитию рака. Как указал Рубин «... есть доказательства того, что более 80% соматических мутаций, обнаруженных в мутаторном фенотипе, ореклере -опухоли человека, возникают до начала терминальной клональной экспансии». [ 20 ] [ 21 ] Точно так же Vogelstein et al. [ 22 ] Указывают, что более половины соматических мутаций, идентифицированных в опухолях, происходило в до-неопластической фазе (в полевом дефекте) во время роста, по-видимому, нормальных клеток.
Недостатки MLH1 были распространены в полевых дефектах (гистологически нормальные ткани), окружающие опухоли; См. Таблицу выше. Эпигенетически молчаливый или мутированный MLH1, вероятно, не даст селективному преимущество стволовой клетке, однако это вызовет повышенные скорости мутаций, и один или несколько мутированных генов могут предоставить клетку селективное преимущество. Затем дефицитный ген MLH1 может быть переносится в виде селективно ближнего нейтрального гена пассажира (Hitch-Hiker), когда мутированная стволовая клетка генерирует расширенный клон. Продолжающееся присутствие клона с эпигенетически репрессированным MLH1 будет продолжать генерировать дальнейшие мутации, некоторые из которых могут вызывать опухоль.
MSI и иммунная блокада контрольной точки
[ редактировать ]Первоначально наблюдалось, что мутации восстановления MMR и несоответствия ассоциируются с эффективностью блокады иммунной контрольной точки в исследовании, в котором изучаются респонденты против PD1. [ 23 ] Связь между позитивностью MSI и положительным ответом на анти-PD1 была впоследствии подтверждена в проспективном клиническом испытании и одобрена FDA. [ 24 ]
Компоненты MMR у людей
[ редактировать ]У людей семь белков восстановления несоответствия ДНК (MMR) ( MLH1 , MLH3 , MSH2 , MSH3 , MSH6 , PMS1 и PMS2 ) работают координированно в последовательных этапах для инициирования восстановления несоответствий ДНК. [ 25 ] Кроме того, существуют EXO1 -зависимые и EXO1 -независимые подборы MMR. [ 26 ]
Другие генные продукты, участвующие в восстановлении несоответствия (после начала инициации генами MMR) у людей, включают дельта ДНК -полимеразы , PCNA , RPA , HMGB1 , RFC и ДНК -лигазы I , плюс гистон и хроматин . факторы, модифицирующие [ 27 ] [ 28 ]
При определенных обстоятельствах путь MMR может рекрутировать подверженную ошибкам ДНК-полимеразу ETA ( POLH ). Это происходит в B-лимфоцитах во время соматической гипермутации , где PolH используется для введения генетической вариации в гены антител. [ 29 ] Тем не менее, этот путь MMR, подверженный ошибкам, может быть запускается у других типов клеток человека при воздействии генотоксинов [ 30 ] И действительно, он широко активен при различных раковых заболеваниях человека, вызывая мутации, которые несут сигнатуру активности PolH. [ 31 ]
MMR и частота мутации
[ редактировать ]Распознавание и восстановление несоответствий и инделей важно для клеток, потому что неспособность сделать это приводит к нестабильности микросателлита (MSI) и повышенной скорости спонтанной мутации (фенотип мутатора). По сравнению с другими типами рака, рак MMR-дефицита (MSI) имеет очень высокую частоту мутаций, близко к меланоме и раку легких, [ 32 ] Типы рака, вызванные большим воздействием ультрафиолетового излучения и мутагенных химических веществ.
В дополнение к очень высокой бремени мутации, дефицит MMR приводит к необычному распределению соматических мутаций по геному человека: это говорит о том, что MMR преимущественно защищает богатые генами, ранние реплицирующиеся эухроматические области. [ 33 ] Напротив, плотные геновые, поздние реплицирующиеся гетерохроматические области генома демонстрируют высокие показатели мутации во многих опухолях человека. [ 34 ]
Модификация гистонов H3K36ME3 , эпигенетическая метка активного хроматина, обладает способностью рекрутировать комплекс MSH2-MSH6 (HMUTSα). [ 35 ] Постоянно, области генома человека с высоким уровнем H3K36ME3 накапливают меньше мутаций из -за активности MMR. [ 31 ]
Потеря множественных путей восстановления ДНК в опухолях
[ редактировать ]Отсутствие MMR часто происходит в координации с потерей других генов репарации ДНК. [ 9 ] Например, гены MMR MLH1 и MLH3, а также 11 других генов репарации ДНК (такие как MGMT и многие гены путей NER ) были значительно понижены в более низкой степени, а также в астроцитомах более высокой степени , в отличие от нормальной ткани мозга. [ 36 ] Более того, экспрессия MLH1 и MGMT тесно коррелировали в 135 образцах рака желудка, а потеря MLH1 и MGMT, по -видимому, синхронно ускорена во время прогрессирования опухоли. [ 37 ]
Недостаточная экспрессия множественных генов репарации ДНК часто обнаруживается при раке, [ 9 ] и может способствовать тысячам мутаций, обычно встречающихся при раке (см. Частоты мутаций при раке ).
Старение
[ редактировать ]Популярной идеей, которая не смогла получить значительную экспериментальную поддержку, является идея, что мутация, отличная от повреждения ДНК, является основной причиной старения. Мыши, дефектные в Mutl Homolog PMS2, имеют примерно 100-кратную повышенную частоту мутации во всех тканях, но, по-видимому, не стареют быстрее. [ 38 ] Эти мыши демонстрируют в основном нормальное развитие и жизнь, за исключением раннего карциногенеза и мужского бесплодия.
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Iyer RR, Pluciennik A, Burdett V, Modrich PL (февраль 2006 г.). «Ремонт несоответствия ДНК: функции и механизмы». Химические обзоры . 106 (2): 302–23. doi : 10.1021/cr0404794 . PMID 16464007 .
- ^ Larrea AA, Lujan SA, Kunkel TA (май 2010 г.). «Снимок: восстановление несоответствия ДНК» . Клетка . 141 (4): 730–730.e1. doi : 10.1016/j.cell.2010.05.002 . PMID 20478261 . S2CID 26969788 .
- ^ Heller RC, Marians KJ (декабрь 2006 г.). «Повторяя сборка и прямой перезапуск застопорившихся вилок репликации». Природные обзоры. Молекулярная клеточная биология . 7 (12): 932–43. doi : 10.1038/nrm2058 . PMID 17139333 . S2CID 27666329 .
- ^ Pluciennik A, Dzantiev L, Iyer RR, Constantin N, Kadyrov FA, Modrich P (сентябрь 2010 г.). «Функция PCNA в направлении активации и цепи эндонуклеазы Mutlα при восстановлении несоответствия» . Труды Национальной академии наук Соединенных Штатов Америки . 107 (37): 16066–71. doi : 10.1073/pnas.1010662107 . PMC 2941292 . PMID 20713735 .
- ^ Кадиров Ф.А., Дзантиев Л., Константин Н., Модрич П. (июль 2006 г.). «Эндонуклеолитическая функция мутлальфы при восстановлении несоответствия человека» . Клетка . 126 (2): 297–308. doi : 10.1016/j.cell.2006.05.039 . PMID 16873062 . S2CID 15643051 .
- ^ Flores-Rozas H, Clark D, Kolodner Rd (ноябрь 2000 г.). «Пролиферирующее ядерное антиген клеток и MSH2P-MSH6P взаимодействуют с образованием активного комплекса распознавания недоступных». Природа генетика . 26 (3): 375–8. doi : 10.1038/81708 . PMID 11062484 . S2CID 20861705 .
- ^ Iyer RR, Pohlhaus TJ, Chen S, Hura GL, Dzantiev L, Beese LS, Modrich P (май 2008 г.). «Мутсальфа-пролиферирующее взаимодействие ядерного антигена клеток при восстановлении несоответствия ДНК человека» . Журнал биологической химии . 283 (19): 13310–9. doi : 10.1074/jbc.m800606200 . PMC 2423938 . PMID 18326858 .
- ^ Онлайн -наследство Менделян в Человеке (Омим): 276300
- ^ Jump up to: а беременный в Бернштейн С, Бернштейн Х (май 2015). «Эпигенетическое восстановление репарации ДНК при прогрессировании на желудочно -кишечный рак» . Всемирный журнал желудочно -кишечной онкологии . 7 (5): 30–46. doi : 10.4251/wjgo.v7.i5.30 . PMC 4434036 . PMID 25987950 .
- ^ Jump up to: а беременный в Truninger K, Menigatti M, Luz J, Russell A, Haider R, Gebbers Jo, et al. (Май 2005 г.). «Иммуногистохимический анализ выявляет высокую частоту дефектов PMS2 при колоректальном раке» . Гастроэнтерология . 128 (5): 1160–71. doi : 10.1053/j.gastro.2005.01.056 . PMID 15887099 .
- ^ Valeri N, Gasparini P, Fabbri M, Braconi C, Veronese A, Lovat F, et al. (Апрель 2010). «Модуляция восстановления несоответствия и стабильности генома с помощью miR-155» . Труды Национальной академии наук Соединенных Штатов Америки . 107 (15): 6982–7. Bibcode : 2010pnas..107.6982V . doi : 10.1073/pnas.1002472107 . PMC 2872463 . PMID 20351277 .
- ^ Kupčinskaitė-Noreikienė R, Skiecevičienė J, Jonaitis L, Ugenskienė R, Kupčinskas J, Markelis R, et al. (2013). Метиланация острова CPG в генах MigMT, MGMT, DAPK и CASP8 в раковых и прилегающих нераковых тканях желудка . Лекарство . 49 (8): 361-6. Doi : 10.3390/medicina49080056 . PMID 24509146 .
- ^ Ваки Т., Тамура Г., Цучия Т., Сато К., Нишизука С., Мотояма Т (август 2002 г.). «Статус метилирования промотора генов E-Cadherin, HMLH1 и P16 в неопухолевом эпителии желудка» . Американский журнал патологии . 161 (2): 399–403. doi : 10.1016/s0002-9440 (10) 64195-8 . PMC 1850716 . PMID 12163364 .
- ^ Endoh Y, Tamura G, Ajioka Y, Watanabe H, Motoyama T (сентябрь 2000 г.). «Частое гиперметилирование промотора гена HMLH1 в опухолях дифференцированного типа желудка с желудочным фенотипом» . Американский журнал патологии . 157 (3): 717–22. doi : 10.1016/s0002-9440 (10) 64584-1 . PMC 1949419 . PMID 10980110 .
- ^ Wani M, Afroze D, Makhdoomi M, Hamid I, Wani B, Bhat G, et al. (2012). «Статус метилирования промотора гена репарации ДНК (HMLH1) у пациентов с раком желудка в долине Кашмира» (PDF) . Азиатско -Тихоокеанский журнал профилактики рака . 13 (8): 4177–81. doi : 10.7314/apjcp.2012.13.8.4177 . PMID 23098428 .
- ^ Chang Z, Zhang W, Chang Z, Song M, Qin Y, Chang F, et al. (Январь 2015). «Экспрессионные характеристики FHIT , p53 , BRCA2 и MLH1 в семьях с историей рака пистофагера в регионе с высокой заболеваемостью раком пистофагера» . Онкологические письма . 9 (1): 430–436. doi : 10.3892/ol.2014.2682 . PMC 4246613 . PMID 25436004 .
- ^ Tawfik HM, El-Maqsoud NM, Hak BH, El-Sherbiny YM (2011). «Плоскоклеточная карцинома голова и шеи: репарация несоответствия иммуногистохимии и гиперметилирование гена HMLH1 HMLH1». Американский журнал отоларингологии . 32 (6): 528–36. doi : 10.1016/j.amjoto.2010.11.005 . PMID 21353335 .
- ^ Zuo C, Zhang H, Spencer HJ, Vural E, Suen Jy, Schichman SA, et al. (Октябрь 2009 г.). «Повышенная нестабильность микросателлита и эпигенетическая инактивация гена HMLH1 при плоскоклеточной карциноме головы и шеи». Отоларингология - голова и хирургия шеи . 141 (4): 484–90. doi : 10.1016/j.othns.2009.07.007 . PMID 19786217 . S2CID 8357370 .
- ^ Safar AM, Spencer H, Su X, Coffey M, Cooney CA, Ratnasinghe LD, et al. (Июнь 2005 г.). «Профилирование метилирования архивированного немелкоклеточного рака легких: многообещающая прогностическая система» . Клиническое исследование рака . 11 (12): 4400–5. doi : 10.1158/1078-0432.ccr-04-2378 . PMID 15958624 .
- ^ Рубин Х (март 2011 г.). «Поля и полевые ракеты: преенепластическое происхождение рака: бессимптомные гиперпластические поля являются предшественниками неоплазии, а их прогрессирование до опухолей может отслеживать плотностью насыщения в культуре». Биологии . 33 (3): 224–31. doi : 10.1002/bies.201000067 . PMID 21254148 . S2CID 44981539 .
- ^ Tsao JL, Yatabe Y, Salovaara R, Järvinen HJ, Mecklin JP, Aaltonen LA, et al. (Февраль 2000 г.). «Генетическая реконструкция отдельных историй колоректальной опухоли» . Труды Национальной академии наук Соединенных Штатов Америки . 97 (3): 1236–41. Bibcode : 2000pnas ... 97.1236t . doi : 10.1073/pnas.97.3.1236 . PMC 15581 . PMID 106555514 .
- ^ Vogelstein B, Papadopoulos N, Velculescu Ve, Zhou S, Diaz LA, Kinzler KW (март 2013 г.). «Ландшафты генома рака» . Наука . 339 (6127): 1546–58. BIBCODE : 2013SCI ... 339.1546V . doi : 10.1126/science.1235122 . PMC 3749880 . PMID 23539594 .
- ^ Ризви, Наййер; Хеллманн, Мэтью; Снайдер, Александра; Квистборг, Пиа; Макаров, Владимир; Хавел, Джонатан; Ли, Уильям; Юань, Цзяна; Вонг, Филипп; Хо, Тереза; Миллер, Мартин; Rekhtman, Наташа; Морейра, Андра; Ибрагим, Фозия; Бруггман, Кэмерон; Гасми, Билл; Заппазоди, Роберта; Маеда, Юка; Сандер, Крис; Гарон, Эдвард; Мерхуб, Таха; Уолчок, Джедд; Шумахер, Тон; Тимоти, Чан (2015). «Мутационный ландшафт определяет чувствительность к блокаде PD-1 при немелкоклеточном раке легких» . Наука . 6230 (348): 124–128. doi : 10.1126/science.aaa1348 . PMC 4993154 . PMID 25765070 .
- ^ Центр оценки лекарств и исследований. «Утвержденные лекарства - FDA -гранты ускорили одобрение Pembrolizumab для первого агностического показателя тканей/сайта» . www.fda.gov . Получено 2017-05-24 .
- ^ Pal T, Permuth-Wey J, Sellers TA (август 2008 г.). «Обзор клинической значимости дефицита несоответствия при раке яичников» . Рак . 113 (4): 733–42. doi : 10.1002/cncr.23601 . PMC 2644411 . PMID 18543306 .
- ^ Goellner EM, Putnam CD, Kolodner Rd (август 2015 г.). «Экзонуклеаза 1-зависимого и независимого восстановления несоответствия» . Репарация ДНК . 32 : 24–32. doi : 10.1016/j.dnarep.2015.04.010 . PMC 4522362 . PMID 25956862 .
- ^ Li GM (январь 2008 г.). «Механизмы и функции восстановления несоответствия ДНК» . Клеточные исследования . 18 (1): 85–98. doi : 10.1038/cr.2007.115 . PMID 18157157 .
- ^ Li GM (июль 2014 г.). «Новое понимание и проблемы в ремонте несоответствия: преодолеть препятствие хроматину» . Репарация ДНК . 19 : 48–54. doi : 10.1016/j.dnarep.2014.03.027 . PMC 4127414 . PMID 24767944 .
- ^ Chahwan R, Edelmann W, Scharff MD, Roa S (август 2012 г.). «Помощь разнообразию антител путем подверженного ошибкам восстановления несоответствия» . Семинары по иммунологии . 24 (4): 293–300. doi : 10.1016/j.smim.2012.05.005 . PMC 3422444 . PMID 22703640 .
- ^ Sieh P (сентябрь 2012 г.). «Ремонт несоответствия ДНК: доктор Джекилл и мистер Хайд?» Полем Молекулярная клетка . 47 (5): 665–6. doi : 10.1016/j.molcel.2012.08.020 . PMC 3457060 . PMID 22980456 .
- ^ Jump up to: а беременный Supek F, Lehner B (июль 2017 г.). «Компания кластеризованных мутационных сигнатур показывает, что подверженные ошибкам, подверженные мутациям репарации ДНК, мутациям активных генов» . Клетка . 170 (3): 534–547.E23. doi : 10.1016/j.cell.2017.07.003 . HDL : 10230/35343 . PMID 28753428 .
- ^ Тунец М, Амос К.И. (ноябрь 2013 г.). «Геномное секвенирование при раке» . Раковые письма . 340 (2): 161–70. doi : 10.1016/j.canlet.2012.11.004 . PMC 3622788 . PMID 23178448 .
- ^ Supek F, Lehner B (май 2015). «Дифференциальное восстановление несоответствия ДНК лежит в основе изменения скорости мутаций в геноме человека» . Природа . 521 (7550): 81–4. Bibcode : 2015natur.521 ... 81S . doi : 10.1038/nature14173 . PMC 44255546 . PMID 25707793 .
- ^ Schuster-Böckler B, Lehner B (август 2012 г.). «Организация хроматина оказывает большое влияние на частоту региональных мутаций в раковых клетках человека». Природа . 488 (7412): 504–7. Bibcode : 2012natur.488..504S . doi : 10.1038/nature11273 . PMID 22820252 . S2CID 205229634 .
- ^ Li F, Mao G, Tong D, Huang J, Gu L, Yang W, Li GM (апрель 2013 г.). «Гистоновая марка H3K36ME3 регулирует восстановление несоответствия ДНК человека посредством его взаимодействия с MUTSα» . Клетка . 153 (3): 590–600. doi : 10.1016/j.cell.2013.03.025 . PMC 3641580 . PMID 23622243 .
- ^ Jiang Z, Hu J, Li X, Jiang Y, Zhou W, Lu D (декабрь 2006 г.). «Анализ экспрессии 27 генов репарации ДНК в астроцитоме с помощью массива низкой плотности Taqman». Нейробиологические буквы . 409 (2): 112–7. doi : 10.1016/j.neulet.2006.09.038 . PMID 17034947 . S2CID 54278905 .
- ^ Kimajima Y, Miyazaki K, Matsukura S, Tanaka M, Sekiguchi M (2003). «Потеря экспрессии ферментов репарации ДНК Mgmt, HMLH1 и HMSH2 во время прогрессирования Tuing в желудочном канморте » Застоподобный Рак 6 (2): 86–95. Doi : 10.1007/s10120-003-0213-z . PMID 12861399
- ^ Нараянан Л., Фрицелл Дж.А., Бейкер С.М., Лискай Р.М., Глейзер П.М. (апрель 1997 г.). «Повышенные уровни мутации в нескольких тканях мышей с дефицитом в гене репарации несоответствия ДНК PMS2» . Труды Национальной академии наук Соединенных Штатов Америки . 94 (7): 3122–7. Bibcode : 1997pnas ... 94.3122N . doi : 10.1073/pnas.94.7.3122 . PMC 20332 . PMID 9096356 .
Дальнейшее чтение
[ редактировать ]- Ши П., Ямане К (2008). «Репарация несоответствия ДНК: молекулярный механизм, рак и старение» . Механизмы старения и развития . 129 (7–8): 391–407. doi : 10.1016/j.mad.2008.02.012 . PMC 2574955 . PMID 18406444 .
- Iyer RR, Pluciennik A, Burdett V, Modrich PL (февраль 2006 г.). «Ремонт несоответствия ДНК: функции и механизмы». Химические обзоры . 106 (2): 302–23. doi : 10.1021/cr0404794 . PMID 16464007 .
- Джозеф Н., Дуппатла В., Д.Н. Рао (2006). Перекрашенная ДНК Procaryard . Тол. 81. стр. 1–49 doi : 10.1016/s0079-6603 (06) 81001-9 . ISBN 9780125400817 Полем PMID 16891168 .
{{cite book}}:|journal=игнорируется ( помощь ) - Ян W (август 2000 г.). «Структура и функция белков восстановления несоответствия» . Мутационные исследования . 460 (3–4): 245–56. doi : 10.1016/s0921-8777 (00) 00030-6 . PMID 10946232 .
- Griffiths JF, Gilbert WM, Lewontin RC, Wessler SR, Suzuki DT, Miller JH (2004). Введение в генетический анализ (8 -е изд.). Нью -Йорк, Нью -Йорк: Фриман. ISBN 978-0-7167-4939-4 .
- Кункель Т.А., Эри Д.А. (2005). «Ремонт несоответствия ДНК» . Ежегодный обзор биохимии . 74 : 681–710. doi : 10.1146/annurev.biochem.74.082803.133243 . PMID 15952900 .
- Friedberg EC, Walker GC, Siede W, Wood Rd , Schultz RA, Ellenberger (2005). Репарация ДНК и мутагенез (2 -е изд.). Вашингтон, округ Колумбия: ASM Press. ISBN 978-1-55581-319-2 .
Внешние ссылки
[ редактировать ]- репарации ДНК Архивировал 2018-02-12 на машине Wayback
- ДНК+несоответствие+восстановление библиотеки США в Национальной медицинской библиотеке Медицинской (Mesh)