Гидрид железа(I)

| |||
| |||
| Имена | |||
|---|---|---|---|
| Систематическое название ИЮПАК
Гидридожелезо(3•) | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| ФеХ 3• | |||
| Молярная масса | 56.853 g mol −1 | ||
| Термохимия | |||
Стандартная энтальпия
образование (Δ f H ⦵ 298 ) |
450,6 кДж раз −1 [ нужна ссылка ] | ||
| Родственные соединения | |||
Родственные соединения
|
Гидриды железа , FeH 2 КрХ , КаН , МгХ | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Гидрид железа(I) , систематически называемый гидридом железа и поли(гидридожелезом), представляет собой твердое неорганическое соединение с химической формулой (FeH).
n (также пишется ([FeH])
н или FeH). Он термодинамически и кинетически неустойчив к разложению при температуре окружающей среды, поэтому о его объемных свойствах мало что известно.
Гидрид железа(I) — простейший полимерный гидрид железа. Из-за своей нестабильности он не имеет практического промышленного применения. Однако в металлургической химии гидрид железа (I) имеет основополагающее значение для некоторых форм железо-водородных сплавов .
Номенклатура
[ редактировать ]Систематическое название гидрид железа , действительное название IUPAC , построено в соответствии с номенклатурой состава. Однако, поскольку название носит композиционный характер, оно не делает различия между соединениями одной и той же стехиометрии, например молекулярными видами, которые проявляют разные химические свойства. Систематические названия поли(гидридожелезо) и поли[ферран(1)] , также действительные названия ИЮПАК, построены в соответствии с аддитивной и электронодефицитной замещающей номенклатурой соответственно. Они отличают титульное соединение от других.
Гидридожелезо
[ редактировать ]Гидридожелезо, также систематически называемое ферраном (1), представляет собой родственное соединение с химической формулой FeH (также пишется [FeH]). Он также нестабилен при температуре окружающей среды и имеет дополнительную склонность к автополимеризации, поэтому его нельзя концентрировать.
Гидридожелезо — простейший молекулярный гидрид железа. Кроме того, его можно рассматривать как мономер гидрида железа (I). Он был обнаружен изолированно только в экстремальных условиях, например, в замороженных благородных газах , в атмосфере холодных звезд или в виде газа при температурах выше точки кипения железа. Предполагается, что он имеет три оборванные валентные связи и, следовательно, является свободным радикалом ; его формула может быть записана FeH 3• подчеркнуть этот факт.
При очень низких температурах (ниже 10 К ) FeH может образовывать комплекс с молекулярным водородом FeH·H 2 . [ 1 ]
Гидридожелезо было впервые обнаружено в лаборатории Б. Клеманом и Л. Окерлиндом в 1950-х годах. [ нужна ссылка ]
Характеристики
[ редактировать ]Радикальность и кислотность
[ редактировать ]Одиночный электрон другого атомного или молекулярного типа может присоединиться к железному центру в гидридожелезе путем замещения:
- [FeH] + RR → [FeHR] + ·R
Из-за захвата одного электрона гидридожелезо имеет радикальный характер. Гидридожелезо – сильный радикал.
Электронная пара основания Льюиса может соединиться с железным центром путем присоединения:
- [FeH] + :L → [FeHL]
Из-за этого захвата присоединенной электронной пары гидридожелезо имеет льюисовский кислотный характер. Следует ожидать, что гидрид железа(I) обладает значительно сниженными радикальными свойствами, но обладает сходными кислотными свойствами, однако скорости реакций и константы равновесия различны.
Структура
[ редактировать ]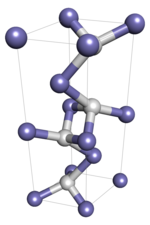
В гидриде железа(I) атомы образуют сеть, причем отдельные атомы связаны между собой ковалентными связями . Поскольку это полимерное твердое вещество, не ожидается, что монокристаллический образец будет претерпевать переходы состояний, такие как плавление и растворение, поскольку это потребует перестройки молекулярных связей и, следовательно, изменения его химической идентичности. Ожидается, что коллоидно-кристаллические образцы, в которых важны межмолекулярные силы, претерпевают переходы состояний.
Гидрид железа(I) имеет двойную гексагональную плотноупакованную кристаллическую структуру с пространственной группой P6 3 /mmc, также называемую эпсилон-простым гидридом железа в контексте системы железо-водород. Прогнозируется, что он проявит полиморфизм, переходящий при некоторой температуре ниже -173 ° C (-279 ° F) в гранецентрированную кристаллическую структуру с пространственной группой Fm 3 m.
Электромагнитные свойства
[ редактировать ]Предполагается, что FeH будет иметь квартет и секстет основных состояний.
Молекула FeH имеет по крайней мере четыре низкоэнергетических электронных состояния, вызванных тем, что несвязывающий электрон занимает позиции на разных орбиталях: X 4 Д, а 6 Д б 6 П, [ 2 ] и с 6 С + . [ 3 ] Состояния с более высокой энергией называются B. 4 С − , С 4 Ф, Д 4 С + , и 4 П и F 4 Д. [ 4 ] Еще более высокие уровни обозначены буквой G. 4 П и Н 4 Δ из квартетной системы, а d 6 С − , и 6 Пф 6 Δ и г 6 Ф. [ 2 ] В квартетных состояниях внутреннее квантовое число J принимает значения 1/2, 3/2, 5/2 и 7/2.
| группа имя |
длина волны нм |
волновое число см −1 |
переход |
|---|---|---|---|
| Винг-Форд | 989.6 | 10100 | Ф 4 Д—Х 4 Д |
| синий | 490 | 20408 | г 6 Ф—а 6 Д |
| зеленый | 530 | 18867 | и 6 П—а 6 Д |
FeH имеет важную полосу поглощения (называемую полосой Винг-Форда ) в ближней инфракрасной области с краем полосы при 989,652 нм и максимальным поглощением при 991 нм. [ 5 ] Он также имеет синие линии от 470 до 502,5 нм и зеленые от 520 до 540 нм. [ 6 ]
Небольшой изотопный сдвиг дейтерированного FeD по сравнению с FeH на этой длине волны показывает , что полоса обусловлена (0,0)-переходом из основного состояния , а именно F 4 Д—Х 4 Д. [ 7 ]
В каждой части спектра существуют различные другие полосы, обусловленные различными колебательными переходами. [ 8 ] Полоса (1,0), также обусловленная F 4 Д—Х 4 Δ переходов составляет около 869,0 нм, а полоса (2,0) около 781,8 нм. [ 4 ]
Внутри каждой полосы имеется большое количество линий. Это связано с переходом между различными состояниями вращения. Линии сгруппированы в поддиапазоны 4 Д 7/2 — 4 Δ 7/2 (самый сильный) и 4 Д 5/2 — 4 Д 5/2 , 4 Д 3/2 — 4 Δ 3/2 и 4 Д 1/2 — 4 Δ 1/2 . Числа типа 7/2 представляют собой значения Ω, компонента спина. [ 8 ] Каждый из них имеет две ветви P и R, а некоторые имеют ветвь Q. Внутри каждого из них происходит так называемое Λ-расщепление, которое приводит к образованию линий с более низкой энергией (обозначаемых «a») и линий с более высокой энергией (называемых «b»). Для каждого из них существует ряд спектральных линий, зависящих от J, вращательного квантового числа, начиная с 3,5 и увеличиваясь с шагом 1. Насколько высоким становится J, зависит от температуры. Кроме того, имеется 12 филиалов-сателлитов. 4 Д 7/2 — 4 Д 5/2 , 4 Д 5/2 — 4 Д 3/2 , 4 Д 3/2 — 4 Д 1/2 , 4 Д 5/2 — 4 Д 7/2 , 4 Д 3/2 — 4 Δ 5/2 и 4 Д 1/2 — 4 Δ 3/2 с ветвями P и R. [ 5 ]
Некоторые линии магниточувствительны, например, 994,813 и 995,825 нм. Они уширены эффектом Зеемана , а другие в той же полосе нечувствительны к магнитным полям, таким как 994,911 и 995,677 нм. [ 9 ] В спектре полосы (0-0) 222 линии. [ 10 ]
Появление в космическом пространстве
[ редактировать ]Гидрид железа — одна из немногих молекул, обнаруженных на Солнце. [ 11 ] Линии FeH в сине-зеленой части солнечного спектра были зарегистрированы в 1972 году, включая множество линий поглощения в 1972 году. [ 6 ] Кроме того, в тенях солнечных пятен хорошо видна полоса Винг-Форда. [ 8 ]
Полосы FeH (и других гидридов переходных металлов и щелочноземельных металлов ) заметно проявляются в спектрах излучения M-карликов и L-карликов , самого горячего вида коричневых карликов. У более холодных T-карликов полосы FeH не появляются, [ 12 ] вероятно, из-за облаков жидкого железа, закрывающих обзор атмосферы и удаляющих ее из газовой фазы атмосферы. У еще более холодных коричневых карликов (<1350 К) вновь появляются сигналы FeH, что объясняется наличием в облаках просветов. [ 13 ]
Объяснение типа звезд, в которых появляется полоса Винг-Форда FeH, заключается в том, что температура составляет около 3000 К, а давление достаточно для образования большого количества молекул FeH. Когда температура достигает 4000 К, как у К-карлика, линия становится слабее из-за диссоциации большего количества молекул. В М- красных гигантах давление газа слишком низкое для образования FeH. [ 7 ]
Эллиптические и линзовидные галактики также имеют наблюдаемую полосу Винг-Форда из-за большого количества их света, исходящего от M-карликов . [ 8 ]
В 2021 году было подтверждено присутствие следов FeH в атмосфере горячего Юпитера WASP-79b . [ 14 ]
Производство
[ редактировать ]Клеман и Окерлинд впервые получили FeH в лаборатории, нагрев железо до 2600 К в печи типа Кинга в тонкой атмосфере водорода.
Молекулярный FeH также можно получить (вместе с FeH 2 и другими видами) путем испарения железа в аргоно-водородной атмосфере и замораживания газа на твердой поверхности при температуре около 10 К (-263 °С ). Соединение можно обнаружить с помощью инфракрасной спектроскопии , и около половины его исчезает при кратковременном нагревании образца до 30 К. [ 15 ] Вариант метода использует атмосферу чистого водорода, конденсированного при 4 К. [ 1 ]
Эта процедура также генерирует молекулы, которые считались FeH 3 (гидридом железа), но позже были отнесены к ассоциации FeH и молекулярного водорода H 2 . [ 16 ]
Молекулярный FeH образуется в результате распада 57 Co заключен в твердый водород. Мессбауэровская спектроскопия выявила изомерный сдвиг 0,59 мм/с по сравнению с металлическим железом и квадрупольное расщепление 2,4 мм/с. [ 17 ] FeH также может быть получен взаимодействием паров пентакарбонила железа и атомарного водорода в микроволновом разряде. [ 18 ]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Перейти обратно: а б Ван, Сюэфэн; Эндрюс, Лестер (2009). «Инфракрасные спектры и теоретические расчеты гидридов металлов и дигидрогенных комплексов Fe, Ru и Os». Журнал физической химии А. 113 (3): 551–563. Бибкод : 2009JPCA..113..551W . дои : 10.1021/jp806845h . ПМИД 19099441 .
- ^ Перейти обратно: а б Халла, Дэниел Ф.; Берроу, Ричард Ф.; Браун, Джон М. (сентябрь 1999 г.). «Низколежащие энергетические уровни молекулы FeH». Молекулярная физика . 97 (1–2): 93–103. Бибкод : 1999MolPh..97...93H . дои : 10.1080/00268979909482812 .
- ^ Гудридж, Дамиан М.; Халла, Дэниел Ф.; Браун, Джон М. (8 января 1998 г.). «Вращательный анализ и отнесение системы полос 630 нм FeH к переходу e 6Π – c 6Σ1». Журнал химической физики . 108 (2): 428–435. Бибкод : 1998JChPh.108..428G . дои : 10.1063/1.475404 .
- ^ Перейти обратно: а б Рам, РС; Бернат, ПФ; Дэвис, СП (10 мая 1996 г.). «Эмиссионная спектроскопия с преобразованием Фурье системы g4Δ – a4Δ FeF» (PDF) . Журнал молекулярной спектроскопии . 179 (2): 297. Бибкод : 1996JMoSp.179..282R . дои : 10.1006/jmsp.1996.0207 . Архивировано из оригинала (PDF) 10 марта 2005 г.
- ^ Перейти обратно: а б Филлипс, Дж. Г.; Дэвис, СП; Линдгрен, Б.; Бальфур, WJ (декабрь 1987 г.). «Ближний инфракрасный спектр молекулы FeH». Серия дополнений к астрофизическому журналу . 65 : 721–778. Бибкод : 1987ApJS...65..721P . дои : 10.1086/191241 . ISSN 0067-0049 .
- ^ Перейти обратно: а б Кэрролл, ПК; МакКормак (1 октября 1972 г.). «Спектр FeH: лабораторная и солнечная идентификация». Письма астрофизического журнала . 177 : L33–L36. Бибкод : 1972ApJ...177L..33C . дои : 10.1086/181047 .
- ^ Перейти обратно: а б Норд, HL; Линдгрен, Б.; Винг, РФ (апрель 1977 г.). «Предлагаемая идентификация FeH в спектрах M-карликов и S-звезд». Астрономия и астрофизика . 56 (1–2): 1–6. Бибкод : 1977A&A....56....1N .
- ^ Перейти обратно: а б с д Скьявон, Рикардо П.; Барбюи, Б.; Сингх, Патан Д. (20 июля 1997 г.). «Полоса FeH Винг-Форда в спектрах M-звезд». Астрофизический журнал . 484 (1). Американское астрономическое общество: 499–510. arXiv : astro-ph/9701186 . Бибкод : 1997ApJ...484..499S . дои : 10.1086/304332 . S2CID 118896684 .
- ^ Райнерс, Ансгар; Шмитт, Юрген ХММ; Лифке, К. (2007). «Быстрая переменность магнитного потока на вспыхивающей звезде CN Leonis» (PDF) . Астрономия и астрофизика . 466 (2): Л13–Л16. arXiv : astro-ph/0703172 . Бибкод : 2007A&A...466L..13R . дои : 10.1051/0004-6361:20077095 . S2CID 17926213 .
- ^ Мулчей, Джон С. (февраль 1989 г.). «Вращательная температура молекулы FeH в солнечном пятне» . Публикации Тихоокеанского астрономического общества . 101 (636). Издательство Чикагского университета: 211–214. Бибкод : 1989PASP..101..211M . дои : 10.1086/132424 . JSTOR 40679297 .
- ^ Синха, К. (1991). «Молекулы на солнце». Труды Астрономического общества Австралии . 9 (1). Астрономическое общество Австралии: 32. Бибкод : 1991PASA....9...32S . дои : 10.1017/S1323358000024814 . S2CID 118585000 . около 11 различных молекул
- ^ Коуэн, Рон (4 июля 1998 г.). «Так здорово, а некоторые до сих пор звезды» . Новости науки .
- ^ Бургассер, Адам Дж.; Марли, Марк С.; Акерман, Эндрю С.; Сомон, Дидье; Лоддерс, Катарина ; Дан, Конард К.; Харрис, Хью К.; Киркпатрик, Дж. Дэви (1 июня 2002 г.). «Свидетельства разрушения облаков при карликовом переходе L/T». Астрофизический журнал . 571 (2): Л151–Л154. arXiv : astro-ph/0205051 . Бибкод : 2002ApJ...571L.151B . дои : 10.1086/341343 . S2CID 17929123 .
- ^ Фут, Тревор О.; Льюис, Николь К.; Килпатрик, Брайан М.; Гоял, Джаеш М.; Бруно, Джованни; Уэйкфорд, Ханна Р.; Роббинс-Бланч, Нина; Катария, Тиффани; Макдональд, Райан Дж.; Лопес-Моралес, «Мерседес»; Синг, Дэвид К.; Микал-Эванс, Томас; Бурье, Винсент; Генри, Грегори; Буххаве, Ларс А. (2022), «Спектр излучения горячего Юпитера WASP-79b от HST/WFC3», The Astronomical Journal , 163 (1): 7, arXiv : 2107.14334 , Bibcode : 2022AJ....163. ...7F , дои : 10.3847/1538-3881/ac2f4a , S2CID 236635028
- ^ Чертихин Георгий Владимирович; Эндрюс, Лестер (1995). «Инфракрасные спектры FeH, FeH 2 и FeH 3 в твердом аргоне». Журнал физической химии . 99 (32): 12131–12134. дои : 10.1021/j100032a013 .
- ^ Эндрюс, Лестер (30 января 2004 г.). «Матричные инфракрасные спектры и расчеты функционала плотности гидридов переходных металлов и диводородных комплексов». Обзоры химического общества . 33 (2): 123–132. дои : 10.1039/B210547K . ПМИД 14767507 .
- ^ Пастернак М.; Ван Дер Хейден, М.; Лангуш, Г. (февраль 1984 г.). «Характеристика молекул FeH методом мессбауэровской спектроскопии» . Письма по химической физике . 104 (4): 398–400. Бибкод : 1984CPL...104..398P . дои : 10.1016/0009-2614(84)80087-1 .
- ^ Браун, Джон М.; Кёрсген, Хельга; Битон, Стюарт П.; Эвенсон, Кеннет М. (2006). «Вращательный спектр и тонкая структура FeH, изученный методом лазерного магнитного резонанса в дальнем инфракрасном диапазоне» . Журнал химической физики . 124 (23). Американский институт физики: 234309. Бибкод : 2006JChPh.124w4309B . дои : 10.1063/1.2198843 . ПМИД 16821920 . S2CID 31889615 .

