Сульфонамид

В органической химии сульфонамидная сульфонамид функциональная группа (также называемая ) представляет собой сероорганическую группу со структурой R-S(=O) 2 -NR 2 . Он состоит из сульфонильной группы ( O=S=O ), связанный с аминогруппой ( −NH 2 ). Условно говоря, эта группа нереактивна . Из-за жесткости функциональной группы сульфаниламиды обычно являются кристаллическими ; по этой причине образование сульфонамида является классическим методом превращения амина в кристаллическое производное, которое можно определить по температуре плавления . Многие важные лекарства содержат сульфаниламидную группу. [1]
Сульфонамид , (соединение) — это химическое соединение содержащее эту группу. Общая формула R-SO 2 NR'R" или R-S(=O) 2 -NR'R" , где каждый R представляет собой некоторую органическую группу; например, "метансульфонамид" (где R = метан , R' = R" = водород ) СН 3 SO 2 NH 2 . Любой сульфаниламид можно рассматривать как производное сульфоновой кислоты путем замены гидроксильной группы ( −OH ) с аминогруппой.
В медицине термин «сульфаниламид» иногда используется как синоним сульфаниламида , производного или разновидности сульфаниламида. Первый сульфаниламид был обнаружен в Германии в 1932 году. [2]
Синтез и реакции
[ редактировать ]Сульфонамиды можно получить в лаборатории разными способами. Классический подход предполагает реакцию сульфонилхлоридов с амином .
- RSO 2 Cl + R' 2 NH → RSO 2 NR' 2 + HCl
Обычно добавляют такое основание, как пиридин, для поглощения образующейся HCl. Показательным является синтез сульфонилметиламида. [3] Реакция первичных и вторичных аминов с бензолсульфонилхлоридом лежит в основе реакции Хинсберга — метода обнаружения первичных и вторичных аминов.
Сульфонамиды вступают в разнообразные кислотно-основные реакции. Связь NH может быть депротонирована. Алкилсульфонамиды могут быть депротонированы по углероду. Арилсульфонамиды подвергаются орто-литированию . [4]
Султамс
[ редактировать ]Сультамы представляют собой циклические сульфаниламиды. Биоактивные сультамы включают противовоспалительный ампироксикам и противосудорожный сультиам . Сультамы получают аналогично другим сульфаниламодам, с учетом того, что сульфокислоты депротонируются аминами. Их часто получают путем окисления дисульфидов или тиолов, связанных с аминами, в одном котле. [5] Альтернативный синтез сультамов включает первоначальное получение линейного сульфонамида с последующим образованием внутримолекулярной связи CC (т.е. циклизацией) - стратегия, которая использовалась при синтезе темно-синего эмиттера на основе сультама для органической электроники . [6]
- Соединения на основе сульфаниламидов
- Сахарин , циклический сульфаниламид, который был одним из первых искусственных подсластителей . обнаруженных
- Сульфаниламид — соединение, которое предвосхитило разработку сульфаниламидных препаратов.
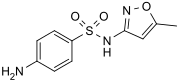
- Сульфаметоксазол – широко используемый антибиотик .
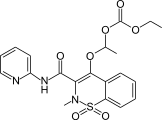
- Ампироксикам — султам, используемый в качестве противовоспалительного препарата.
- Гидрохлоротиазид – препарат, содержащий как ациклические, так и циклические сульфонамидные группы.
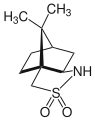
- Камфорсултам — сультам, используемый в качестве хирального вспомогательного средства в органическом синтезе.
Сульфинамиды
[ редактировать ]Родственные сульфинамиды (R(S=O)NHR) представляют собой амиды сульфиновых кислот (R(S=O)OH) (см. сульфинил ). Хиральные сульфинамиды, такие как трет-бутансульфинамид , п-толуолсульфинамид. [7] [8] и 2,4,6-триметилбензолсульфинамид [9] имеют отношение к асимметричному синтезу .
Дисульфонимиды
[ редактировать ]Бис(трифторметансульфонил)анилин является источником трифлила ( CF 3 SO + 2 ) группа.
Дисульфонимиды типу относятся к R-S(=O) 2 -N(H)-S(=O) 2 -R' с двумя сульфонильными группами, фланкирующими амин. [10] Как и сульфинамиды, этот класс соединений используется в качестве катализаторов в энантиоселективном синтезе. [10] [11] [12]
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Актер, П.; Чоу, AW; Дутко, Ф.Дж.; Маккинли, магистр «Химиотерапия». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a06_173 . ISBN 978-3527306732 .
{{cite encyclopedia}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Леви, Стюарт Б. (2002). Парадокс антибиотиков: как неправильное использование антибиотиков разрушает их лечебную силу (2-е изд.). Кембридж, Массачусетс: Perseus Publ. п. 51. ИСБН 9780738204406 .
- ^ де Бур, Т. Дж.; Бэкер, HJ (1954). «п-толуолсульфонилнитрозамид». Орг. Синтез . 34 : 96. дои : 10.15227/orgsyn.034.0096 .
- ^ Танака, Казухико (1991). «Сульфоновые кислоты, сложные эфиры, амиды и галогениды как синтоны». У Саула Патая, Цви Раппопорта (ред.). Сульфоновые кислоты, сложные эфиры и их производные (1991) . Химия функциональных групп ПАТАИ. стр. 401–452. дои : 10.1002/0470034394.ch11 . ISBN 978-0-470-03439-2 .
- ^ Рассадин, В.; Грошева Д.; Томашевский, А. Соколов, В. «Методы синтеза сультама» Химия гетероциклических соединений 2013, Том. 49, с39-65. 27. дои : 10.1007/s10593-013-1231-3 .
- ^ Вирк, Тарунприт Сингх; Илаве, Ниранджан В.; Чжан, Госянь; Ю, Крейг П.; Вонг, Брайан М.; Чан, Джулиан М.В. (2016). «Гетеро[5]гелицен на основе сультама: синтез, структура и усиление эмиссии, вызванное кристаллизацией» . АСУ Омега . 1 (6): 1336–1342. дои : 10.1021/acsomega.6b00335 . ПМК 6640820 . ПМИД 31457199 .
- ^ Органические синтезы, Сб. Том. 10, с.47 (2004); Том. 77, с.50 (2000). Связь
- ^ Орг. Синтез. 2007, 84, 129-138 Ссылка
- ^ Орг. Синтез. 2006, 83, 131-140 Ссылка
- ^ Jump up to: а б Джеймс, Томас; ван Геммерен, Мануэль; Список, Бенджамин (2015). «Разработка и применение дисульфонимидов в энантиоселективном органокатализе». хим. Преподобный . 115 (17): 9388–9409. doi : 10.1021/acs.chemrev.5b00128 . ПМИД 26147232 .
- ^ Трескоу, М.; Нойдорфль, Дж.; Гирнот, Р. (2009). «БИНБАМ - новый мотив для сильных и хиральных кислот Бренстеда». Евро. Дж. Орг. Хим . 2009 (22): 3693–3697. дои : 10.1002/ejoc.200900548 .
- ^ Гарсия-Гарсия, П.; Лэй, Ф.; Гарсия-Гарсия, П.; Рабалакос, К.; Лист, Б. (2009). «Мощный хиральный контранионный мотив для асимметричного катализа» . Энджью. хим. Межд. Эд . 48 (24): 4363–4366. дои : 10.1002/anie.200901768 . ПМИД 19437518 .