Ацетат железа(II)
 | |
| Имена | |
|---|---|
| Название ИЮПАК Ацетат железа(II) | |
| Другие имена Ацетат железа | |
| Идентификаторы | |
3D model ( JSmol ) |
|
| ХимическийПаук | |
| Информационная карта ECHA | 100.019.492 |
ПабХим CID | |
| номер РТЭКС |
|
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 4 Н 6 Fe O 4 | |
| Молярная масса | 173.933 g·mol −1 |
| Появление | Белые кристаллы (безводные) Светло-зеленые кристаллы (тетрагидрат) |
| Запах | Без запаха |
| Плотность | 1,734 г/см 3 (−73 ° С) [1] |
| Температура плавления | 190–200 ° C (374–392 ° F; 463–473 К) разлагается [2] [3] |
| Растворимый [2] | |
| Структура | |
| Орторомбический , oP75 (200 К) | |
| Пбкн, № 60 (200 К) [1] | |
| 2/м 2/м 2/м (200 К) | |
а = 18,1715(4) Å, b = 22,1453(5) Å, c = 8,2781(2) Å (200 К) α = 90°, β = 90°, γ = 90° | |
| Опасности | |
| СГС Маркировка : | |
 [3] [3] | |
| Предупреждение | |
| Х315 , Х319 , Х335 [3] | |
| П261 , П305+П351+П338 [3] | |
| NFPA 704 (огненный алмаз) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
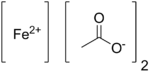
Ацетат железа(II) представляет собой координационный комплекс формулы Fe(CH 3 COO) 2 . Это белое твердое вещество, хотя нечистые образцы могут слегка окрашиваться. [1] Известен также светло-зеленый тетрагидрат , хорошо растворимый в воде.
Подготовка и структура
[ редактировать ]
Порошок железа реагирует с уксусной кислотой при электролизе с образованием ацетата железа с выделением газообразного водорода: [1]
- Fe + 2 CH 3 CO 2 H → Fe(CH 3 CO 2 ) 2 + H 2
Его также можно получить из нерастворимого карбоната железа (II) оливково-зеленого цвета . [ нужна ссылка ]
Он имеет полимерную структуру с октаэдрическими центрами Fe(II), связанными между собой ацетатными лигандами. Это координационный полимер . [1]
Гидратную форму получают реакцией оксида или гидроксида железа с уксусной кислотой . [5]
Реакция железного лома с уксусной кислотой дает коричневую смесь различных ацетатов железа (II) и железа (III), которые используются при крашении. [6]
Использование
[ редактировать ]Ацетат железа используется в качестве протравы в красильной промышленности. Эбонизация древесины – один из таких процессов. [7]
Ссылки
[ редактировать ]- ^ Jump up to: а б с д и ж Вебер, Биргит; Бетц, Ричард; Бауэр, Вольфганг; Шламп, Стефан (2011). «Кристаллическая структура ацетата железа (II)». Журнал неорганической и общей химии . 637 : 102-107. дои : 10.1002/zaac.201000274 .
- ^ Jump up to: а б Лиде, Дэвид Р., изд. (2009). Справочник CRC по химии и физике (90-е изд.). Бока-Ратон, Флорида : CRC Press . ISBN 978-1-4200-9084-0 .
- ^ Jump up to: а б с д Sigma-Aldrich Co. , Ацетат железа(II) . Проверено 3 мая 2014 г.
- ^ «Паспорт безопасности ацетата железа» . fishersci.ca . Fair Lawn : Fisher Scientific . Проверено 2 августа 2014 г.
- ^ «Синтез гидрата ацетата железа(II) (ацетата железа)» . Архивировано из оригинала 25 августа 2013 г. Проверено 7 января 2009 г.
- ^ Вильдермут, Эгон; Старк, Ганс; Фридрих, Габриэле; Эбенхёх, Франц Людвиг; Кюборт, Бриджит; Сильвер, Джек; Ритупер, Рафаэль (2000). «Соединения железа». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a14_591 . ISBN 978-3527306732 .
- ^ Эбонизация древесины ацетатом железа
