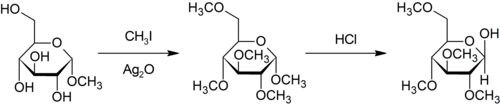Метилирование
Метилирование в химических науках является добавлением метильной группы на субстрат или замену атома (или группы) метильной группой. Метилирование является формой алкилирования , с метильной группой, заменяющей атом водорода . Эти термины обычно используются в химии , биохимии , науке о почве и биологии .
В биологических метилирование катализируется ферментами ; системах Такое метилирование может участвовать в модификации тяжелых металлов , регуляции экспрессии генов , регуляции функции белка и обработки РНК . Метилирование образцов ткани in vitro также является способом уменьшить некоторые гистологические окрашивающие артефакты . Обратной метилированием является деметилирование .
В биологии
[ редактировать ]В биологических системах метилирование достигается ферментами. Метилирование может модифицировать тяжелые металлы и может регулировать экспрессию генов, обработку РНК и функцию белка. Это ключевой процесс, лежащий в основе эпигенетики . Источники метильных групп включают S-метилметионин, метилфолат, метил B12. [ 1 ]
Метаногенез
[ редактировать ]Метаногенез , процесс, который генерирует метатан из CO 2 , включает серию реакций метилирования. Эти реакции вызваны набором ферментов, которые питались семейством анаэробных микробов. [ 2 ]

В обратном метаногенезе метан является метилирующим агентом. [ 3 ]
О-метилтрансферазы
[ редактировать ]Широкое разнообразие фенолов подвергается О-метилированию, чтобы получить анизола производные . Этот процесс, катализируемый такими ферментами, как кофеоил-коа-о-метилтрансфераза , является ключевой реакцией в биосинтезе лигнолов , перкурсоров для лигнина , основного структурного компонента растений.
Растения производят флавоноиды и изофлавоны с метилированием на гидроксильных группах, то есть метокси -связях . Это 5-O-метилирование влияет на растворимость водой флавоноида. Примерами являются 5-O-метилгенистейн , 5-O-метилмирицитин и 5-O-метилкетин (азалин).
Белки
[ редактировать ]Наряду с убиквитинированием и фосфорилированием , метилирование является основным биохимическим процессом для модификации функции белка. Наиболее распространенные метилирование белка влияют на остаток аргинина и лизина специфических гистонов. В противном случае гистидин, глутамат, аспарагин, цистеин подвержен метилированию. Некоторые из этих продуктов включают S -метилцистеин , два изомера N -метилхистидина и два изомера N -метиларгинина. [ 4 ]
Метиониновая синтаза
[ редактировать ]
Метионинсинтаза регенерирует метионин (MET) из гомоцистеина (HCY). Общая реакция трансформирует 5-метилтетрагидрофолат (n 5 -Матф) в тетрагидрофолат (ТГФ) при переносе метильной группы в Hcy для образования. Синтезы метионина могут быть кобаламин-зависимыми и кобаламин-независимыми: растения имеют оба животных зависят от метилкобаламина-зависимой формы.
В метилкобаламин-зависимых формах фермента реакция проходит на два этапа реакции пинг-пенга. Фермент первоначально заправляется в реактивное состояние путем переноса метильной группы из N 5 -Матф к Co (i) в ферментативном связанном кобаламине ((COB), также известном как витамин B12)), , образуя метилкобаламин (ME-COB), который теперь содержит ME-CO (III) и активирует фермент. Затем HCY, который скоординировал с ферментом цинком , образуя реактивный тиолат, реагирует с Me-Cob. Активированная метильная группа переносится из Me-Cob в Hcy Thiolate, который регенерирует Co (i) в COB, и Met высвобождается из фермента. [ 5 ]
Тяжелые металлы: мышьяк, ртуть, кадмий
[ редактировать ]Биометилирование - это путь для преобразования некоторых тяжелых элементов в более мобильные или более летальные производные, которые могут попасть в пищевую цепь . Биометилирование мышьяка соединений начинается с образования метанемонатов . Таким образом, тривалентные неорганические мышьяковые соединения метилируются, чтобы получить метанеарсон. S-аденозилметионин является донором метила. Метанерсоны являются предшественниками диметиларсонов, опять же из -за цикла восстановления (к метиларсовой кислоте) с последующим вторым метилированием. [ 6 ] Связанные пути обнаруживаются в микробном метилировании ртути в метилртути .
Эпигенетическое метилирование
[ редактировать ]Метилирование ДНК
[ редактировать ]Метилирование ДНК является превращением цитозина в 5-метилцитозин . Образование ME-CPG катализируется ферментом ДНК метилтрансферазы . У позвоночных метилирование ДНК обычно происходит в сайтах CPG (сайты цитозин-фосфата-гуанина, то есть сайты, где цитозин непосредственно следует гуанин в последовательности ДНК). У млекопитающих метилирование ДНК распространено в клетках тела, [ 7 ] и метилирование сайтов CPG, по -видимому, по умолчанию. [ 8 ] [ 9 ] ДНК человека имеет около 80–90% участков CPG метилированными, но есть определенные области, известные как острова CPG , которые являются богатыми CG (высокое содержание цитозина и гуанина, состоящие из примерно 65% остатков CG ), где никто не метилирован Полем Они связаны с промоторами 56% генов млекопитающих, включая все повсеместно экспрессируемые гены . Один -два процента генома человека являются кластерами CPG, и существует обратная связь между метилированием CPG и транскрипционной активностью. Метилирование, способствующее эпигенетическому наследованию, может происходить через метилирование ДНК или метилирование белка. Неправильные метилирование генов человека могут привести к развитию заболеваний, [ 10 ] [ 11 ] в том числе рак. [ 12 ] [ 13 ]
У медоносных пчел метилирование ДНК связано с альтернативным сплайсингом и регуляцией генов на основе функциональных геномных исследований, опубликованных в 2013 году. [ 14 ] Кроме того, метилирование ДНК связано с изменениями экспрессии в иммунных генах, когда медовые пчелы находились при летальной вирусной инфекции. [ 15 ] Несколько обзоров были опубликованы по темам метилирования ДНК у социальных насекомых. [ 16 ] [ 17 ]
РНК метилирование
[ редактировать ]Метилирование РНК происходит у разных видов РНК, а именно. тРНК , рРНК , мРНК , тмРНК , снРНК , снорна , miRNA и вирусная РНК. Различные каталитические стратегии используются для метилирования РНК различными РНК-метилтрансферазами. Считается, что метилирование РНК существовало до метилирования ДНК в ранних формах жизни, развивающихся на Земле. [ 18 ]
N6-метиладенозин (M6A) является наиболее распространенной и обильной модификацией метилирования в молекулах РНК (мРНК), присутствующих у эукариот. 5-метилцитозин (5-MC) также обычно встречается в различных молекулах РНК. Недавние данные убедительно свидетельствуют о том, что метилирование РНК M6A и 5-MC влияет на регуляцию различных биологических процессов, таких как стабильность РНК и трансляция мРНК, [ 19 ] и что аномальное метилирование РНК способствует этиологии заболеваний человека. [ 20 ]
У социальных насекомых, таких как медоносные пчелы, метилирование РНК изучается как возможный эпигенетический механизм, лежащий в основе агрессии через взаимные скрещивания. [ 21 ]
Метилирование белка
[ редактировать ]Метилирование белка обычно происходит на остатках аргинина или лизина аминокислотных в последовательности белка. [ 22 ] Аргинин может быть метилирован один раз (монометилированный аргинин) или два раза, либо обеими метильные группы на одном терминальном азоте ( асимметричный диметиларгинин ) или одну на обоих нитрогенах (симметричный диметиларгинин), с помощью белковых метилтрансфераз (PRMT). Лизин может быть метилирован один, два, два раза или три раза с помощью метилтрансфераз лизина . Метилирование белка было наиболее изучено в гистонах . Передача метильных групп из S-аденозилметионина в гистоны катализируется ферментами, известными как гистон-метилтрансферазы . Гистоны, которые метилированы на определенных остатках, могут эпигенетически действовать для подавления или активации экспрессии генов. [ 23 ] [ 24 ] Метилирование белка является одним из типов посттрансляционной модификации .
Эволюция
[ редактировать ]Метильный метаболизм очень древний и может быть обнаружен во всех организмах на земле, от бактерий до людей, что указывает на важность метаболизма метила для физиологии. [ 25 ] Действительно, фармакологическое ингибирование глобального метилирования у видов, начиная от человека, мыши, рыбы, мухи, круглого червя, растения, водорослей и цианобактерий, вызывает такое же влияние на их биологические ритмы, демонстрируя консервативную физиологическую роль метилирования во время эволюции. [ 26 ]
В химии
[ редактировать ]Термин метилирование в органической химии относится к процессу алкилирования, используемому для описания доставки Ch 3 Группа. [ 27 ]
Электрофильное метилирование
[ редактировать ]Метилирования обычно выполняются с использованием электрофильных метил -источников, таких как йодометан , [ 28 ] диметилсульфат , [ 29 ] [ 30 ] диметил карбонат , [ 31 ] или хлорид тетраметиламмония . [ 32 ] Менее распространенные, но более мощные (и более опасные) метилирующие реагенты включают метил трифлат , [ 33 ] диазометан , [ 34 ] и метилторульфонат ( магия метил ). Все эти реагенты реагируют через S N 2 нуклеофильные замены . Например, карбоксилат может быть метилирован на кислороде с получением метилового эфира ; алкоксидная соль Рост − может быть также метилирован, чтобы дать эфир , Роч 3 ; или кетоновый энолат может быть метилирован на углероде для получения нового кетона .
Метилирование Purdie является специфичным для метилирования на кислороде углеводов с использованием йодометана и оксида серебра . [ 35 ]
Метилирование Eschweiler -clarke
[ редактировать ]Реакция Eschweiler -Clarke является методом метилирования аминов . [ 36 ] Этот метод позволяет избежать риска кватернизации , который возникает, когда амины метилируются метилгалогентами.

Диазометан и триметилсилидазометан
[ редактировать ]Диазометан и более безопасные аналоговые триметилсилдилдиазометановые метилированные карбоновые кислоты, фенолы и даже спирты:
Метод дает преимущество в том, что боковые продукты легко удаляются из смеси продуктов. [ 37 ]
Нуклеофильное метилирование
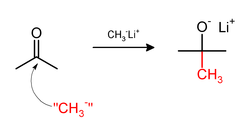
[ редактировать ]Метилирование иногда включает использование нуклеофильных метильных реагентов. Сильно нуклеофильные метилирующие агенты включают метиллит ( Ch 3 LI ) [ 38 ] или реагенты Grignard, такие как бромид метилмагности ( CH 3 MGX ). [ 39 ] Например, CH 3 LI добавит метильные группы в карбонил (C = O) кетонов и альдегида.:
Более мягкие метилирующие агенты включают тетраметилтин , диметилцинк и триметилалиминие . [ 40 ]
Смотрите также
[ редактировать ]Биологические темы
[ редактировать ]- Секвенирование бисульфита - биохимический метод, используемый для определения наличия или отсутствия метильных групп в последовательности ДНК
- MethDB База данных метилирования ДНК
- Микромасштабный термофорез - биофизический метод для определения состояния метилизации ДНК [ 41 ]
- Remethilation , обратимое удаление метильной группы в метионине и 5-метилцитозин
Темы органической химии
[ редактировать ]- Алкилирование
- Метокси
- Титан -цинк метиленация
- Петазис реагент
- Нистед реагент
- Реакция остроумия
- Реагент Теббе
Ссылки
[ редактировать ]- ^ Ragsdale, Stephen W. (2008). «Катализ переводов метильной группы с участием тетрагидрофолата и B12». Фолиевая кислота и фолосы . Витамины и гормоны. Тол. 79. С. 293–324. doi : 10.1016/s0083-6729 (08) 00410-x . ISBN 978-0-12-374232-2 Полем PMC 3037834 . PMID 18804699 .
- ^ Thauer, RK, «Биохимия метаногенеза: дань уважения Марджори Стивенсону», Microbiology, 1998, том 144, страницы 2377-2406.
- ^ Тиммерс, сверстник ха; Welte, Cornelia U.; Koehorst, Jasper J.; Plugge, Caroline M.; Джеттен, Майк С.М.; Stams, Alfons JM (2017). «Обратный метаногенез и дыхание в метанотрофной археи» . Археи . 2017 : 1–22. doi : 10.1155/2017/1654237 . HDL : 1822/47121 .
- ^ Кларк, Стивен Г. (2018). «Рибосома: горячая точка для идентификации новых типов белковых метилтрансфераз» . Журнал биологической химии . 293 (27): 10438–10446. doi : 10.1074/jbc.aw118.003235 . PMC 6036201 . PMID 29743234 .
- ^ Мэтьюз, RG; Смит, Ае; Чжоу, ZS; Таурог, re; Бандаряна, В.; Эванс, JC; Людвиг, М. (2003). «Кобаламин-зависимые и кобаламин-независимые метиониновые синтазы: есть ли два решения одной и той же химической задачи?». Helvetica Chimica Acta . 86 (12): 3939–3954. doi : 10.1002/hlca.200390329 .
- ^ Styblo, M.; Del Razo, LM; Vega, L.; Гермолек, доктор; Lecluyse, El; Гамильтон, Джорджия; Рид, W.; Ван, C.; Каллен, WR; Томас, DJ (2000). «Сравнительная токсичность тривалентных и пентавалентных неорганических и метилированных мышьяков в клетках крыс и человека». Архив токсикологии . 74 (6): 289–299. doi : 10.1007/s002040000134 . PMID 11005674 . S2CID 1025140 .
- ^ Tost J (2010). «Метилирование ДНК: введение в биологию и связанные с заболеванием изменения перспективного биомаркера». Мол биотехнол . 44 (1): 71–81. doi : 10.1007/s12033-009-9216-2 . PMID 19842073 . S2CID 20307488 .
- ^ Lister R, Pelizzola M, Dowen RH, Hawkins Rd, Hon G, Tonti-Filippini J, Nery Jr, Lee L, Ye Z, NGO QM, Edsall L, Antosiewicz-Bourget J, Stewart R, Ruotti V, Millar AH, Thomson JA, Ren B, Ecker Jr (ноябрь 2009 г.). «Метиломы ДНК человека в разрешении на основе демонстрируют широко распространенные эпигеномные различия» . Природа . 462 (7271): 315–22. Bibcode : 2009natur.462..315L . doi : 10.1038/nature08514 . PMC 2857523 . PMID 19829295 .
- ^ Статус MB, Marc, Burger L, Ivanek R, Flood F, Schöler A, Van Nim, Gross C, Oakeley EJ, Gaids D, House VK, Schübeler D (декабрь 2011 г.). «ДНК-связывающие факторы формируют метитом мыши в дистальных регуляторных областях» . Природа . 480 (7378): 490–5. doi : 10.1038/ nature1 PMID 22170606 .
- ^ Rotondo JC, Selvatici R, Di Domenico M, Marci R, Vesce F, Tognon M, Martini F (сентябрь 2013 г.). «Потеря метилирования в гене с импринтированным H19 коррелирует с гиперметилированием гена метилентетрагидрофолатредуктазы гиперметилирования в образцах спермы от бесплодных мужчин» . Эпигенетика . 8 (9): 990–7. doi : 10.4161/epi.25798 . PMC 3883776 . PMID 23975186 .
- ^ Rotondo JC, Bosi S, Bazzan E, Di Domenico M, De Mattei M, Selvatici R, Patella A, Marci R, Tognon M, Martini F (декабрь 2012 г.). «Гиперметилирование гена метилентетрагидрофолатредуктазы гиперметилирование в образцах спермы бесплодных пар коррелирует с рецидивирующим спонтанным абортом» . Человеческое воспроизведение . 27 (12): 3632–8. doi : 10.1093/Humrep/des319 . HDL : 11392/1689715 . PMID 23010533 .
- ^ Rotondo JC, Borghi A, Selvatici R, Magri E, Bianchini E, Montinari E, Corazza M, Virgili A, Tognon M, Martini F (2016). «Инактивация гена IRF6, индуцированная гиперметилированием как возможного раннего события в прогрессировании плоскоклеточного карциномы вульвара, связанного с лишайным склерозом». Джама Дерматология . 152 (8): 928–33. doi : 10.1001/jamadermatol.2016.1336 . PMID 27223861 .
- ^ Rotondo JC, Borghi A, Selvatici R, Mazzoni and, Bononi I, Corazza M, Kussini J, Montinari and, Gafà R, Tognon M, Martini F (2018). «Ассоциация β-гена рецептора ретиноевой кислоты с появлением и прогрессированием лишайного склерозу-аглиадоцированного плоскоклеточного рака вульвы» . Джама Дерматология . 154 (7): 819–823. Doi : 10,1001/Jamadermatol . PMC 6128494 . PMID 29898214 .
- ^ Li-Byarlay, Hongmei; Ли, Ян; Страуд, Хьюм; Фэн, Сухуа; Ньюман, Томас С.; Канеда, Меган; Хоу, Кирк К.; Уорли, Ким С.; Эльсик, Кристина Г.; Виклин, Самуил А.; Джейкобсен, Стивен Э.; Ма, Цзянь; Робинсон, Джин Э. (30 июля 2013 г.). «Норкдаун РНК-интерференции ДНК метил-трансферазы 3 влияет на альтернативную сплайсинг генов в медовой пчел» . Труды Национальной академии наук . 110 (31): 12750–12755. Bibcode : 2013pnas..11012750L . doi : 10.1073/pnas.1310735110 . PMC 3732956 . PMID 23852726 .
- ^ Li-Byarlay, Hongmei; Бонкристиани, Гумберто; Хауэлл, Гэри; Герман, Джейк; Кларк, Линдсей; Стрэнд, Мишелин К.; Тарпи, Дэвид; Рюппелл, Олав (24 сентября 2020 г.). «Транскриптомная и эпигеномная динамика медоносных пчел в ответ на смертельную вирусную инфекцию» . Границы в генетике . 11 doi : 10.3389/fgene.2020.566320 . PMC 7546774 . PMID 33101388 .
- ^ Li-Byarlay, Hongmei (19 мая 2016 г.). «Функция метилирования ДНК у социальных насекомых» . Границы в экологии и эволюции . 4 doi : 10.3389/fevo.2016.00057 .
- ^ Ван, Инг; Li-Byarlay, Hongmei (2015). Физиологические и молекулярные механизмы питания у медоносных пчел . Достижения в области физиологии насекомых. Тол. 49. С. 25–58. doi : 10.1016/bs.aiip.2015.06.002 . ISBN 978-0-12-802586-4 .
- ^ Рана, Аджай К.; Анкри, Серж (6 июня 2016 г.). «Возрождение мира РНК: понимание появления РНК метилтрансферазы» . Границы в генетике . 7 : 99. doi : 10.3389/fgene.2016.00099 . PMC 4893491 . PMID 27375676 .
- ^ Chhoi, Junhong; IEong, A-Weng; Демирци, Хашан; Чен, Джин; Петр, Алексей; Прабхамс, Арджун; О'Лири, Шон Е; Доминсис, Дэн; Решави, Гидеон; Seltis, S Michael; Эренберг, Монс; Джозеф, Джозеф Д (февраль 2016 г.). МРНК Структура и молекулярный биологический 23 (2): 110–115. doi : 10.1038/nsmm . PMC 482618 . PMID 26751643 .
- ^ Стюарт, Кендал (15 сентября 2017 г.). «Метилирование (MTHFR) тестирование и дефицит фолата» . Архивировано с оригинала 12 октября 2017 года . Получено 11 октября 2017 года .
- ^ Бреснахан, Шон Т.; Ли, Эллен; Кларк, Линдсей; Ма, Ронг; Рангель, Джулиана; Грозингер, Кристина М.; Li-Byarlay, Hongmei (12 июня 2023 г.). «Изучение влияния родителей-аоригин на транскрипцию и метилирование РНК в опосредовании агрессивного поведения у медовых пчел (APIS Mellifera)» . BMC Genomics . 24 (1): 315. DOI : 10.1186/S12864-023-09411-4 . PMC 10258952 . PMID 37308882 .
- ^ Уолш, Кристофер (2006). «Метилирование белка» . Посттрансляционная модификация белков: расширение инвентаризации природы . Робертс и издатели компании. С. 121–149. ISBN 978-0-9747077-3-0 .
- ^ Grewal, Шив; Райс, Джадд С (июнь 2004 г.). «Регуляция гетерохроматина с помощью метилирования гистонов и небольших РНК» . Современное мнение в клеточной биологии . 16 (3): 230–238. doi : 10.1016/j.ceb.2004.04.002 . PMID 15145346 .
- ^ Накаяма, Джун-Ичи; Райс, Джадд С.; Страл, Брайан Д.; Аллис, С. Дэвид; Гревал, Шив (6 апреля 2001 г.). «Роль гистона H3 лизин 9 метилирование в эпигенетическом контроле гетерохроматинового сборки». Наука . 292 (5514): 110–113. Bibcode : 2001sci ... 292..110N . doi : 10.1126/science.1060118 . PMID 11283354 .
- ^ Kozbial, Piotr Z; Мушегиан, Аркади Р. (декабрь 2005 г.). «Естественная история s-аденозилметиониновых связывающих белков» . BMC Структурная биология . 5 (1): 19. doi : 10.1186/1472-6807-5-19 . PMC 1282579 . PMID 16225687 .
- ^ Фустин, Жан-Мишель; Ye, шики; Рейкерс, Кристин; Канеко, Кенсуке; Фукумото, Казуки; Ямано, Маю; Versteven, Marijke; Грюневальд, Эллен; Каргилл, Саманта Дж.; Тамай, Т. Кэтрин; Сюй, Яо; Джаббур, Мария Луиса; Кодзима, Рика; Lamberti, Melisa L.; Йошиока-Кобаяши, Кумико; Уитмор, Дэвид; Таммам, Стефани; Хауэлл, П. Линн; Kageyama, Ryoichiro; Мацуо, Такуя; Станевский, Ральф; Golombek, Diego A.; Джонсон, Карл Хирши; Kakeya, Hideaki; Van Ooijen, Gerben; Окамура, Хитоши (6 мая 2020 г.). «Дефицит метилирования нарушает биологические ритмы от бактерий до людей» . Биология связи . 3 (1): 211. DOI : 10.1038 / S42003-020-0942-0 . PMC 7203018 . PMID 32376902 .
- ^ «Ароматическая замещение, нуклеофильная и органометаллическая». Продвинутая органическая химия марта . 2006. С. 853–933. doi : 10.1002/9780470084960.CH13 . ISBN 978-0-471-72091-1 .
- ^ Вьяс, Гн; Шах, Н.М. (1951). «Кунинацетофенон монометиловый эфир». Органические синтезы . 31 : 90. DOI : 10.15227/orgsyn.031.0090 .
- ^ Hiers, GS (1929). "Анизол". Органические синтезы . 9 : 12. doi : 10.15227/orgsyn.009.0012 .
- ^ ICKE, Roland N.; Редеманн, Эрнст; Wisegarver, Burnett B.; Аллес, Гордон А. (1949). "M-метоксибензальдегид". Органические синтезы . 29 : 63. doi : 10.15227/orgsyn.029.0063 .
- ^ Тундо, Пьетро; Сельва, Маурицио; Бомб, Андреа (1999). «Моно-C-метилатион арилацетонитрилов и метилрилацетатов с помощью диметилболидата: общий метод синтеза чистых 2-арилпропионических кислот. 2-фенилпропионовая кислота». Органические синтезы . 76 : 169. doi : 10.15227/orgsyn.076.0169 .
- ^ Ненад, Мараш; Поланк, Словвенко; Kočevar, Marijan (2008). «Микроволновое метилирование фенолов с хлоридом тетраметиламмония в присутствии K 2 CO 3 или CS 2 CO 3 ». Тетраэдр . 64 (51): 11618–11624. doi : 10.1016/j.tet.2008.10.024 .
- ^ Пун, Кевин Вк; Albiniak, Philip A.; Дадли, Грегори Б. (2007). «Защита спиртов с использованием 2-бензилокси-1-метилпиридиния трифторметансульфанонат: метил (r)-(-)-3-бензилокси-2-метил пропаноат». Органические синтезы . 84 : 295. DOI : 10.15227/orgsyn.084.0295 .
- ^ Neeman, M.; Джонсон, Уильям С. (1961). "Холестаниловый метил -эфир". Органические синтезы . 41 : 9. doi : 10.15227/orgsyn.041.0009 .
- ^ Purdie, T.; Ирвин, JC (1903). «С.? Алкилирование сахаров» . Журнал химического общества, транзакции . 83 : 1021–1037. doi : 10.1039/ct9038301021 .
- ^ ICKE, Roland N.; Wisegarver, Burnett B.; Аллес, Гордон А. (1945). «β-фенилэтидиметиламин». Органические синтезы . 25 : 89. doi : 10.15227/orgsyn.025.0089 .
- ^ Шиори Т., Аояма Т., Сноуден Т. (2001). «Тримитилсилидазометан». Энциклопедия реагентов для органического синтеза . Энциклопедия E-Eeros реагентов для органического синтеза . doi : 10.1002/047084289x.rt298.pub2 . ISBN 978-0-471-93623-7 .
- ^ Липски, Шарон Д.; Холл, Стэн С. (1976). «Ароматические углеводороды из ароматических кетонов и альдегидов: 1,1-дифенилэтан». Органические синтезы . 55 : 7. doi : 10.15227/orgsyn.055.0007 .
- ^ Граммитт, Оливер; Беккер, Эрнест И. (1950). "Транс-1-фенил-1,3-бутадиен". Органические синтезы . 30 : 75. doi : 10.15227/orgsyn.030.0075 .
- ^ Негиши, Эй-Ичи; Matsushita, Hajime (1984). «Катализируемый палладием синтез 1,4-диений путем аллилирования алкениалана: α-фарнесена». Органические синтезы . 62 : 31. doi : 10.15227/orgsyn.062.0031 .
- ^ Wienken CJ, Baaske P, Duhr S, Braun D (2011). «Термофоретические кривые плавления количественно определяют конформацию и стабильность РНК и ДНК» . Исследование нуклеиновых кислот . 39 (8): E52. doi : 10.1093/nar/gkr035 . PMC 3082908 . PMID 21297115 .
Внешние ссылки
[ редактировать ]- Deltamasses Обнаружение метилирования после масс -спектрометрии