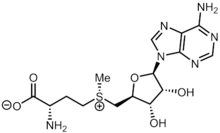
S- Аденозилметионин
 | |
 | |
 | |
| Имена | |
|---|---|
| Систематическое название ИЮПАК (2 S )-2-Амино-4-[( S )-{[(2 S ,3 S ,4 R ,5 R )-5-(4-амино-9 H -пурин-9-ил)-3 ,4-дигидроксиоксолан-2-ил]метил}метилсульфаниумил]бутаноат | |
| Другие имена S- аденозил- L -метионин; Такой же; SAMe, AdoMet , Гепараб (Индия), адеметионин | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ЧЕМБЛ | |
| ХимическийПаук | |
| Информационная карта ECHA | 100.045.391 |
| КЕГГ | |
| МеШ | S-аденозилметионин |
ПабХим CID | |
| НЕКОТОРЫЙ | |
Панель управления CompTox ( EPA ) | |
| Характеристики | |
| С 15 Ч 22 Н 6 О 5 С | |
| Молярная масса | 398.44 g·mol −1 |
| Фармакология | |
| A16AA02 ( ВОЗ ) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
S -Аденозилметионин ( SAM ), также известный под коммерческими названиями SAMe , SAM-e или AdoMet , является распространенным косубстратом, участвующим в переносе метильных групп , транссульфурировании и аминопропилировании. Хотя эти анаболические реакции происходят по всему организму, большая часть SAM вырабатывается и потребляется в печени. [1] Известно более 40 переносов метила от SAM к различным субстратам, таким как нуклеиновые кислоты , белки , липиды и вторичные метаболиты . Он производится из аденозинтрифосфата (АТФ) и метионина под действием метионин-аденозилтрансферазы . SAM был впервые обнаружен Джулио Кантони в 1952 году. [1]
У бактерий SAM связан с рибопереключателем SAM , который регулирует гены, участвующие в биосинтезе метионина или цистеина . В эукариотических клетках SAM служит регулятором множества процессов, включая ДНК , тРНК и рРНК метилирование ; иммунный ответ ; [2] аминокислотный обмен; транссульфурация ; и многое другое. У растений SAM имеет решающее значение для биосинтеза этилена , важного растительного гормона и сигнальной молекулы. [3]
Структура
[ редактировать ]S -Аденозилметионин состоит из аденозильной группы, присоединенной к сере метионина, что придает ему положительный заряд. Он синтезируется из АТФ и метионина ферментом S -аденозилметионинсинтетазой по следующей реакции:
- АТФ + L -метионин + H 2 O фосфат + дифосфат + S -аденозил- L -метионин
Сульфониевая S функциональная группа, присутствующая в - аденозилметионине, является центром его своеобразной реакционной способности. В зависимости от фермента S -аденозилметионин может превращаться в один из трех продуктов:
- аденозильный радикал, который превращается в дезоксиаденозин (AdO): классическая реакция rSAM, также когенерирует метионин.
- S -аденозилгомоцистеин , высвобождающий метильный радикал
- метилтиоаденозин (SMT), гомоаланиновый радикал
Биохимия
[ редактировать ]Цикл ЗРК
[ редактировать ]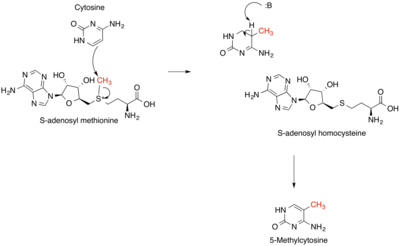
Реакции, которые производят, потребляют и регенерируют SAM, называются циклом SAM. На первом этапе этого цикла SAM-зависимые метилазы (EC 2.1.1), использующие SAM в качестве субстрата, производят S -аденозилгомоцистеин. в качестве продукта [4] S -Аденозилгомоцистеин является сильным негативным регулятором почти всех SAM-зависимых метилаз, несмотря на их биологическое разнообразие. Он гидролизуется до гомоцистеина и аденозина EC S -аденозилгомоцистеингидролазой 3.3.1.1, а гомоцистеин рециркулируется обратно в метионин посредством переноса метильной группы от 5-метилтетрагидрофолата одним из двух классов метионинсинтаз (т.е. кобаламин -зависимых ( EC) 2.1.1.13 ) или кобаламинонезависимый ( EC 2.1.1.14 )). Этот метионин затем может быть преобразован обратно в SAM, завершая цикл. [5] На лимитирующей стадии цикла SAM MTHFR (метилентетрагидрофолатредуктаза) необратимо восстанавливает 5,10-метилентетрагидрофолат до 5-метилтетрагидрофолата. [6]
Радикальные ферменты SAM
[ редактировать ]Большое количество ферментов восстановительно расщепляет SAM с образованием радикалов: 5'-дезоксиаденозил-5'-радикала , метилового радикала и других. Эти ферменты называются радикальными SAM . Все они имеют железо-серный кластер . в своих активных центрах [7] Большинство ферментов, обладающих такой способностью, имеют общую область гомологии последовательности, которая включает мотив CxxxCxxC или близкий вариант. Эта последовательность обеспечивает три цистеинилтиолатных лиганда, которые связываются с тремя из четырех металлов в кластере 4Fe-4S. Четвертый Fe связывает SAM.
Радикальные промежуточные продукты, генерируемые этими ферментами, выполняют широкий спектр необычных химических реакций. Примеры радикальных SAM-ферментов включают лиазу фотопродукта спор , активазы пируватформиат-лиазы и анаэробных сульфатаз, лизин-2,3-аминомутазу и различные ферменты биосинтеза кофакторов, модификации пептидов, образования металлопротеиновых кластеров, тРНК модификации , метаболизма липидов и т. д. Некоторые радикальные ферменты Ферменты SAM используют второй SAM в качестве донора метила. Радикальные ферменты SAM гораздо более распространены у анаэробных бактерий, чем у аэробных организмов. Их можно найти во всех сферах жизни, и они практически не изучены. Недавнее биоинформатическое исследование пришло к выводу, что это семейство ферментов включает по меньшей мере 114 000 последовательностей, включая 65 уникальных реакций. [8]
Дефицит радикальных ферментов SAM связан с различными заболеваниями, включая врожденные пороки сердца , боковой амиотрофический склероз и повышенную восприимчивость к вирусам. [8]
Биосинтез полиаминов
[ редактировать ]Другая важная роль SAM заключается в биосинтезе полиаминов . Здесь SAM декарбоксилируется аденозилметиониндекарбоксилазой ( EC 4.1.1.50 ) с образованием S -аденозилметионинамина . Это соединение затем жертвует свою н- пропиламиновую группу при биосинтезе полиаминов, таких как спермидин и спермин , из путресцина . [9]
SAM необходим для роста и восстановления клеток. Он также участвует в биосинтезе некоторых гормонов и нейротрансмиттеров, влияющих на настроение, таких как адреналин . Метилтрансферазы также ответственны за добавление метильных групп к 2'-гидроксилам первого и второго нуклеотидов рядом с 5'-кэпом в информационной РНК . [10] [11]
Терапевтическое использование
[ редактировать ]Боль при остеоартрите
[ редактировать ]По состоянию на 2012 год данные о том, может ли SAM облегчить боль при остеоартрите, были неубедительными ; Проведенные клинические испытания были слишком малы, чтобы можно было делать обобщения. [12]
Заболевания печени
[ редактировать ]Цикл SAM тесно связан с печенью с 1947 года, поскольку у людей с алкогольным циррозом печени в крови накапливается большое количество метионина. [13] Хотя многочисленные данные лабораторных испытаний на клетках и моделях животных позволяют предположить, что SAM может быть полезен для лечения различных заболеваний печени , по состоянию на 2012 год SAM не изучался ни в каких крупных рандомизированных плацебо-контролируемых клинических исследованиях, которые позволили бы оценить его эффективность. и безопасность. [14] [15]
Депрессия
[ редактировать ]Кокрейновский обзор 2016 года пришел к выводу, что в отношении большого депрессивного расстройства «учитывая отсутствие доказательств высокого качества и невозможность сделать твердые выводы на основе этих данных, следует продолжить изучение использования SAMe для лечения депрессии у взрослых». [16]
Систематический обзор 2020 года показал, что он действует значительно лучше, чем плацебо, и дает такие же результаты, как и другие широко используемые антидепрессанты (имипрамин и эсциталопрам). [17]
Противораковое лечение
[ редактировать ]Недавно было показано, что SAM играет роль в эпигенетической регуляции. Метилирование ДНК является ключевым регулятором эпигенетической модификации во время развития и дифференцировки клеток млекопитающих. В моделях на мышах избыточные уровни SAM были вовлечены в ошибочные паттерны метилирования, связанные с диабетической нейропатией. SAM служит донором метила при метилировании цитозина, которое является ключевым процессом эпигенетической регуляции. [18] Из-за такого влияния на эпигенетическую регуляцию SAM был протестирован в качестве противоракового средства. При многих видах рака пролиферация зависит от низкого уровня метилирования ДНК. Было показано, что добавление in vitro при таких видах рака реметилирует последовательности промотора онкогена и снижает выработку протоонкогенов. [19] При таких видах рака, как колоректальный рак, аберрантное глобальное гиперметилирование может ингибировать промоторные области генов, подавляющих опухоль. Вопреки прежней информации, колоректальный рак (КРР) характеризуется глобальным гипометилированием и промотор-специфичным метилированием ДНК. [20]
Фармакокинетика
[ редактировать ]При пероральном приеме САМ достигает пиковых концентраций в плазме через три-пять часов после приема таблетки с энтеросолюбильным покрытием (400–1000 мг). Период полувыведения составляет около 100 минут. [21]
Доступность в разных странах
[ редактировать ]В Канаде, Великобритании, [22] и в США SAM продается в виде пищевой добавки под торговым названием SAM-e (также пишется SAME или SAMe). [23] Он был представлен в США в 1999 году, после Закона о пищевых добавках, здравоохранении и образовании . принятия в 1994 году [24]
Он был представлен как рецептурный препарат в Италии в 1979 году, в Испании в 1985 году и в Германии в 1989 году. [24] По состоянию на 2012 год он продавался как рецептурный препарат в России, Индии, Китае, Италии, Германии, Вьетнаме и Мексике. [15]
Побочные эффекты
[ редактировать ]желудочно-кишечные расстройства, диспепсия и беспокойство . При употреблении SAM могут возникнуть [21] Долгосрочные эффекты неизвестны. SAM является слабым ДНК- алкилирующим агентом. [25]
Другим зарегистрированным побочным эффектом SAM является бессонница ; поэтому добавку часто принимают утром. Другие сообщения о легких побочных эффектах включают отсутствие аппетита, запор, тошноту, сухость во рту, потливость и беспокойство/нервозность, но в плацебо-контролируемых исследованиях эти побочные эффекты возникают примерно с такой же частотой в группах плацебо. [ нужна медицинская ссылка ]
Взаимодействие и противопоказания
[ редактировать ]Прием SAM одновременно с некоторыми лекарствами может увеличить риск серотонинового синдрома — потенциально опасного состояния, вызванного избытком серотонина. Эти препараты включают, помимо прочего, декстрометорфан (Робитуссин), меперидин (Демерол), пентазоцин (Талвин) и трамадол (Ультрам). [26]
SAM также может взаимодействовать со многими антидепрессантами, включая триптофан и растительное лекарственное средство Hypericum perforatum (зверобой), увеличивая вероятность серотонинового синдрома или других побочных эффектов, а также может снижать эффективность леводопы при болезни Паркинсона. [27] СЭМ может увеличить риск маниакальных эпизодов у людей с биполярным расстройством . [27]
Токсичность
[ редактировать ]Исследование 2022 года пришло к выводу, что SAMe может быть токсичным. Жан-Мишель Фустин из Манчестерского университета сообщил, что исследователи обнаружили, что избыток SAMe распадается на аденин и метилтиоаденозин в организме , что приводит к парадоксальному эффекту ингибирования метилирования. Это было обнаружено у лабораторных мышей , наносящее вред здоровью, и при испытаниях in vitro на клетках человека. [28] [22]
См. также
[ редактировать ]- ДНК-метилтрансфераза
- Рибопереключатель SAM-I
- Рибопереключатель SAM-II
- Рибопереключатель SAM-III
- Рибопереключатель SAM-IV
- SAM-V riboswitch
- Рибопереключатель SAM-VI
- Список исследуемых антидепрессантов
Ссылки
[ редактировать ]- ^ Jump up to: а б Кантони, GL (1952). «Природа активного донора метила, образующегося ферментативно из L-метионина и аденозинтрифосфата». J Am Chem Soc . 74 (11): 2942–3. дои : 10.1021/ja01131a519 .
- ^ Дин, Вэй; Смулан, Лорисса Дж.; Хоу, Николь С.; Тауберт, Стефан; Уоттс, Дженнифер Л.; Уокер, Эми К. (6 октября 2015 г.). « Уровни S -аденозилметионина регулируют врожденный иммунитет посредством различных путей, зависимых от метилирования» . Клеточный метаболизм . 22 (4): 633–645. дои : 10.1016/j.cmet.2015.07.013 . ПМЦ 4598287 . ПМИД 26321661 .
- ^ Ван, X.; О, МВт; Комацу, С. (01 июня 2016 г.). «Характеристика S -аденозилметионинсинтетаз в соевых бобах в условиях наводнения и засухи» . Биология Плантарум . 60 (2): 269–278. дои : 10.1007/s10535-016-0586-6 . ISSN 0006-3134 . S2CID 15567646 .
- ^ Финкельштейн Дж., Мартин Дж. (2000). «Гомоцистеин». Международный журнал биохимии и клеточной биологии . 32 (4): 385–9. дои : 10.1016/S1357-2725(99)00138-7 . ПМИД 10762063 .
- ^ Фёдингер М., Хёрл В., Сундер-Плассманн Г. (январь – февраль 2000 г.). «Молекулярная биология 5,10-метилентетрагидрофолатредуктазы». Дж. Нефрол . 13 (1): 20–33. ПМИД 10720211 .
- ^ Гойетт, П.; Самнер, Дж.С.; Милош, Р.; Дункан, AM; Розенблатт, Д.С.; Мэтьюз, Р.Г.; Розен, Р. (1 июня 1994 г.). «Метилентетрагидрофолатредуктаза человека: выделение кДНК, картирование и идентификация мутаций». Природная генетика . 7 (2): 195–200. дои : 10.1038/ng0694-195 . ISSN 1061-4036 . ПМИД 7920641 . S2CID 23877329 .
- ^ Букер, С.Дж.; Гроув, ТЛ (2010). «Механистическая и функциональная универсальность радикальных ферментов SAM» . Отчеты о биологии F1000 . 2:52 . дои : 10.3410/B2-52 . ПМЦ 2996862 . ПМИД 21152342 .
- ^ Jump up to: а б Ландграф, Брэдли Дж.; Маккарти, Эрин Л.; Букер, Сквайр Дж. (13 июня 2016 г.). «Радикальные S -аденозилметиониновые ферменты в здоровье и болезнях человека». Ежегодный обзор биохимии . 85 : 485–514. doi : 10.1146/annurev-biochem-060713-035504 . ПМИД 27145839 .
- ^ Роже С (2006). « S -Аденозил-L-метионин: помимо универсального донора метильной группы». Фитохимия . 67 (15): 1686–98. Бибкод : 2006PChem..67.1686R . doi : 10.1016/j.phytochem.2006.04.019 . ПМИД 16766004 .
- ^ Лоенен В. (2006). « S -Аденозилметионин: мастер на все руки и мастер всего?». Биохим Соц Транс . 34 (Часть 2): 330–3. дои : 10.1042/BST20060330 . ПМИД 16545107 .
- ^ Чианг П., Гордон Р., Тал Дж., Цзэн Дж., Доктор Б., Пардхасарадхи К., Макканн П. (1996). « S -Аденозилметионин и метилирование» . ФАСЕБ Дж . 10 (4): 471–80. дои : 10.1096/fasebj.10.4.8647346 . ПМИД 8647346 . S2CID 11214528 .
- ^ Рутьес, AW; Нюеш, Э; Райхенбах, С; Юни, П. (7 октября 2009 г.). « S -Аденозилметионин при остеоартрите коленного или тазобедренного сустава» (PDF) . Кокрановская база данных систематических обзоров . 2009 (4): CD007321. дои : 10.1002/14651858.CD007321.pub2 . ПМК 7061276 . ПМИД 19821403 .
- ^ Мато, Хосе М (1997). « Синтез S -аденозилметионина: Молекулярные механизмы и клиническое значение». Фармакология и терапия . 73 (3): 265–280. дои : 10.1016/s0163-7258(96)00197-0 . hdl : 10261/79246 . ПМИД 9175157 .
- ^ Ансти, КМ; Дэй, КП (ноябрь 2012 г.). « Терапия S -аденозилметионином (SAMe) при заболеваниях печени: обзор современных данных и клинической пользы» . Журнал гепатологии . 57 (5): 1097–109. дои : 10.1016/j.jhep.2012.04.041 . ПМИД 22659519 .
- ^ Jump up to: а б Лу, Южная Каролина; Мато, Дж. М. (октябрь 2012 г.). « S -Аденозилметионин для здоровья печени, травм и рака» . Физиологические обзоры . 92 (4): 1515–42. doi : 10.1152/physrev.00047.2011 . ПМЦ 3698976 . ПМИД 23073625 .
- ^ Галиция, я; Олдани, Л; Макритчи, К; Амари, Э; Дугалл, Д; Джонс, Теннесси; Лам, RW; Массей, Дж.Дж.; Ятам, Л.Н.; Янг, АХ (10 октября 2016 г.). « S -Аденозилметионин (SAMe) при депрессии у взрослых» . Кокрановская база данных систематических обзоров . 2016 (10): CD011286. дои : 10.1002/14651858.CD011286.pub2 . ПМК 6457972 . ПМИД 27727432 .
- ^ Куомо, Алессандро; Беккарини Крещенци, Бруно; Болоньези, Симона; Гораччи, Арианна; Кукуна, Деспойна; Росси, Родольфо; Фаджолини, Андреа (05 сентября 2020 г.). «S-Аденозилметионин (SAMe) при большом депрессивном расстройстве (БДР): систематический обзор, ориентированный на врачей» . Анналы общей психиатрии . 19 (1). Springer Science and Business Media LLC: 50. doi : 10.1186/s12991-020-00298-z . ISSN 1744-859X . ПМЦ 7487540 . ПМИД 32939220 .
- ^ Варела-Рей, Марта (2014). « Уровни S -аденозилметионина регулируют метилом ДНК шванновских клеток» . Нейрон . 81 (5): 1024–1039. дои : 10.1016/j.neuron.2014.01.037 . ПМЦ 3960855 . ПМИД 24607226 .
- ^ Шмидт, Томас; Леха, Андреас; Салинас-Ристер, Габриэла (31 декабря 2016 г.). «Обработка клеток рака простаты S- аденозилметионином приводит к полногеномным изменениям профилей транскрипции». Джин . 595 (2): 161–167. дои : 10.1016/j.gene.2016.09.032 . ПМИД 27688072 .
- ^ Це, Янсон (12 сентября 2017 г.). «Аберрантное метилирование ДНК при колоректальном раке: на что нам следует ориентироваться?» . Национальная медицинская библиотека . 3 (10): 698–712. дои : 10.1016/j.trecan.2017.08.003 . ПМИД 28958388 .
- ^ Jump up to: а б Наджм В.И., Рейнш С., Хелер Ф., Тобис Дж.С., Харви П.В. (февраль 2004 г.). « S -Аденозилметионин (SAMe) в сравнении с целекоксибом для лечения симптомов остеоартрита: двойное слепое перекрестное исследование. ISRCTN36233495» . BMC Расстройство опорно-двигательного аппарата . 5 :6. дои : 10.1186/1471-2474-5-6 . ПМЦ 387830 . ПМИД 15102339 .
- ^ Jump up to: а б Маккай, Робин (10 апреля 2022 г.). «Биологи предостерегают от токсичных «здоровых» добавок SAMe» . Наблюдатель .
- ^ Вулстон, Крис (31 декабря 2020 г.). «Что такое САМ-е?» . День здоровья . Архивировано из оригинала 12 августа 2020 г.
- ^ Jump up to: а б Боттильери, Т. (ноябрь 2002 г.). « S -Аденозил-L-метионин (SAMe): от скамейки до постели — молекулярная основа плейотрофной молекулы» . Американский журнал клинического питания . 76 (5): 1151С–1157С. дои : 10.1093/ajcn/76.5.1151S . ПМИД 12418493 .
- ^ Ридберг Б., Линдал Т. (1982). «Неферментативное метилирование ДНК внутриклеточным донором метильной группы S -аденозил-L-метионином является потенциально мутагенной реакцией» . ЭМБО Дж . 1 (2): 211–6. дои : 10.1002/j.1460-2075.1982.tb01149.x . ПМК 553022 . ПМИД 7188181 .
- ^ «САМе – Клиника Мэйо» . Клиника Мэйо .
- ^ Jump up to: а б « S -аденозил-L-метионин (SAMe): подробно» . Национальный центр дополнительного и интегративного здравоохранения (NCCIH). 11 января 2017 г.
- ^ Фукумото, Кадзуки; Ито, Какеру; Саер, Бенджамин; Тейлор, Джордж; Йе, Шики; Ямано, Маю; Ториба, Юки; Хейс, Эндрю; Окамура, Хитоши; Фустин, Жан-Мишель (5 апреля 2022 г.). «Избыток S-аденозилметионина ингибирует метилирование посредством катаболизма до аденина» . Коммуникационная биология . 5 (1). Издательская группа Nature : 313. doi : 10.1038/s42003-022-03280-5 . hdl : 2433/269415 . ISSN 2399-3642 . ПМЦ 8983724 . ПМИД 35383287 .
Внешние ссылки
[ редактировать ]- Номер EINECS 249-946-8
- Шиппи, Р. Эндрю; Мендес, Дуглас; Джонс, Кристина; Цергнул, Ирен; Карпиак, Стивен Э. (2004). « S -Аденозилметионин (SAM-e) для лечения депрессии у людей, живущих с ВИЧ/СПИДом» . БМК Психиатрия . 4:38 . дои : 10.1186/1471-244X-4-38 . ПМЦ 535560 . ПМИД 15538952 .
