Цитотоксические Т -клетки
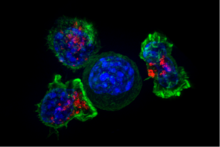
Цитотоксическая Т-клетка (также известная как T C , цитотоксический Т-лимфоцит , CTL , T-Killer , цитолитическая Т-клетка , CD8 + Т-клетки или киллера Т-клетки )-это Т-лимфоцит (тип лейкоцитов ), который убивает раковые клетки, клетки, которые инфицированы внутриклеточными патогенами (такими как вирусы или бактерии), или клетки, которые повреждены другими способами. [ 1 ]
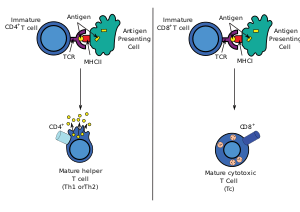
Большинство цитотоксических Т-клеток экспрессируют Т-клеточные рецепторы (TCR), которые могут распознавать специфический антиген . Антиген - это молекула, способная стимулировать иммунный ответ и часто продуцируется раковыми клетками , вирусами, бактериями или внутриклеточными сигналами. Антигены внутри клетки связаны с молекулами MHC класса I и выводятся на поверхность клетки молекулой MHC класса I, где они могут быть распознаны Т -клетками. Если TCR специфичен для этого антигена, он связывается с комплексом молекулы MHC класса I и антигена, а Т -клетка разрушает клетку.
Чтобы TCR связывался с молекулой MHC класса I, первое должно сопровождаться гликопротеином , называемым CD8 , который связывается с постоянной частью молекулы MHC класса I. Следовательно, эти Т -клетки называются CD8 + Т -клетки .
Аффинность , а клетка-мишени была между CD8 и молекулой MHC сохраняет клетку T C тесно связана во время антиген-специфической активации. CD8 + Т-клетки распознаются как клетки T C после того, как они становятся активированными и, как правило, классифицируются как имеющие предварительно определенную цитотоксическую роль в иммунной системе. Однако CD8 + Т-клетки также обладают способностью производить некоторые цитокины , такие как TNF-α и IFN-γ , с противоопухолевыми и антимикробными эффектами.
Разработка
[ редактировать ]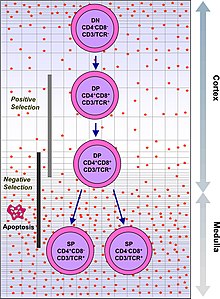
Иммунная система должна распознавать миллионы потенциальных антигенов. В человеческом организме наблюдается менее 30 000 генов, поэтому невозможно иметь один ген для каждого антигена. Вместо этого ДНК в миллионах лейкоцитов в костном мозге перетасовывается для создания клеток с уникальными рецепторами, каждый из которых может связываться с различным антигеном. Некоторые рецепторы связываются с тканями в самом организме человека, поэтому, чтобы предотвратить атаку организма, эти самореактивные лейкоциты разрушаются во время дальнейшего развития в тимусе , в котором йод необходим для его развития и активности. [ 2 ]
TCR имеют две части, обычно альфа и бета -цепь. некоторых TCR есть гамма и дельта . ( У [ 3 ] ) Гемопоэтические стволовые клетки в костном мозге мигрируют в тимус , где они подвергаются рекомбинации V (D) J своей бета-цепной ДНК TCR с образованием формы развития белка TCR, известной как Pre-TCR. Если эта перестройка является успешной, клетки затем переставляют свою ДНК TCR альфа-цепи, чтобы создать функциональный альфа-бета-комплекс TCR. Этот высоко переменный генетический продукт перестройки в генах TCR помогает создавать миллионы различных Т-клеток с различными TCR, помогая иммунной системе организма реагировать практически на любой белок захватчика. Подавляющее большинство Т-клеток экспрессируют альфа-бета-TCR (αβ Т-клетки), но некоторые Т-клетки в эпителиальных тканях (например, кишечник) экспрессируют гамма-дельта ( гамма-дельта-Т-клетки ), которые распознают небетральные антигены. Последние характеризуются их способностью распознавать антигены, которые не представлены. Кроме того, они могут распознавать белки микробного токсического шока и белки стресса на самообеспечение. [ 4 ] Клетки T γδ обладают широкой функциональной пластичностью после распознавания инфицированных или трансформированных клеток, так как они способны продуцировать цитокины (IFN-γ, TNF-α, IL-17) и хемокины (IP-10, лимфотактин), запускают цитолиз клеток-мишеней. (перфорины, гранзимы ...) и взаимодействуют с другими клетками, такими как эпителиальные клетки, моноциты, дендритные клетки, нейтрофилы и В -клетки. В некоторых инфекциях, таких как цитомегаловирус человека , существует клональная экспансия периферических γδ T -клеток, которые имеют специфические TCR, что указывает на адаптивную природу иммунного ответа, опосредованного этими клетками. [ 5 ]
Т-клетки с функционально стабильными TCR экспрессируют как , так и CD8, CD4 и, следовательно, называются «двойные положительные» (DP) T-клетки (CD4 + CD8 + ) Двойные Т-клетки подвергаются воздействию широкого спектра самоантигенов в тимусе и подвергаются двум критериям отбора:
- Положительный отбор , в котором те двойные положительные Т-клетки, которые связываются с инородным антигеном в присутствии самого MHC. Они будут дифференцироваться в любом CD4 + или CD8 + В зависимости от того, какой MHC связан с представленным антигеном (MHC1 для CD8, MHC2 для CD4). В этом случае клетки были бы представлены антиген в контексте MHC1. Положительный отбор означает выбор тех TCR, способных распознавать молекулы MHC.
- Отрицательный отбор , при котором те двойные положительные Т -клетки, которые слишком сильно связываются с MHC -представленными самогенами , подвергаются апоптозу, потому что они иначе могли стать аутореактивными, что приводит к аутоиммунитету .
Только те Т-клетки, которые связываются с комплексами MHC-Self-Antigen, слабо отобранные. Те клетки, которые переживают положительный и отрицательный отбор, дифференцируются в одноположительные Т-клетки (любой CD4 + или CD8 + ), в зависимости от того, распознает ли их TCR антиген II -представленного MHC (CD8) или MHC класса II , антиген (CD4). Это CD8 + Т-клетки, которые будут созревать и становятся цитотоксическими Т-клетками после их активации антигеном, ограниченным I,.
Активация
[ редактировать ]Этот раздел может быть запутанным или неясным для читателей . ( Август 2023 г. ) |
Т -клетки проходят через разные стадии, в зависимости от количества раз, когда они контактировали с антигеном. Во-первых, наивные Т-лимфоциты-это те клетки, которые еще не столкнулись с антигеном в тимусе. Затем Т-лимфоциты становятся Т-клетками памяти. Этот тип Т -клеток - это те, которые были в контакте с антигеном хотя бы один раз, но впоследствии вернулись в покоящее или неактивное состояние, готовое снова реагировать на антиген, на который они стимулировались. Наконец, когда запускается специфический иммунный ответ, эти наивные и Т -клетки памяти активируются, что приводит к воздействию эффекторных Т -клеток, способных уничтожить патогенные микроорганизмы или опухолевые клетки. [ 6 ] [ 7 ]
Порог для активации этих клеток очень высок, и процесс может происходить через два пути: независимый от тимуса (инфицированными APC ) или тимус-зависимым ( CD4+ T-клетками ). В рамках независимого от тимуса пути, поскольку APC инфицирован, он высоко активирован и экспрессирует большое количество со-рецепторов для коактивации. Если APC не инфицированы, необходимо участвовать клетки CD4: либо для активации APC путем костимуляции (чаще всего), либо для непосредственной активации клетки TC путем выделения IL-2 .
Если происходит активация, лимфоциты поляризуют свои гранулы к месту синапса и высвобождают их, создавая «смертельный удар». В этот момент он отделяется от целевой ячейки и может перейти к другому и другому. Целевая клетка умирает примерно через 6 часов, обычно от апоптоза. [ 8 ]
MHC класса I экспрессируется всеми клетками- хозяевами , за исключением не зародышевых , таких как эритроциты . Когда эти клетки инфицированы внутриклеточным патогеном , клетки деградируют инородные белки посредством обработки антигена . Они приводят к пептидным фрагментам, некоторые из которых представлены MHC класса I для рецептора антигена Т -клеток (TCR) на CD8 + Т -клетки.
Активация цитотоксических Т-клеток зависит от нескольких одновременных взаимодействий между молекулами, экспрессируемыми на поверхности Т-клеток и молекул на поверхности антиген-презентативной клетки (APC). Например, рассмотрим две сигнальные модели для T C. активации ячейки
| Сигнал | Т -клетка | Апк | Описание |
|---|---|---|---|
| Первый сигнал | Тк | Пептид-связанный класса I MHC- молекула | Существует второе взаимодействие между CD8 Coreceptor и молекулой MHC класса I, чтобы стабилизировать этот сигнал. |
| Второй сигнал | Молекула CD28 на Т -клетках | CD80 ( или CD86 также называемый B7-1 и B7-2) | CD80 и CD86 известны как костимуляторы для активации Т -клеток. Этот второй сигнал может помочь (или заменен), стимулируя клетку T C с помощью цитокинов, высвобождаемых из T -Helper Clems . |
Простая активация наивного CD8 + Т-клетки требуют взаимодействия с профессиональными антиген-презентативными клетками, в основном со зрелыми дендритными клетками . Для генерации Т -клеток памяти и для обеспечения повторяющейся стимуляции цитотоксических Т -клеток дендритные клетки должны взаимодействовать с обоими активированными CD4 + Helper T -клетки и CD8 + Т -клетки. [ 9 ] [ 7 ] Во время этого процесса CD4 + Помощные Т -клетки «Лицензия» Дендритные клетки дают мощный активирующий сигнал на наивный CD8 + Т -клетки. [ 10 ] Это лицензирование антиген-презентативных клеток CD4 + Т-хелперные клетки проходят путем передачи сигналов между CD154/CD40L на клетках T Helper и рецептором CD40 на антиген-презентативной клетке во время образования иммунологического синапса. [ 11 ]
Хотя в большинстве случаев активация зависит от распознавания антигена TCR, были описаны альтернативные пути активации. Например, было показано, что цитотоксические Т -клетки активируются, когда нацелены на другие CD8 T -клетки, ведущие к толеризации последних. [ 12 ]
После активации клетка T C подвергается клональной экспансии с помощью цитокинового интерлейкина 2 (IL-2), что является фактором роста и дифференцировки для Т-клеток. Это увеличивает количество клеток, специфичных для целевого антигена, которые затем могут проходить по всему телу в поисках антиген-позитивных соматических клеток .
Эффекторные функции
[ редактировать ]При воздействии инфицированных/дисфункциональных соматических клеток TC клеток выделяют цитотоксины перфорина , гранзимы и гранулизин . Благодаря действию перфорина гранзимы попадают в цитоплазму клетки -мишени, а их функция сериновой протеазы запускает каскад каспазы , который представляет собой серию цистеиновых протеаз, которые в конечном итоге приводят к апоптозу (запрограммированная гибель клеток). Это называется «смертельным ударом» и позволяет наблюдать за волноподобной смертью клеток-мишеней. [ 13 ] Из -за высокого порядка липидов и негативно заряженного фосфатидилсерина, присутствующего в их плазматической мембране, клетки T C устойчивы к эффектам их перфорина и гранзимных цитотоксинов. [ 14 ]
Второй способ вызвать апоптоз-это взаимодействие клеточной поверхности между T C и инфицированной клеткой. Когда T C активируется, он начинает экспрессировать поверхностный белок Fas лиганд (FASL) (APO1L) (CD95L), который может связываться с молекулами Fas (APO1) (CD95), экспрессируемыми на клетке -мишени. Тем не менее, это взаимодействие Fas-Fas-лиганда, как полагают, является более важным для утилизации нежелательных Т-лимфоцитов во время их развития или для литической активности определенных ТН - клеток, чем для цитолитической активности T C. эффекторных клеток Взаимодействие с FAS с FASL позволяет привлечь к набору сигнального комплекса, вызванного смертью (DISC). [ 15 ] ФАС-ассоциированный домен смерти (FADD) транслоцируется с диском, что позволяет набирать прокаспаз 8 и 10. [ 15 ] Затем эти каспазы активируют эффекторные каспазы 3, 6 и 7, что приводит к расщеплению субстратов смерти, таких как ламина А , Ламин В1, Ламин В2, ПАРП ( поли-полимераза Рибозы АДП ) и ДНК-ПКС (ДНК-активированная протеинкиназа)) Полем Окончательным результатом является апоптоз клетки, которая экспрессировала Fas. CD8 Т -клетки также могут демонстрировать активацию, вызванную гибелью клеток или AICD, которая опосредована комплексом рецептора CD3. Недавно было показано, что белок TLT-1, выпущенный тромбоцитами. [ 16 ]
транскрипции играет ключевую роль в CD8 эомезодермин Предполагается, что + Функция Т -клеток, действующая как регуляторный ген в адаптивном иммунном ответе. [ 17 ] Исследования, исследующие эффект эомезодермина потери функции, показали, что снижение экспрессии этого фактора транскрипции привело к снижению количества перфорина, полученного CD8 + Т -клетки. [ 17 ]
Роль в патогенезе заболевания
[ редактировать ]В отличие от антител , которые эффективны как против вирусных , так и бактериальных инфекций, цитотоксические Т -клетки в основном эффективны против вирусов. [ 18 ]
Во время инфекции вируса гепатита В (HBV) цитотоксические Т -клетки убивают инфицированные клетки и продуцируют противовирусные цитокины, способные очищать HBV из жизнеспособных гепатоцитов. Они также играют важную патогенную роль, способствуя практически всем повреждениям печени, связанной с инфекцией HBV. [ 19 ] Было показано, что тромбоциты облегчают накопление вирус-специфических цитотоксических Т-клеток в инфицированную печень. [ 20 ] В некоторых исследованиях с мышами инъекция с CXCR5+ CD8+ T -клетками демонстрирует значительное снижение HBSAG . Кроме того, повышение уровней CXCL13 способствовало рекрутированию внутрипеченочных CXCR5+CD8+T-клеток, и эти типы клеток продуцировали высокие уровни HBV-специфического интерферона (IFN) -γ и IL-21 , которые могут помочь улучшить контроль Хроническая инфекция HBV. [ 21 ]
Цитотоксические Т -клетки участвуют в прогрессировании артрита . Основным участием ревматоидного артрита является его участие сустава. Синовиальная мембрана характеризуется гиперплазией , повышенной васкулярией и проникновением воспалительных клеток; В основном CD4+ T-лимфоциты, которые являются основными организаторами клеточных иммунных ответов. В различных исследованиях ревматоидный артрит тесно связан с основными антигенами класса II класса II. Единственными клетками в организме, которые экспрессируют антигены MHC класса II, являются конститутивными антиген-презентативными клетками . Это убедительно говорит о том, что ревматоидный артрит вызван неопознанными артритогенными антигенами. Антиген может быть любым экзогенным антигеном, таким как вирусные белки или эндогенный белок. [ 22 ] В последнее время был идентифицирован ряд возможных эндогенных антигенов, например, гликопротеин 39 хряща человека, белок, связывающий тяжелую цепь и цитруллизированный белок. Активированные CD4+ T-лимфоциты стимулируют моноциты, макрофаги и синовиальные фибробласты, чтобы разработать цитокины интерлейкин-1 , интерлейкин-6 и фактор некроза опухоли Alpha (TNFA), а также секретные металлопротеиназы. Первые три из которых являются ключевыми в управлении воспалением при ревматоидном артрите. Эти активированные лимфоциты также стимулируют B -клетки с образованием иммуноглобулинов, включая ревматоидный фактор. [ 23 ] Их патогенная роль неизвестна, но может быть связана с активацией комплемента посредством образования иммунного комплекса. Более того, несколько исследований на животных предполагают, что цитотоксические Т -клетки могут иметь преимущественно провоспалительный эффект при заболевании. Также изучается, что производство цитокинов клетками CD8+ может ускорить прогрессирование болезни артрита. [ 24 ]
CD8 + Было обнаружено, что Т -клетки играют роль в ВИЧ -инфекции. ВИЧ со временем разработал много стратегий, чтобы уклониться от иммунной системы клеток -хозяев. Например, ВИЧ принял очень высокие показатели мутаций, чтобы позволить им избежать распознавания CD8 + Т -клетки. [ 25 ] Они также способны подавить экспрессию поверхностных белков MHC класса I клеток, которые они заражают, чтобы дополнительно уклониться от разрушения CD8 + Т -клетки. [ 25 ] Если CD8 + Т -клетки не могут найти, распознавать и связываться с инфицированными клетками, вирус не будет разрушен и будет продолжать расти.
Кроме того, CD8 + Т -клетки могут участвовать в диабете 1 типа . [ 26 ] Исследования на модели с диабетом показали, что клетки CD4+ ответственны за массивную инфильтрацию мононуклеарных лейкоцитов в островки поджелудочной железы . Тем не менее, было показано, что клетки CD8+ играют эффекторную роль, ответственную за окончательное разрушение бета -клеток островков. Однако в исследованиях с NOD-мышами, несущими нулевую мутацию в локусе бета-2 микроглобулина (B2M) и, таким образом, отсутствует основной гистосовместимости комплексных молекул класса I и CD8+ T-клеток, было обнаружено, что у них не развился диабет. [ 27 ]
CD8 + Т-клетки могут быть необходимы для разрешения индуцированной химиотерапией периферической невропатии (CIPN). [ 28 ] [ 29 ] Мыши без CD8 + Т -клетки показывают длительный CIPN по сравнению с нормальными мышами и инъекцией образованного CD8 + Т -клетки разрешают или предотвращают CIPN.
Цитотоксические Т-лимфоциты были вовлечены в развитие различных заболеваний и расстройств, например, в отторжении трансплантации (цитотоксические Т-лимфоциты атакуют новый орган после обнаружения его как иностранного, из-за изменения HLA между донором и получателем); [ 30 ] При чрезмерной продукции цитокинов при тяжелой инфекции SARS-COV-2 (из-за преувеличенного ответа лимфоцитов генерируется большое количество провоспалительных цитокинов , повреждающих субъект); [ 31 ] [ 32 ] Воспалительные и дегенеративные заболевания центральной нервной системы, такие как рассеянный склероз (Т -клетки становятся сенсибилизированными к определенным белкам, таким как миелин , атакуют здоровые клетки и рекрутирующие больше иммунных клеток, усугубляя заболевание). [ 33 ]
Смотрите также
[ редактировать ]- CTL-опосредованная цитотоксичность
- CD4 + Т -клетки
- Список отдельных типов клеток в теле человека человека
Ссылки
[ редактировать ]- ^ Аль-Шура и (2020). «Лимфоциты». Расширенная гематология в интегрированной сердечно -сосудистой китайской медицине . Elsevier. С. 41–46. doi : 10.1016/b978-0-12-817572-9.00007-0 . ISBN 978-0-12-817572-9 Полем S2CID 241913878 .
Helper T -клетки/CD4+ • Экспрессируют гликопротеины CD4 на их клеточной поверхности, которые активируются в присутствии пептидных антигенов на поверхности вторгающихся патогенов; • Ответьте немедленно, чтобы защитить иммунную систему; • Отделите различные цитокиновые белки в соответствии с иммунным ответом.
- ^ Вентури С., Вентури М (сентябрь 2009 г.). «Йод, тимус и иммунитет». Питание . 25 (9): 977–979. doi : 10.1016/j.nut.2009.06.002 . PMID 19647627 .
- ^ Кабелиц Д., Уэш Д. (2003). «Особенности и функции гамма -дельта -лимфоцитов: сосредоточиться на хемокинах и их рецепторах». Критические обзоры иммунологии . 23 (5–6): 339–370. doi : 10.1615/critrevimmunol.v23.i56.10 . PMID 15030305 .
- ^ Deseke M, Prinz I (сентябрь 2020 г.). «Распознавание лиганда γδ TCR и различение гомеостаза и условий стресса» . Клеточная и молекулярная иммунология . 17 (9): 914–924. doi : 10.1038/s41423-020-0503-y . PMC 7608190 . PMID 32709926 .
- ^ Tuenengel J, Ranchal S, Maslova A, Aulakh G, Papadopolou M, Drissler S, et al. (Октябрь 2021 г.). «Харарактивный адаптивно-подобный γδ T-клетки у угандийских младенцев во время первичной цитомегаловирусной инфекции » Вирусы 13 (10): 1987. DOI : 10.3390/v13101987 . PMC 8537190 PMID 34696417
- ^ Rojas-espinosa O (2017). Иммунология (по памяти) (четвертое издание изд.). Мехико: пан -американец. ISBN 978-968-7988-28-3 Полем OCLC 1022564980 .
- ^ Jump up to: а беременный Hoyer S, Prommersberger S, Pfeiffer IA, Schuler-Thurner B, Schuler G, Dörrie J, Schaft N (декабрь 2014 г.). «Одновременное взаимодействие DCs с CD4 (+) и CD8 (+) Т -клетками улучшает вторичное расширение CTL: для этого требуется три танго» . Европейский журнал иммунологии . 44 (12): 3543–3559. doi : 10.1002/eji.201444477 . PMID 25211552 . S2CID 5655814 .
- ^ Я Аббас, Лихтман А.Х., Пиллай С. (2018). Клеточная и молекулярная иммунология (девятое изд.). Филадельфия, Пенсильвания. ISBN 978-0-323-52323-3 Полем OCLC 973917896 .
{{cite book}}: CS1 Maint: местоположение отсутствует издатель ( ссылка ) - ^ Hivroz C, Chemin K, Tourret M, Bohineust A (2012). «Перекрестка между Т -лимфоцитами и дендритными клетками». Критические обзоры иммунологии . 32 (2): 139–155. doi : 10.1615/critrevimmunol.v32.i2.30 . PMID 23216612 .
- ^ Lanzavecchia A (июнь 1998 г.). «Иммунология. Лицензия на убийство» . Природа . 393 (6684): 413–414. Bibcode : 1998natur.393..413L . doi : 10.1038/30845 . PMID 9623994 .
- ^ Беннетт С.Р., Карбон Ф.Р., Карамалис Ф., Флавелл Р.А., Миллер Дж. Ф., Хит В.Р. (июнь 1998 г.). «Помощь для цитотоксических реакций T-клеток опосредуется передачей сигналов CD40». Природа . 393 (6684): 478–480. Bibcode : 1998natur.393..478b . doi : 10.1038/30996 . PMID 9624004 . S2CID 4325396 .
- ^ Милштейн О., Хагин Д., Ласк А., Рейх-Зелигер С., Шезен Е., Офир Е. и др. (Январь 2011). «CTL реагируют с активацией и секрецией гранул при служении в качестве целей для распознавания Т-клеток» . Кровь . 117 (3): 1042–1052. doi : 10.1182/blood-2010-05-283770 . PMC 3035066 . PMID 21045195 .
- ^ Чанг Х.Ф., Бзеи Х., Читирала П., Равичандран К., Слейман М., Краузе Е. и др. (Февраль 2017 г.). «Подготовка смертельного удара: взаимодействие между экзо- и эндоцитарными путями в цитотоксических Т-лимфоцитах» . Клеточные и молекулярные науки о жизни . 74 (3): 399–408. doi : 10.1007/s00018-016-2350-7 . PMC 5241346 . PMID 27585956 .
- ^ Rudd-Schmidt JA, Hodel AW, Noori T, Lopez JA, Cho HJ, Verschoor S, et al. (Ноябрь 2019). «Порядок липидов и заряда защищают убийственные Т -клетки от случайной смерти» . Природная связь . 10 (1): 5396. Bibcode : 2019natco..10.5396r . doi : 10.1038/s41467-019-13385-x . PMC 6881447 . PMID 31776337 .
- ^ Jump up to: а беременный Bakshi RK, Cox MA, Zajac AJ (2014). «Цитотоксические Т -лимфоциты». Энциклопедия медицинской иммунологии . С. 332–342. doi : 10.1007/978-0-387-84828-0_36 . ISBN 978-0-387-84827-3 .
- ^ Тяги, Тарун; и др. (2023). «TLT-1, полученный из тромбоцитов, способствует прогрессированию опухоли путем подавления CD8+ T-клеток» . Журнал экспериментальной медицины . 220 (1). doi : 10.1084/jem.20212218 . PMC 9814191 . PMID 36305874 .
- ^ Jump up to: а беременный Pearce El, Mullen AC, Martins GA, Krawczyk CM, Hutchins AS, Zediak VP, et al. (Ноябрь 2003). «Контроль эффекторной функции CD8+ T -клеток с помощью эомезодермина транскрипции». Наука . 302 (5647): 1041–1043. Bibcode : 2003sci ... 302.1041p . doi : 10.1126/science.1090148 . PMID 14605368 . S2CID 43479181 .
- ^ Kemball CC, Alirezaei M, Whitton JL (сентябрь 2010 г.). «Тип B Coxsackieviruses и их взаимодействие с врожденной и адаптивной иммунной системой» . Будущая микробиология . 5 (9): 1329–1347. doi : 10.2217/fmb.10.101 . PMC 3045535 . PMID 20860480 .
- ^ Iannacone M, Sitia G, Guidotti LG (2006). «Патогенетические и противовирусные иммунные реакции против вируса гепатита В». Будущая вирусология . 1 (2): 189–96. doi : 10.2217/17460794.1.2.189 .
- ^ Iannacone M, Sitia G, Isogawa M, Marchese P, Castro MG, Lowenstein PR, et al. (Ноябрь 2005 г.). «Тромбоциты опосредуют цитотоксическое Т-лимфоцитовое повреждение печени» . Природная медицина . 11 (11): 1167–1169. doi : 10.1038/nm1317 . PMC 2908083 . PMID 16258538 .
- ^ Li Y, Tang L, Guo L, Chen C, Gu S, Zhou Y, et al. (Март 2020 г.). "CXCL13-опосредованный набор интрапеченочных CXCR5 + CD8 + Т -клетки благоприятствуют вирусному контролю при хронической инфекции HBV » . Журнал гепатологии . 72 (3): 420–430. : 10.1016 /j.jhep.2019.09.031 . PMID 31610223. S2CID DOI 204702318 .
- ^ Чанг М.Х., Нигрович Па (март 2019 г.). «Антитело -зависимые и -независимые механизмы воспалительного артрита» . JCI Insight . 4 (5): E125278. doi : 10.1172/jci.insight.125278 . PMC 6483516 . PMID 30843881 . S2CID 73512236 .
- ^ Cope AP, Schulze-Koops H, Aringer M (сентябрь 2007 г.). «Центральная роль Т -клеток при ревматоидном артрите» . Клиническая и экспериментальная ревматология . 25 (5 Suppl 46): S4-11. PMID 17977483 .
- ^ Carvalheiro H, Da Silva JA, Souto-Carneiro MM (январь 2013 г.). «Потенциальная роль для CD8 (+) Т -клеток при ревматоидном артрите». Обзоры аутоиммунитета . 12 (3): 401–409. Doi : 10.1016/j.autrev.2012.07.011 . PMID 22841983 .
- ^ Jump up to: а беременный Гульзар Н., Коупленд К.Ф. (январь 2004 г.). «CD8+ T-клетки: функция и реакция на ВИЧ-инфекцию». Текущее исследование по ВИЧ . 2 (1): 23–37. doi : 10.2174/1570162043485077 . PMID 15053338 .
- ^ Цай С., Шамели А., Сантамария П. (2008). «Глава 4 CD8+ T -клетки при диабете 1 типа». Иммунопатогенез сахарного диабета 1 типа . Достижения в области иммунологии. Тол. 100. С. 79–124. doi : 10.1016/s0065-2776 (08) 00804-3 . ISBN 9780123743268 Полем PMID 19111164 .
- ^ Ван Б., Гонсалес А., Бенуист С., Матис Д. (август 1996 г.). «Роль CD8+ Т-клеток в инициации инсулинозависимого сахарного диабета». Европейский журнал иммунологии . 26 (8): 1762–1769. doi : 10.1002/eji.1830260815 . PMID 8765018 . S2CID 26229701 .
- ^ Laumet G, Edralin JD, Dantzer R, Heijnen CJ, Kavelaars A (июнь 2019 г.). «Цисплатин обучает CD8+ T-клетки для предотвращения и разрешения периферической невропатии, вызванной химиотерапией, у мышей» . Боль . 160 (6): 1459–1468. doi : 10.1097/j.pain.0000000000001512 . PMC 6527475 . PMID 30720585 .
- ^ Krukowski K, Eijkelkamp N, Laumet G, Hack CE, Li Y, Dougherty PM, et al. (Октябрь 2016). «CD8+ T-клетки и эндогенные IL-10 необходимы для разрешения химиотерапии, вызванной невропатической болей» . Журнал нейробиологии . 36 (43): 11074–11083. doi : 10.1523/jneurosci.3708-15.2016 . PMC 5098842 . PMID 27798187 .
- ^ Wiebe C, Nickerson PW (февраль 2020 г.). «Молекулярное несоответствие антигена лейкоцитов человека для риска стратификации получателей трансплантации почки». Текущее мнение о трансплантации органов . 25 (1): 8–14. doi : 10.1097/mot.0000000000000714 . PMID 31789952 . S2CID 208537995 .
- ^ Channappanavar R, Perlman S (июль 2017 г.). «Патогенные инфекции коронавируса человека: причины и последствия цитокинового шторма и иммунопатологии» . Семинары в иммунопатологии . 39 (5): 529–539. doi : 10.1007/s00281-017-0629-x . PMC 7079893 . PMID 28466096 .
- ^ Sarzi-Puttini P, Giorgi V, Sirotti S, Marotto D, Ardizzone S, Rizzardini G, et al. (Март 2020 г.). «Covid-19, цитокины и иммуносупрессия: чему мы можем научиться из тяжелого острого респираторного синдрома?» Полем Клиническая и экспериментальная ревматология . 38 (2): 337–342. doi : 10.55563/clinexprheumatol/xcdary . PMID 32202240 . S2CID 214609305 .
- ^ Neumann H, Medana IM, Bauer J, Lassmann H (июнь 2002 г.). «Цитотоксические Т -лимфоциты при аутоиммунных и дегенеративных заболеваниях ЦНС». Тенденции в нейронауках . 25 (6): 313–319. doi : 10.1016/s0166-2236 (02) 02154-9 . PMID 12086750 . S2CID 12593103 .
Внешние ссылки
[ редактировать ] СМИ, связанные с цитотоксическими Т -клетками в Wikimedia Commons
СМИ, связанные с цитотоксическими Т -клетками в Wikimedia Commons - T-Cell Group-Университет Кардиффа