Ацетоацетил-КоА
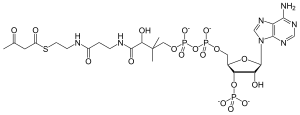
| |
| Имена | |
|---|---|
| Имя IUPAC
3'- O -фосфоноаденозин 5 '-[(3 R ) -3-гидрокси-2,2-диметил-4-оксо-4-{[3-оксо-3-({2-[(3-оксобутаноил) сульфанил ] этил} амино) пропил] амино} бутило дигидроген дифхосфат]
| |
| Систематическое имя IUPAC
А 1 -{[(2 r , 3 с , 4 r , 5 r ) -5- (6-амино-9 H -purin-9-ил) -4-гидрокси-3- (фосфоноооооооооооооооооооооооооооооооаааааааааааааааааааааааааа } O 3 -[(3 R ) -3-гидрокси-2,2-диметил-4-оксо-4-{[3-оксо-3-({2-[(3-оксобутаноил) сульфанил] этил} амино) пропил] амино } butyl] дигидроген дифхосфат | |
| Идентификаторы | |
3D model ( JSmol )
|
|
| Чеби | |
| Chemspider | |
| Echa Infocard | 100.014.378 |
| Сетка | ацетоацетил+коа |
PubChem CID
|
|
Comptox Dashboard ( EPA )
|
|
| Характеристики | |
| C 25 H 40 N 7 O 18 P 3 S | |
| Молярная масса | 851.61 g·mol −1 |
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |
Ацетоацетиловый COA является предшественником HMG-COA на пути мевалоната , что необходимо для биосинтеза холестерина . Он также принимает аналогичную роль в пути синтеза кетоновых тел ( кетогенез ) печени . [ 1 ] В пути пищеварения кетоновых тел (в ткани) он больше не связан с наличием HMG-COA в качестве продукта или в качестве реагента.
Он создан из ацетил-КоА , тиоэфира, который реагирует с энота второй молекулы ацетил-КоА в реакции конденсации клайазена , [ 2 ] и он действует HMG-COA-синтазой с образованием HMG-COA . [ 1 ] Во время метаболизма лейцина эта последняя реакция перевернута. Некоторые люди могут испытывать дефицит ацетоацетил-КоА. [ 3 ] Этот дефицит классифицируется как кетоновое тело расстройства и метаболизм изолейцина, который может быть унаследован. [ Цитация необходима ] Дополнительные мутации включают мутации с ферментами в пути, связанных с ацетоацетиловым COA, включая дефицит бета-кетотиолазы и митохондриальную 3-гидрокси-3-метилглютарил-коа-синтазу.

Кроме того, он реагирует с NADPH-зависимым ацетоацетил-коферментом areductase, также известной как PHAB, в пути, который продуцирует полиэфир полигидроксиалканоат (PHA). Снижение ацетоацетил-КоА с помощью PHA создает (r) -3-гидроксибутирил-CoA, который полимеризуется для PHA. [ 4 ] Путь присутствует у бактерий, таких как Ralstonia eutropha и штамм PCC6803 Synechocystis . [ 5 ] Средство, ацетоацетил-КоА связана с развитием нейронов, включающим липогенез и обеспечение жиров и холестерина для нейрональных клеток.
Мутации
[ редактировать ]Митохондриальная ацетоацетил-коа-тиолаза , также известная как тиолаза II, фермент, ответственный за катализирование синтеза ацетоацетил-КоА в кетогенезе, как упомянуто, также участвует в расщеплении ацетоацетил-КоА в кетолизе. Наблюдается, что он играет роль в расщеплении ацетил-КоА от ацетоацетил-КоА и 2-метилацетоацетил-КоА. Фермент участвует в аутосомно-рецессивных расстройствах, которые влияют на катаболизм кетоновых тел и изолецина: дефицит бета-кетотиолазы , что приводит к их дефициту в митохондриях. Мутация происходит в гене ацетоацетил-КоА тиолазы (ACAT), отображаемого на хромосоме 11q22.3-23.1. [ 6 ]
Мутации в митохондриальной 3-гидрокси-3-метилглютарил-CoA-синтазе (HMG-CoA-синтаза) является еще одним унаследованным аутосомно-рецессивным расстройством, влияющим на катаболизм кетоновых тел и может привести к наращиванию ацетоацетил-COA. [ 7 ]
Дополнительное приложение
[ редактировать ]Ацетоацетил-КоА также ведет себя как продукт ацетоацетил-КоА-синтетазы (AAC) в цитозоле, используя ацетоацетат в качестве субстрата, реакция обеспечивает ацетильные группы для липогенеза . [ 8 ] Понимание ацетоацетил-КоА важно для развития холестерина и липогенеза, а ацетоацетил-коа-синтетазы играет роль в его развитии, оно также играет значительную роль в мозге. Холестерин и жиры наблюдались в высоких концентрациях в нейрональной ткани , а также высокие уровни экспрессии мРНК AACS в клетках гиппокампа и кортикальной области. Кроме того, они играют значительную роль в развитии нейронов на ранних стадиях эмбриона и развития плода. [ 9 ]
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Jump up to: а беременный Хасегава, Шинья; Нода, Казуки; Маэда, Акина; Мацуока, Масару; Ямасаки, Масахиро; Fukui, Tetsuya (2012-11-01). «Ацетоацетил-коа-синтетаза, фермент, использующий телес, контролируется кетоновым ферментом, контролируется SREBP-2 и влияет на уровень холестерина в сыворотке» . Молекулярная генетика и метаболизм . 107 (3): 553–560. doi : 10.1016/j.ymgme.2012.08.017 . ISSN 1096-7192 . PMID 22985732 .
- ^ Брюс П.Ю. (2017). Органическая химия . Пирсон. ISBN 978-0-13-404228-2 Полем OCLC 974910578 .
- ^ Цуда Х, Шираки М., Иноуэ Э, Сайто Т (август 2016 г.). «Генерация поли-β-гидроксибутирата из ацетата в более высоких растениях: обнаружение активности ацетоацетила-редуктазы-синтазы-синтазы в рисе». Журнал физиологии растений . 201 : 9–16. Bibcode : 2016jpphy.201 .... 9t . doi : 10.1016/j.jplph.2016.06.007 . PMID 27372278 .
- ^ Matsumoto K, Tanaka Y, Watanabe T, Motohashi R, Ikeda K, Tobitani K, et al. (Октябрь 2013). «Переданная эволюция и структурный анализ NADPH-зависимой ацетоацетиловой кофермента A (ацетоацетил-КоА) редуктазы из ралстонии эвтрофа выявляет две мутации, ответственные за усиленную кинетику» . Прикладная и экологическая микробиология . 79 (19): 6134–6139. Bibcode : 2013Apenm..79.6134M . doi : 10.1128/aem.01768-13 . PMC 3811355 . PMID 23913421 .
- ^ Taroncher Oldenburg G, Nishina K, Stephanopoulos G (октябрь 2000 г.). «Идентификация и анализ полигидроксиалканоат-специфического бета-кетотиолазы и ацетоацетила коэнзимента A-редуктазы в цианобактерии Synechocystis sp. Штамм PCC6803» . Прикладная и экологическая микробиология . 66 (10): 4440–4448. Bibcode : 2000apenm..66.4440t . doi : 10.1128/aem.66.10.4440-4448.2000 . PMC 92322 . PMID 11010896 .
- ^ Биссоннетт, Бруно; Luginbuehl, Igor; Marciniak, Bruno; Dalens, Bernard J. (2006), «Дефицит митохондриальной ацетоацетил-коа-тиолазы (ACAT)» , Синдромы: быстрое распознавание и периоперационные последствия , Нью-Йорк, Нью-Йорк: компании McGraw-Hill , извлечены 2022-12-08
- ^ Альдо, Роза; Zschocke, Johannes; Пи, Хуан; Мир, Сесилия; Физель, Соня; Mayatepek, Ertan; Хоффманн, Георг Ф.; Казальс, Нурия; Hegardt, Fausto G. (2001-07-01). «Генетическая основа митохондриальной дефицита HMG-CoAсинтазы» . Человеческая генетика . 109 (1): 19–23. Doi : 10.1007/s004390100554 . ISSN 1432-1203 . PMID 11479731 . S2CID 24115345 .
- ^ Хасегава, Шинья; Икеда, Йотаро; Ямасаки, Масахиро; Fukui, Tetsuya (2012). «Роль ацетоацетил-КоА-синтетазы, фермента, использующего кетон, в дифференцировке адипоцитов 3T3-L1» . Биологический и фармацевтический бюллетень . 35 (11): 1980–1985. doi : 10.1248/bpb.b12-00435 . ISSN 1347-5215 . PMID 23123469 .
- ^ Хасегава, Шинья; Кум, Хироки; Я пью это, Саюри; Ямаси, Масахиро; Такахаши, Норико; Fukui, Tetsuya (2012-10-19). «Ацетоацетил-КоА-синтетаза необходима для нормального развития нейронов » Биохимическая и биофизическая исследовательская коммуникация 427 (2): 398–4 Doi : 10.1016/ j.bbrc.2012.09.0 ISSN 0006-291X PMID 2300407