Мышьякорганическая химия
Мышьякорганическая химия — химия соединений , содержащих химическую связь между мышьяком и углеродом . Некоторые мышьякорганические соединения, также называемые «мышьяковоорганическими соединениями», производятся в промышленности и используются в качестве инсектицидов , гербицидов и фунгицидов . В целом количество таких применений сокращается по мере растущей обеспокоенности по поводу их воздействия на окружающую среду и здоровье человека. Исходными соединениями являются арсан и мышьяковая кислота . Несмотря на свою токсичность, мышьякорганические биомолекулы хорошо известны.
История
[ редактировать ]
Мышьякорганическая химия сыграла заметную роль в истории химии, что удивительно для области, которая сейчас считается второстепенной. Самое старое известное мышьяковистое соединение, дурно пахнущий какодил, было описано в «Какодиле» (1760 г.) и иногда классифицируется как первое синтетическое металлоорганическое соединение . Соединение Сальварсан было одним из первых фармацевтических препаратов, получивших Нобелевскую премию Пауля Эрлиха . Различные другие мышьякорганические соединения ранее находили применение в качестве антибиотиков (Соларсон) или в других медицинских целях. [2]
Синтез и классификация
[ редактировать ]Мышьяк обычно встречается в степенях окисления (III) и (V), иллюстрируемых галогенидами AsX 3 ( X = F, Cl, Br, I) и AsF 5 . Соответственно, мышьякорганические соединения обычно находятся в этих двух степенях окисления. [3]
Соединения гидроксимышьяка известны: [3]
- мышьяковистые кислоты (RAs(OH) 2 ), редкие ( мышьяковистая кислота (As(OH) 3 ) хорошо известна)
- мышьяковистые кислоты (R 2 AsOH), редкие
- мышьяковые кислоты (R 2 As(O)OH), распространенные, например, какодиловая кислота (R = CH 3 )
- мышьяковые кислоты (RAs(O)(OH) 2 ), распространенные, на примере фениларсоновой кислоты (R = C 6 H 5 )
Мышьякорганические соединения и их применение
[ редактировать ]Соединения мышьяка(V) обычно содержат функциональные группы RAsO(OH) 2 или R 2 AsO(OH) (R = алкил или арил). Какодиловая кислота, занимающая центральное место в химии мышьяка, возникает в результате метилирования оксида мышьяка (III). (Напротив, диметилфосфоновая кислота играет меньшую роль в соответствующей химии фосфора.) Фениларсоновые кислоты можно получить в результате реакции мышьяковой кислоты с анилином , так называемой реакции Бешана .
Монометилированная кислота, метанарсоновая кислота (CH 3 AsO(OH) 2 ), является предшественником фунгицидов (торговое название Неоазозин) при выращивании риса и хлопка. производные фениларсоновой кислоты (C 6 H 5 AsO(OH) 2 В качестве кормовых добавок для скота применяют ), в том числе 4-гидрокси-3-нитробензоленарсоновую кислоту (3-NHPAA или роксарсон), уреидофениларсоновую кислоту и п -арсаниловую кислоту . Эти применения являются спорными, поскольку они приводят к попаданию растворимых форм мышьяка в окружающую среду.
Соединения мышьяка(V), содержащие только органические лиганды, редки, наиболее выдающимся представителем является производное пентафенила As(C 6 H 5 ) 5 . [4]
Мышьякорганические соединения и их применение
[ редактировать ]Многие мышьякорганические соединения получают алкилированием AsCl 3 и его производных с использованием литийорганических соединений и реактивов Гриньяра . [4] Например, ряд триметиларсин ((CH 3 ) 3 As), хлорид диметилмышьяка ((CH 3 ) 2 AsCl) и дихлорид метиларсена (CH 3 AsCl 2 известен ). Восстановление хлоридных производных реагентами, восстанавливающими гидриды, дает соответствующие гидриды, такие как диметиларсин ((CH 3 ) 2 AsH) и метиларсин (CH 3 AsH 2 ). Аналогичные манипуляции применимы и к другим хлорорганическим соединениям мышьяка.
Подобно прямому процессу в кремнийорганической химии , метилгалогениды реагируют с элементарным As, как показано в следующем идеализированном уравнении: [5]
- 3 CH 3 Br + 2 As → (CH 3 ) 2 AsBr + CH 3 AsBr 2
Такие реакции требуют медных катализаторов и проводятся при температуре около 360 °С.
Другой путь к соединениям диметилмышьяка начинается с восстановления As. V соединение какодиловой кислоты :
- (CH 3 ) 2 AsO 2 H + 2 Zn + 4 HCl → (CH 3 ) 2 AsH + 2 ZnCl 2 + 2 H 2 O
- (CH 3 ) 2 AsO 2 H + SO 2 + HI → (CH 3 ) 2 AsI + SO 3 + H 2 O
Известны разнообразные гетероциклы, содержащие мышьяк(III). К ним относятся арсол , мышьяковый аналог пиррола , и арсабензол , мышьяковый аналог пиридина .
Симметричные мышьякорганические соединения(III), например триметиларсин и трифениларсин , обычно используются в качестве лигандов в координационной химии . Они ведут себя как фосфиновые лиганды, но менее основные. Диарсин C 6 H 4 (As(CH 3 ) 2 ) 2 , известный как диарс , представляет собой хелатирующий лиганд . Торин является индикатором нескольких металлов.
Мышьякорганические соединения низшего порядка и их применение
[ редактировать ]Согласно правилу двойной связи , соединения со связями As=As, As=C и As≡C встречаются редко. Они наблюдаются в газовой фазе, но необходима значительная стерическая защита, чтобы ингибировать их превращение в олигомеры в жидком или твердом виде.
К олигомерам со связями As-As относятся противосифилические препараты Сальварсан и Неосальварсан . [ нужна ссылка ] Обычно они трехкоординатны в As и имеют формальную степень окисления As. я . Маленькие заместители, такие как (MeAs) n , уравновешивают трех-, четырех- и пятичленные кольца, но более объемные заместители обычно располагаются в четырехчленной конфигурации. Синтез обычно осуществляется путем восстановительного дегалогенирования с металлом. [6] : 563–565
Реакции
[ редактировать ]Протонные арсины окисляются до олигомеров. [6] : 318 Например, метиларсин сначала окисляется до циклометиларсина (I):
- MeAsH 2 + O → H 2 O + (MeAs) n
Эти соединения имеют структуру, подобную сульфидам фосфора .
Связи мышьяк-мышьяк очень слабы, и олигомерные соединения мышьяка даже более склонны к окислению, чем их гидрированные предшественники. [6] : 318–320 Однако следующую реакцию можно провести электрохимическим восстановлением в ячейке с сульфатом цинка . [6] : 473 При окислении сначала образуются полимерные арсиноксиды, например:
- MeAs + O → MeAsO
Дальнейшее окисление затем деполимеризует их до мышьяковистых кислот. [6] : 318
Соединения арсина (III) присоединяются к кратным связям как нуклеофилы , но кольца арсина (I) вместо этого могут вставлять связь в кольцо. [6] : 319, 573, 843 В целом арсины менее бренстедовские, чем фосфины (но более стибины ). [6] : 322–326
Арсин -илиды обычно менее стабильны, чем фосфин-илиды , и самопроизвольно разлагаются в отсутствие вицинального карбонила. Стабилизированные илиды олефинируются до смеси стереоизомеров, тогда как нестабилизированные илиды имеют тенденцию к эпоксидированию (как реагент Кори-Чайковского ). С енонами они либо олефинируются, либо циклопропанируются. С нитрозосоединениями они образуют имины или нитроны . [6] : 662–672
Химическая война
[ редактировать ]Мышьякоорганические соединения, особенно содержащие связи As-Cl, использовались в качестве химического оружия , особенно во время Первой мировой войны . Печально известные примеры включают « люизит » (хлорвинил-2-мышьяк дихлорид) и «Кларк I» ( хлордифениларсин ). Фенилдихлорарсин – еще один.
На природе
[ редактировать ]Поскольку мышьяк токсичен для большинства форм жизни и в некоторых районах он встречается в повышенных концентрациях, было разработано несколько стратегий детоксикации. Неорганический мышьяк и его соединения, попадая в пищевую цепь , постепенно метаболизируются в менее токсичную форму мышьяка посредством процесса метилирования . [7] Мышьякорганические соединения возникают в результате биометилирования неорганических соединений мышьяка. [8] посредством процессов, опосредованных ферментами, связанными с витамином B 12 . [9] Например, плесень Scopulariopsis brevicaulis производит значительные количества триметиларсина, если присутствует неорганический мышьяк. [10] Биометилирование соединений мышьяка начинается с образования метанарсонатов . Таким образом, трехвалентные неорганические соединения мышьяка метилируются с образованием метанарсоната. S- аденозилметионин является донором метила. Метанарсонаты являются предшественниками диметиларсонатов, опять же в результате цикла восстановления (до метиларсоновой кислоты) с последующим вторым метилированием. [11] Это диметиловое соединение представляет собой какодиловую кислоту ((CH 3 ) 2 AsO 2 H),
Органическое соединение арсенобетаин ) (бетаин содержится в некоторых морских продуктах, таких как рыба и водоросли, а также в грибах в больших концентрациях. Потребление среднестатистического человека составляет около 10-50 мкг/день. Значения около 1000 мкг не являются чем-то необычным после употребления рыбы или грибов. Но есть небольшая опасность в употреблении в пищу рыбы, поскольку это соединение мышьяка практически нетоксично. [12] Арсенобетаин был впервые обнаружен у западного каменного лобстера. [13] [14]
Сахариды, связанные с мышьяком, известные под общим названием арсеносахара , особенно обнаружены в морских водорослях . мышьяксодержащие липиды . Известны также [15] Хотя мышьяк и его соединения токсичны для человека, одним из первых синтетических антибиотиков был Сальварсан , применение которого давно прекращено.
Единственное полимышьяковое соединение, выделенное из природного источника, — это арсеницин А , обнаруженный в Новой Каледонии морской губке Echinochalina bargibanti . [16]
Мышьякорганические соединения могут представлять значительную опасность для здоровья в зависимости от их вида. Мышьяковистая кислота (As(OH) 3 ) имеет ЛД50 34,5 мг/кг (мыши), тогда как бетаин (CH 3 ) 3 As + СН 2 СО 2 − ЛД50 превышает 10 г/кг. [12]
Типичные соединения
[ редактировать ]Некоторые иллюстративные мышьякорганические соединения перечислены в таблице ниже:
| Имя | Заместители | Структура | Молярная масса | Номер CAS | Характеристики |
|---|---|---|---|---|---|
| 10,10'-оксибис-10 H -феноксарсин | Эрил |  | 502.2318 | 58-36-6 | |
| Трифениларсин | Фенил |  | 306.23 | 603-32-7 | Плавится 58-61 °С. |
| Фенилдихлорарсин | Фенил , хлор | 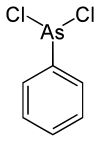 | 222.93 | 696-28-6 | |
| Роксарсон | Фенил , кислород | 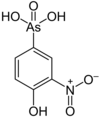 | 263.04 | 121-19-7 | |
| Арсенобетаин | Метил | 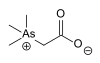 | 64436-13-1 | ||
| Арсеницин А | Метил , кислород | ![2,4,6-Триокса-1,3,5,7-тетраарсатрицикло[3.3.1.13,7]декан](http://upload.wikimedia.org/wikipedia/commons/thumb/4/42/Arsenicin_A.png/100px-Arsenicin_A.png) | 389.76 | 925705-41-5 | Плавится 182–184 ° C (360–363 ° F). |
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Сейферт, Дитмар (2001). «Кадетская дымящая мышьяковая жидкость и какодильные соединения Бунзена» . Металлоорганические соединения . 20 (8): 1488–1498. дои : 10.1021/om0101947 .
- ^ Сингх, Р. Синтетические наркотики. Публикации Миттала (2002). ISBN 817099831X
- ^ Jump up to: а б Грунд, Южная Каролина; Хануш, К.; Вольф, Х.У. «Мышьяк и соединения мышьяка». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a03_113.pub2 . ISBN 978-3527306732 .
- ^ Jump up to: а б Эльшенбройх, К. «Металлоорганические соединения» (2006) Wiley-VCH: Weinheim. ISBN 978-3-527-29390-2
- ^ Майер, Л.; Рохов, Э.Г.; Фернелиус, WC (1961). «Прямой синтез мышьякорганических и сурьмяорганических соединений». Журнал неорганической и ядерной химии . 16 (3–4): 213–218. дои : 10.1016/0022-1902(61)80492-2 .
- ^ Jump up to: а б с д и ж г час Патай, Саул , изд. (1994). Химия органических соединений мышьяка, сурьмы и висмута . Химия функциональных групп. Чичестер, Великобритания: Wiley. дои : 10.1002/0470023473 . ISBN 047193044X .
- ^ Реймер, К.Дж.; Кох, И.; Каллен, WR (2010). «Мышьякорганические соединения. Распространение и трансформация в окружающей среде». Ионы металлов в науках о жизни . 7 . Кембридж: Издательство RSC: 165–229. дои : 10.1039/9781849730822-00165 . ISBN 978-1-84755-177-1 . ПМИД 20877808 .
- ^ Допп, Э.; Клигерман, А.Д.; Диас-Боун, РА (2010). «Мышьякорганические соединения. Поглощение, метаболизм и токсичность». Ионы металлов в науках о жизни . 7 . Кембридж: Издательство RSC: 231–265. дои : 10.1515/9783110436600-012 . ISBN 978-1-84755-177-1 . ПМИД 20877809 .
- ^ Тошиказу Кайсе; Мицуо Огура; Такао Нодзаки; Казухиса Сайто; Теруаки Сакураи; Чиё Мацубара; Чуичи Ватанабэ; Кеничи Ханаока (1998). «Биометилирование мышьяка в пресноводной среде, богатой мышьяком» . Прикладная металлоорганическая химия . 11 (4): 297–304. doi : 10.1002/(SICI)1099-0739(199704)11:4<297::AID-AOC584>3.0.CO;2-0 .
- ^ Бентли, Рональд; Честин, Томас Г. (2002). «Микробное метилирование металлоидов: мышьяк, сурьма и висмут» . Обзоры микробиологии и молекулярной биологии . 66 (2): 250–271. дои : 10.1128/MMBR.66.2.250-271.2002 . ПМК 120786 . ПМИД 12040126 .
- ^ Стибло, М.; Дель Разо, LM; Вега, Л.; Гермолец, ДР; ЛеКлюиз, Эль; Гамильтон, Джорджия; Рид, В.; Ван, К.; Каллен, WR; Томас, диджей (2000). «Сравнительная токсичность трехвалентных и пятивалентных неорганических и метилированных мышьяков в клетках крысы и человека». Архив токсикологии . 74 (6): 289–299. дои : 10.1007/s002040000134 . ПМИД 11005674 . S2CID 1025140 .
- ^ Jump up to: а б Каллен, Уильям Р.; Реймер, Кеннет Дж. (1989). «Видообразование мышьяка в окружающей среде». Химические обзоры . 89 (4): 713–764. дои : 10.1021/cr00094a002 . hdl : 10214/2162 .
- ^ Франческони, Кевин А.; Эдмондс, Джон С. (1998). «Виды мышьяка в морских пробах» (PDF) . Хорватия Химика Акта . 71 (2): 343–359. Архивировано из оригинала (PDF) 9 марта 2008 г.
- ^ Джон С. Эдмондс; Кевин А. Франческони; Джек Р. Кэннон; Колин Л. Растон ; Брайан В. Скелтон и Аллан Х. Уайт (1977). «Выделение, кристаллическая структура и синтез арсенобетаина, мышьяковистого компонента западного лангуста panulirus longipes cygnus George». Буквы тетраэдра . 18 (18): 1543–1546. дои : 10.1016/S0040-4039(01)93098-9 .
- ^ Элис Румплер; Джон С. Эдмондс; Марико Катсу; Кеннет Б. Дженсен; Уолтер Гесслер; Георг Рабер; Хельга Гуннлаугсдоттир; Кевин А. Франческони (2008). «Мышьяксодержащие длинноцепочечные жирные кислоты в рыбьем жире: результат биосинтетической неверности?». Энджью. хим. Межд. Эд . 47 (14): 2665–2667. дои : 10.1002/anie.200705405 . ПМИД 18306198 .
- ^ Jump up to: а б Манчини, Инес; Гуэлла, Грациано; Фростин, Мэривонн; Уайт, Эдуард; Лоран, Доминик; Дебит, Сесиль; Пьетра, Франческо (2006). «О первом полимышьяковом органическом соединении в природе: мышьяк а из новокаледонской морской губки Echinochalina bargibanti» Химия: Европейский журнал . 12 (35): 8989–94. дои : 10.1002/chem.200600783 . ПМИД 17039560 .
- ^ "Дом" . sigmaaldrich.com .