Ацеталь

При органической химии ацеталь - это функциональная группа с связностью R 2 C (или ') 2 . Здесь R -группы могут быть органическими фрагментами ( атом углерода , с произвольными другими атомами, прикрепленными к этому) или водородом , в то время как R 'группы должны быть органическими фрагментами, а не водородом. Две группы R могут быть эквивалентны друг другу («симметричный ацеталь») или нет («смешанный ацеталь»). Ацеталы образуются и кабриочны к альдегидам или кетонам и имеют одинаковое состояние окисления в центральном углероде, но имеют существенно различную химическую стабильность и реакционную способность по сравнению с аналогичными карбонильными соединениями. Центральный атом углерода имеет четыре связи, и поэтому он насыщен и имеет тетраэдрическую геометрию .
Термин ктал иногда используется для идентификации структур, связанных с кетонами (обе группы органических фрагментов, а не водорода), а не альдегиды , и, исторически, термин ацетал использовался специально для случаев, связанных с альдегидом (имея хотя бы один водород на месте на месте r на центральном углероде). [ 1 ] IUPAC первоначально установил использование слова Ketal в целом, но с тех пор изменил свое решение. Однако, в отличие от исторического использования, кеталы в настоящее время являются подмножеством ацеталов, термин, который теперь охватывает как альдегидные, так и кетоновые структуры.
Если одна из групп R имеет кислород в качестве первого атома (то есть, существует более двух оксигенов с одним связью с центральным углеродом), функциональная группа вместо этого является ортоэфиром . В отличие от вариаций R, обе группы R 'являются органическими фрагментами. Если один r 'является водородом, функциональная группа вместо этого является гемиааковой , а если оба H - H, функциональная группа - это гидрат кетона или гидрат альдегида.
Образование ацетала возникает, когда гидроксильная группа гемиацетала становится протонированной и теряется как вода. Полученная карбокация . быстро атаковается молекулой спирта затем Потеря протона из прикрепленного алкоголя дает ацетал.
Ацеталы стабильны по сравнению с гемиаатическими такими, но их образование представляет собой обратимое равновесие , как и с эфирами . В качестве реакции для создания ацетальных доходов необходимо удалить воду из реакционной смеси, например, с аппаратом для декана -Stard , чтобы он не гидролизировал продукт обратно в гемиацеталь. Образование ацеталов уменьшает общее количество присутствующих молекул (карбонил + 2 спирта → ацетальная вода) и, следовательно, обычно не является благоприятным для энтропии . одна молекула диола Одна ситуация, когда она не является энтропически неблагоприятной, - это когда используется , а не две отдельные молекулы спирта (карбонил + диол → ацетальная + вода).
Ацетализация и кетализация
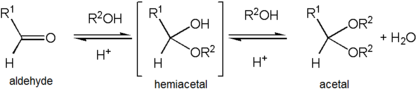
[ редактировать ]Ацетализация и кетализация являются органическими реакциями , которые включают образование ацетальных (или кеталов) из альдегидов и кетонов, соответственно. Эти конверсии кислоты катализированы . Они устраняют воду. Поскольку каждый шаг часто является быстрым равновесием, реакция должна быть обусловлена удалением воды. Методы удаления воды включают азеотропную дистилляцию и захватывающую воду с помощью высыхающих, таких как оксид алюминия и молекулярные сита . Предполагается, что шаги представлены: протонирование карбонильного кислорода, добавление алкоголя в протонированный карбонил, протонолиз полученного гемиацетали или полукетала и добавление второго алкоголя. Эти шаги проиллюстрированы альдегидом RCH = O и алкоголем R'OH:
- Rch = o + h + ⇌ rch = OH +
- Rch = о + + R'oh ⇌ rch (OH) (или ') + h +
- Rch (OH) (или ') + h + ⇌ RC + H (или ') + h 2 o
- Дольдо + H (или ') + r'oh ⇌ rch (или') 2 + h +
Другим способом избежать энтропийных затрат является выполнение синтеза с помощью ацетального обмена, используя ранее существовавший реагент ацетального типа в качестве донора или донора или простого добавления самих спиртов. Одним из типов реагента, используемого для этого метода, является ортоэфир. В этом случае вода, произведенная вместе с ацетальным продуктом, разрушается, когда она гидролизует остаточные молекулы ортоэфира, и эта боковая реакция также приводит к большему количеству спирта для использования в основной реакции.
Примеры
[ редактировать ]Сахар
[ редактировать ]Поскольку многие сахара являются полигидрокси альдегидами и кетонами, сахары являются богатым источником ацеталов и кеталов. Большинство гликозидных связей в углеводах и других полисахаридах являются ацетальными связями. [ 2 ] Целлюлоза является повсеместным примером полиацеталии.
Бензилиденцетальный и ацетонид в качестве защиты групп, используемых при исследованиях модифицированных сахаров.
Хиральные производные
[ редактировать ]Ацеталы также находят применение как хиральные вспомогательные. Действительно, ацеталы хиральных гликолей, например, производные татарной кислоты, можно асимметрично открыть с высокой селективностью. Это позволяет строить новые хиральные центры. [ 3 ]

Формальдегид и ацетальдегид
[ редактировать ]Формальдегид образует богатую коллекцию ацеталов. Эта тенденция отражает тот факт, что альдегиды с низкой молекулярной массой склонны к самоконденсации, так что связь C = O заменяется ацеталем. Ацеталь, образованный из формальдегида (два гидрогина, прикрепленные к центральному углероду) иногда называют формальным [ 4 ] или группа метилендиокси . Ацеталь, образованный из ацетона , иногда называют ацетонидом . Формальдегид формирует паральдегид и 1,3,5-триоксан . Полиоксиметилен (POM), также известный как «ацетальный» или «полиацетальный», представляет собой полиацетальный (и полиэфир) и полимер формальдегида . Ацетальдегид обращается в метальдегид .
Необычные ацеталы
[ редактировать ]Фенилсульфонилэтилиден (PSE) ацеталь является примером арилсульфонил -ацетала, обладающего нетипичными свойствами, такими как устойчивость к кислотному гидролизу, что приводит к селективному введению и удалению защитной группы. [ 5 ]
Ароматы и ароматы
[ редактировать ]1,1-диэтоксиэтан (ацетальдегид-диэтилацетал), иногда называемый просто «ацетальным», является важным ароматизающим соединением в дистиллированных напитках . [ 6 ] Два кетала этилацетоацетата используются в коммерческих ароматах. [ 7 ] Фруктон ( CH 3 C (O 2 C 2 H 4 ) CH 2 CO 2 C 2 H 5 ), Кетал этиленгликоля и фрайстон ( CH 3 C (O 2 C 2 H 3 CH 3 ) CH 2 CO 2 C 2 H 5 ), пропиленгликол кетал, коммерческие ароматы.
Связанные соединения
[ редактировать ]Используемый в более общем смысле, термин X , Y - ацетал также относится к любой функциональной группе, которая состоит из углерода, несущих два X и Y. гетероатома Например, n , o -Acetal относится к соединениям типа R 1 Ведущий 2 C (OR) (NR ' 2 ) (R, R' ↓ H) также известен как гемиминальный эфир или аминал , он же аминоцетальный.
S , S -Acetal относится к соединениям типа R 1 Ведущий 2 C (SR) (SR ') (R, R' ♠ H, также известный как тиоацетальные и тиокеталы .
Смотрите также
[ редактировать ]Ссылки
[ редактировать ]- ^ Iupac , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) " Кеталс ". doi : 10.1351/goldbook.k03376
- ^ Iupac , сборник химической терминологии , 2 -е изд. («Золотая книга») (1997). Онлайн -исправленная версия: (2006–) « гликозиды ». doi : 10.1351/goldbook.g02661
- ^ PJ Kocieński: защита групп , S. 164–167.
- ^ Моррисон, Роберт Т. и Бойд, Роберт Н., «Органическая химия (6 -е изд)». P683. Prentice-Hall Inc (1992).
- ^ Чери, Флоренция; Роллин, Патрик; Де Лукчи, Отторино; Cossu, Sergio (2000). «Фенилсульфониллетилиденовые (PSE) ацеталы как атепичные группы, защищающие углеводы». Тетраэдр буквы . 41 (14): 2357–2360. doi : 10.1016/s0040-4039 (00) 00199-4 . ISSN 0040-4039 .
- ^ Maarse, Henk (1991-03-29). Летучие соединения в продуктах и напитках . CRC Press. ISBN 978-0-8247-8390-7 .
- ^ Пентен, Йоханнес; Сурбург, Хорст (2016). «Ароматы и ароматы, 3. ароматические и гетероциклические соединения». Энциклопедия промышленной химии Уллмана . С. 1–45. doi : 10.1002/14356007.t11_t02 . ISBN 978-3-527-30673-2 .