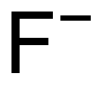Фторид
| |||
| Имена | |||
|---|---|---|---|
| Имя IUPAC
Фторид [ 1 ]
| |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| Чеби | |||
| Химический | |||
| Chemspider | |||
| 14905 | |||
| Кегг | |||
| Сетка | Фторид | ||
PubChem CID
|
|||
| НЕКОТОРЫЙ | |||
| Характеристики | |||
| Фон − | |||
| Молярная масса | 18.998 403 163 g·mol −1 | ||
| Сопряженная кислота | Фторид водорода | ||
| Термохимия | |||
Std Molar
энтропия ( с ⦵ 298 ) |
145,58 J/моль K (газообразной) [ 2 ] | ||
Энтальпия STD
образование (Δ f h ⦵ 298 ) |
-333 кДж раз −1 | ||
| Связанные соединения | |||
Другие анионы
|
|||
За исключением случаев, когда отмечены, данные приведены для материалов в их стандартном состоянии (при 25 ° C [77 ° F], 100 кПа).
| |||
Фторид ( / ˈ f l ʊər aɪ d , ˈ f l ɔːr - / ) [ 3 ] это неорганический монатомный анион , фтора формулой с химической F −
(Также написано [F] −
), чьи соли обычно белые или бесцветные. Фторидные соли обычно имеют отличительные горькие вкусы и не имеют запаха. Его соли и минералы являются важными химическими реагентами и промышленными химическими веществами, которые в основном используются при производстве фторида водорода для фтор -красот . Фторид классифицируется как слабое основание, поскольку он только частично ассоциируется в растворе, но концентрированный фторид является коррозийным и может атаковать кожу.
Фторид является самым простым анионом фтора . С точки зрения заряда и размера, ион фтора напоминает гидроксид -ион. Ионы фторида встречаются на Земле в нескольких минералах, в частности фторита , но присутствуют только в следовых количествах в телах воды в природе.
Номенклатура
[ редактировать ]Фтоориды включают соединения, которые содержат ионный фторид, и те, в которых фторид не диссоциации. Номенклатура не отличает эти ситуации. Например, гексафторид серы и тетрафлюорид углерода не являются источниками ионов фторида в обычных условиях.
Систематическое фторид имени , допустимое имя IUPAC , определяется в соответствии с аддитивной номенклатурой. названия Тем не менее, фторид также используется в номенклатуре композиции IUPAC, которая не учитывает характер связи вовлеченной во внимание. Фторид также используется несистематически для описания соединений, которые высвобождают фторид при растворении. Фторид водорода сам по себе является примером несистематического имени такой природы. Тем не менее, это также тривиальное имя , и предпочтительное название iupac для флуорана . [ Цитация необходима ]
Возникновение
[ редактировать ]
фтор Предполагается, что является 13-м самым распространенным элементом в коре Земли и широко рассеян по своей природе, полностью в виде фторидов. Подавляющее большинство удерживается в месторождениях минералов , наиболее коммерчески важной из которых является флуорит (CAF 2 ). [ 4 ] Естественное выветривание каких -либо камней, [ 5 ] [ 6 ] Помимо человеческой активности, выпускает фториды в биосферу через то, что иногда называют фториновым циклом .
В воде
[ редактировать ]Фторид естественным образом присутствует в подземных водах, источниках свежих и соленой воды , а также в дождевой воде, особенно в городских районах. [ 7 ] Уровни фторида морской воды обычно находятся в диапазоне от 0,86 до 1,4 мг/л, а в среднем 1,1 мг/л [ 8 ] (миллиграммы на литр ). Для сравнения, концентрация хлорида в морской воде составляет около 19 г/л. Низкая концентрация фтора отражает нерастворимость щелочных фторидов Земли , например, CAF 2 .
Концентрации в пресной воде различаются более значительно. Поверхностные воды , такие как реки или озера, обычно содержит от 0,01 до 0,3 мг/л. [ 9 ] Концентрации подземных вод (Well Water) варьируются еще больше, в зависимости от присутствия локальных фторсодержащих минералов. Например, естественные уровни менее 0,05 мг/л были обнаружены в некоторых частях Канады, но до 8 мг/л в некоторых частях Китая; в общем уровне редко превышают 10 мг/литр [ 10 ]
- В некоторых частях Азии подземные воды могут содержать опасно высокий уровень фтора, что приводит к серьезным проблемам со здоровьем . [ 11 ]
- Во всем мире 50 миллионов человек получают воду из водоснабжения, которые, естественно, имеют близкие к «оптимальному уровню». [ 12 ]
- В других местах уровень фтора очень низкий, иногда приводит к фторированию общественных водоснабжений, чтобы довести уровень до 0,7–1,2 м.д..
- Горнодобывающая промышленность может повысить локальный уровень фторида [ 13 ]
Фторид может присутствовать под дождем, причем его концентрация значительно увеличивается при воздействии вулканической активности [ 14 ] или атмосферное загрязнение, полученное в результате сжигания ископаемого топлива или других видов промышленности, [ 15 ] [ 16 ] Особенно алюминиевые плавки . [ 17 ]
В растениях
[ редактировать ]Вся растительность содержит фторид, который поглощается из почвы и воды. [ 10 ] Некоторые растения концентрируют фторид в своей среде больше, чем другие. Все чайные листья содержат фторид; Тем не менее, зрелые листья содержат до 10-20 раз превышают уровень фтора молодых листьев с того же растения. [ 18 ] [ 19 ] [ 20 ]
Химические свойства
[ редактировать ]Основность
[ редактировать ]Фторид может действовать как основание . Он может сочетаться с протоном ( ч + ):
| Фон − + H + → HF | ( 1 ) |
Эта реакция нейтрализации образует фторид водорода (HF), конъюгатную кислоту фтора.
В водном растворе фторид имеет значение P k b 10,8. Поэтому это слабая основа , и, как правило, остается ион фторида, а не генерирует значительное количество фторида водорода. То есть следующее равновесие способствует левой стороне в воде:
| Фон − + H 2 o HF + H. − | ( 2 ) |
Однако при длительном контакте с влажностью растворимые соли фтора будут разлагаться до их соответствующих гидроксидов или оксидов, когда фторид водорода сбегает. Фторид отличается в этом отношении среди галогенидов. Идентичность растворителя может оказать резкое влияние на равновесие, смещающее его в правую сторону, значительно увеличивая скорость разложения.
Структура фторидных солей
[ редактировать ]Соли, содержащие фторид, являются многочисленными и принимают множество структур. Обычно фторидный анион окружен четырьмя или шестью катионами, как это типично для других галогенидов. Фторид натрия и хлорид натрия применяют ту же структуру. Для соединений, содержащих более одного фтора на катион, структуры часто отклоняются от структур хлоридов, как показано основным фторидом минерального флюорита (CAF 2 ), где CA 2+ ионы окружены восемью f − центры. В Cacl 2 , каждый Ca 2+ Ион окружен шестью Cl − центры. Дифлюориды переходных металлов часто принимают структуру рутила , тогда как дихлориды имеют хлорида кадмия структуры .
Неорганическая химия
[ редактировать ]После обработки стандартной кислотой соли фтора преобразуются в фторид водорода и соли металлов . С сильными кислотами его можно вдвойне протонировать, чтобы дать H
2 ф +
Полем Окисление фторида дает фтор. Растворы неорганических фторидов в воде содержат f − и бифлюорид HF −
2 . [ 21 ] Немногие неорганические фториды растворим в воде без значительного гидролиза. С точки зрения его реакционной способности фторид значительно отличается от хлорида и других галогенидов и более сильно растворится в протетических растворителях из -за его меньшего соотношения радиуса/заряда. Его ближайший химический родственник - гидроксид , поскольку оба имеют сходную геометрию.
Голый фторид
[ редактировать ]Большинство фторидных солей растворяются, чтобы дать бифлуорид ( HF −
2 ) Анион. Источники истинного − Анионы редки, потому что очень основные фторидные анионы тезисы от многих, даже случайных источников. Относительный неразрушенный фторид, который существует в апротонных растворителях, называется «голым». Голый фторид - сильная база Льюиса , [ 22 ] и мощный нуклеофил. Некоторые четвертичные соли аммония обнаженного фторида включают тетраметиламмоний и фторид тетрабутиламмония . [ 23 ] Кобальтоцениальный фторид является еще одним примером. [ 24 ] Тем не менее, у всех них не хватает структурной характеристики в апротонных растворителях. Из-за их высокой основности многие так называемые обнаженные фторидные источники на самом деле являются солями бифлюоридов. В конце 2016 года был синтезирован фторид имидазолия , который является ближайшим приближением термодинамически стабильного и структурно охарактеризованного примера «обнаженного» источника фторида в Approtice Prostict (ацетонитрил). [ 25 ] Стерически требовательный имидазолийский катион стабилизирует дискретные анионы и защищает их от полимеризации. [ 26 ] [ 27 ]
Биохимия
[ редактировать ]При физиологических pH фторид водорода обычно полностью ионизируется на фторид. В биохимии фторид фторида и водорода эквивалентны. Фтор, в форме фтора, считается микроэлементом для здоровья человека, необходимым для предотвращения зубных полостей и для содействия здоровому росту костей. [ 28 ] Чайное растение ( Camellia sinensis L.) является известным аккумулятором фториновых соединений, высвобождаемых при формировании инфузий, таких как общий напиток. Фториновые соединения разлагаются на продукты, включая ионы фторида. Фторид является наиболее биодоступной формой фтора, и, как таковой, чай является потенциально средством для дозирования фтора. [ 29 ] Приблизительно, 50% поглощенного фтора выделяется почечным путем с двадцатью часовым периодом. Остальная часть может быть сохранена в полости рта, а нижний пищеварительный тракт. Пост резко увеличивает скорость поглощения фтора до 100%, с 60% до 80% при получении пищи. [ 29 ] Согласно исследованию 2013 года, было обнаружено, что потребление одного литра чая в день может поставлять ежедневное рекомендуемое потребление 4 мг в день. Некоторые бренды более низкого качества могут поставлять до 120% от этой суммы. Пост может увеличить это до 150%. Исследование показывает, что сообщества по употреблению чая подвергаются повышенному риску зубного и скелетного флуороза , в тех случаях, когда действует фторирование воды. [ 29 ] Ион фторида в низких дозах во рту уменьшает распад зубов. [ 30 ] По этой причине он используется в зубной пасте и фторировании воды. При гораздо более высоких дозах и частых воздействиях фторид вызывает осложнения в отношении здоровья и может быть токсичным.
Приложения
[ редактировать ]Фторидные соли и гидрофторическая кислота являются основными фторидами промышленной ценности.
Органофлюориновая химия
[ редактировать ]Органофлюорийные соединения распространены. Многие лекарства, многие полимеры, хладагенты и многие неорганические соединения изготовлены из фторидсодержащих реагентов. Часто фториды превращаются в фторид водорода, который является основным реагентом и предшественником реагентов. Гидрофлуорическая кислота и ее безводная форма, фторид водорода , особенно важны. [ 4 ]
Производство металлов и их соединений
[ редактировать ]Основное использование фторида, с точки зрения объема, заключается в производстве криолит, Na 3 Alf 6 . Он используется в плавке из алюминия . Раньше он был добыт, но теперь он получен из фторида водорода. Флуорит используется в больших масштабах, чтобы отделить шлак в стали. Mineed Fluorite (CAF 2 )-это товарное химическое вещество, используемое в стали. Урановый гексафторид используется для очистки изотопов урана.
Профилактика полости
[ редактировать ]
Флуоридсодержащие соединения, такие как фторид натрия или монофторфосфат натрия, используются в местной и системной терапии фторидом для предотвращения распада зубов . Они используются для фторирования воды и во многих продуктах, связанных с гигиеной полости рта . [ 31 ] Первоначально фторид натрия использовался для фторидации воды; Гексафторосиликовая кислота (H 2 SIF 6 ) и ее соляная натрия гексафторосиликат (NA 2 SIF 6 ) являются чаще используемыми добавками, особенно в Соединенных Штатах. Известно, что фторирование воды предотвращает распад зубов [ 32 ] [ 33 ] и рассматривается Центрами США по контролю и профилактике заболеваний как «одним из 10 великих достижений общественного здравоохранения 20 -го века». [ 34 ] [ 35 ] В некоторых странах, где крупные централизованные системы водоснабжения редки, фторид доставляется в популяцию фторирующей столовой солью. Метод действия по профилактике полости см. В фторидной терапии . Фторирование воды имеет свои критики . [ 36 ] Фторидированная зубная паста в общем использовании. Метаанализ показывает эффективность фторида 500 ч / млн в зубных пастах. [ 37 ] [ 38 ] Тем не менее, никакого полезного эффекта не может быть обнаружено, когда для ежедневного ухода за полостью рта используется более одного источника фтора. [ 39 ] [ необходима цитата для проверки ]
Лабораторный реагент
[ редактировать ]Соли фтора обычно используются в биологической обработке анализа, чтобы ингибировать активность фосфатаз , таких как серин / треонинфосфатазы . [ 40 ] Фторид имитирует нуклеофильный гидроксид -ион в активных участках этих ферментов. [ 41 ] фторид и алюминиевый фторид В качестве ингибиторов фосфатазы также используются , поскольку эти соединения являются структурными имитирами фосфатной группы и могут действовать как аналоги переходного состояния реакции. [ 42 ] [ 43 ]
Диетические рекомендации
[ редактировать ]Институт медицины США (МОМ) обновил расчетные средние требования (уши) и рекомендованные диетические пособия (RDA) для некоторых минералов в 1997 году. Там, где не было достаточного количества информации для установления ушей и RDA, была использована оценка адекватного потребления (ИИ). вместо. ИИ, как правило, соответствуют фактическому среднему потреблению, с предположением, что, по -видимому, существует, и эта потребность удовлетворяется тем, что люди потребляют. Нынешний ИИ для женщин 19 лет и старше составляет 3,0 мг/день (включая беременность и лактацию). ИИ для мужчин составляет 4,0 мг/день. ИИ для детей в возрасте от 1 до 18 лет увеличивается с 0,7 до 3,0 мг/день. Основным известным риском дефицита фторида , по-видимому, является повышенный риск, связанные с бактериями зубных полостей. Что касается безопасности, МОМ устанавливает терпимые уровни верхнего потребления (ULS) для витаминов и минералов, когда доказательства достаточны. В случае фторида UL составляет 10 мг/день. В совокупности уши, RDA, AIS и ULS называются диетическими эталонными потребностями (DRIS). [ 44 ]
Европейское управление по безопасности пищевых продуктов (EFSA) относится к коллективному набору информации как диетических справочных значений, при этом потребление ссылки на население (PRI) вместо RDA и средним требованием вместо уха. ИИ и UL определяются так же, как в Соединенных Штатах. Для женщин в возрасте 18 лет и старше ИИ установлен на уровне 2,9 мг/день (включая беременность и лактацию). Для мужчин значение составляет 3,4 мг/день. Для детей в возрасте 1–17 лет AIS увеличивается с возрастом с 0,6 до 3,2 мг/день. Эти ИИ сравнимы с ИИ США. [ 45 ] EFSA рассмотрела доказательства безопасности и установила взрослый UL на 7,0 мг/день (ниже для детей). [ 46 ]
Для нас целей маркировки пищевых добавок для пищевых продуктов и пищевых добавок количество витамина или минерала в порции выражается в процентах от суточной стоимости (%DV). Хотя есть информация для установления адекватного потребления, фторид не имеет ежедневного значения и не требуется показать на метках питания. [ 47 ]
Расчетное ежедневное потребление
[ редактировать ]Ежедневное потребление фтора может значительно варьироваться в зависимости от различных источников воздействия. Значения в диапазоне от 0,46 до 3,6–5,4 мг/день были зарегистрированы в нескольких исследованиях (IPCS, 1984). [ 28 ] В районах, где вода фторирована, это можно ожидать, что это будет значительным источником фторида, однако фторид также естественным образом присутствует практически во всех продуктах и напитках в широком диапазоне концентраций. [ 48 ] Максимальное безопасное ежедневное потребление фтора составляет 10 мг/день для взрослого (США) или 7 мг/день (Европейский союз). [ 44 ] [ 46 ]
Верхний предел потребления фторида из всех источников (фторированная вода, пищевые продукты, напитки, зубные продукты фторида и пищевые фторидные добавки) устанавливается на уровне 0,10 мг/кг/день для детей, малышей и детей до 8 лет. Для детей старшего возраста и взрослых, которые больше не подвергаются риску флюороза зубов, верхний предел фторида устанавливается на уровне 10 мг/день независимо от веса. [ 49 ]
| Еда/напиток | Фторид (мг на 1000 г/ч/млн) |
Часть | Фторид (мг за часть) |
|---|---|---|---|
| Черный чай (варево) | 3.73 | 1 стакана, 240 г (8 Fl Oz) | 0.884 |
| Изюм, без семян | 2.34 | Маленькая коробка, 43 г (1,5 унции) | 0.101 |
| Столовое вино | 1.53 | Бутылка, 750 мл (26 Imp wr Oz) | 1.150 |
| Муниципальная водопроводная вода, (Фторировано) |
0.81 | Рекомендуется ежедневное потребление, 3 литра (0,79 американская девушка) |
2.433 |
| Запеченный картофель, рассеянный | 0.45 | Средний картофель, 140 г (0,31 фунт) | 0.078 |
| Ягненок | 0.32 | Чоп, 170 г (6,0 унции) | 0.054 |
| Морковь | 0.03 | 1 большая морковь, 72 г (2,5 унции) | 0.002 |
| Источник: Данные, полученные из Министерства сельского хозяйства США, Национальная база данных питательных веществ, архив 2014-03-01 на машине Wayback [ 50 ] | |||
Безопасность
[ редактировать ]Проглатывание
[ редактировать ]По данным Министерства сельского хозяйства США, диетические эталонные потребления, который является «самым высоким уровнем ежедневного потребления питательных веществ, которые, вероятно, не представляют риска неблагоприятных воздействий на здоровье», указывают 10 мг/день для большинства людей, что соответствует 10 л фторируемых вода без риска. Для маленьких детей значения меньше, в диапазоне от 0,7 мг/сут до 2,2 мг/сут для младенцев. [ 51 ] Вода и пищевые источники фторида включают в себя фторирование воды, морепродукты, чай и желатин. [ 52 ]
Растворимые фторидные соли, из которых фторид натрия является наиболее распространенными, являются токсичными и привели к случайным и нанесенным на себя смерти от острого отравления . [ 4 ] Смертельная доза для большинства взрослых людей оценивается в 5-10 г (что эквивалентно от 32 до 64 мг элементарного фторида на кг массы тела). [ 53 ] [ 54 ] [ 55 ] Случай фатального отравления взрослого с 4 граммами фторида натрия задокументирован, [ 56 ] и доза 120 г фтора натрия была выжита. [ 57 ] Для флуоросиликата натрия (NA 2 SIF 6 ) средняя летальная доза (LD 50 ) перорально у крыс составляет 125 мг/кг, что соответствует 12,5 г для взрослого 100 кг. [ 58 ]
Обработка может включать пероральное введение гидроксида кальция или хлорида кальция для предотвращения дальнейшего поглощения и инъекции глюконата кальция для повышения уровня кальция в крови. [ 56 ] Фторид водорода более опасен, чем соли, такие как NAF, потому что он является коррозийным и летучим, и может привести к смертельному воздействию за счет ингаляции или при контакте с кожей; Глюконатный гель кальция является обычным противоядием. [ 59 ]
В более высоких дозах, используемых для лечения остеопороза , фторид натрия может вызывать боль в ногах и неполные стрессовые переломы, когда дозы слишком высоки; Это также раздражает желудок, иногда настолько сильно, что вызывает язвы. Версии фторида натрия с медленным высвобождением и кишечника не имеют побочных эффектов желудка каким -либо значительным образом и имеют более мягкие и менее частые осложнения в костях. [ 60 ] В более низких дозах, используемых для фторирования воды , единственным ясным побочным эффектом является зубной флюороз , который может изменить появление зубов детей во время развития зубов ; Это в основном мягкое и вряд ли будет представлять какое -либо реальное влияние на эстетический вид или на общественное здравоохранение. [ 61 ] Известно, что фторид усиливает минеральную плотность кости в поясничном отделе позвоночника, но он не был эффективен для переломов позвонков и вызвал больше переломов без страданий. [ 62 ] В районах, которые имеют природный высокий уровень фтора в подземных водах , которые используются для питьевой воды , как зубной , так и скелетный флюороз может быть распространенным и тяжелым. [ 63 ]
В 2024 году в Соединенных Штатах в Соединенных Штатах, проведенных на 300 страницах Национальных институтов здоровья, связал скупкурную воду в Соединенных Штатах, в областях, где уровни немного более чем в два раза превышают рекомендуемый лимит, с снижением IQ у развития детей. [ 64 ] [ 65 ] [ 66 ] [ 67 ]
Карты опасности для фтора в подземных водах
[ редактировать ]Около одной трети населения пьет воду из ресурсов подземных вод. Из этого около 10%, приблизительно 300 миллионов человек, получают воду из ресурсов подземных вод, которые сильно загрязнены мышьяком или фторидом. [ 68 ] Эти следовые элементы происходят в основном из минералов. [ 69 ] Карты, расположенные потенциальные проблемные скважины. [ 70 ]
Актуально
[ редактировать ]Концентрированные фторидные растворы являются коррозионными. [ 71 ] Перчатки, изготовленные из нитрильного резины , носят при обработке фторидных соединений. Опасности растворов растворов фторидных солей зависят от концентрации. В присутствии сильных кислот соли фтора выделяют фторид водорода , который является коррозийным, особенно в направлении стекла. [ 4 ]
Другие производные
[ редактировать ]Органические и неорганические анионы производятся из фторида, в том числе:
- Бифлуорид , используемый в качестве травления для стекла [ 72 ]
- Тетрафлюоробериллат
- Гексафтороплатинат
- Тетрафлюороборат, используемый при организме на организм.
- Гексафторофосфат используется в качестве электролита в коммерческих вторичных батареях.
- Трифторметанесульфонат
Смотрите также
[ редактировать ]- PER- и POLEFLUOROALKYL вещества
- Фтор-ядерная магнитно-резонансная спектроскопия
- Дефицит фтора
- Селективный электрод фторида
- Фторидная терапия
- Натрий монофтоорофосфат
Ссылки
[ редактировать ]- ^ «Фтоориды - Pubchem Public Chemical Database» . Проект PUBCHEM . США: Национальный центр биотехнологической информации. Идентификация.
- ^ Чейз, MW (1998). «Фториновый анион» . Нист. С. 1–1951 . Получено 4 июля 2012 года .
- ^ Уэллс, JC (2008). Лонгман Словарь произношения (3 -е изд.). Харлоу, Англия: Pearson Education Limited/Longman. п. 313. ISBN 9781405881180 Полем Полем Согласно этому источнику, / ˈ f l uː ə r aɪ d / является возможным произношением в британском английском.
- ^ Jump up to: а беременный в дюймовый Aigueperse, Джин; Моллард, Пол; Devilliers, Didier; Химла, Мариус; Фарон, Роберт; Романо, Рене; Cuer, Жан Пьер (2000). «Фториновые соединения, неорганические». Энциклопедия промышленной химии Уллмана . Doi : 10.1002/14356007.a11_307 . ISBN 978-3527306732 .
- ^ Деракшани, R; Raoof, a; Махви, ах; Chathrouz, H (2020). «Сходство отпечатков пальцев добычи угля, высокого фторида грунтовых вод и флуороза зубов в районе Заранд, провинция Керман, Иран». Фторид . 53 (2): 257–267.
- ^ Derakhhani, R; Tavallaie, M; Малек Мухаммед, т; Аббаснеджад, а; Haghdoost, A (2014). «Основное фторид в подземных водах региона Заранда, провинция Керман, Иран» фториде 47 (2): 133–1
- ^ «Заявление общественного здравоохранения для фторидов, фторида водорода и фтора» . Atsdr . Сентябрь 2003 г.
- ^ «Критерии качества окружающей среды для фторида» . Правительство Британской Колумбии. Архивировано с оригинала 24 сентября 2015 года . Получено 8 октября 2014 года .
- ^ Liteplo, Dr R.; Gomes, R.; Хоу, П.; Малкольм, Хит (2002). Фториды - Критерии здоровья окружающей среды 227: 1 -й проект . Женева: Всемирная организация здравоохранения. ISBN 978-9241572279 .
- ^ Jump up to: а беременный Fawell, JK; и др. «Фторид в фоновом документе по питьевой воде для разработки руководящих принципов ВОЗ по качеству питьевой воды» (PDF) . Всемирная организация здравоохранения . Получено 6 мая 2016 года .
- ^ Ядав, Кришна Кумар; Кумар, Сандип; Фам, Quoc Bao; Гупта, Неха; Резания, Шахабалдин; Камиб, Хесам; Ядав, Шалини; Вимазал, Ян; Кумар, Винит; Три, Доан Куанг; Talaiekhozani, Amirreza; Прасад, Шив; Прием, Лиза М.; Сингх, Нираджа; Маурья, Прадип Кумар; Чо, Джинву (октябрь 2019). «Загрязнение фторида, проблемы со здоровьем и методы восстановления в азиатских подземных водах: всесторонний обзор». Экотоксикология и безопасность окружающей среды . 182 : 109362. Bibcode : 2019ecoes.18209362Y . Doi : 10.1016/j.ecoenv.2019.06.045 . PMID 31254856 . S2CID 195764865 .
- ^ Тиманн, Мэри (5 апреля 2013 г.). «Фторид в питьевой воде: обзор вопросов фторирования и регулирования» (PDF) . Исследовательская служба Конгресса. п. 3 Получено 6 мая 2016 года .
- ^ Чандио, Тасавар Али; Хан, Мухаммед Насируддин; Мухаммед, Мария Тадж; Yalcinkaya, Ozcan; Васим, Ага Арслан; Кайс, Ахмет Фуркан (январь 2021 г.). «Загрязнение фторида и мышьяка в питьевой воде из -за горнодобывающей деятельности и ее влияния на население местных мест». Наука по окружающей среде и исследование загрязнения . 28 (2): 2355–2368. Bibcode : 2021espr ... 28.2355c . doi : 10.1007/s11356-020-10575-9 . PMID 32880840 . S2CID 221463681 .
- ^ Белломо, Серхио; Aiuppa, Alessandro; Д'Алессандро, Уолтер; Парелло, Франческо (август 2007 г.). «Влияние на окружающую среду магматического излучения фтора в области Mt. etna». Журнал вулканологии и геотермальных исследований . 165 (1–2): 87–101. Bibcode : 2007jvgr..165 ... 87b . doi : 10.1016/j.jvolgeores.2007.04.013 .
- ^ Смит, Фрэнк А.; Ходж, Гарольд С.; Динман, BD (9 января 2009 г.). «Флоориды и человек: часть I». Критические обзоры CRC в контроле окружающей среды . 8 (1–4): 293–371. doi : 10.1080/10643387709381665 .
- ^ Смит, Фрэнк А.; Ходж, Гарольд С.; Динман, BD (9 января 2009 г.). «Фториды воздуха и человек: часть II». Критические обзоры CRC в контроле окружающей среды . 9 (1): 1–25. doi : 10.1080/10643387909381666 .
- ^ Arnesen, AKM; Абрахамсен, Г.; Сандвик, Г.; Крогстад Т. (февраль 1995 г.). «Алюминиевые сбезлы и загрязнение фторида почвы и почвенного раствора в Норвегии». Наука общей среды . 163 (1–3): 39–53. Bibcode : 1995 Scess.163 ... 39a . doi : 10.1016/0048-9697 (95) 04479-K .
- ^ Wong MH, Fung KF, Carr HP (2003). «Содержание алюминия и фторида чая, с акцентом на кирпичный чай и их последствия для здоровья». Токсикологические письма . 137 (1–2): 111–20. doi : 10.1016/s0378-4274 (02) 00385-5 . PMID 12505437 .
- ^ Малиновская Е., Инкиевевич I, Чарнвски В., Сефер П. (2008). «Оценка концентрации фтора и ежедневного потребления человеком от чая и травяных инфузий». Пищевая химия. Токсиколовый . 46 (3): 1055–61. doi : 10.1016/j.fct.2007.10.039 . PMID 18078704 .
- ^ Gardner EJ, Ruxton CH, Leeds AR (2007). «Черный чай - очень вредный или вредный? Обзор доказательств». Европейский журнал клинического питания . 61 (1): 3–18. doi : 10.1038/sj.ejcn.1602489 . PMID 16855537 .
- ^ Wiberg; Холмен, AF (2001). Неорганическая химия (1 -е английское изд., [Отредактировано] Nils Wiberg. Ed.). Сан -Диего, Калифорния: Берлин: Академическая пресса, В. де Грюйтер. ISBN 978-0-12-352651-9 .
- ^ Швезингер, Рейнхард; Ссылка, Рейнхард; Венцл, Питер; Коссек, Себастьян (2005). «Безводные фториды фосфазения в качестве источников для чрезвычайно реактивных ионов фтора в растворе». Химия: европейский журнал . 12 (2): 438–45. doi : 10.1002/chem.200500838 . PMID 16196062 .
- ^ Haoran Sun & Stephen G. Dimagno (2005). «Безводный фторид тетрабутиламмония». Журнал Американского химического общества . 127 (7): 2050–1. doi : 10.1021/ja0440497 . PMID 15713075 .
- ^ Беннетт, Брайан К.; Харрисон, Роджер Г.; Ричмонд, Томас Г. (1994). «Фторид кобальтоцениума: новый источник« обнаженного »фторида, образованного активацией углеродной флюориновой связи в насыщенном перфторуглеродном углу». Журнал Американского химического общества . 116 (24): 11165–11166. doi : 10.1021/ja00103a045 .
- ^ Алич, Б.; Тавчар, Г. (2016). «Реакция N-гетероциклического карбена (NHC) с различными источниками и соотношениями HF-свободного фторида реагента на основе фторида имидазолия». J. Fluorine Chem . 192 : 141–146. doi : 10.1016/j.jfluchem.2016.11.004 .
- ^ Алич, Б.; Трамшка, м.; Kokalj, A.; Тавчар, Г. (2017). «Дискретный GEF5 - анион, структурно охарактеризованный с легко синтезированным имидазолием, реагент обнаженного фторида». Inorg. Химический 56 (16): 10070–10077. doi : 10.1021/acs.inorgchem.7b01606 . PMID 28792216 .
- ^ Zupanek, ž.; Трамшка, м.; Kokalj, A.; Тавчар, Г. (2018). «Реакционная способность VOF3 с N-гетероциклическим карбеном и фторидом имидазолия: анализ связи лиганд-VOF3 с признаками минутной π-донации фторида». Inorg. Химический 57 (21): 13866–13879. doi : 10.1021/acs.inorgchem.8b02377 . PMID 30353729 . S2CID 53031199 .
- ^ Jump up to: а беременный Fawell, J. «Фторид в питьевой воде» (PDF) . Всемирная организация здравоохранения . Получено 10 марта 2016 года .
- ^ Jump up to: а беременный в Чан, Лора; Мехра, Арадхана; Сайкат, Сохель; Линч, Пол (май 2013). «Оценка воздействия на человека из чая ( Camellia sinensis L.): британский вопрос?». Food Research International . 51 (2): 564–570. doi : 10.1016/j.foodres.2013.01.025 .
- ^ «Зубная паста без фтора - фторид (наконец -то!) Объяснил» . 27 июня 2016 года.
- ^ McDonagh MS; Whiting PF; Уилсон ПМ; Саттон AJ; Каштан I.; Купер Дж.; Misso K.; Брэдли М.; Сокровище E.; Kleijnen J. (2000). «Систематический обзор фторирования воды» . Британский медицинский журнал . 321 (7265): 855–859. doi : 10.1136/bmj.321.7265.855 . PMC 27492 . PMID 11021861 .
- ^ Гриффин С.О., Регнье Э., Гриффин П.М., Хантли В. (2007). «Эффективность фторида в предотвращении кариеса у взрослых». J. Dent. Резерв 86 (5): 410–5. doi : 10.1177/154405910708600504 . HDL : 10945/60693 . PMID 17452559 . S2CID 58958881 .
- ^ Уинстон А.Е; Bhaskar SN (1 ноября 1998 г.). «Профилактика кариеса в 21 веке» . J. Am. Вмятина. Ассоциация 129 (11): 1579–87. doi : 10.14219/jada.archive.1998.0104 . PMID 9818575 . Архивировано из оригинала 15 июля 2012 года.
- ^ «Фтоорирование водой сообщества» . Центры для контроля и профилактики заболеваний . Получено 10 марта 2016 года .
- ^ «Десять великих достижений общественного здравоохранения в 20 -м веке» . Центры для контроля и профилактики заболеваний. Архивировано с оригинала 13 марта 2016 года . Получено 10 марта 2016 года .
- ^ Ньюбрун Э. (1996). «Война с фторированием: научный спор или религиозный аргумент?». Журнал общественного здравоохранения . 56 (5 Spec no): 246–52. doi : 10.1111/j.1752-7325.1996.tb02447.x . PMID 9034969 .
- ^ Уолш, Таня; Уортингтон, Хелен v.; Гленни, Энн-Мари; Мариньо, Валерия CC; Иерончич, Ана (4 марта 2019 г.). «Зубные пасти фторида различных концентраций для предотвращения кариеса» . Кокрановская база данных систематических обзоров . 3 (3): CD007868. doi : 10.1002/14651858.cd007868.pub3 . ISSN 1469-493X . PMC 6398117 . PMID 30829399 .
- ^ «Реминерализация первоначальных кариозных поражений в лиственной эмале после применения зубных данных различных концентраций фтора» . Springermedizin.de (на немецком языке) . Получено 24 февраля 2021 года .
- ^ Hausen, H.; Kärkkäinen, S.; Seppä, L. (февраль 2000 г.). «Применение стратегии высокого риска для контроля стоматологического кариеса» . Сообщество Стоматология и устная эпидемиология . 28 (1): 26–34. doi : 10.1034/j.1600-0528.2000.280104.x . ISSN 0301-5661 . PMID 10634681 .
- ^ Накай С., Томас Дж.А. (1974). «Свойства фосфопротеинфосфатазы из бычьего сердца с активностью на гликогенсинтазе, фосфорилазе и гистоне» . Дж. Биол. Химический 249 (20): 6459–67. doi : 10.1016/s0021-9258 (19) 42179-0 . PMID 4370977 .
- ^ Schenk G, Elliott TW, Leung E, et al. (2008). «Кристаллические структуры фиолетовой кислотной фосфатазы, представляющие различные этапы каталитического цикла этого фермента» . BMC Struct. Биол . 8 : 6. doi : 10.1186/1472-6807-8-6 . PMC 2267794 . PMID 18234116 .
- ^ Wang W, Cho HS, Kim R, et al. (2002). «Структурная характеристика пути реакции в фосфосеринофосфатазе: кристаллографические« снимки »промежуточных состояний». J. Mol. Биол . 319 (2): 421–31. doi : 10.1016/s0022-2836 (02) 00324-8 . PMID 12051918 .
- ^ Чо Х., Ван В., Ким Р. и соавт. (2001). «BEF (3) (-) действует как фосфатный аналог в белках, фосфорилированном на аспартате: структура комплекса BEF (3) (-) с фосфосеринофосфатазой» . Прокурор Нат. Академический Наука США . 98 (15): 8525–30. Bibcode : 2001pnas ... 98.8525c . doi : 10.1073/pnas.131213698 . PMC 37469 . PMID 11438683 .
- ^ Jump up to: а беременный Институт медицины (1997). «Фторид» . Диетические эталонные потребления для кальция, фосфора, магния, витамина D и фторида . Вашингтон, округ Колумбия: Национальная академическая пресса. С. 288–313. doi : 10.17226/5776 . ISBN 978-0-309-06403-3 Полем PMID 23115811 .
- ^ «Обзор диетических эталонных значений для популяции ЕС, полученных панелью EFSA по диетическим продуктам, питанию и аллергии» (PDF) . 2017.
- ^ Jump up to: а беременный Допустимые уровни верхнего потребления для витаминов и минералов (PDF) , Европейское управление по безопасности пищевых продуктов, 2006
- ^ реестр 27 мая 2016 г. « Федеральный
- ^ «Списки питательных веществ» . Служба сельскохозяйственных исследований Министерства сельского хозяйства США. Архивировано из оригинала 26 мая 2014 года . Получено 25 мая 2014 года .
- ^ Леви, Стивен М.; Guha-Chowdhury, Nupur (1999). «Общее потребление фтора и последствия для пищевых добавок фторида». Журнал общественного здравоохранения . 59 (4): 211–223. doi : 10.1111/j.1752-7325.1999.tb03272.x . PMID 10682326 .
- ^ «Базы данных пищевого состава: поиск пищи: фторид» . Служба сельскохозяйственных исследований , Министерство сельского хозяйства США . Архивировано из оригинала 5 декабря 2018 года . Получено 5 декабря 2018 года .
- ^ «Диетические эталонные потребления: ухо, RDA, AI, приемлемые диапазоны распределения макронутриентов и UL» . Министерство сельского хозяйства США . Получено 9 сентября 2017 года .
- ^ «Фторид в рационе» . Национальная библиотека медицины США . Получено 10 марта 2016 года .
- ^ Госселин, Re; Смит Р.П.; Hodge HC (1984). Клиническая токсикология коммерческих продуктов . Балтимор (MD): Уильямс и Уилкинс. С. III - 185–93. ISBN 978-0-683-03632-9 .
- ^ Baselt, RC (2008). Расположение токсичных препаратов и химикатов у человека . Фостер Сити (Калифорния): биомедицинские публикации. С. 636–40. ISBN 978-0-9626523-7-0 .
- ^ МПК (2002). Критерии здоровья окружающей среды 227 (фторид) . Женева: Международная программа по безопасности химической безопасности, Всемирная организация здравоохранения. п. 100. ISBN 978-92-4-157227-9 .
- ^ Jump up to: а беременный Rabinowitch, IM (1945). «Острый отравление фтором» . Канадская медицинская ассоциация журнала . 52 (4): 345–9. PMC 1581810 . PMID 20323400 .
- ^ Abukurah AR, Moser AM Jr, Baird CL, Randall Re Jr, Setter JG, Blanke RV (1972). «Острый отравление фторидом натрия». Джама . 222 (7): 816–7. doi : 10.1001/Jama.1972.03210070046014 . PMID 4677934 .
- ^ Merck Index, 12th Edition, Merck & Co., Inc., 1996
- ^ Муриал Л., Ли Е., Дженовезе Дж., Тренд С. (1996). «Стательность из -за острого отравления фтора после кожного контакта с гидрофторической кислотой в лаборатории палинологии». Энн. Оккупация Гиг . 40 (6): 705–710. doi : 10.1016/s0003-4878 (96) 00010-5 . PMID 8958774 .
- ^ Мюррей Т.М., Стемари Л.Г. (1996). «Профилактика и лечение остеопороза: консенсусные заявления от научного консультативного совета Общества остеопороза Канады. 7. Фторидная терапия при остеопорозе» . CMAJ . 155 (7): 949–54. PMC 1335460 . PMID 8837545 .
- ^ Национальный совет здравоохранения и медицинских исследований (Австралия) (2007). Систематический обзор эффективности и безопасности фторирования (PDF) . ISBN 978-1-86496-415-8 Полем Архивировано из оригинала (PDF) 14 октября 2009 года . Получено 21 февраля 2010 года . Краткое содержание: Yeung CA (2008). «Систематический обзор эффективности и безопасности фторирования» . На основе Dent . 9 (2): 39–43. doi : 10.1038/sj.ebd.6400578 . PMID 18584000 .
- ^ Haguenauer, D; Уэлч, V; Ши, б; Tugwell, P; Адачи, JD; Уэллс, Г. (2000). «Фторид для лечения постменопаузальных остеопоротических переломов: метаанализ». Остеопороз International . 11 (9): 727–38. doi : 10.1007/s001980070051 . PMID 11148800 . S2CID 538666 .
- ^ Всемирная организация здравоохранения (2004). «Фторид в питьевой воде» (PDF) . Архивировано из оригинала (PDF) 4 марта 2016 года . Получено 13 февраля 2014 года .
{{cite journal}}: CITE Journal требует|journal=( помощь ) - ^ «Воздействие фторида: развитие нейродийности и познание» . Национальная токсикологическая программа . Получено 25 августа 2024 года .
- ^ Стоун, Уильям (23 августа 2024 г.). "Flouride и IQ" . npr.org . Получено 25 августа 2024 года .
- ^ Alltucker, Ken. «Сколько слишком много фтора в питьевой воде? Новый отчет поднимает вопросы» . USA сегодня . Получено 25 августа 2024 года .
- ^ Исследования связывают высокий уровень фтора в воде с снижением IQ у детей . 23 августа 2024 года . Получено 25 августа 2024 года - через www.wcvb.com.
- ^ Eawag (2015) Справочник по геогенному загрязнению - адресация мышьяка и фторида в питьевой воде. CA Johnson, A. Bretzler (Eds.), Швейцарский федеральный институт водной науки и техники (EAWAG), DudeBendorf, Швейцария. (Скачать: www.eawag.ch/en/research/humanwelfare/dringwater/wrq/geogency-contamination-handbook/)
- ^ Rodríguez-Lado, L.; Солнце, Г.; Берг, М.; Чжан, Q.; XUE, H.; Zheng, Q.; Джонсон, Калифорния (2013). «Загрязнение мышьяка подземных вод по всему Китаю» . Наука . 341 (6148): 866–868. Bibcode : 2013sci ... 341..866r . doi : 10.1126/science.1237484 . PMID 23970694 . S2CID 206548777 .
- ^ Платформа оценки подземных вод
- ^ Накагава М., Мацуя С., Ширайши Т., Охта М. (1999). «Влияние концентрации фтора и рН на коррозионное поведение титана для стоматологического использования». Журнал стоматологических исследований . 78 (9): 1568–72. doi : 10.1177/00220345990780091201 . PMID 10512392 . S2CID 32650790 .
- ^ «Бифлуорид аммония в стеклянной промышленности - Chimex Ltd» .