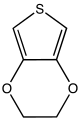
Тиофен
| |||
| |||
| Имена | |||
|---|---|---|---|
| Предпочтительное название ИЮПАК
Тиофен [ 1 ] | |||
| Другие имена
Тиофуран
Тиациклопентадиен Тиол | |||
| Идентификаторы | |||
3D model ( JSmol )
|
|||
| КЭБ | |||
| ХЭМБЛ | |||
| ХимическийПаук | |||
| Информационная карта ECHA | 100.003.392 | ||
ПабХим CID
|
|||
| номер РТЭКС |
| ||
| НЕКОТОРЫЙ | |||
Панель управления CompTox ( EPA )
|
|||
| Характеристики | |||
| С 4 Ч 4 С | |||
| Молярная масса | 84.14 g/mol | ||
| Появление | бесцветная жидкость | ||
| Плотность | 1,051 г/мл, жидкость | ||
| Температура плавления | -38 ° C (-36 ° F; 235 К) | ||
| Точка кипения | 84 ° С (183 ° F; 357 К) | ||
| -57.38·10 −6 см 3 /моль | |||
Показатель преломления ( n D )
|
1.5287 | ||
| Вязкость | 0,8712 с П и 0,2 °С 0,6432 с П и 22,4 °С | ||
| Опасности | |||
| Безопасность и гигиена труда (OHS/OSH): | |||
Основные опасности
|
Токсичный | ||
| СГС Маркировка : [ 2 ] | |||
 
| |||
| Опасность | |||
| Х225 , Х302 , Х319 , Х412 | |||
| П210 , П260 , П262 , П273 , П305+П351+П338 , П403+П235 | |||
| NFPA 704 (огненный алмаз) | |||
| точка возгорания | −1 ° C (30 ° F; 272 К) | ||
| Паспорт безопасности (SDS) | Внешний паспорт безопасности материала , Внешний паспорт безопасности материала | ||
| Родственные соединения | |||
Родственные тиоэфиры
|
Тетрагидротиофен Диэтилсульфид | ||
Родственные соединения
|
Открыть Селенофен Пиррол | ||
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа).
| |||
Тиофен представляет собой гетероциклическое соединение с формулой C 4 H 4 S. Состоящее из плоского пятичленного кольца, оно является ароматическим , о чем свидетельствуют его обширные реакции замещения . Это бесцветная жидкость с запахом бензола . В большинстве реакций он напоминает бензол . Соединения, аналогичные тиофену, включают фуран (C 4 H 4 O), селенофен (C 4 H 4 Se) и пиррол (C 4 H 4 NH), каждое из которых варьируется в зависимости от гетероатома в кольце.
Выделение и возникновение
[ редактировать ]Тиофен был открыт Виктором Мейером в 1882 году как примесь в бензоле. [ 3 ] Было замечено, что изатин ( индол ) образует синий краситель , если его смешать с серной кислотой и сырым бензолом. Долгое время считалось, что образование синего индофенина является реакцией самого бензола. Виктор Мейер смог выделить тиофен как вещество, ответственное за эту реакцию. [ 4 ]
Тиофен и особенно его производные встречаются в нефти , иногда в концентрациях до 1–3%. Тиофеновые соединения из нефти и угля удаляются с помощью процесса гидрообессеривания (HDS). В HDS жидкое или газообразное сырье пропускают через катализатор на основе дисульфида молибдена под давлением H 2 . Тиофены подвергаются гидрогенолизу с образованием углеводородов и сероводорода . Таким образом, сам тиофен превращается в бутан и H 2 S. Более распространенными и более проблематичными в нефти являются бензотиофен и дибензотиофен .
На Марсе
[ редактировать ]Производные тиофена были обнаружены на уровне наномолей в отложениях марсианской почвы возрастом 3,5 миллиарда лет (формация Мюррей, холмы Парамп) марсоходом Curiosity в кратере Гейла (Марс) в период с 2012 по 2017 год. [ 5 ] Это важная веха в миссии Марсианской научной лаборатории (MSL) в долгих и неуловимых поисках органического вещества на Красной планете. Нагрев при высокой температуре (от 500° до 820°C) образцов озерных аргиллитов с помощью прибора Sample Analysis at Mars (SAM) позволил провести газовую хроматографию-масс-спектрометрию ( ГХ-МС ) для анализа выделяющихся газов и обнаружения ароматических и алифатических молекул. включая несколько тиофеновых соединений. [ 6 ] Наличие связей углерод-сера в макромолекулах могло способствовать сохранению органического вещества на очень длительный срок. Подсчитано, что ~ 5 % органических молекул, анализируемых прибором SAM , содержат органическую серу. Остается неизвестным, является ли происхождение и способ образования этих молекул биотическим или абиотическим . [ 7 ] но их открытие выдвинуло загадочный вопрос о тиофеновых соединениях как возможной древней биосигнатуре Марса. Детальный анализ изотопов углерода (δ 13 C) на уровне следов марсианских марсоходов следующего поколения, таких как Розалинда Франклин , [ 8 ] необходимо будет определить, обогащены ли такие органические молекулы легким углеродом ( 12 в) как живые микроорганизмы обычно присутствуют на Земле.
Синтез и производство
[ редактировать ]Отражая свою высокую стабильность, тиофены возникают в результате многих реакций с участием источников серы и углеводородов, особенно ненасыщенных. Первый синтез тиофена, о котором Мейер сообщил в том же году, когда он сделал свое открытие, включает ацетилен и элементарную серу. Тиофены классически получают реакцией 1,4-дикетонов , диэфиров или дикарбоксилатов с сульфидирующими реагентами, такими как P 4 S 10 , например, в синтезе тиофена Паала-Кнорра . Специализированные тиофены могут быть синтезированы аналогичным образом с использованием реактива Ловессона в качестве сульфидирующего агента или с помощью реакции Гевальда , которая включает конденсацию двух сложных эфиров в присутствии элементарной серы. Другой метод — циклизация Фольхарда – Эрдмана .
Тиофен производится в скромных масштабах - около 2000 метрических тонн в год во всем мире. Производство включает в себя реакцию паровой фазы источника серы, обычно сероуглерода , и источника C-4, обычно бутанола . Эти реагенты контактируют с оксидным катализатором при температуре 500–550 °С. [ 9 ]
Свойства и структура
[ редактировать ]При комнатной температуре тиофен представляет собой бесцветную жидкость со слегка приятным запахом, напоминающим бензол . [ нужна ссылка ] с которым тиофен имеет некоторые сходства. Высокая реакционная способность тиофена по отношению к сульфированию является основой отделения тиофена от бензола, которые трудно отделить перегонкой из-за схожих температур кипения (разница в 4 °C при давлении окружающей среды). Как и бензол, тиофен образует азеотроп с этанолом.
Молекула плоская; валентный угол у серы составляет около 93 °, угол C – C – S составляет около 109 °, а два других углерода имеют валентный угол около 114 °. [ 10 ] Связи C–C с атомами углерода, соседними с серой, составляют около 1,34 Å , длина связи C–S составляет около 1,70 Å, а другая связь C–C составляет около 1,41 Å. [ 10 ]
Реактивность
[ редактировать ]Тиофен считается ароматическим, хотя теоретические расчеты показывают, что степень ароматичности меньше, чем у бензола. «Электронные пары» серы значительно делокализованы в пи-электронной системе. Из-за своей ароматичности тиофен не проявляет свойств, наблюдаемых у обычных сульфидов . Например, атом серы сопротивляется алкилированию и окислению.
Окисление
[ редактировать ]Окисление может происходить как по сере, давая тиофен S -оксид, так и по 2,3-двойной связи, давая тиофен-2,3-эпоксид, с последующей перегруппировкой сдвига NIH . [ 11 ] Окисление тиофена трифторперуксусной кислотой также демонстрирует оба пути реакции. Основной путь образует S -оксид в качестве промежуточного продукта, который подвергается последующей Дильса-Альдера типа димеризации и дальнейшему окислению, образуя смесь сульфоксидных и сульфоновых продуктов с совокупным выходом 83% (по данным ЯМР ): [ 12 ] [ 13 ]

На малом пути реакции происходит эпоксидирование Прилежаева. [ 14 ] приводит к образованию тиофен-2,3-эпоксида, который быстро перегруппировывается в изомер тиофен-2-он. [ 12 ] Эксперименты по ловле [ 15 ] демонстрируют, что этот путь не является побочной реакцией промежуточного S -оксида, в то время как изотопная метка дейтерием и, следовательно , подтверждает, что происходит 1,2-гидридный сдвиг участвует катионный промежуточный продукт. [ 12 ] Если реакционная смесь не безводна , этот второстепенный путь реакции подавляется, поскольку вода выступает в качестве конкурирующего основания. [ 12 ]
Окисление тиофенов может иметь отношение к метаболической активации различных тиофенсодержащих препаратов, таких как тиениловая кислота и исследуемый противораковый препарат OSI-930. [ 16 ] [ 17 ] [ 18 ] [ 19 ]
Алкилирование
[ редактировать ]Хотя атом серы относительно инертен, фланкирующие углеродные центры, 2-е и 5-е положения, очень чувствительны к атаке электрофилов . Галогены сначала дают 2-галогенпроизводные, а затем 2,5-дигалотиофены; пергалогенирование легко осуществляется с образованием C 4 X 4 S (X = Cl, Br, I). [ 20 ] Тиофена броматы 10 7 раз быстрее, чем бензол. Ацетилирование происходит легко с образованием 2-ацетилтиофена , предшественника тиофен-2-карбоновой кислоты и тиофен-2-уксусной кислоты . [ 9 ]
Хлорметилирование и хлорэтилирование легко происходят по 2,5-положениям. Восстановление хлорметильного продукта дает 2-метилтиофен. Гидролиз с последующей дегидратацией хлорэтильных соединений дает 2-винилтиофен. [ 21 ] [ 22 ]
Десульфуризация никелем Ренея
[ редактировать ]Десульфуризация тиофена никелем Ренея дает бутан . В сочетании с легкой 2,5-дифункционализацией тиофена десульфуризация открывает путь к 1,4-дизамещенным бутанам.

Полимеризация
[ редактировать ]Полимер, образующийся путем связывания тиофена через его 2,5-положения, называется политиофеном . Полимеризация проводится путем окисления с использованием электрохимических методов ( электрополимеризация ) или реагентов переноса электрона. Показано идеализированное уравнение:
- n C 4 H 4 S → (C 4 H 2 S) n + 2n H + + 2н е −
Политиофен сам по себе имеет плохие технологические свойства и поэтому мало изучен. Более полезными являются полимеры, полученные из тиофенов, замещенных в положениях 3, 3 и 4, такие как ЭДОТ (этилендиокситиофен) . Политиофены становятся электропроводными при частичном окислении, т.е. приобретают некоторые характеристики, обычно наблюдаемые у металлов. [ 23 ]
Координационная химия
[ редактировать ]Тиофен мало похож на сульфид, но он служит пи-лигандом, образующим комплексы фортепианного стула, такие как Cr( η 5 -C4H4S ) 3 ) ( CO . [ 24 ]
Производные тиофена
[ редактировать ]- Некоторые тиофены
-
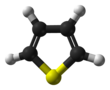
Тиено[3,2- b ]тиофен, один из четырех тиенотиофенов.
-
3,4-Этилендиокситиофен (EDOT), предшественник коммерческих антистатических и электрохромных дисплеев.
Тиенил
[ редактировать ]При депротонировании тиофен превращается в тиенильную группу C 4 H 3 S. − . Хотя аниона как такового не существует, литийорганические производные существуют. Таким образом, реакция тиофена с бутиллитием дает 2-литиотиофен, также называемый 2-тиениллитием. Этот реагент реагирует с электрофилами с образованием тиенильных производных, таких как тиол. [ 25 ] Окисление тиениллития дает 2,2'-дитиенил, (C 4 H 3 S) 2 . Тиениллитий используется при получении смешанных купратов более высокого порядка . [ 26 ] Сочетание эквивалентов тиениланиона дает дитиенил , аналог бифенила.
Кольцеконденсированные тиофены
[ редактировать ]Слияние тиофена с бензольным кольцом дает бензотиофен . Слияние с двумя бензольными кольцами дает либо дибензотиофен (ДБТ), либо нафтотиофен. Слияние пары тиофеновых колец дает изомеры тиенотиофена .
Использование
[ редактировать ]Тиофены являются важными гетероциклическими соединениями, которые широко используются в качестве строительных блоков во многих агрохимических и фармацевтических препаратах. [ 9 ] Бензольное кольцо биологически активного соединения часто можно заменить тиофеном без потери активности. [ 27 ] Это видно на таких примерах, как НПВП лорноксикам , тиофеновый аналог пироксикама , и суфентанил , тиофеновый аналог фентанила .
Ссылки
[ редактировать ]- ^ Международный союз теоретической и прикладной химии (2014). Номенклатура органической химии: Рекомендации ИЮПАК и предпочтительные названия 2013 . Королевское химическое общество . п. 141. дои : 10.1039/9781849733069 . ISBN 978-0-85404-182-4 .
- ^ СГС: ГЕСТИС 010090.
- ^ Мейер, Виктор (1883). «О веществе, сопровождающем бензол в каменноугольной смоле». Отчеты Немецкого химического общества . 16 : 1465–1478. дои : 10.1002/cber.188301601324 .
- ^ Уорд К., Самптер (1944). «Химия изатина». Химические обзоры . 34 (3): 393–434. дои : 10.1021/cr60109a003 .
- ^ Воосен, Пол (2018). «Ровер НАСА сталкивается с органической грязью на Марсе» . Наука . дои : 10.1126/science.aau3992 . ISSN 0036-8075 . S2CID 115442477 .
- ^ Эйгенброде, Дженнифер Л.; Вызов, Роджер Э.; Стил, Эндрю; Фрессине, Кэролайн; Миллан, Маэва; Наварро-Гонсалес, Рафаэль; Саттер, Брэд; Макадам, Эми С.; Франц, Хизер Б.; Главин, Дэниел П.; Арчер, Пол Д.; Махаффи, Пол Р.; Конрад, Памела Г.; Гуровиц, Джоэл А.; Гротцингер, Джон П.; Гупта, Санджив; Мин, Дуг В.; Самнер, Дон Ю.; Шопа, Кирилл; Малеспин, Чарльз; Бух, Арно; Колл, Патрис (2018). «Органическое вещество сохранилось в аргиллитах возрастом 3 миллиарда лет в кратере Гейла на Марсе» (PDF) . Наука . 360 (6393): 1096–1101. Бибкод : 2018Sci...360.1096E . дои : 10.1126/science.aas9185 . ISSN 0036-8075 . ПМИД 29880683 . S2CID 46983230 .
- ^ Хайнц, Джейкоб; Шульце-Макух, Дирк (2020). «Тиофены на Марсе: биотическое или абиотическое происхождение?» . Астробиология . 20 (4): 552–561. Бибкод : 2020AsBio..20..552H . дои : 10.1089/ast.2019.2139 . ПМИД 32091933 .
- ^ «Ровер Curiosity обнаружил на Марсе органические молекулы. Вот почему они так интересны» . CNN . 6 марта 2020 г.
- ^ Jump up to: а б с Суонстон, Джонатан (2006). «Тиофен». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a26_793.pub2 . ISBN 3527306730 . .
- ^ Jump up to: а б Кембриджская база данных структурных конструкций
- ^ Трайбер А., Дансетт П.М., Амри Х.Э., Жиро Ж.-П., Гиндероу Д., Морнон Ж.-П., Мансуи Д.; Дансетт; Эль Амри; Жиро; Гиндероу; Морнон; Мансуй (1997). «Химическое и биологическое окисление тиофена: получение и полная характеристика димеров тиофена S-оксида и доказательства того, что тиофен S -оксид является промежуточным продуктом в метаболизме тиофена in vivo и in vitro ». Дж. Ам. хим. Соц . 119 (7): 1565–1571. дои : 10.1021/ja962466g .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Jump up to: а б с д Трейбер, Александр (2002). «Механизм ароматического гидроксилирования тиофена путем кислотно-катализируемого окисления перкислот». Дж. Орг. хим. 67 (21): 7261–7266. дои : 10.1021/jo0202177 . ПМИД 12375952 .
- ^ Кастер, Кеннет К.; Рао, А. Сомасекар; Мохан, Х. Рама; МакГрат, Николас А.; Бричачек, Мэтью (2012). «Трифторперуксусная кислота». Энциклопедия реагентов для органического синтеза . Электронная энциклопедия реагентов для органического синтеза EROS . дои : 10.1002/047084289X.rt254.pub2 . ISBN 978-0471936237 .
- ^ Хаген, Тимоти Дж. (2007). «Реакция Прилежаева» . Ин Ли, Цзе Джек; Кори, Э.Дж. (ред.). Название Реакции превращений функциональных групп . Джон Уайли и сыновья . стр. 274–281. ISBN 9780470176504 .
- ^ Анслин, Эрик В .; Догерти, Деннис А. (2006). «8.8 Разные эксперименты по изучению механизма» . Современная физико-органическая химия . Университетские научные книги. стр. 471–482. ISBN 9781891389313 .
- ^ Мансуи Д., Валадон П., Эрдельмейер И., Лопес Гарсиа П., Амар К., Жиро Дж. П. и Дансетт П. М. (1991). «Тиофен S -оксиды как новые реактивные метаболиты: образование путем цитохром-P450-зависимого окисления и реакции с нуклеофилами». Дж. Ам. хим. Соц . 113 (20): 7825–7826. дои : 10.1021/ja00020a089 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Радемахер П.М., Вудс К.М., Хуан К., Шкларц Г.Д., Нельсон С.Д.; Вудс; Хуан; Шклярц; Нельсон (2012). «Дифференциальное окисление двух тиофенсодержащих региоизомеров до реакционноспособных метаболитов цитохромом P450 2C9» . хим. Рез. Токсикол . 25 (4): 895–903. дои : 10.1021/tx200519d . ПМЦ 3339269 . ПМИД 22329513 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Мансуи Д., Dansette PM; Дансетт (2011). «Сульфеновые кислоты как реактивные интермедиаты метаболизма ксенобиотиков» . Архив биохимии и биофизики . 507 (1): 174–185. дои : 10.1016/j.abb.2010.09.015 . ПМИД 20869346 .
- ^ Дансетт, П.М., Рози, Дж., Дебернарди, Дж., Берто Дж., Мансуи Д.; Рози; Дебернарди; Берто; Мансуй (2012). «Метаболическая активация прасугрела: природа двух конкурентных путей, приводящих к открытию его тиофенового кольца». хим. Рез. Токсикол. 25 (5): 1058–1065. дои : 10.1021/tx3000279 . ПМИД 22482514 .
{{cite journal}}: CS1 maint: несколько имен: список авторов ( ссылка ) - ^ Генри Ю. Лью и Ч. Р. Ноллер (1963). «2-Йодолтиофен» . Органические синтезы ; Сборник томов , т. 4, с. 545 .
- ^ У.С. Эмерсон и Т.М. Патрик младший (1963). «2-Винилтиофен» . Органические синтезы ; Сборник томов , т. 4, с. 980 .
- ^ КБ Виберг и Х. Ф. МакШейн (1955). «2-Хлорметилтиофен» . Органические синтезы ; Сборник томов , т. 3, с. 1 .
- ^ Дж. Ронкали (1992). «Сопряженные поли(тиофены): синтез, функционализация и применение». хим. Откр. 92 (4): 711–738. дои : 10.1021/cr00012a009 .
- ^ Раухфусс, ТБ, «Координационная химия тиофена», Прогресс в неорганической химии, 1991, том 39, стр. 259-311. ISBN 978-0-471-54489-0
- ^ Э. Джонс и И. М. Муди (1988). «2-Тиофенетиол» . Органические синтезы ; Сборник томов , т. 6, с. 979 .
- ^ Липшуц, Брюс Х .; Моретти, Роберт; Кроу, Роберт (1990). «Смешанные эпоксидные отверстия высшего порядка, индуцированные цианокупратом: 1-бензилокси-4-пентен-2-ол». Орг. Синтез . 69 : 80. дои : 10.15227/orgsyn.069.0080 .
- ^ Дэниел Леднисер (1999). Органическая химия синтеза лекарств . Том. 6. Нью-Йорк: Wiley Interscience. п. 187. ИСБН 0-471-24510-0 .
Внешние ссылки
[ редактировать ]- Международная карта химической безопасности 1190
- Чисхолм, Хью , изд. (1911). . Британская энциклопедия . Том. 26 (11-е изд.). Издательство Кембриджского университета.




![Тиено[3,2-b]тиофен, один из четырех тиенотиофенов.](http://upload.wikimedia.org/wikipedia/commons/thumb/c/cf/Thienothiophene251-41-2.png/180px-Thienothiophene251-41-2.png)