Эмерджентный вирус
Эмерджентный вирус (или эмерджентный вирус ) — это вирус , который либо появился недавно , заметно увеличивая заболеваемость / географический ареал , либо имеет потенциал для увеличения в ближайшем будущем. [1] Эмерджентные вирусы являются основной причиной возникновения новых инфекционных заболеваний и создают проблемы общественного здравоохранения во всем мире, учитывая их потенциал вызывать вспышки заболеваний, которые могут привести к эпидемиям и пандемиям . [2] не только вызывают болезни Эмерджентные вирусы , но и могут иметь серьезные экономические последствия. [3] Недавние примеры включают связанные с атипичной пневмонией коронавирусы , которые вызвали ) в 2002–2004 годах ( вспышку атипичной пневмонии SARS -CoV-1 и ) в 2019–2023 годах пандемию COVID -19 ( SARS-CoV-2 . [4] [5] Другие примеры включают вирус иммунодефицита человека , вызывающий ВИЧ/СПИД ; вирусы, ответственные за Эболу ; [6] вирус гриппа H5N1, вызывающий птичий грипп ; [7] и H1N1/09 , вызвавшие пандемию свиного гриппа в 2009 году. [8] (более ранний возникший штамм H1N1 в вызвал пандемию испанского гриппа 1918 году ). [9] Появление вируса у людей часто является следствием зооноза , который предполагает межвидовой переход вирусного заболевания к человеку от других животных. Поскольку зоонозные вирусы существуют в животных-резервуарах , их гораздо труднее искоренить , и поэтому они могут вызывать стойкие инфекции в популяциях людей. [10]
Эмерджентные вирусы не следует путать с вновь появляющимися вирусами или вновь обнаруженными вирусами. Вновь возникшим вирусом обычно считается ранее появившийся вирус, который переживает возрождение. [1] [11] например корь . [12] Вновь обнаруженный вирус — это ранее нераспознанный вирус, который циркулировал среди вида как эндемичная или эпидемическая инфекция. [13] Недавно обнаруженные вирусы могли ускользнуть от классификации , поскольку они не оставили никаких отличительных признаков и/или не могли быть выделены или размножены в клеточной культуре . [14] Примеры включают риновирус человека (основная причина простудных заболеваний, впервые выявленная в 1956 году), [15] гепатит С (в конечном итоге выявленный в 1989 г.), [16] и метапневмовирус человека (впервые описанный в 2001 году, но предположительно циркулирующий с 19 века). [17] Поскольку обнаружение таких вирусов осуществляется с помощью технологий, их число, вероятно, увеличится.
Зооноз
[ редактировать ]Учитывая редкость спонтанного развития новых видов вирусов, наиболее частой причиной возникновения эмерджентных вирусов у человека является зооноз . По оценкам, на это явление приходится 73% всех возникающих или вновь появляющихся патогенов , причем вирусы играют непропорционально большую роль. [18] РНК-вирусы встречаются особенно часто: на их долю приходится 37% новых и вновь возникающих патогенов. [18] широкий спектр животных включая диких птиц, грызунов и летучих мышей . , С зоонозными вирусами связан [19] Невозможно предсказать конкретные зоонозные события, которые могут быть связаны с конкретным животным-резервуаром в любой момент времени. [20]
Зоонозное распространение может привести либо к самоограничивающимся «тупиковым» инфекциям, при которых дальнейшая передача от человека к человеку не происходит (как в случае с вирусом бешенства ), [21] или в инфекционных случаях, когда зоонозный патоген способен поддерживать передачу от человека к человеку (как в случае с вирусом Эбола ). [6] Если зоонозный вирус способен поддерживать успешную передачу от человека к человеку, может возникнуть вспышка . [22] Некоторые побочные эффекты могут также привести к тому, что вирус адаптируется исключительно для заражения человека (как это произошло с вирусом ВИЧ ). [23] в этом случае люди становятся новым резервуаром возбудителя.
Успешный зоонозный «прыжок» зависит от контакта человека с животным, несущим вариант вируса, способный заразить человека. Чтобы преодолеть ограничения по кругу хозяев и обеспечить эффективную передачу вируса от человека к человеку, вирусы, происходящие из животного резервуара, обычно подвергаются мутациям , генетической рекомбинации и рекомбинации . [20] Благодаря быстрой репликации и высокой частоте мутаций РНК-вирусы с большей вероятностью успешно адаптируются к инвазии в новую популяцию хозяев. [3]
Примеры источников животного происхождения
[ редактировать ]Летучие мыши
[ редактировать ]
Хотя летучие мыши являются важными членами многих экосистем, [24] они также часто являются частыми источниками новых вирусных инфекций. [25] Их иммунная система развилась таким образом, что подавляет любую воспалительную реакцию на вирусные инфекции, что позволяет им стать толерантными хозяевами к развивающимся вирусам и, следовательно, обеспечивать основные резервуары зоонозных вирусов. [26] Они связаны с большим количеством зоонозных вирусов на вид хозяина, чем любое другое млекопитающее, а молекулярные исследования показали, что они являются естественными хозяевами для нескольких широко известных зоонозных вирусов, включая тяжелым острым респираторным синдромом , коронавирусы, связанные с и филовирусы геморрагической лихорадки Эбола / Марбург . [27] С точки зрения возможности возникновения побочных эффектов, летучие мыши взяли на себя ведущую роль, ранее отведенную грызунам. [26] Вирусы могут передаваться от летучих мышей несколькими способами, включая укусы, [28] аэрозолизация слюны (например, во время эхолокации ) и кала/мочи. [29]
Из-за своей особой экологии и поведения летучие мыши, естественно, более восприимчивы к вирусным инфекциям и их передаче. Некоторые виды летучих мышей (например, бурые летучие мыши) собираются в скоплениях, что способствует внутри- и межвидовой передаче вируса. Более того, поскольку летучие мыши широко распространены в городских районах, люди время от времени вторгаются в их среду обитания, загрязненную гуано и мочой. Их способность летать и характер миграции также означают, что летучие мыши способны распространять болезни на большой географической территории, а также приобретать новые вирусы. [30] Кроме того, летучие мыши страдают от стойких вирусных инфекций, что в сочетании с их чрезвычайной продолжительностью жизни (продолжительность жизни некоторых видов летучих мышей достигает 35 лет) помогает сохранять вирусы и передавать их другим видам. Другие характеристики летучих мышей, которые способствуют их эффективности в качестве вирусных хозяев, включают: их выбор пищи, привычки к оцепенению / гибернации и восприимчивость к повторному заражению. [30]
Драйверы возникновения вируса
[ редактировать ]Появление вируса часто является следствием как природы, так и деятельности человека . В частности, экологические изменения могут значительно способствовать появлению и повторному появлению зоонозных вирусов. [31] Такие факторы, как вырубка лесов , лесовосстановление , фрагментация среды обитания и ирригация, могут влиять на способы контакта людей с дикими животными и, следовательно, способствовать появлению вируса. [3] [32] В частности, значительную роль в появлении зоонозов играет утрата среды обитания резервуарных видов-хозяев . [33] Кроме того, изменение климата может повлиять на экосистемы и распространение переносчиков , что, в свою очередь, может повлиять на появление трансмиссивных вирусов. Другие экологические изменения — например, интродукция видов и исчезновение хищников — также могут повлиять на возникновение и распространенность вируса. Некоторые ведения сельского хозяйства методы — например, интенсификация животноводства и ненадлежащее обращение/удаление фекалий сельскохозяйственных животных — также связаны с повышенным риском зооноза. [3] [34]
Вирусы могут также появиться в результате формирования человеческих популяций, уязвимых к инфекции. Например, вирус может появиться после потери перекрестного защитного иммунитета , что может произойти из-за потери дикого вируса или прекращения программы вакцинации . В хорошо развитых странах также выше доля стареющих граждан и заболеваний, связанных с ожирением , что означает, что их население может иметь более низкий иммунитет и, следовательно, подвергаться риску заражения. [3] Напротив, в более бедных странах население может иметь ослабленный иммунитет из-за недоедания или хронической инфекции; эти страны также вряд ли будут иметь стабильную программу вакцинации. [3] Кроме того, изменения в демографии населения [3] — например, рождение и/или миграция иммунологически наивных людей — может привести к развитию восприимчивой популяции, которая делает возможным крупномасштабное вирусное заражение.
Другие факторы, которые могут способствовать возникновению вируса, включают глобализацию ; в частности, международная торговля людей и путешествия/ миграция могут привести к проникновению вирусов в новые районы. [3] Более того, поскольку густонаселенные города способствуют быстрой передаче патогенов, неконтролируемая урбанизация (т. е. увеличение перемещения и расселения людей в городских районах ) может способствовать возникновению вируса. [35] Миграция животных также может привести к появлению вирусов, как это произошло с вирусом Западного Нила , который распространялся мигрирующими популяциями птиц. [36] Кроме того, человеческая практика производства и потребления продуктов питания также может способствовать риску возникновения вируса. В частности, влажные рынки (т.е. рынки живых животных) являются идеальной средой для передачи вируса из-за высокой плотности присутствия людей и диких/сельскохозяйственных животных. [29] Потребление мяса диких животных также связано с появлением патогенов. [29]
Профилактика
[ редактировать ]Контроль и профилактика зоонозных заболеваний зависят от надлежащего глобального надзора на различных уровнях, включая выявление новых патогенов, надзор за общественным здравоохранением (включая серологические исследования ) и анализ рисков передачи. [37] Сложность зоонозных явлений во всем мире требует междисциплинарного подхода к профилактике. [37] Модель «Единое здоровье» была предложена в качестве глобальной стратегии, помогающей предотвратить появление зоонозных заболеваний у людей, включая новые вирусные заболевания. [37] Концепция «Единое здоровье» направлена на содействие здоровью животных, людей и окружающей среды, как на местном, так и на глобальном уровне, путем содействия взаимопониманию и сотрудничеству между специалистами-практиками различных взаимосвязанных дисциплин, включая биологию дикой природы , ветеринарию , медицину , сельское хозяйство , экологию , микробиологию , эпидемиология и биомедицинская инженерия . [37] [38]
Вирулентность возникающих вирусов
[ редактировать ]Поскольку хозяева иммунологически невосприимчивы к патогенам, с которыми они раньше не сталкивались, возникающие вирусы часто чрезвычайно вирулентны с точки зрения их способности вызывать заболевания. Их высокая вирулентность обусловлена также отсутствием адаптации к новому хозяину; Вирусы обычно оказывают сильное давление отбора на иммунную систему своих естественных хозяев, что, в свою очередь, оказывает сильное давление отбора на вирусы. [39] Эта коэволюция означает, что естественный хозяин способен справиться с инфекцией. Однако когда вирус переходит к новому хозяину (например, человеку), новый хозяин не может справиться с инфекцией из-за отсутствия коэволюции, что приводит к несоответствию между иммуноэффекторами хозяина и иммуномодуляторами вируса . [ нужна ссылка ]
Кроме того, чтобы максимизировать передачу, вирусы часто естественным образом подвергаются аттенуации (т. е. вирулентность ), так что инфицированные животные могут выжить достаточно долго, чтобы более эффективно заражать других животных. снижается [40] Однако, поскольку для достижения ослабления требуется время, новые популяции хозяев изначально не получат выгоды от этого явления. Более того, поскольку зоонозные вирусы естественным образом существуют и в животных-резервуарах , [10] их выживание не зависит от передачи между новыми хозяевами; это означает, что возникающие вирусы с еще меньшей вероятностью будут ослабляться с целью максимальной передачи и остаются вирулентными. [ нужна ссылка ]
Хотя эмерджентные вирусы часто обладают высокой вирулентностью, они ограничиваются несколькими факторами хозяина, включая врожденный иммунитет , естественные антитела и специфичность рецептора . Если хозяин ранее был инфицирован патогеном, похожим на появившийся вирус, хозяин также может получить пользу от перекрестного защитного иммунитета . [ нужна ссылка ]
Примеры новых вирусов
[ редактировать ]Грипп А
[ редактировать ]
Грипп — это высококонтагиозная респираторная инфекция, от которой страдает примерно 9% населения планеты и ежегодно становится причиной от 300 000 до 500 000 смертей. [41] [42] В зависимости от основных белков вирусы гриппа подразделяются на типы A, B, C и D. [43] [44] Хотя грипп А и В могут вызывать эпидемии у людей, грипп А также обладает пандемическим потенциалом и более высокой частотой мутаций и, следовательно, имеет наиболее важное значение для общественного здравоохранения. [44] [45]
Вирусы гриппа А подразделяются на подтипы на основе комбинации поверхностных гликопротеинов гемагглютинина (НА) и нейраминидазы (NA). Основным естественным резервуаром большинства подтипов гриппа А являются дикие водоплавающие птицы; [44] однако благодаря серии мутаций небольшая группа этих вирусов адаптировалась к заражению людей (и других животных). [46] Ключевым фактором, определяющим, может ли конкретный подтип гриппа А заразить людей, является его специфичность связывания. Птичий грипп А преимущественно связывается с рецепторами клеточной поверхности с терминальной α2,3-связанной сиаловой кислотой , тогда как человеческий грипп А преимущественно связывается с рецепторами клеточной поверхности с терминальной α2,6-связанной сиаловой кислотой. Путем мутации некоторые вирусы птичьего гриппа А успешно изменили свою специфичность связывания с α2,3- на α2,6-связанную сиаловую кислоту. [47] Однако, чтобы появиться у человека, вирусы птичьего гриппа А должны также адаптировать свои РНК-полимеразы для функционирования в клетках млекопитающих. [48] а также мутации для обеспечения стабильности в кислых дыхательных путях человека. [49]
После адаптации и смены хозяина вирусы гриппа А могут вызывать эпидемии и пандемии у людей. Незначительные изменения в структуре HA и NA ( антигенный дрейф ) происходят часто, что позволяет вирусу вызывать повторяющиеся вспышки (например, сезонный грипп ), уклоняясь от иммунного распознавания. [43] Серьезные изменения в структуре HA и NA ( антигенный сдвиг ), вызванные генетической реассортацией между различными подтипами гриппа А (например, между подтипами человека и животных), могут вместо этого вызывать крупные региональные/глобальные пандемии . [43] Из-за появления у человека антигенно различных штаммов гриппа А четыре пандемии гриппа . только в ХХ веке произошло [50]
Кроме того, хотя вирусы гриппа А животных (например, свиного гриппа ) отличаются от вирусов гриппа человека, они все же могут вызывать зоонозную инфекцию у людей. Эти инфекции в основном приобретаются в результате прямого контакта с инфицированными животными или загрязненной окружающей средой, но не приводят к эффективной передаче инфекции от человека к человеку; примеры этого включают грипп H5N1 и грипп H7N9 . [44]
SARS-CoV-1
[ редактировать ]
В 2002 году из зоонозного резервуара вышел высокопатогенный штамм SARS-CoV (коронавирус тяжелого острого респираторного синдрома); во всем мире было инфицировано около 8000 человек, а уровень смертности среди пожилых людей приближался к 50% и более. [51] Поскольку SARS-CoV-1 является наиболее заразным после появления симптомов, введение строгих мер общественного здравоохранения эффективно остановило эпидемию. [51] Считается, что естественным резервуарным хозяином SARS-CoV-1 являются подковоносы , хотя вирус также был идентифицирован у нескольких мелких хищников (например, пальмовых цивет и енотовидных собак ). Считается, что появлению SARS-CoV-1 способствовали китайские влажные рынки, на которых циветты, положительные по вирусу, выступали в качестве промежуточных хозяев и передавали SARS-CoV-1 людям (и другим видам). [51] [52] Однако более поздний анализ показывает, что SARS-CoV-1 мог напрямую перейти от летучих мышей к человеку с последующей перекрестной передачей между людьми и циветами. [51]
Чтобы инфицировать на поверхности шипа клетки, SARS-CoV-1 использует гликопротеин хозяина для распознавания и связывания с ACE-2 , который он использует в качестве рецептора входа в клетку; [51] развитие этой характеристики имело решающее значение для того, чтобы SARS-CoV-1 «перепрыгнул» от летучих мышей к другим видам.
БВРС-КоВ
[ редактировать ]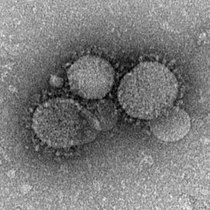
Впервые зарегистрированный в 2012 году, MERS-CoV (коронавирус ближневосточного респираторного синдрома) знаменует собой второе известное заражение человека высокопатогенным коронавирусом из зоонозного резервуара. Уровень смертности от этого нового вируса составляет примерно 35%, при этом 80% всех случаев зарегистрировано в Саудовской Аравии. [53] Хотя MERS-CoV, скорее всего, возник у летучих мышей, [54] Верблюды-дромадеры рассматривались как возможные промежуточные хозяева. Считается, что MERS-CoV циркулирует у этих млекопитающих уже более 20 лет. [54] Считается, что новые методы разведения верблюдов привели к распространению БВРС-КоВ на людей. [55] Исследования показали, что люди могут заразиться БВРС-КоВ через прямой или косвенный контакт с инфицированными дромадерами, при этом передача вируса от человека к человеку ограничена. [53]
БВРС-КоВ проникает в клетку, используя белок с шипами на поверхности для связывания с поверхностным рецептором DPP4 хозяина ; основной субдомен этого поверхностного белка с шипами имеет сходство с субдоменом SARS-CoV, но его рецептор-связывающий субдомен (RBSD) значительно отличается. [54]
Болезнь голубого языка
[ редактировать ]
Болезнь блютанг – незаразное трансмиссивное заболевание, вызываемое вирусом блютанга, поражающее виды жвачных животных (особенно овец ). [56] Изменение климата привело к возникновению и глобальному распространению этого заболевания из-за его воздействия на распространение переносчиков. Естественным переносчиком вируса блютанга является африканская мошка C. imicola , которая обычно обитает в Африке и субтропической Азии. Однако глобальное потепление расширило географический ареал C. imicola , так что теперь он перекрывается с другим переносчиком ( C. pulcaris или C. obsoletus ) с гораздо более северным географическим ареалом. Это изменение позволило вирусу блютанга перейти вектор, вызывая тем самым распространение болезни блютанга на север в Европу. [57]
См. также
[ редактировать ]- Биобезопасность
- Новые инфекционные заболевания
- Открытие возбудителей болезней
- Биологическое сдерживание
- Вирусные квазивиды
Ссылки
[ редактировать ]- ^ Jump up to: а б Голландский диджей (февраль 1998 г.). «Новые вирусы». Современное мнение в педиатрии . 10 (1): 34–40. дои : 10.1097/00008480-199802000-00007 . ПМИД 9529635 .
- ^ Дево, Калифорния (февраль 2012 г.). «Новые и вновь возникающие вирусы: глобальная проблема, иллюстрируемая вспышками вируса Чикунгунья» . Всемирный журнал вирусологии . 1 (1): 11–22. дои : 10.5501/wjv.v1.i1.11 . ПМЦ 3782263 . ПМИД 24175207 .
- ^ Jump up to: а б с д и ж г час Линдал Дж. Ф., Грейс Д. (2015). «Последствия действий человека на риски инфекционных заболеваний: обзор» . Экология и эпидемиология инфекций . 5 (1): 30048. Бибкод : 2015InfEE...530048L . дои : 10.3402/iee.v5.30048 . ПМЦ 4663196 . ПМИД 26615822 .
- ^ Моренс Д.М., Фаучи А.С. (сентябрь 2020 г.). «Новые пандемические заболевания: как мы дошли до COVID-19» . Клетка . 182 (5): 1077–1092. дои : 10.1016/j.cell.2020.08.021 . ПМЦ 7428724 . ПМИД 32846157 .
- ^ Чжэн Дж (2020). «SARS-CoV-2: новый коронавирус, вызывающий глобальную угрозу» . Международный журнал биологических наук . 16 (10): 1678–1685. дои : 10.7150/ijbs.45053 . ПМК 7098030 . ПМИД 32226285 .
- ^ Jump up to: а б Холмс Э.К., Дудас Г., Рамбо А., Андерсен К.Г. (октябрь 2016 г.). «Эволюция вируса Эбола: выводы из эпидемии 2013-2016 годов» . Природа . 538 (7624): 193–200. Бибкод : 2016Natur.538..193H . дои : 10.1038/nature19790 . ПМК 5580494 . ПМИД 27734858 .
- ^ Вэй П., Цай З., Хуа Дж., Ю В., Чен Дж., Кан К. и др. (2016). «Боль и выгода от опыта Китая в борьбе с возникающими эпидемиями: от атипичной пневмонии до H7N9» . БиоМед Исследования Интернэшнл . 2016 : 5717108. doi : 10.1155/2016/5717108 . ПМЦ 4971293 . ПМИД 27525272 .
- ^ Смит Г.Дж., Виджайкришна Д., Бахл Дж., Лисетт С.Дж., Воробей М., Пибус О.Г. и др. (июнь 2009 г.). «Происхождение и эволюционная геномика эпидемии гриппа А свиного происхождения H1N1 в 2009 году» . Природа . 459 (7250): 1122–5. Бибкод : 2009Natur.459.1122S . дои : 10.1038/nature08182 . ПМИД 19516283 .
- ^ Таубенбергер Дж. К., Моренс Д. М. (январь 2006 г.). «Грипп 1918 года: мать всех пандемий» . Новые инфекционные заболевания . 12 (1): 15–22. дои : 10.3201/eid1201.050979 . ПМЦ 3291398 . ПМИД 16494711 .
- ^ Jump up to: а б Эйдсон М. «Зоонозные болезни» . Британника . Проверено 16 апреля 2020 г.
- ^ Майкл Порта, изд. (2008). Словарь эпидемиологии . Издательство Оксфордского университета, США. п. 78. ИСБН 978-0-19-971815-3 .
- ^ Фрейзер-Белл С (2019). «Глобальное возрождение кори – обновленная информация 2019 г.» . Глобальная биобезопасность . 1 (3). дои : 10.31646/gbio.43 . ISSN 2652-0036 .
- ^ Вулхаус М., Скотт Ф., Хадсон З., Хоуи Р., Чейз-Топпинг М. (октябрь 2012 г.). «Человеческие вирусы: открытие и возникновение» . Философские труды Лондонского королевского общества. Серия Б, Биологические науки . 367 (1604): 2864–71. дои : 10.1098/rstb.2011.0354 . ПМЦ 3427559 . ПМИД 22966141 .
- ^ Леланд Д.С., Гиноккио CC (январь 2007 г.). «Роль клеточной культуры для обнаружения вирусов в век технологий» . Обзоры клинической микробиологии . 20 (1): 49–78. дои : 10.1128/CMR.00002-06 . ПМК 1797634 . ПМИД 17223623 .
- ^ Кеннеди Дж.Л., Тернер Р.Б., Брасиале Т., Хейманн П.В., Бориш Л. (июнь 2012 г.). «Патогенез риновирусной инфекции» . Современное мнение в вирусологии . 2 (3): 287–93. дои : 10.1016/j.coviro.2012.03.008 . ПМЦ 3378761 . ПМИД 22542099 .
- ^ Хоутон М. (ноябрь 2009 г.). «Долгий и извилистый путь, ведущий к идентификации вируса гепатита С» . Журнал гепатологии . 51 (5): 939–48. дои : 10.1016/j.jhep.2009.08.004 . ПМИД 19781804 .
- ^ де Грааф М., Остерхаус А.Д., Фушье Р.А., Холмс Э.К. (декабрь 2008 г.). «Эволюционная динамика метапневмовирусов человека и птиц» . Журнал общей вирусологии . 89 (Часть 12): 2933–2942. дои : 10.1099/vir.0.2008/006957-0 . ПМИД 19008378 .
- ^ Jump up to: а б Woolhouse ME , Gowtage-Sequeria S (декабрь 2005 г.). «Круг хозяев, а также возникающие и вновь возникающие патогены» . Новые инфекционные заболевания . 11 (12): 1842–7. дои : 10.3201/eid1112.050997 . ПМЦ 3367654 . ПМИД 16485468 .
- ^ Крузе Х., Киркемо А.М., Ханделанд К. (декабрь 2004 г.). «Дикая природа как источник зоонозных инфекций» . Новые инфекционные заболевания . 10 (12): 2067–72. дои : 10.3201/eid1012.040707 . ПМЦ 3323390 . ПМИД 15663840 .
- ^ Jump up to: а б Доминго Э (2010). «Механизмы возникновения вирусов» . Ветеринарное исследование . 41 (6): 38. doi : 10.1051/vetres/2010010 . ПМЦ 2831534 . ПМИД 20167200 .
- ^ Баум С.Г. (2008). «Зооноз – с такими друзьями, кому нужны враги?» . Труды Американской клинической и климатологической ассоциации . 119 : 39–51, обсуждение 51–2. ПМК 2394705 . ПМИД 18596867 .
- ^ Пэрриш CR, Холмс EC, Моренс DM, Парк EC, Берк DS, Калишер CH и др. (сентябрь 2008 г.). «Межвидовая передача вируса и возникновение новых эпидемических заболеваний» . Обзоры микробиологии и молекулярной биологии . 72 (3): 457–70. дои : 10.1128/MMBR.00004-08 . ПМК 2546865 . ПМИД 18772285 .
- ^ ИНСТИТУТ СПИДА. «Откуда взялся ВИЧ?» . ИНСТИТУТ СПИДА . Проверено 16 апреля 2020 г.
- ^ Национальный научный фонд. «Ночная жизнь: почему нам нужны летучие мыши постоянно, а не только на Хэллоуин» . Национальный научный фонд . Проверено 14 апреля 2020 г.
- ^ Ши Зи (август 2013 г.). «Новые инфекционные заболевания, связанные с вирусами летучих мышей» . Наука Китай Науки о жизни . 56 (8): 678–82. дои : 10.1007/s11427-013-4517-x . ПМК 7088756 . ПМИД 23917838 .
- ^ Jump up to: а б Субудхи С., Рапин Н., Мисра В. (2019). «Модуляция иммунной системы и устойчивость вируса у летучих мышей: понимание распространения вируса» . Вирусы . 11 (2): 192. дои : 10.3390/v11020192 . ПМК 6410205 . ПМИД 30813403 .
- ^ О'Ши Т.Дж., Крайан П.М., Каннингем А.А., Фукс А.Р., Хейман Д.Т., Луис А.Д. и др. (май 2014 г.). «Полёт летучих мышей и зоонозные вирусы» . Новые инфекционные заболевания . 20 (5): 741–5. дои : 10.3201/eid2005.130539 . ПМЦ 4012789 . ПМИД 24750692 .
- ^ Ван Л.Ф., Андерсон Д.Э. (февраль 2019 г.). «Вирусы у летучих мышей и потенциальное распространение на животных и людей» . Современное мнение в вирусологии . 34 : 79–89. дои : 10.1016/j.coviro.2018.12.007 . ПМК 7102861 . ПМИД 30665189 .
- ^ Jump up to: а б с Кузьмин И.В., Бозик Б., Гуальярдо С.А., Кункель Р., Шак Дж.Р., Тонг С., Рупрехт К.Э. (июнь 2011 г.). «Летучие мыши, новые инфекционные заболевания и новый взгляд на парадигму бешенства» . Журнал «Новые угрозы здоровью» . 4 : 7159. дои : 10.3402/ehtj.v4i0.7159 . ПМК 3168224 . ПМИД 24149032 .
- ^ Jump up to: а б Калишер Ч. , Чайлдс Дж.Э., Филд Х.Э., Холмс К.В., Шоунц Т. (июль 2006 г.). «Летучие мыши: важные резервуарные хозяева новых вирусов» . Обзоры клинической микробиологии . 19 (3): 531–45. дои : 10.1128/CMR.00017-06 . ПМК 1539106 . ПМИД 16847084 .
- ^ Вулхаус М., Гонт Э. (2007). «Экологическое происхождение новых патогенов человека». Критические обзоры по микробиологии . 33 (4): 231–42. дои : 10.1080/10408410701647560 . ПМИД 18033594 . S2CID 19213392 .
- ^ фон Чефалвай С. (2023), «Хост-вектор и многохостовые системы» , Вычислительное моделирование инфекционных заболеваний , Elsevier, стр. 121–149, doi : 10.1016/b978-0-32-395389-4.00013-x , ISBN 978-0-323-95389-4 , получено 2 марта 2023 г.
- ^ Пеналапати Дж., Свартаут Дж., Делахой М.Дж., Макалили Л., Водник Б., Леви К., Фриман М.К. (октябрь 2017 г.). «Воздействие фекалий животных и здоровье человека: систематический обзор и предлагаемые приоритеты исследований» . Экологические науки и технологии . 51 (20): 11537–11552. Бибкод : 2017EnST...5111537P . doi : 10.1021/acs.est.7b02811 . ПМЦ 5647569 . ПМИД 28926696 .
- ^ Нейдеруд CJ (2015). «Как урбанизация влияет на эпидемиологию возникающих инфекционных заболеваний» . Экология и эпидемиология инфекций . 5 (1): 27060. Бибкод : 2015InfEE...527060N . дои : 10.3402/iee.v5.27060 . ПМК 4481042 . ПМИД 26112265 .
- ^ Раппол Дж. Х., Дерриксон С. Р., Хубалек З. (2000). «Перелетные птицы и распространение вируса Западного Нила в Западном полушарии» . Новые инфекционные заболевания . 6 (4): 319–28. дои : 10.3201/eid0604.000401 . ПМК 2640881 . ПМИД 10905964 .
- ^ Jump up to: а б с д Рахман М.Т., Собур М.А., Ислам М.С. и др. (сентябрь 2020 г.). «Зоонозные заболевания: этиология, влияние и борьба» . Микроорганизмы . 8 (9): 1405. doi : 10.3390/microorganisms8091405 . ПМЦ 7563794 . ПМИД 32932606 .
- ^ фон Чефалвай С. (2023), «Хост-вектор и многохостовые системы» , Вычислительное моделирование инфекционных заболеваний , Elsevier, стр. 121–149, doi : 10.1016/b978-0-32-395389-4.00013-x , ISBN 978-0-323-95389-4 , получено 2 марта 2023 г.
- ^ Домингес-Андрес Х., Netea MG (декабрь 2019 г.). «Влияние исторических миграций и эволюционных процессов на иммунитет человека» . Тенденции в иммунологии . 40 (12): 1105–1119. дои : 10.1016/j.it.2019.10.001 . ПМК 7106516 . ПМИД 31786023 .
- ^ Лонгдон Б., Хэдфилд Дж.Д., Дэй Дж.П., Смит С.С., МакГонигл Дж.Э., Когни Р. и др. (март 2015 г.). «Причины и последствия изменения вирулентности в результате смены хозяина возбудителя» . ПЛОС Патогены . 11 (3): e1004728. дои : 10.1371/journal.ppat.1004728 . ПМК 4361674 . ПМИД 25774803 .
- ^ Клейвилл Л.Р. (октябрь 2011 г.). «Обновленная информация о гриппе: обзор доступных в настоящее время вакцин» . П&Т . 36 (10): 659–84. ПМЦ 3278149 . ПМИД 22346299 .
- ^ ЮНИСЕФ. «Грипп» . ЮНИСЕФ . Проверено 14 апреля 2020 г.
- ^ Jump up to: а б с Всемирная организация здравоохранения. «Грипп» . Всемирная организация здравоохранения. Архивировано из оригинала 17 июня 2013 года . Проверено 13 апреля 2020 г. .
- ^ Jump up to: а б с д Всемирная организация здравоохранения. «Грипп (птичий и другие зоонозные)» . ВОЗ . Проверено 13 апреля 2020 г. .
- ^ Центры по контролю и профилактике заболеваний (18 ноября 2019 г.). «Грипп (Грипп)» . CDC . Проверено 13 апреля 2020 г. .
- ^ Берд-Леотис Л., Каммингс Р.Д., Штайнхауэр Д.А. (июль 2017 г.). «Взаимодействие между рецептором хозяина и гемагглютинином и нейраминидазой вируса гриппа» . Международный журнал молекулярных наук . 18 (7): 1541. doi : 10.3390/ijms18071541 . ПМК 5536029 . ПМИД 28714909 .
- ^ Льюис Д.Б. (2006). «Птичий грипп — человеческий грипп». Ежегодный обзор медицины . 57 : 139–54. дои : 10.1146/annurev.med.57.121304.131333 . ПМИД 16409141 .
- ^ Лонг Дж.С., Джотис Э.С., Монкорже О., Фризе Р., Мистри Б., Джеймс Дж. и др. (январь 2016 г.). «Видовые различия в ANP32A лежат в основе ограничения полимеразы вируса гриппа А у хозяина» . Природа . 529 (7584): 101–4. Бибкод : 2016Natur.529..101L . дои : 10.1038/nature16474 . ПМЦ 4710677 . ПМИД 26738596 .
- ^ Ди Лелла С., Херрманн А., Майр К.М. (июнь 2016 г.). «Модуляция стабильности pH гемагглютинина вируса гриппа: стратегия адаптации клетки-хозяина» . Биофизический журнал . 110 (11): 2293–2301. Бибкод : 2016BpJ...110.2293D . дои : 10.1016/j.bpj.2016.04.035 . ПМК 4906160 . ПМИД 27276248 .
- ^ Александр DJ (2006). «Вирусы птичьего гриппа и здоровье человека». Разработки в области биологических препаратов . 124 : 77–84. ПМИД 16447497 .
- ^ Jump up to: а б с д и Боллес М., Дональдсон Э., Барик Р. (декабрь 2011 г.). «SARS-CoV и эмерджентные коронавирусы: вирусные детерминанты межвидовой передачи» . Современное мнение в вирусологии . 1 (6): 624–34. дои : 10.1016/j.coviro.2011.10.012 . ПМЦ 3237677 . ПМИД 22180768 .
- ^ Ван Л.Ф., Eaton BT (2007). «Летучие мыши, циветты и появление атипичной пневмонии». Дикая природа и новые зоонозные заболевания: биология, обстоятельства и последствия межвидовой передачи . Актуальные темы микробиологии и иммунологии. Том. 315. С. 325–44. дои : 10.1007/978-3-540-70962-6_13 . ISBN 978-3-540-70961-9 . ПМК 7120088 . ПМИД 17848070 .
- ^ Jump up to: а б ВОЗ. «Коронавирус ближневосточного респираторного синдрома (MERS-CoV)» . ВОЗ . Проверено 15 апреля 2020 г.
- ^ Jump up to: а б с Шариф-Якан А., Кандж С.С. (декабрь 2014 г.). «Появление MERS-CoV на Ближнем Востоке: происхождение, передача, лечение и перспективы» . ПЛОС Патогены . 10 (12): e1004457. дои : 10.1371/journal.ppat.1004457 . ПМЦ 4256428 . ПМИД 25474536 .
- ^ Фараг Э., Сиккема Р.С., Винкс Т., Ислам М.М., Нур М., Аль-Ромайхи Х. и др. (декабрь 2018 г.). «Стимулы возникновения MERS-CoV в Катаре» . Вирусы . 11 (1): 22. дои : 10.3390/v11010022 . ПМК 6356962 . ПМИД 30602691 .
- ^ Центр продовольственной безопасности и общественного здравоохранения ИС. «Блутонг» (PDF) . ЦФСПХ . Проверено 14 апреля 2020 г.
- ^ Пёрс Б.В., Меллор П.С., Роджерс Д.Д., Сэмюэл А.Р., Мертенс П.П., Бэйлис М. (февраль 2005 г.). «Изменение климата и недавнее появление блютанга в Европе». Обзоры природы. Микробиология . 3 (2): 171–81. дои : 10.1038/nrmicro1090 . ПМИД 15685226 . S2CID 62802662 .
Дальнейшее чтение
[ редактировать ]- Артика И.М., Маруф К.Н. (май 2017 г.). «Лабораторная биобезопасность при обращении с новыми вирусами» . Азиатско-Тихоокеанский журнал тропической биомедицины . 7 (5): 483–491. дои : 10.1016/j.apjtb.2017.01.020 . ПМК 7103938 . ПМИД 32289025 .
Внешние ссылки
[ редактировать ]- «Новые вирусы» . МикробиологияBytes . 2007. Архивировано из оригинала 24 февраля 2007 г.
- «Национальный центр новых и зоонозных инфекционных заболеваний (NCEZID)» . 19 ноября 2021 г.