гидроперекись

Гидропероксиды или пероксолы представляют собой соединения формы ROOH, где R означает любую группу, обычно органическую , которая содержит гидроперокси- функциональную группу ( −ОХ ). Гидропероксид также относится к гидропероксид-аниону ( − OOH ) и его соли , а нейтральный гидропероксильный радикал (•OOH) состоит из несвязывающей гидропероксигруппы. Когда R является органическим, соединения называются органическими гидропероксидами . Такие соединения представляют собой разновидность органических пероксидов , имеющих формулу ROOR. Органические гидропероксиды могут намеренно или непреднамеренно инициировать взрывную полимеризацию материалов с ненасыщенными химическими связями . [ 1 ]
Характеристики
[ редактировать ]The O-O Длина связи в пероксидах составляет около 1,45 Å , а Углы R-O-O (R = H , C ) около 110° ( водоподобные ). Характерно, что C-O-O-H Двугранные углы составляют около 120 °. Связь O-O относительно слабая, с энергией диссоциации связи 45–50 ккал / моль (190–210 кДж / моль), что менее половины прочности связи. С-С , C−H и С-О связи. [ 2 ] [ 3 ]
Гидропероксиды обычно более летучи, чем соответствующие спирты :
- трет -BuOOH ( точка кипения 36 °C) и трет -BuOH (точка кипения 82–83 °C)
- CH 3 OOH (точка кипения 46 °C) по сравнению CH 3 OH (точка кипения 65 °C)
- гидроперекись кумола (точка кипения 153 °C) и кумиловый спирт (точка кипения 202 °C)
Разные реакции
[ редактировать ]Гидроперекиси имеют слабую кислотность . Диапазон обозначен цифрой 11,5 для CH 3 OOH до 13,1 для Ф 3 СООН . [ 4 ]
Гидроперекиси можно восстановить до спиртов с помощью алюмогидрида лития , как описано в этом идеализированном уравнении:
- 4 ROOH + LiAlH 4 → LiAlO 2 + 2 H 2 O + 4 ROOH
Эта реакция лежит в основе методов анализа органических пероксидов. [ 5 ] Другим способом оценки содержания надкислот и пероксидов является объемное титрование алкоголятами, например этилатом натрия . [ 6 ] Эфиры фосфита и третичные фосфины также способствуют восстановлению:
- РОХ + ПР 3 → ОПР 3 + РОХ
Использование
[ редактировать ]Прекурсоры эпоксидов
[ редактировать ]«Самым важным синтетическим применением алкилгидропероксидов, без сомнения, является катализируемое металлами эпоксидирование алкенов». В процессе Halcon трет-бутилгидропероксид (TBHP) используется для производства оксида пропилена . [ 7 ]
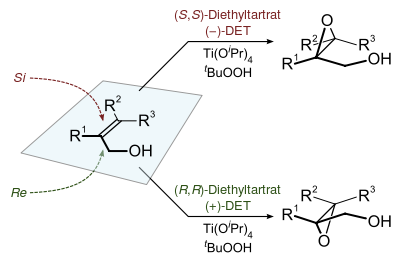
Особый интерес представляют хиральные эпоксиды , полученные с использованием гидропероксидов в качестве реагентов при эпоксидировании по Шарплессу . [ 8 ]
Производство циклогексанона и капролактона
[ редактировать ]Гидропероксиды являются промежуточными продуктами производства многих органических соединений в промышленности. Например, катализируемое кобальтом окисление циклогексана в циклогексанон : [ 9 ]
- C 6 H 12 + O 2 → (CH 2 ) 5 C=O + H 2 O
Олифы , содержащиеся во многих красках и лаках, действуют за счет образования гидропероксидов.
Хок-процессы
[ редактировать ]
соединения с аллильными и бензильными связями C-H. Особенно чувствительны к оксигенированию [ 10 ] Такая реакционная способность используется в промышленности в больших масштабах для производства фенола с помощью кумолового процесса или процесса Хока для получения его кумола и промежуточных продуктов гидропероксида кумола . [ 11 ] Такие реакции основаны на радикальных инициаторах , которые реагируют с кислородом с образованием промежуточного соединения, отрывающего атом водорода от слабой связи CH. Образующийся радикал связывается O 2 , с образованием гидропероксила (ROO•), который затем продолжает цикл отрыва атома водорода. [ 12 ]

Формирование
[ редактировать ]Путем автоокисления
[ редактировать ]Наиболее важные (в коммерческом смысле) пероксиды получают путем автоокисления — прямой реакции O 2 с углеводородом. Автоокисление — радикальная реакция, которая начинается с отрыва атома H от относительно слабой связи CH . Важные соединения, полученные таким способом, включают гидропероксид трет-бутила , гидропероксид кумола и гидропероксид этилбензола : [ 7 ]
- R−H + O 2 → R−OOH
Реакция автоокисления также наблюдается с обычными эфирами , такими как диэтиловый эфир , диизопропиловый эфир , тетрагидрофуран и 1,4-диоксан . Показательным продуктом является пероксид диэтилового эфира . Такие соединения могут привести к серьезному взрыву при перегонке. [ 12 ] Чтобы свести к минимуму эту проблему, коммерческие образцы ТГФ часто ингибируют бутилированным гидрокситолуолом (БНТ). Перегонку ТГФ досуха избегают, поскольку взрывоопасные пероксиды концентрируются в остатке.
Хотя гидропероксиды эфира часто образуются случайно (т.е. в результате автоокисления), их можно получить с высоким выходом катализируемым кислотой добавлением пероксида водорода к виниловым эфирам: [ 13 ]
- C 2 H 5 OCH=CH 2 + H 2 O 2 → C 2 H 5 OCH(OOH)CH 3
Из перекиси водорода
[ редактировать ]Многие промышленные пероксиды производятся с использованием перекиси водорода. Реакции с альдегидами и кетонами в зависимости от условий дают ряд соединений. Конкретные реакции включают присоединение перекиси водорода по двойной связи C=O:
- R 2 C=O + H 2 O 2 → R 2 C(OH)OOH
В некоторых случаях эти гидропероксиды превращаются в циклические дипероксиды:
- [R 2 C(O 2 H)] 2 O 2 → [R 2 C] 2 (O 2 ) 2 + 2 H 2 O
Добавление этого исходного аддукта ко второму эквиваленту карбонила:
- R 2 C=O + R 2 C(OH)OOH → [R 2 C(OH)] 2 O 2
Дальнейшая замена спиртовых групп:
- [R 2 C(OH)] 2 O 2 + 2 H 2 O 2 → [R 2 C(O 2 H)] 2 O 2 + 2 H 2 O
Трифенилметанол реагирует с перекисью водорода, образуя необычайно стабильный гидроперекись. Ф 3 СООН . [ 14 ]
Природные гидропероксиды
[ редактировать ]Многие гидропероксиды производятся из жирных кислот, стероидов и терпенов. На биосинтез этих видов сильно влияют ферменты.

Ссылки
[ редактировать ]- ^ Кленк, Герберт; Гетц, Питер Х.; Зигмайер, Райнер; Майр, Уилфрид. «Перекисные соединения органические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a19_199 . ISBN 978-3527306732 .
- ^ Бах, Роберт Д.; Айяла, Филипп Ю.; Шлегель, Х.Б. (1996). «Переоценка энергии диссоциации связей пероксидов. Исследование ab initio ». Дж. Ам. хим. Соц. 118 (50): 12758–12765. дои : 10.1021/ja961838i .
- ^ Отто Экснер (1983). «Стереохимические и конформационные аспекты пероксисоединений». У Саула Патая (ред.). Химия функциональных групп ПАТАИ . Уайли. стр. 85–96. дои : 10.1002/9780470771730.ch2 . ISBN 978-0-470-77173-0 .
- ^ Кленк, Герберт; Гетц, Питер Х.; Зигмайер, Райнер; Майр, Уилфрид. «Перекисные соединения органические». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a19_199 . ISBN 978-3527306732 .
- ^ Хигучи, Т.; Цук, Дональд Антон (1951). «Поведение некоторых соединений как индикаторов при титровании функциональных групп литий-алюминийгидридом». Журнал Американского химического общества . 73 (6): 2676. doi : 10.1021/ja01150a073 .
- ^ Мартин, Эй Джей (1957). «Потенциометрическое титрование гидроперекиси и надкислоты в безводном этилендиамине». Аналитическая химия . 29 : 79–81. дои : 10.1021/ac60121a022 .
- ^ Jump up to: а б Роджер А. Шелдон (1983). Патай, Саул (ред.). Синтез и применение гидропероксидов и диалкилпероксидов . Химия функциональных групп ПАТАИ. Джон Уайли и сыновья. дои : 10.1002/9780470771730.ch6 .
- ^ Хилл, Дж. Г.; Шарплесс, КБ ; Экзон, СМ; Реженье, Р. (1985). «Энантиоселективное эпоксидирование аллиловых спиртов: (2s,3s)-3-пропилоксиранметанол». Орг. Синтез. 63 : 66. дои : 10.15227/orgsyn.063.0066 .
- ^ Майкл Т. Массер (2005). «Циклогексанол и Циклогексанон». Энциклопедия промышленной химии Ульмана . Вайнхайм: Wiley-VCH. дои : 10.1002/14356007.a08_217 . ISBN 978-3527306732 .
- ^ Найт, HB; Сверн, Дэниел (1954). «Гидропероксид тетралина». Орг. Синтез . 34 : 90. дои : 10.15227/orgsyn.034.0090 . .
- ^ Брюкнер, Р. Механизмы реакции: органические реакции, стереохимия, современные методы синтеза , стр. 41–42, Spektrum Akademischer Verlag, Мюнхен, 2004, ISBN 3-8274-1579-9 (на немецком языке)
- ^ Jump up to: а б Хайнц Г.О. Беккер Органикум , Wiley-VCH, 2001 г., ISBN 3-527-29985-8 стр. 206–207.
- ^ Милас, Николас А.; Пилер, Роберт Л.; Магели, Орвилл Л. (1954). «Органические пероксиды. XIX. α-гидропероксиэфиры и родственные пероксиды». Журнал Американского химического общества . 76 (9): 2322–2325. дои : 10.1021/ja01638a012 .
- ^ Брайант Э. Росситер и Майкл О. Фредерик «Трифенилметилгидропероксид» Энциклопедия реагентов для органического синтеза E-EROS, 2013. два : 10.1002/047084289X.rt363m.pub2
- ^ Мацуи К (2006). «Летучие вещества зеленых листьев: гидропероксидлиазный путь метаболизма оксилипина». Современное мнение в области биологии растений . 9 (3): 274–80. дои : 10.1016/j.pbi.2006.03.002 . ПМИД 16595187 .
