Hsp70
| Белок Hsp70 | |||
|---|---|---|---|
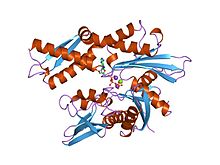 Структура АТФазного фрагмента родственного белка теплового шока 70К. [ 1 ] | |||
| Идентификаторы | |||
| Символ | HSP70 | ||
| Пфам | PF00012 | ||
| Пфам Клан | CL0108 | ||
| ИнтерПро | ИПР013126 | ||
| PROSITE | PDOC00269 | ||
| ОБЛАСТЬ ПРИМЕНЕНИЯ 2 | 3hsc / SCOPe / СУПФАМ | ||
| |||

Белки теплового шока массой 70 килодальтон ( Hsp70 или DnaK ) представляют собой семейство консервативных, повсеместно экспрессируемых белков теплового шока . Белки сходной структуры существуют практически во всех живых организмах. Внутриклеточно локализованные Hsp70 являются важной частью клеточного механизма сворачивания белков , выполняют функции шаперона и помогают защитить клетки от неблагоприятного воздействия физиологических стрессов . [ 2 ] [ 3 ] Кроме того, мембраносвязанные Hsp70 были идентифицированы как потенциальная мишень для лечения рака. [ 4 ] и их внеклеточно локализованные аналоги были идентифицированы как имеющие как мембраносвязанные, так и безмембранные структуры. [ 5 ]
Открытие
[ редактировать ]Члены семейства Hsp70 очень сильно активируются тепловым стрессом и токсичными химическими веществами, особенно тяжелыми металлами, такими как мышьяк, кадмий, медь, ртуть и т. д. Тепловой шок был первоначально обнаружен Ферруччо Ритосса в 1960-х годах, когда работник лаборатории случайно усилил инкубацию. температура дрозофилы (дрозофилы). Исследуя хромосомы, Ритосса обнаружил «паттерн вздутия», который указывал на повышенную транскрипцию гена неизвестного белка. [ 6 ] [ 7 ] Позже это было описано как «реакция на тепловой шок», а белки были названы «белками теплового шока» (Hsps).
Структура
[ редактировать ]
Белки Hsp70 имеют три основных функциональных домена :
- N-концевой АТФазы домен – связывает АТФ ( аденозинтрифосфат ) и гидролизует его до АДФ ( аденозиндифосфат ). NBD (нуклеотидсвязывающий домен) состоит из двух долей с глубокой щелью между ними, в нижней части которой связываются нуклеотиды (АТФ и АДФ). Обмен АТФ и АДФ приводит к конформационным изменениям в двух других доменах.
- Субстрат-связывающий домен – состоит из субдомена β-листа массой 15 кДа и спирального субдомена массой 10 кДа. Субдомен β-листа состоит из скрученных β-листов с выступающими вверх петлями, образующими типичный β-цилиндр , которые окружают пептидный остов субстрата. SBD содержит бороздку, имеющую сродство к нейтральным гидрофобным аминокислотным остаткам. Бороздка достаточно длинная, чтобы взаимодействовать с пептидами длиной до семи остатков.
- С-концевой домен , богатый альфа-спиральной структурой, действует как «крышка» для домена, связывающего субстрат. Спиральный субдомен состоит из пяти спиралей, две из которых упакованы с двух сторон субдомена β-листа, стабилизируя внутреннюю структуру. Кроме того, одна из спиралей образует солевой мостик и несколько водородных связей с внешними петлями, тем самым закрывая субстрат-связывающий карман как крышку. Три спирали в этом домене образуют еще одно гидрофобное ядро, которое может служить стабилизацией «крышки». Когда белок Hsp70 связан с АТФ, крышка открыта, и пептиды связываются и высвобождаются относительно быстро. Когда белки Hsp70 связываются с ADP, крышка закрывается, и пептиды прочно связываются с доменом связывания субстрата. [ 9 ]

Фосфорилирование белков, посттрансляционная модификация, помогает регулировать функцию белков и включает фосфорилирование аминокислот с гидроксильными группами в их боковых цепях (у эукариот). Аминокислоты серин, треонин и тирозин являются общими мишенями фосфорилирования. Сравнительно недавно фосфорилирование Hsp70 стало предметом более пристального изучения в научной литературе. Публикация 2020 года предполагает, что фосфорилирование остатка серина между NBD и субстратсвязывающим доменом в дрожжевых Hsp70 приводит к резкому снижению нормальной реакции Hsp70 на тепловой шок. [ 10 ] Эта дезактивация посредством фосфорилирования белка является распространенным мотивом регуляции белка и демонстрирует, как относительно небольшие изменения в структуре белка могут иметь биологически значимые эффекты на функцию белка.
Функция
[ редактировать ]Система Hsp70 взаимодействует с расширенными пептидными сегментами белков, а также с частично свернутыми белками, вызывая агрегацию белков в ключевых путях подавления активности. [ 11 ] [ 8 ] Когда Hsp70 не взаимодействует с пептидом-субстратом, он обычно находится в связанном с АТФ состоянии. Hsp70 сам по себе характеризуется очень слабой АТФазной активностью, поэтому спонтанный гидролиз не происходит в течение многих минут. Когда вновь синтезированные белки выходят из рибосом , субстратсвязывающий домен Hsp70 распознает последовательности гидрофобных аминокислотных остатков и взаимодействует с ними. Это спонтанное взаимодействие обратимо, и в связанном с АТФ состоянии Hsp70 может относительно свободно связывать и высвобождать пептиды . Однако присутствие пептида в связывающем домене стимулирует АТФазную активность Hsp70, увеличивая обычно медленную скорость гидролиза АТФ. Когда АТФ гидролизуется до АДФ, карман связывания Hsp70 закрывается, прочно связывая теперь захваченную пептидную цепь. Дальнейшим ускорением гидролиза АТФ являются так называемые кошапероны J-домена: в первую очередь Hsp40 у эукариот и DnaJ у прокариот . Эти кошапероны резко повышают АТФазную активность Hsp70 в присутствии взаимодействующих пептидов.

Плотно связываясь с частично синтезированными пептидными последовательностями (неполными белками), Hsp70 предотвращает их агрегацию и потерю функциональности. После того, как весь белок синтезирован, фактор обмена нуклеотидов прокариотических GrpE , эукариотических BAG1 и HspBP1 ( среди идентифицированных ) стимулирует высвобождение АДФ и связывание свежего АТФ, открывая связывающий карман. Затем белок может свободно сворачиваться самостоятельно или передаваться другим шаперонам для дальнейшей обработки. [ 12 ] HOP ( Hsp70 /Hsp90 белок организующий ) может связываться как с Hsp70, так и с Hsp90 одновременно, и опосредует перенос пептидов от Hsp70 к Hsp90. [ 13 ]
Hsp70 также способствует трансмембранному транспорту белков, стабилизируя их в частично свернутом состоянии. Также известно, что он фосфорилирован. [ 14 ] который регулирует ряд его функций. [ 15 ] [ 16 ] [ 17 ]
Белки Hsp70 могут защищать клетки от термического или окислительного стресса. Эти стрессы обычно повреждают белки, вызывая частичное разворачивание и возможную агрегацию. Временно связываясь с гидрофобными остатками, подвергшимися стрессу, Hsp70 предотвращает агрегацию этих частично денатурированных белков и ингибирует их рефолдинг. Низкий уровень АТФ характерен для теплового шока, и устойчивое связывание рассматривается как подавление агрегации, тогда как восстановление после теплового шока включает связывание субстрата и циклический цикл нуклеотидов. У термофильного анаэроба ( Thermotoga maritima ) Hsp70 демонстрирует окислительно-восстановительное связывание с модельными пептидами, что указывает на второй способ регуляции связывания, основанный на окислительном стрессе.
Hsp70, по-видимому, способен участвовать в утилизации поврежденных или дефектных белков. Взаимодействие с CHIP ( карбоксильный конец H sp70 взаимодействующего белка позволяет ) – убиквитинлигазой E3 – Hsp70 клетки передавать белки по путям убиквитинирования и протеолиза . [ 18 ]
Наконец, помимо улучшения общей целостности белка, Hsp70 напрямую ингибирует апоптоз . [ 19 ] Одним из признаков апоптоза является высвобождение цитохрома с , который затем рекрутирует Apaf-1 и dATP/ATP в апоптосомный комплекс. Затем этот комплекс расщепляет прокаспазу-9, активируя каспазу-9 и, в конечном итоге, индуцируя апоптоз посредством активации каспазы 3 . Hsp70 ингибирует этот процесс, блокируя рекрутирование прокаспазы-9 в апоптосомный комплекс Apaf-1/dATP/цитохром c. Он не связывается напрямую с сайтом связывания прокаспазы-9, но, вероятно, вызывает конформационные изменения, которые делают связывание прокаспазы-9 менее благоприятным. Показано, что Hsp70 взаимодействует с сенсорным белком эндоплазматического ретикулума IRE1alpha, тем самым защищая клетки от апоптоза, вызванного стрессом ER. Это взаимодействие продлевало сплайсинг мРНК XBP-1, тем самым вызывая усиление транскрипции мишеней сплайсированного XBP-1, таких как EDEM1, ERdj4 и P58IPK, спасая клетки от апоптоза. [ 20 ] Другие исследования показывают, что Hsp70 может играть антиапоптотическую роль на других этапах, но не участвует в апоптозе, опосредованном Fas-лигандом (хотя Hsp 27 участвует). Таким образом, Hsp70 не только сохраняет важные компоненты клетки (белки), но и непосредственно сохраняет клетку в целом. Учитывая, что белки реакции на стресс (такие как Hsp70) развивались до апоптотического механизма, непосредственная роль Hsp70 в ингибировании апоптоза дает интересную эволюционную картину того, как более поздний (апоптотический) механизм адаптировался к предыдущему механизму (Hsps), тем самым выравнивая улучшенную целостность клеточных белков. с улучшенными шансами на выживание этой конкретной клетки.
У мышей экзогенный рекомбинантный человеческий Hsp70 (eHsp70), введенный интраназально , увеличивает продолжительность жизни. Хотя максимальная продолжительность жизни увеличилась лишь умеренно, общий уровень смертности у обработанных животных был намного ниже по сравнению с контрольной группой. Также такое лечение eHsp70 улучшает обучаемость и память мышей в старости, повышает их любознательность. [ 21 ]
Рак
[ редактировать ]Hsp70 сверхэкспрессируется при злокачественной меланоме. [ 22 ] и недостаточно экспрессируется при почечно-клеточном раке . [ 23 ] [ 24 ] В клеточной линии рака молочной железы (MCF7) было обнаружено, что не только Hsp90 взаимодействовал с рецептором эстрогена альфа (ERα), но также Hsp70-1 и Hsc70 также взаимодействовали с ERα. [ 25 ]
Учитывая роль белков теплового шока как древней защитной системы для стабилизации клеток и уничтожения старых и поврежденных клеток, эта система была использована раковыми клетками для стимулирования их роста. [ 26 ] В частности, было показано, что повышение Hsp70 ингибирует апоптоз раковых клеток. [ 27 ] и было показано, что повышение Hsp70 связано с эндометрием или непосредственно индуцирует его, [ 28 ] легкое, [ 29 ] толстая кишка, [ 30 ] простата, [ 31 ] и грудь [ 32 ] рак, а также лейкемия. [ 33 ] Hsp70 в раковых клетках может быть ответственен за онкогенез и прогрессирование опухоли, обеспечивая устойчивость к химиотерапии. Показано, что ингибирование Hsp70 уменьшает размер опухолей и может вызвать их полную регрессию. [ 34 ] Hsp70/Hsp90 является особенно привлекательной мишенью для терапии, поскольку регулируется путем ингибирования его АТФазной активности, в то время как другие HSP регулируются нуклеотидами. [ 35 ] Для Hsp70 было разработано несколько ингибиторов, которые в настоящее время проходят клинические испытания. [ 36 ] хотя на данный момент ингибиторы HSP90 оказались более успешными. [ 37 ] Кроме того, было показано, что Hsp70 является регулятором иммунной системы, активируя иммунную систему в качестве антигена. [ 38 ] Таким образом, полученный из опухоли Hsp70 был предложен в качестве потенциальной вакцины. [ 39 ] или путь к иммунотерапии. [ 40 ] Учитывая повышенную экспрессию Hsp70 при раке, его можно использовать в качестве биомаркера для прогноза рака, причем высокие уровни предвещают плохой прогноз. [ 41 ] Онкогенный механизм иллюстрирует, как внеклеточные везикулы, экспрессирующие HSP70, продуцируются пролиферативными клетками острого лимфобластного лейкоза и могут нацеливаться на здоровую систему кроветворения и подвергать ее риску во время развития лейкемии. [ 42 ]
Экспрессия в тканях кожи
[ редактировать ]Было показано, что как Hsp70, так и HSP47 экспрессируются в дерме и эпидермисе после лазерного облучения , а пространственные и временные изменения в характере экспрессии HSP определяют зону термического повреждения, индуцированного лазером, и процесс заживления в тканях. Hsp70 может биохимически определять зону термического повреждения, в которой клетки подвергаются разрушению, а HSP47 может иллюстрировать процесс восстановления после термически вызванного повреждения. [ 43 ] HSP70 помогает защитить кожу от увеличения количества меланина и образования морщин, вызванных воздействием ультрафиолета. [ 44 ]
нейродегенерация
[ редактировать ]Ингибирование Hsp90 приводит к усилению регуляции Hsp70 и Hsp40, что может направлять неправильно свернутый белок на деградацию протеасом, что потенциально может ингибировать прогрессирование нейродегенеративных заболеваний. [ 45 ] Например, сверхэкспрессия Hsp70 в клетках нейроглиомы человека, трансфицированных мутантным альфа-синуклеином, привела к уменьшению на 50% количества олигомерных видов альфа-синуклеина. [ 46 ] указывая на возможность того, что увеличение его экспрессии может уменьшить распространение болезни Паркинсона. Аналогично, сверхэкспрессия Hsp70 подавляла поли-Q-зависимую агрегацию и нейродегенерацию в клеточных культурах, дрожжах, [ 47 ] летать, [ 48 ] и мышь [ 49 ] модели, а удаление hsp70 увеличивало размер телец включения PolyQ, [ 50 ] предполагая, что увеличение его экспрессии может помочь предотвратить болезнь Хантингтона. Аналогично, снижение уровня Hsp70 было показано на моделях БАС на трансгенных мышах и у пациентов со спорадическим БАС. [ 51 ] Наконец, повышенная экспрессия или активность Hsp70 была предложена в качестве метода предотвращения прогрессирования болезни Альцгеймера, поскольку нокдаун Hsp70 способствовал токсичности А-бета. [ 52 ] Было показано, что Hsp70 способствует стабильности тау, тогда как уровни Hsp70 снижаются при тауопатиях, таких как болезнь Альцгеймера. [ 53 ] Учитывая сложное взаимодействие между различными белками-шаперонами, терапевтические разработки в этой области направлены на изучение того, как можно манипулировать сетью шаперонов в целом и влияние этих манипуляций на прогрессирование нейродегенеративных заболеваний, но баланс уровней Hsp70 и Hsp90 по-видимому, занимает центральное место в этой патофизиологии.
При диабете
[ редактировать ]Колебания уровней шаперона HSP70 влияют на гомеостаз. Диабет приводит к нескольким заболеваниям микроциркуляторного и микроциркуляторного русла, таким как ретинопатия. Toll-подобные рецепторы являются неотъемлемой частью врожденной иммунной системы, а eHSP70 связывается с toll-подобными рецепторами и активирует путь MyD88, дополнительно стимулируя NF-kB, цитокины, такие как TNFα и IL1β, увеличивая выработку активные формы кислорода, способствующие резистентности к инсулину и диабету. Тогда как наблюдается снижение уровня iHSP70. [ 54 ]
При сердечно-сосудистых заболеваниях
[ редактировать ]HSP70 является вездесущим компаньоном. [ 55 ] Он имеет решающее значение для сердечно-сосудистой системы. HSP70 обычно способствует сворачиванию и агрегации белков; при наличии в клетке действует как противовоспалительная молекула; однако в условиях стресса он локализуется во внеклеточной среде, где участвует в индукции воспалительных путей и вносит вклад в патогенез заболевания. [ 56 ] Хорошо известно, что внутриклеточные уровни HSP70 (iHSP70) играют защитную роль, тогда как внеклеточные уровни HSP70 (eHSP70) в циркулирующей крови связаны с патофизиологией в микро- и микроциркуляторном русле, что приводит к множеству сердечно-сосудистых заболеваний. Гомологи HSP70, идентифицированные в цитозоле человека, включают HSPA1A, HSPA1B, HSPA1L, HSPA12B, HSPA13, HSPA14, тогда как HSPA9 в митохондриях. HSP70 действует как DAMP и активирует врожденный иммунный ответ, который участвует в прогрессировании сердечно-сосудистых заболеваний. [ 57 ]
Белок-шаперон действует как аутоантиген при атеросклерозе. Повышенный окислительный стресс вызывает образование окисленных ЛПНП высокой плотности, что является первым этапом образования бляшек. Это активирует HSP70 и его промотор в эндотелиальных и гладкомышечных клетках, что способствует атеросклерозу, индуцируя экспрессию пути JAK/STAT. [ 58 ] [ 59 ]
HSP70 также связан с высоким кровяным давлением, которое является проблемой во всем мире и фактором риска развития различных сердечно-сосудистых заболеваний. Гипертония вызывает эндотелиальную дисфункцию и повреждение сосудистой стенки, оба из которых способствуют жесткости артерий и атеросклерозу. [ 60 ] HSPA1A, HSPA1B и HSPA1L — это три гена человека, кодирующие HSP70, и их полиморфизм связан с возникновением высокого кровяного давления и сердечно-сосудистых заболеваний. [ 61 ] Ангиотензин II, эндотелин-1 или фенилэпинефрин вызывают сверхэкспрессию HSP70, которая активирует несколько молекулярных путей, что приводит к увеличению продукции АФК, СРБ, IL-10, TNF-альфа и IL-6. [ 62 ] [ 61 ] Эти воспалительные сигналы мешают антиоксидантному механизму и приводят к быстрому прогрессированию заболевания.
Экспрессия HSP70 увеличивается после операции коронарного шунтирования. Физические упражнения оказывают положительное и защитное воздействие на сердечно-сосудистые заболевания и стимулируют повышенное производство белка-шаперона, который, как известно, обладает кардиозащитным действием.
Члены семьи
[ редактировать ]Прокариоты экспрессируют три белка Hsp70: DnaK , HscA (Hsc66) и HscC (Hsc62) . [ 63 ]
Эукариотические организмы экспрессируют несколько немного отличающихся белков Hsp70. Все они имеют общую доменную структуру, но каждый имеет уникальный образец экспрессии или субклеточную локализацию. Это, среди прочего:
- Hsc70 (Hsp73/HSPA8) представляет собой конститутивно экспрессируемый белок-шаперон. Обычно он составляет от одного до трех процентов от общего клеточного белка.
- Hsp70 (кодируемый тремя очень близкими паралогами: HSPA1A , HSPA1B и HSPA1L ) представляет собой белок, индуцируемый стрессом. Высокие уровни могут вырабатываться клетками в ответ на гипертермию, окислительный стресс и изменения pH .
- Связывающий белок иммуноглобулина ( BiP или Grp78 ) представляет собой белок, локализованный в эндоплазматическом ретикулуме . Там он участвует в сворачивании белка и может активироваться в ответ на стресс или голодание.
- mtHsp70 или Grp75 представляет собой митохондриальный Hsp70.
Ниже приводится список генов Hsp70 человека и соответствующих им белков: [ 2 ]
| ген | белок | синонимы | субклеточное расположение |
|---|---|---|---|
| HSPA1A | Hsp70 | HSP70-1, Hsp72 | Нук / Цито |
| HSPA1B | Hsp70 | HSP70-2 | Нук/Цито |
| HSPA1L | Hsp70 | ? | |
| HSPA2 | Hsp70-2 | ? | |
| HSPA5 | Hsp70-5 | БиП/Группа78 | ЯВЛЯЕТСЯ |
| HSPA6 | Hsp70-6 | ? | |
| HSPA7 | Hsp70-7 | ? | |
| HSPA8 | Hsp70-8 | Hsc70 | Нук/Цито |
| HSPA9 | Hsp70-9 | Группа75/mtHsp70 | Миф |
| HSPA12A | Hsp70-12a | ? | |
| HSPA14 | Hsp70-14 | ? |
HSP70 обнаружены во многих растениях , включая Arabidopsis , сою ( Glycine max ), ячмень ( Hordeum vulgare ) и пшеницу ( Triticum aestivum ). [ 64 ]
HSP 90 и 110
[ редактировать ]
Hsp90 необходимы для ремоделирования белков, подобно белкам Hsp70, и играют особенно важную роль у эукариот, где было высказано предположение, что Hsp90 взаимодействует с системой DnaK (состоящей из DnaK, GrpE и либо DnaJ, либо CbpA), чтобы облегчить этот процесс. ремоделирования белка. [ 65 ] В E. coli Hsp90s работает совместно с Hsp70s, облегчая ремоделирование и активацию белка. Hsp90Ec и DnaK являются шаперонами Hsp90 и Hsp70 соответственно. DnaK первоначально связывает и стабилизирует неправильно свернутый белок, а затем взаимодействует с Hsp90Ec, чтобы повторно свернуть этот субстрат и вызвать его активацию. Было обнаружено, что в условиях избытка DnaK этот шаперон ингибирует ремоделирование белков. Однако присутствие Hsp90Ec может смягчить этот эффект и обеспечить ремоделирование белка, несмотря на избыток DnaK. [ 66 ]
Суперсемейство Hsp70 также включает семейство белков Hsp110 / Grp170 (Sse), которые представляют собой более крупные белки, родственные Hsp70. [ 67 ] Семейство белков Hsp110 имеет разные функции: дрожжевой Sse1p обладает небольшой АТФазной активностью, но сам по себе является шапероном, а также фактором обмена нуклеотидов для Hsp70, в то время как близкородственный Sse2p имеет небольшую разворачивающую активность. [ 12 ]
Ниже приводится список названных в настоящее время генов HSP110 человека. HSPH2-4 — это предложенные имена, а текущее имя связано: [ 67 ]
| ген | синонимы | субклеточное расположение |
|---|---|---|
| HSPH1 | HSP105 | Цито |
| HSPH2 | HSPA4 ; АПГ-2; HSP110 | Цито |
| HSPH3 | HSPA4L ; АПГ-1 | Нук |
| HSPH4 | ХЁУ1 /Группа170; ОРП150; HSP12A | ЯВЛЯЕТСЯ |
См. также
[ редактировать ]Ссылки
[ редактировать ]- ^ Флаэрти К.М., ДеЛука-Флаэрти С., Маккей Д.Б. (август 1990 г.). «Трехмерная структура фрагмента АТФазы родственного белка теплового шока 70K». Природа . 346 (6285): 623–8. Бибкод : 1990Natur.346..623F . дои : 10.1038/346623a0 . ПМИД 2143562 . S2CID 4338916 .
- ^ Jump up to: а б Тавария М., Габриэле Т., Кола И., Андерсон Р.Л. (апрель 1996 г.). «Автостопом по человеческому семейству Hsp70» . Клеточные стрессы и шапероны . 1 (1): 23–8. doi : 10.1379/1466-1268(1996)001<0023:ahsgtt>2.3.co;2 (неактивен 22 июня 2024 г.). ПМК 313013 . ПМИД 9222585 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на июнь 2024 г. ( ссылка ) - ^ Морано К.А. (октябрь 2007 г.). «Новые трюки для старой собаки: развивающийся мир Hsp70». Анналы Нью-Йоркской академии наук . 1113 (1): 1–14. Бибкод : 2007NYASA1113....1M . дои : 10.1196/анналы.1391.018 . ПМИД 17513460 . S2CID 20917046 .
- ^ Гири Б., Сетхи В., Моди С., Гарг Б., Банерджи С., Салуджа А., Дудея В. (июль 2017 г.). « Белок теплового шока 70 при заболеваниях поджелудочной железы: друг или враг » . Журнал хирургической онкологии . 116 (1): 114–122. дои : 10.1002/jso.24653 . ПМЦ 5714583 . ПМИД 28543919 .
- ^ Де Майо А (май 2014 г.). «Внеклеточный Hsp70: экспорт и функции». Современная наука о белках и пептидах . 15 (3): 225–31. дои : 10.2174/1389203715666140331113057 . ПМИД 24694368 .
- ^ Ритосса Ф (1962). «Новый образец пыхтения, вызванный температурным шоком и ДНП у дрозофилы». Клеточные и молекулярные науки о жизни . 18 (12): 571–573. дои : 10.1007/BF02172188 . S2CID 32525462 .
- ^ Ритосса Ф (июнь 1996 г.). «Открытие реакции на тепловой шок» . Клеточные стрессы и шапероны . 1 (2): 97–8. doi : 10.1379/1466-1268(1996)001<0097:dothsr>2.3.co;2 (неактивен 26 апреля 2024 г.). ПМК 248460 . ПМИД 9222594 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на апрель 2024 г. ( ссылка ) - ^ Jump up to: а б с Востоколаи М.А., Хатами-Барух Л., Бабаи Г., Молави О., Корди С., Абдолализаде Дж. (май 2021 г.). «Hsp70 при раке: двойной агент в битве между выживанием и смертью». Журнал клеточной физиологии . 236 (5): 3420–3444. дои : 10.1002/jcp.30132 . ПМИД 33169384 . S2CID 226295557 .
- ^ Депутат Майера (август 2010 г.). «Гимнастика молекулярных шаперонов» . Молекулярная клетка . 39 (3): 321–31. doi : 10.1016/j.molcel.2010.07.012 . ПМИД 20705236 .
- ^ Као Ч., Рю С.В., Ким М.Дж., Вэнь Х, Вималаратне О., Полл Т.Т. (май 2020 г.). «Регулируемое ростом фосфорилирование Hsp70 регулирует реакцию на стресс и поддержание прионов» . Молекулярная и клеточная биология . 40 (12). дои : 10.1128/MCB.00628-19 . ПМЦ 7261718 . ПМИД 32205407 .
- ^ Машаги А., Безрукавников С., Минде Д.П., Вентинк А.С., Китык Р., Захманн-Бранд Б. и др. (ноябрь 2016 г.). «Альтернативные режимы привязки клиента обеспечивают функциональную пластичность Hsp70». Природа . 539 (7629): 448–451. Бибкод : 2016Natur.539..448M . дои : 10.1038/nature20137 . ПМИД 27783598 . S2CID 4401991 .
- ^ Jump up to: а б Брейчер А., Вергезе Дж. (2015). «Белки домена GrpE, Hsp110/Grp170, HspBP1/Sil1 и BAG: факторы нуклеотидного обмена для молекулярных шаперонов Hsp70». Сеть сопровождающих через со-сопровождающих . Субклеточная биохимия. Том. 78. стр. 1–33. дои : 10.1007/978-3-319-11731-7_1 . ISBN 978-3-319-11730-0 . ПМИД 25487014 .
- ^ Вегеле Х., Мюллер Л., Бюхнер Дж. (2004). «Hsp70 и Hsp90 — эстафета сворачивания белка». Hsp70 и Hsp90 — эстафета сворачивания белка . Обзоры физиологии, биохимии и фармакологии. Том. 151. стр. 1–44. дои : 10.1007/s10254-003-0021-1 . ISBN 978-3-540-22096-1 . ПМИД 14740253 .
{{cite book}}:|journal=игнорируется ( помогите ) - ^ Цворо А, Дунджерски Дж, Трайкович Д, Матич Г (1 апреля 1999 г.). «Уровень и фосфорилирование Hsp70 в цитозоле печени крыс после адреналэктомии и гипертермии». Международная клеточная биология . 23 (4): 313–20. дои : 10.1006/cbir.1998.0247 . ПМИД 10600240 . S2CID 9113738 .
- ^ Гао Т., Ньютон AC (август 2002 г.). «Мотив поворота — это переключатель фосфорилирования, который регулирует связывание Hsp70 с протеинкиназой C» . Журнал биологической химии . 277 (35): 31585–92. дои : 10.1074/jbc.M204335200 . ПМИД 12080070 .
- ^ Трумэн А.В., Кристьянсдоттир К., Вольфгехер Д., Хасин Н., Полиер С., Чжан Х. и др. (декабрь 2012 г.). «CDK-зависимое фосфорилирование Hsp70 контролирует количество циклина G1 и развитие клеточного цикла» . Клетка . 151 (6): 1308–18. дои : 10.1016/j.cell.2012.10.051 . ПМЦ 3778871 . ПМИД 23217712 .
- ^ Мюллер П., Рукова Э., Халада П., Коутс П.Дж., Хрстка Р., Лейн Д.П., Войтесек Б. (июнь 2013 г.). «С-концевое фосфорилирование Hsp70 и Hsp90 регулирует поочередное связывание с кошаперонами CHIP и HOP для определения баланса сворачивания/деградации клеточных белков» . Онкоген . 32 (25): 3101–10. дои : 10.1038/onc.2012.314 . ПМИД 22824801 . S2CID 12604151 .
- ^ Людерс Дж., Деманд Дж., Хёфельд Дж. (февраль 2000 г.). «Связанный с убиквитином BAG-1 обеспечивает связь между молекулярными шаперонами Hsc70/Hsp70 и протеасомой» . Журнал биологической химии . 275 (7): 4613–7. дои : 10.1074/jbc.275.7.4613 . ПМИД 10671488 .
- ^ Бир Х.М., Вольф Б.Б., Каин К., Моссер Д.Д., Махбуби А., Кувана Т. и др. (август 2000 г.). «Белок теплового шока 70 ингибирует апоптоз, предотвращая привлечение прокаспазы-9 к апоптосоме Apaf-1». Природная клеточная биология . 2 (8): 469–75. дои : 10.1038/35019501 . ПМИД 10934466 . S2CID 1507966 .
- ^ Гупта С., Дипти А., Диган С., Лиссабона Ф., Хец С., Самали А. (июль 2010 г.). Келли Дж.В. (ред.). «HSP72 защищает клетки от апоптоза, вызванного стрессом ER, посредством усиления передачи сигналов IRE1alpha-XBP1 посредством физического взаимодействия» . ПЛОС Биология . 8 (7): е1000410. дои : 10.1371/journal.pbio.1000410 . ПМЦ 2897763 . ПМИД 20625543 .
- ^ Бобкова Н.В., Евгеньев М., Гарбуз Д.Г., Куликов А.М., Морозов А., Самохин А. и др. (декабрь 2015 г.). «Экзогенный Hsp70 задерживает старение и улучшает когнитивные функции у стареющих мышей» . Труды Национальной академии наук Соединенных Штатов Америки . 112 (52): 16006–16011. Бибкод : 2015PNAS..11216006B . дои : 10.1073/pnas.1516131112 . ПМК 4702952 . ПМИД 26668376 .
- ^ Риканиадис Н., Катаки А., Агнантис Н., Андрулакис Г., Каракусис С.П. (февраль 2001 г.). «Долгосрочное прогностическое значение экспрессии HSP-70, c-myc и HLA-DR у пациентов со злокачественной меланомой». Европейский журнал хирургической онкологии . 27 (1): 88–93. дои : 10.1053/ejso.1999.1018 . ПМИД 11237497 .
- ^ Рэмп Ю, Махотка С, Хейкаус С, Шибата Т, Гримм М.О., Виллерс Р., Габберт Х.Е. (октябрь 2007 г.). «Экспрессия белка теплового шока 70 при почечно-клеточном раке и ее связь с прогрессированием опухоли и прогнозом». Гистология и гистопатология . 22 (10): 1099–107. дои : 10.14670/HH-22.1099 . ПМИД 17616937 .
- ^ Шерман М., Мультхофф Дж. (октябрь 2007 г.). «Белки теплового шока при раке». Анналы Нью-Йоркской академии наук . 1113 (1): 192–201. Бибкод : 2007NYASA1113..192S . дои : 10.1196/анналы.1391.030 . ПМИД 17978282 . S2CID 39372827 .
- ^ Дхамад А.Е., Чжоу З, Чжоу Дж, Ду Ю (2016). «Систематическая протеомная идентификация белков теплового шока (Hsp), которые взаимодействуют с рецептором эстрогена альфа (ERα), и биохимическая характеристика взаимодействия ERα-Hsp70» . ПЛОС ОДИН . 11 (8): e0160312. Бибкод : 2016PLoSO..1160312D . дои : 10.1371/journal.pone.0160312 . ПМЦ 4970746 . ПМИД 27483141 .
- ^ Мартинкова В, Трчка Ф, Войтешек Б, Мюллер П (2018). «Роль HSP70 при раке и его использование в качестве терапевтической мишени» . Клиническая онкология . 31 (Приложение 2): 46–54. дои : 10.14735/amko20182S46 . ПМИД 31023024 .
- ^ Моради-Марджане Р., Пасебан М., Моради Марджане М. (декабрь 2019 г.). «Ингибиторы Hsp70: значение для лечения колоректального рака» . ИУБМБ Жизнь . 71 (12): 1834–1845. дои : 10.1002/iub.2157 . ПМИД 31441584 . S2CID 201619393 .
- ^ Ду XL, Цзян Т, Вэнь ZQ, Гао Р, Цуй М, Ван Ф (апрель 2009 г.). «Подавление экспрессии белка теплового шока 70 повышает эффективность лучевой терапии и ингибирует инвазию клеток в клеточную линию рака эндометрия» . Хорватский медицинский журнал . 50 (2): 143–50. дои : 10.3325/cmj.2009.50.143 . ПМК 2681060 . ПМИД 19399947 .
- ^ Гюнтер С., Остхаймер С., Штангл С., Шпехт Х.М., Мозес П., Йезингхаус М. и др. (2015). «Корреляция уровней Hsp70 в сыворотке с общим объемом опухоли и составом субпопуляций лимфоцитов у пациентов с плоскоклеточным и адено-немелкоклеточным раком легкого» . Границы в иммунологии . 6 : 556. дои : 10.3389/fimmu.2015.00556 . ПМЦ 4629690 . ПМИД 26579130 .
- ^ Блэк Джей Ди, Резвани К (2016). «Белки теплового шока 70 как потенциальные молекулярные мишени для лечения рака толстой кишки». Современная медицинская химия . 23 (28): 3171–3188. дои : 10.2174/0929867323666160627105033 . ПМИД 27356538 .
- ^ Мозес М.А., Ким Ю.С., Ривера-Маркес Г.М., Осима Н., Уотсон М.Дж., Бибе К.Е. и др. (июль 2018 г.). «Нацеливание на шаперонную ось Hsp40/Hsp70 как новую стратегию лечения резистентного к кастрации рака простаты» . Исследования рака . 78 (14): 4022–4035. дои : 10.1158/0008-5472.CAN-17-3728 . ПМК 6050126 . ПМИД 29764864 .
- ^ Барнс Дж.А., Дикс DJ, Коллинз Б.В., Люфт С., Аллен Дж.В. (октябрь 2001 г.). «Экспрессия индуцибельного Hsp70 усиливает пролиферацию клеток рака молочной железы MCF-7 и защищает от цитотоксических эффектов гипертермии» . Клеточные стрессы и шапероны . 6 (4): 316–25. doi : 10.1379/1466-1268(2001)006<0316:eoihet>2.0.co;2 (неактивен 22 июня 2024 г.). ПМК 434414 . ПМИД 11795468 .
{{cite journal}}: CS1 maint: DOI неактивен по состоянию на июнь 2024 г. ( ссылка ) - ^ Го Д., Чжан А., Хуан Дж., Суо М., Чжун Ю., Лян Ю. (ноябрь 2019 г.). «Подавление HSP70 ингибирует развитие острого лимфобластного лейкоза посредством TAK1/Egr-1» . Биомедицина и фармакотерапия . 119 : 109399. doi : 10.1016/j.biopha.2019.109399 . ПМИД 31521893 . S2CID 202582093 .
- ^ Кумар С., Стоукс Дж., Сингх У.П., Сциссум Ганн К., Ачарья А., Манне У., Мишра М. (апрель 2016 г.). «Нацеливание на Hsp70: возможная терапия рака» . Письма о раке . 374 (1): 156–166. дои : 10.1016/j.canlet.2016.01.056 . ПМЦ 5553548 . ПМИД 26898980 .
- ^ Пауэрс М.В., Джонс К., Бариллари С., Вествуд И., ван Монфор Р.Л., Уоркман П. (апрель 2010 г.). «Нацеленность на HSP70: второй потенциально лекарственный белок теплового шока и молекулярный шаперон?». Клеточный цикл . 9 (8): 1542–50. дои : 10.4161/cc.9.8.11204 . ПМИД 20372081 . S2CID 37329279 .
- ^ Albakova Z, Armeev GA, Kanevskiy LM, Kovalenko EI, Sapozhnikov AM (March 2020). "HSP70 Multi-Functionality in Cancer" . Cells . 9 (3): 587. doi : 10.3390/cells9030587 . PMC 7140411 . PMID 32121660 .
- ^ Меллатяр Х., Талаи С., Пилевар-Солтанахмади Ю., Барзегар А., Акбарзаде А., Шахаби А. и др. (июнь 2018 г.). «Таргетная терапия рака с помощью 17-DMAG в качестве ингибитора Hsp90: обзор и современное состояние». Биомедицина и фармакотерапия . 102 : 608–617. дои : 10.1016/j.biopha.2018.03.102 . ПМИД 29602128 . S2CID 4505299 .
- ^ Кумар С., Дипак П., Кумар С., Кишор Д., Ачарья А. (2009). «Аутологичный Hsp70 индуцирует антигенспецифические иммунные ответы Th1 при мышиной Т-клеточной лимфоме». Иммунологические исследования . 38 (6): 449–65. дои : 10.1080/08820130902802673 . ПМИД 19811405 . S2CID 24747281 .
- ^ Гужова И.В., Маргулис Б.А. (октябрь 2016 г.). «Противораковая иммунотерапия на основе HSP70» . Человеческие вакцины и иммунотерапия . 12 (10): 2529–2535. дои : 10.1080/21645515.2016.1190057 . ПМК 5084976 . ПМИД 27294301 .
- ^ Коттке Т., Санчес-Перес Л., Диас Р.М., Томпсон Дж., Чонг Х., Харрингтон К. и др. (декабрь 2007 г.). «Индукция hsp70-опосредованного аутоиммунитета Th17 может быть использована в качестве иммунотерапии метастатического рака простаты» . Исследования рака . 67 (24): 11970–9. дои : 10.1158/0008-5472.CAN-07-2259 . ПМИД 18089828 .
- ^ Шантелуп Г., Кордонье М., Исамбер Н., Берто А., Эрвье А., Хеннекен А. и др. (2020). «Мониторинг экзосом HSP70 при наблюдении онкологических больных: клиническое проспективное пилотное исследование» . Журнал внеклеточных везикул . 9 (1): 1766192. doi : 10.1080/20013078.2020.1766192 . ПМК 7301715 . ПМИД 32595915 .
- ^ Георгиевски А., Мишель А., Томас С., Мламла З., Паис де Баррос Ж.П., Лемэр-Юинг С. и др. (2022). «Внеклеточные везикулы, вызванные острым лимфобластным лейкозом, влияют на состояние покоя гемопоэтических стволовых клеток и клеток-предшественников» . Смерть клетки Дис . 12 (4): 337. doi : 10.1038/s41419-022-04761-5 . ПМК 9005650 . ПМИД 35414137 . S2CID 248127986 .
- ^ Саджади А.Ю., Митра К., Грейс М. (октябрь 2013 г.). «Экспрессия белков теплового шока 70 и 47 в тканях после короткоимпульсного лазерного облучения: оценка термического повреждения и заживления» (PDF) . Медицинская инженерия и физика . 35 (10): 1406–14. дои : 10.1016/j.medengphy.2013.03.011 . ПМИД 23587755 .
- ^ Мацуда М., Хосино Т., Ямакава Н., Тахара К., Адачи Х., Собуэ Г. и др. (апрель 2013 г.). «Подавление образования морщин, вызванного УФ-излучением, путем индукции экспрессии HSP70 у мышей» . Журнал исследовательской дерматологии . 133 (4): 919–928. дои : 10.1038/jid.2012.383 . ПМИД 23096703 .
- ^ Лаки Р.Э., Мациевски А., Остапченко В.Г., Маркес-Лопес Дж., Чой В.Ю., Дуэннвальд М.Л. и др. (2017). «Шаперонный механизм Hsp70/Hsp90 при нейродегенеративных заболеваниях» . Границы в неврологии . 11 : 254. дои : 10.3389/fnins.2017.00254 . ПМЦ 5433227 . ПМИД 28559789 .
- ^ Оутейро Т.Ф., Путча П., Тецлафф Дж.Э., Спельген Р., Кокер М., Карвальо Ф. и др. (апрель 2008 г.). «Образование токсичных олигомерных видов альфа-синуклеина в живых клетках» . ПЛОС ОДИН . 3 (4): е1867. Бибкод : 2008PLoSO...3.1867O . дои : 10.1371/journal.pone.0001867 . ПМК 2270899 . ПМИД 18382657 .
- ^ Кармайкл Дж., Шателье Дж., Вульфсон А., Мильштейн С., Фершт А.Р., Рубинштейн Д.К. (август 2000 г.). «Бактериальные и дрожжевые шапероны уменьшают как образование агрегатов, так и гибель клеток в клеточных моделях болезни Хантингтона у млекопитающих» . Труды Национальной академии наук Соединенных Штатов Америки . 97 (17): 9701–5. Бибкод : 2000PNAS...97.9701C . дои : 10.1073/pnas.170280697 . ЧВК 16928 . ПМИД 10920207 .
- ^ Уоррик Дж. М., Чан Х. И., Грей-Борд Г. Л., Чай Ю., Полсон Х. Л., Бонини Н. М. (декабрь 1999 г.). «Подавление полиглутамин-опосредованной нейродегенерации у дрозофилы с помощью молекулярного шаперона HSP70». Природная генетика . 23 (4): 425–8. дои : 10.1038/70532 . ПМИД 10581028 . S2CID 24632055 .
- ^ Вакер Дж.Л., Зари М.Х., Фонг Х., Сарикая М., Муховски П.Дж. (декабрь 2004 г.). «Hsp70 и Hsp40 ослабляют образование сферических и кольцевых олигомеров полиглутамина за счет разделения мономера». Структурная и молекулярная биология природы . 11 (12): 1215–22. дои : 10.1038/nsmb860 . ПМИД 15543156 . S2CID 43035 .
- ^ Вакер Дж.Л., Хуанг С.Ю., Стил А.Д., Арон Р., Лотц Г.П., Нгуен К. и др. (июль 2009 г.). «Потеря Hsp70 усугубляет патогенез, но не уровень фибриллярных агрегатов в мышиной модели болезни Хантингтона» . Журнал неврологии . 29 (28): 9104–14. doi : 10.1523/JNEUROSCI.2250-09.2009 . ПМК 2739279 . ПМИД 19605647 .
- ^ Чен Х.Дж., Митчелл Дж.К., Новоселов С., Миллер Дж., Нисимура А.Л., Скоттер Э.Л. и др. (май 2016 г.). «Реакция на тепловой шок играет важную роль в клиренсе TDP-43: доказательства дисфункции при боковом амиотрофическом склерозе» . Мозг . 139 (Часть 5): 1417–32. дои : 10.1093/brain/aww028 . ПМЦ 4845254 . ПМИД 26936937 .
- ^ Бреме М., Вуазин С., Роллан Т., Вачи С., Сопер Дж.Х., Чжу Ю. и др. (ноябрь 2014 г.). «Подсеть шаперомов защищает протеостаз при старении и нейродегенеративных заболеваниях» . Отчеты по ячейкам . 9 (3): 1135–50. дои : 10.1016/j.celrep.2014.09.042 . ПМЦ 4255334 . ПМИД 25437566 .
- ^ Доу Ф., Нетцер В.Дж., Танемура К., Ли Ф., Хартл Ф.У., Такашима А. и др. (январь 2003 г.). «Шапероны увеличивают связь тау-белка с микротрубочками» . Труды Национальной академии наук Соединенных Штатов Америки . 100 (2): 721–6. Бибкод : 2003PNAS..100..721D . дои : 10.1073/pnas.242720499 . ПМК 141063 . ПМИД 12522269 .
- ^ Муляни В.Р., Сандживани М.И., Прабава И.П., Лестари А.А., Вихандани Д.М., Суастика К. и др. (февраль 2020 г.). «Терапевтическая целевая инновация на основе шаперонов: белок теплового шока 70 (HSP70) для лечения сахарного диабета 2 типа» . Диабет, метаболический синдром и ожирение: цели и терапия . 13 : 559–568. дои : 10.2147/dmso.s232133 . ПМК 7051252 . ПМИД 32161482 .
- ^ Хавалова Х, Ондровичова Г, Керестешова Б, Бауэр Й.А., Певала В, Кутейова Е, Кунова Н (июль 2021 г.). «Митохондриальная шаперонная система HSP70 — влияние посттрансляционных модификаций и участие в заболеваниях человека» . Международный журнал молекулярных наук . 22 (15): 8077. doi : 10.3390/ijms22158077 . ПМЦ 8347752 . ПМИД 34360841 .
- ^ Линдер М., Погге фон Страндманн Э. (сентябрь 2021 г.). «Роль внеклеточного HSP70 в функции опухолеассоциированных иммунных клеток» . Раки . 13 (18): 4721. doi : 10.3390/cancers13184721 . ПМЦ 8466959 . ПМИД 34572948 .
- ^ Цай В.Ф., Чжан С.В., Ян Х.М., Ма Ю.Г., Ван XX, Ян Дж. и др. (октябрь 2010 г.). «Внутриклеточный или внеклеточный белок теплового шока 70 по-разному регулирует ремоделирование сердца у мышей с перегрузкой давлением». Сердечно-сосудистые исследования . 88 (1): 140–149. дои : 10.1093/cvr/cvq182 . ПМИД 20542874 .
- ^ Уик С (2019). «Белок теплового шока 60: медиатор атеросклероза и его потенциальная терапевтическая роль». Шаперокиновая активность белков теплового шока . Том. 16. Чам: Международное издательство Springer. стр. 81–103. дои : 10.1007/978-3-030-02254-9_4 . ISBN 978-3-030-02253-2 . S2CID 104325416 .
- ^ Ленг Х, Ван Х, Пан В., Чжан Р., Чжан З., Ван Л. и др. (июль 2013 г.). «Доказательства роли как антитела против Hsp70, так и Hsp70 поверхностной мембраны эндотелия при атеросклерозе» . Клеточные стрессы и шапероны . 18 (4): 483–493. дои : 10.1007/s12192-013-0404-4 . ПМК 3682019 . ПМИД 23334859 .
- ^ Галло Дж., Вольпе М., Савойя К. (20 января 2022 г.). «Эндотелиальная дисфункция при гипертонии: современные концепции и клинические последствия» . Границы в медицине . 8 : 798958. doi : 10.3389/fmed.2021.798958 . ПМЦ 8811286 . ПМИД 35127755 .
- ^ Jump up to: а б Чэнь Ю, Чжао Г, Ли Н, Луо Х, Ван X, Гу Дж (январь 2023 г.). «[Исправление] Роль 4-аминобутират-аминотрансферазы (ABAT) и сети совместной экспрессии днРНК в развитии миелодиспластического синдрома» . Отчеты онкологии . 49 (1): 1223–1229. дои : 10.1161/01.cir.92.5.1223 . ПМЦ 9685366 . ПМИД 36416343 .
- ^ Шривастава К., Наранг Р., Бхатия Дж., Салуджа Д. (18 марта 2016 г.). «Экспрессия гена белка теплового шока 70 и его корреляция с маркерами воспаления при эссенциальной гипертонии» . ПЛОС ОДИН . 11 (3): e0151060. Бибкод : 2016PLoSO..1151060S . дои : 10.1371/journal.pone.0151060 . ПМЦ 4798713 . ПМИД 26989902 .
- ^ Ёсимунэ К., Ёсимура Т., Накаяма Т., Нишино Т., Эсаки Н. (май 2002 г.). «Hsc62, Hsc56 и GrpE, третья шаперонная система Hsp70 Escherichia coli». Связь с биохимическими и биофизическими исследованиями . 293 (5): 1389–95. дои : 10.1016/S0006-291X(02)00403-5 . ПМИД 12054669 .
- ^ Берка М, Копецка Р, Беркова В, Брзобогаты Б, Черный М (апрель 2022 г.). «Регуляция белков теплового шока 70 и их роль в иммунитете растений» . Обзорная статья. Журнал экспериментальной ботаники . 73 (7). Издательство Оксфордского университета (ОУП): 1894–1909. дои : 10.1093/jxb/erab549 . ПМЦ 8982422 . ПМИД 35022724 . Общество экспериментальной биологии (SEB).
- ^ Дженест О., Хоскинс-младший, Камберг Дж.Л., Дойл С.М., Викнер С. (май 2011 г.). «Белок теплового шока 90 из Escherichia coli сотрудничает с системой шаперонов DnaK в ремоделировании клиентского белка» . Труды Национальной академии наук Соединенных Штатов Америки . 108 (20): 8206–11. Бибкод : 2011PNAS..108.8206G . дои : 10.1073/pnas.1104703108 . ПМК 3100916 . ПМИД 21525416 .
- ^ Дженест О., Викнер С., Дойл С.М. (февраль 2019 г.). «Шапероны Hsp90 и Hsp70: участники ремоделирования белка» . Журнал биологической химии . 294 (6): 2109–2120. дои : 10.1074/jbc.REV118.002806 . ПМК 6369297 . ПМИД 30401745 .
- ^ Jump up to: а б Кампинга Х.Х., Хагеман Дж., Вос М.Дж., Кубота Х., Тангуай Р.М., Бруфорд Э.А. и др. (январь 2009 г.). «Руководство по номенклатуре белков теплового шока человека» . Клеточные стрессы и шапероны . 14 (1): 105–11. дои : 10.1007/s12192-008-0068-7 . ПМК 2673902 . ПМИД 18663603 .
Внешние ссылки
- HSP70 + Тепловой шок + Белки в Национальной медицинской библиотеке США по медицинским предметным рубрикам (MeSH)