Американский(III) хлорид
 | |
| Имена | |
|---|---|
| Название ИЮПАК Американский(III) хлорид | |
| Систематическое название ИЮПАК Хлорид америция (3+) | |
| Другие имена Америций хлорид Америция трихлорид | |
| Идентификаторы | |
3D model ( JSmol ) | |
| ХимическийПаук | |
ПабХим CID | |
| Характеристики | |
| AmClAmCl3 | |
| Молярная масса | 349 g·mol −1 |
| Появление | Светло-красные, непрозрачные кристаллы |
| Плотность | 5,87 г см −3 [1] |
| Температура плавления | 715 ° C (1319 ° F; 988 К) [2] |
| Точка кипения | 850 ° C (1560 ° F; 1120 К) [1] |
| Структура | |
| шестиугольный ( UCl 3 тип ), hP8 | |
| Р6 3 /м, №176 | |
| Треугольная треугольная призматика (девятикоординатный) | |
| Родственные соединения | |
Другие анионы | Американский(III) фторид Американ(III) бромид Американский(III) йодид |
Другие катионы | Хлорид плутония(III) Хлорид кюрия(III) Хлорид европия(III) |
| Хлорид америция(II) | |
Если не указано иное, данные приведены для материалов в стандартном состоянии (при 25 °C [77 °F], 100 кПа). | |
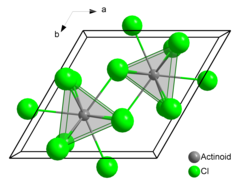
Хлорид америция(III) или трихлорид америция представляет собой соединение химическое америция и хлора с формулой AmCl 3 . Эта соль образует розовые шестиугольные кристаллы. В твердом состоянии каждый атом америция имеет девять атомов хлора в качестве ближайших соседей, примерно на одинаковом расстоянии, в трехглавой тригональной призматической конфигурации. [3] [4]
Гексагидрат имеет моноклинальную кристаллическую структуру с: а = 970,2 пм, b = 656,7 пм и с = 800,9 пм; β = 93°37'; пространственная группа: P 2/ n . [5]
Реакции
[ редактировать ]хлорида америция (III) Метод электрорафинирования был исследован для разделения смесей актинидов , поскольку стандартная свободная энергия Гиббса образования хлорида америция (III) сильно отличается от энергии остальных хлоридов актинидов. [6] Это можно использовать для удаления америция из плутония путем плавления сырой смеси вместе с солями, такими как хлорид натрия . [7]
Ссылки
[ редактировать ]- ^ Jump up to: а б «Химия: Таблица Менделеева: америций: данные о соединениях (хлорид америция (III))» . ВебЭлементы . Проверено 24 июня 2008 г.
- ^ Перри, Дейл Л.; Филлипс, Сидни Л. (1995), Справочник по неорганическим соединениям , CRC Press, стр. 15, ISBN 0-8493-8671-3 , получено 25 июня 2008 г.
- ^ Л. Б. Аспри, Т. К. Кинан, Ф. Х. Крузе: «Кристаллические структуры трифторидов, трихлоридов, трибромидов и трииодидов америция и кюрия», Inorg. хим. 1965 , 4 (7) , 985–986; дои : 10.1021/ic50029a013 .
- ^ А.Ф. Уэллс: Структурная неорганическая химия, 5-е издание (1984) Oxford Science Publications, ISBN 0-19-855370-6 .
- ^ Джон Х. Бернс, Джозеф Ричард Петерсон: «Кристаллические структуры гексагидрата трихлорида америция и гексагидрата трихлорида берклия», Inorg. хим. 1971 , 10 (1) , 147–151; два : 10.1021/ic50095a029 .
- ^ Агентство по ядерной энергии (2001), Материалы семинара по пирохимическому разделению , Авиньон, Франция: Издательство ОЭСР, стр. 276–277, ISBN. 92-64-18443-0 , получено 24 июня 2008 г.
- ^ Переработка плутония в комплексе ядерного оружия , Diane Publishing, 1992, с. 21, ISBN 1-56806-568-Х , получено 24 июня 2008 г.